Introducción
El garbanzo blanco tipo blanco-cremoso para exportación se cultiva principalmente en el noroeste de México en los estados de Sonora, Sinaloa y Baja California Sur (Morales y Durón, 2004), principalmente en las áreas de riego. Esta leguminosa se ha posicionado como un cultivo estratégico dentro de la agricultura del noroeste de México gracias a la producción de grano grande (calibre 40-44, número de granos en 30 g), de color blanco-cremoso, con calidad de exportación.
No obstante, en este panorama favorable, existen problemas que amenazan su permanencia como un cultivo rentable en la región y competitivo a nivel internacional, entre las principales limitantes de producción del garbanzo está Fusarium oxysporum Schlechtend.: Fr. f. sp. ciceris (Padwick) Matuo & K. Sato (Foc) y pudriciones radiculares de la raíz que son causadas por un complejo de hongos tales como, Fusarium solani Mart. Amend. Sacc., Macrophomina phaseolina (Tassi) Goid., Sclerotium rolfsii Sacc. y Rhizoctonia solani Kühn. En la Costa de Hermosillo se han reportado a F. solani, M. phaseolina y R. solani, siendo el género Fusarium el predominante (Ramírez, 1975).
Estas enfermedades se controlan con el uso de variedades resistentes; sin embargo, se ha observado que al utilizar extensivamente un cultivar resistente, paulatinamente se incrementan el resto de los patógenos en el suelo (Mathur y Sarbhoy, 1978). La rotación de cultivos también puede modificar la población de patógenos. Por ejemplo, al rotar con gramíneas se desfavorece la presencia de Fusarium spp; pero se beneficia a M. phaseolina, que ataca numerosos cultivos (Muñoz-Cabañas et al., 2005), aumentando su presencia en mayor proporción.
A nivel mundial la fusariosis vascular del garbanzo originado por Fusarium oxysporum f. sp. ciceris es el agente causal más común de la marchites del garbanzo (Trapero y Jiménez, 1985; Meyer et al., 1997; Sharma et al., 2005), esto hace que sea la especie más estudiada y con fuentes de resistencia genética identificadas. Sin embargo, el panorama regional es complicado ya que se han identificado cuatro especies causando pudriciones de raíz en garbanzo con diferente nivel de distribución en la región. Por lo anterior, el objetivo del estudio fue identificar y determinar la distribución y el riesgo potencial para el cultivo, de los hongos asociados a la fusariosis vascular y pudriciones de raíz del garbanzo con base en la distribución en áreas agrícolas de la Costa de Hermosillo, Sonora, México.
Materiales y métodos
Descripción del área de estudio
La región agrícola de la Costa de Hermosillo es una planicie costera con una elevación menor de 100 msnm, predominando el clima cálido (BWh), con suelo Yermosol Háplico de textura media. Los principales cultivos son cereales, árboles frutales y en el ciclo de otoño-invierno se produce garbanzo de grano blanco-cremosos para exportación.
Metodología de muestreo en campos con plantas enfermas
La Costa de Hermosillo se muestreó durante el ciclo otoño-invierno de 2012-13. Se realizó un muestreo dirigido. Se colectaron plantas que mostraban los síntomas típicos de fusariosis vascular (amarillamiento y marchitez), necrosis, pudriciones de raíz y tallo.
El muestreo realizado fue mixto (Casal y Mateu, 2003), al combinar un muestreo aleatorio por conglomerados, dividiéndose cada campo en grupos con plantas que mostraban síntomas similares. La etapa fenológica en donde se realizó el muestreo fue desde formación de grano hasta llenado de grano. Los puntos de muestreo se referenciaron geográficamente (GPS marca Garmín modelo Oregon 450). Se elaboró una base de datos integrándose a un sistema de información geográfica (SIG) en la aplicación comercial ESRI ArcMap Versión 10, donde se conjugaron la capa de muestreos parcelarios, el uso de suelo, cuerpos de agua, carreteras, un modelo digital de elevación, así como el tipo de clima y suelo.
Mediante el analizador espacial incorporado a ArcMap V10, se realizaron interpolaciones para la información de cada patógeno con la función ponderada del inverso de la distancia (IDW) entre puntos de muestreo. Adicionalmente se creó una quinta interpolación denominada “índice de severidad”, la clasificación se puede observar en el Cuadro 1. Debido a la uniformidad del ambiente del área de estudio y por la presencia del monocultivo de garbanzo, se juzgó innecesario verificar la significancia estadística de las interpolaciones.
Cuadro 1 Claves para el índice de riesgo de patógenos asociados a la fusariosis vascular y pudriciones de raíz del garbanzo en la Costa de Hermosillo, Sonora, México.
| Criterio | Índice de riesgo | Color |
| Parcela con una especie patogénica identificada | Bajo | Verde |
| Parcela con dos especies patogénicas identificadas | Medio | Amarillo |
| Parcelas con tres especies patogénicas identificadas | Alto | Naranja |
| Parcela con cuatro especies patogénicas identificadas en el sitio | Muy alto | Rojo |
Colecta e identificación de los patógenos presentes
Las muestras colectadas se colocaron en bolsas de polietileno y se llevaron al laboratorio de biotecnología del Campo Experimental Valle de Culiacán (CEVACU) del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP). Las plantas se lavaron con abundante agua destilada con la ayuda de un cepillo suave. Se cortaron porciones de 0.5 cm de tejidos enfermos y aparentemente sanos y se desinfectaron con hipoclorito de sodio al 2% por un minuto; las muestras se lavaron con agua destilada estéril para eliminar el exceso de hipoclorito de sodio, y se colocaron sobre papel filtro estéril para eliminar el exceso de humedad. Se colocaron 5 fragmentos de 2 mm en cajas Petri con medio de cultivo papa dextrosa agar (PDA) acidificado, y se incubaron a una temperatura de 25 °C. Las cajas se revisaron al microscopio compuesto (Olympus C x 31; utilizando el objetivo 4 x) a las 24, 48 y 72 h para observar crecimiento de hongos surgiendo de los fragmentos, de éstos se extrajeron puntas de hifa y grupos de hifas que se transfirieron a nuevas cajas Petri con PDA (Komada, 1975). Los aislamientos se purificaron por cultivos monoconidiales o punta de hifa, dependiendo del hongo aislado.
Una vez que se detectó crecimiento fúngico, se procedió a la purificación de las cepas para poder confirmar su identidad; la identificación a nivel de género se realizó utilizando las claves de Barnet y Hunter (1998). Del crecimiento de los fragmentos se seleccionaron patógenos que ocasionan la marchitez, entre ellos; Fusarium sp, Macrophomina phaseolina y Rhizoctonia solani. Para Fusarium sp, del micelio crecido en medio PDA se cortó un fragmento que fue suspendido en 1 mL de agua destilada estéril. Se estimó la cantidad de esporas con un hematocitómetro y mediante diluciones seriadas se obtuvieron cultivos monospóricos (Hernández-Martínez y Rangel-Montoya, 2011). Los cultivos se observaron al microscopio compuesto para ubicar esporas individuales germinadas; se marcó el sitio sobre el agar y un fragmento de este con la espora germinada y seleccionada se transfirió a una nueva caja de Petri con medio PDA suplementado con PCNB y cloranfenicol, incubándose en condiciones adecuadas para su crecimiento.
La identificación de los patógenos a nivel de especie, se hizo mediante la observación de las estructuras al microscopio y comparando con la descripción correspondiente a cada una. Por ejemplo, la identificación de Fusarium se realizó con base a la morfología del micelio y microconidias en las fiálides, de acuerdo a lo propuesto por Leslie y Summerell (2006). En un estudio previo Velarde et al. (2015), verificaron la capacidad de los aislados para causar los síntomas de F. oxysporum f. sp. ciceris en genotipos susceptibles y de ser el caso identificar la raza del patógeno mediante variedades diferenciales y marcadores moleculares asociados. En cuanto a phaseolina, los aislamientos se purificaron transfiriendo porciones de medio de cultivo con crecimiento fungoso en medio de cultivo papa-dextrosa-agar (PDA) fresco, acidificado con 1 mL L-1 de ácido láctico y se incubó a 30 °C durante cinco a siete días para la obtención del aislamiento puro (Gil-Langarica et al., 2008).
Categorización de predios y elaboración de figuras
Con la información sobre el número de especies causantes de pudriciones de raíz se realizó la categorización de los predios y áreas establecidas con garbanzo de acuerdo a las claves presentadas en el Cuadro 1. Por ejemplo, para categorizar un predio o área con un índice de riesgo relativamente bajo, fueron en los que se identificó una sola especie, cualquiera de las descritas abajo; mientras que en las fincas y áreas consideradas de alto riesgo se identificaron las cuatro especies causando daño al cultivo. Es conveniente aclarar que esta clasificación de riesgo es relativa porque la presencia abundante de una sola especie y una variedad susceptible sin protección, puede resultar en un alto daño. Para el procesamiento de datos y elaboración de mapas, se relacionó la incidencia de los patógenos en cada punto de muestreo mediante tablas de datos con los puntos de muestreo obteniéndose índices de riesgo basados en el número de especies de los patógenos identificados y a partir de estos se generó una tabla combinada, se realizaron interpolaciones para cada patógeno mediante el uso del interpolador IDW, es decir se generó espacialmente los índices de riesgo para las diferentes áreas agrícolas de la costa de Hermosillo clasificándose de acuerdo a las especies encontradas en cada punto en índice de riesgo.
Resultados y discusión
Colecta de plantas con síntomas de pudrición de raíz
Se colectaron 221 muestras de plantas de garbanzo en 46 campos agrícolas de la Costa de Hermosillo con síntomas característicos de fusariosis vascular, pudrición de raíz, clorosis, achaparramiento, xilema de color marrón y marchitez. Este complejo de patógenos causantes de pudriciones de raíz es favorecido por climas cálidos y suelos con textura arenosa. Las plantas son susceptibles en cualquier estado de desarrollo. Los síntomas son más evidentes en etapas posteriores a la floración. Cuarenta y dos de los campos resultaron positivos a hongos de los cuales se obtuvieron 197 aislamientos.
Durante el desarrollo del cultivo ocurrieron temperaturas favorables a los diferentes patógenos responsables de la enfermedad (Figura 1) de acuerdo a requerimientos de temperatura de cada especie; por ejemplo, M. phaseolina es agresiva bajo temperaturas altas y suelo seco durante la etapa reproductiva del cultivo (Gupta y Sharma, 2015). Además, éste hongo ataca a un amplio espectro de especies (Muñoz-Cabañas et al., 2005), lo que dificulta su control y erradicación.
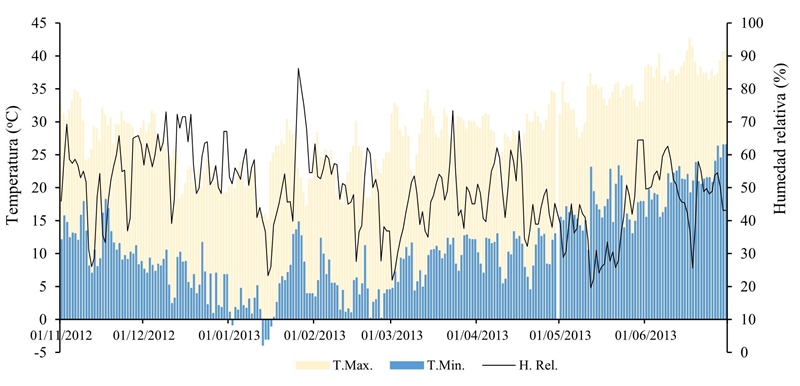
Figura 1 Temperatura máxima, mínima y humedad relativa diaria durante el ciclo de desarrollo del cultivo de garbanzo en el Campo Experimental Costa de Hermosillo, sitio representativo de la región.
En cuanto a Foc, se ha investigado que a una temperatura alrededor de 25 oC y una cantidad de inóculo de 104-105 g-1 de suelo, de micro o macroconidias, son las condiciones óptimas para desarrollar la enfermedad en garbanzo (Landa et al., 2001). Asímismo, diversos autores mencionan que bajo condiciones controladas del grado de la temperatura y la densidad del inoculo de Fusarium sp., así como de la humedad del suelo, se puede estimar el riesgo potencial de las enfermedades, así como la resistencia y susceptibilidad del genotipo de garbanzo (Bhatti y Kraft, 1992a,1992b; Sharma y Muehlbauer, 2007; Navas et al., 2007; Andrabi et al., 2009). Las variedades mejoradas desarrolladas para la región de la Costa de Hermosillo poseen resistencia a Fusarium sp; sin embargo, la presencia de diferentes razas de F. oxysporum fsp ciceris y el uso de grano como semilla dificultan su control (Velarde et al., 2015).
Distribución de especies en la región de estudio
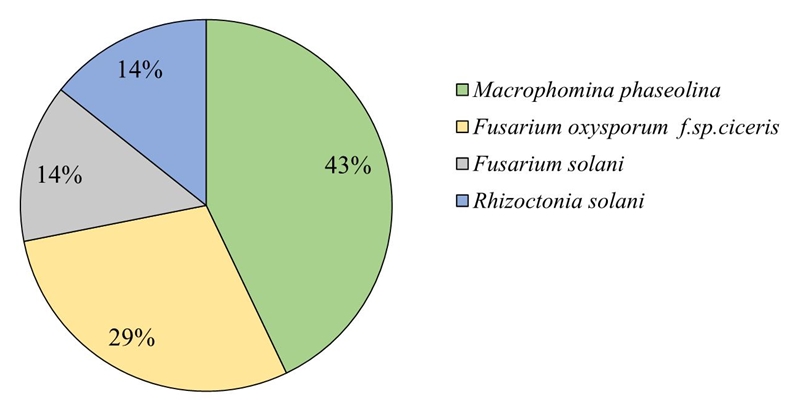
Los resultados indican que la especie con mayor distribución en el área de estudio fue M. phaseolina con 41% de frecuencia de aparición en el total de las muestras y el 77% de los sitios; Foc con presencia en el 27% de las muestras y en el 65% de los sitios; F. solani se detectó en el 13% de las muestras y en el 41% de los campos y R. Solani en el 14% de las muestras y con presencia en el 27% de los sitios muestreados (Figura 2). En un estudio similar realizado en el estado de Sinaloa, se detectó que el principal género fue Fusarium sp. con un 48% del total de las muestras (Ramírez et al., 2012). Ghosh et al., (2013) realizaron un muestreo en el Centro y Sur de la India y señalaron la presencia de diversos patógenos causando marchitez y pudriciones de raíz en garbanzo; concluyeron que Sclerotium rolsfii y Macrophomina phaseolina estuvieron ampliamente distribuidos en la región estudiada. Asímismo, en un trabajo de muestreo realizado en el sur de España, Trapero y Jiménez (1985) encontraron en 99% de 108 campos inspeccionados la presencia de F. oxysporum f. sp. ciceris, F. solani y M. phaseolina.
Mapeo de distribución de patógenos causando marchitez y pudriciones de raíz en garbanzo
Los sitios de bajo riesgo, con al menos una especie identificada, no necesariamente la misma, correspondieron al 22.5%, que representan 34 142 ha de un potencial de 151 820 ha (esto asumiendo que la superficie total de la Costa de Hermosillo se sembrara con garbanzo), localizándose estas áreas en una franja que se extiende del noreste al poniente de la región. Estas zonas son teóricamente las zonas con menor presencia de patógenos asociados con la secadera y pudrición de la raíz del garbanzo, y en las que preferentemente se debería establecer el cultivo.
Áreas de severidad media con dos especies identificadas (no necesariamente las mismas a través de localidades) representan el 41% de la superficie que corresponde a 62 236 ha localizadas la mayor parte en la región central del área agrícola y en algunas zonas al norte de esta región (Figura 3). Las de severidad alta, con al menos tres especies de patógenos detectados, en 50 628 ha que corresponde al 33.3% de la superficie agrícola básicamente localizada al sur y una zona al norte de la carretera Hermosillo-Bahía de Kino. De severidad muy alta, con los cuatro patógenos antes mencionados, presentes en sólo el 3.2% de la superficie en estudio correspondiente a 4 813 ha que teóricamente serían las de mayor riesgo asociado con patógenos que originan la fusariosis vascular y pudriciones de raíz del garbanzo.
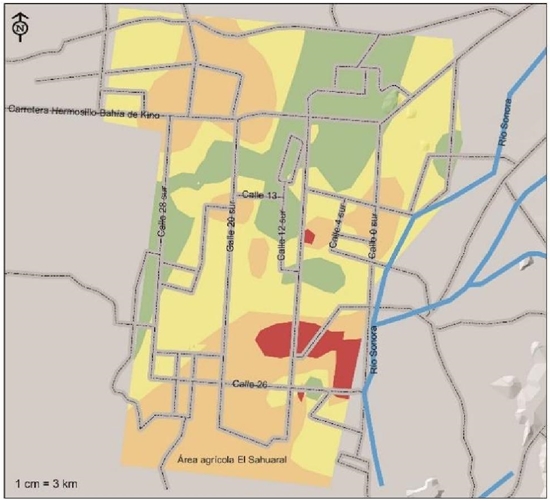
Figura 3 Índices de riesgo basados en la presencia de patógenos asociados a las pudriciones de raíz del garbanzo, aislados e identificados en la Costa de Hermosillo, Sonora. En color verde las áreas de riesgo bajo, en color amarillo se consideran de riesgo medio y las áreas de color naranja y rojo de riesgo alto y muy alto, respectivamente.
Esta superficie se localiza en forma de focos aislados al sur de la región agrícola entre las calles 4, 12 y 26 y dos pequeños focos por la calle 12 sur y la calle 26 (Figura 3). El mantenimiento de los sistemas de producción depende en gran medida de la protección a la planta. La solución sencilla sería evitar la siembra de garbanzo y rotación de cultivos necesario para que disminuya el inoculo en el suelo. Otra solución de mediano y largo plazo es piramidar diferentes genes de resistencia en contra de los cuatro distintos patógenos; mientras se desarrollan esos cultivares, el uso de semilla limpia, micoorganismos antagonistas (Paredes et al., 2009) y una nutrición adecuada del cultivo (Huber y Haneklaus, 2007), para la producción y productividad del garbanzo en la región.
En la Figura 4, se observan las áreas agrícolas de la Costa de Hermosillo en donde se aisló e identificó a M. phaseolina; este patógeno fue el de mayor distribución con alto índice de riesgo en las áreas agrícolas de la Costa de Hermosillo, con presencia potencial en 105 572 ha que representan el 69.5% del total. Esta especie representa un problema sanitario fuerte en caso de ocurrir las condiciones ambientales para que este hongo se manifieste dañando al cultivo del garbanzo. Nagama et al. (2015) mencionan que el uso de agroquímicos para control de este hongo se dificulta debido a la amplia gama de especies hospederas.
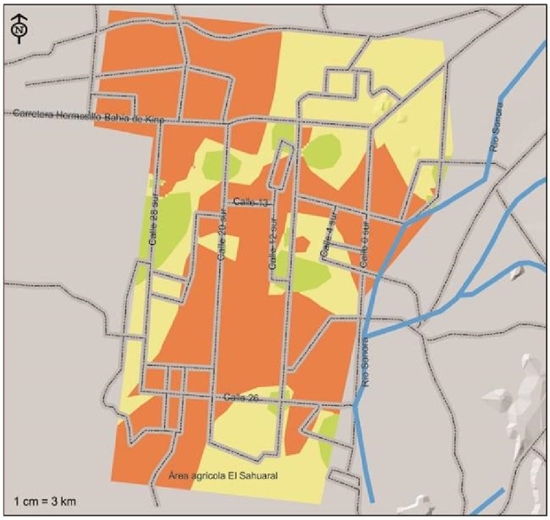
Figura 4 Índices de severidad de presencia de Macrophomina phaseolina, patógeno asociado a las pudriciones de raíz del garbanzo, aislado e identificado en la Costa de Hermosillo, Sonora.
Su presencia se extiende de norte a sur y de oriente a poniente, se definieron áreas agrícolas con índices de severidad moderada correspondiendo a 37 192 ha, representando el 24.5% de la superficie total, localizándose hacia al suroeste de la región extendiéndose hacia el sur-oriente, se localizaron además 2 subregiones con este mismo índice de severidad hacia el centro de la calle 20 sur y otro al nor-poniente, una subregión por la calle 28 sur y otra al centro de la región agrícola de la Costa de Hermosillo. Las áreas en donde se detectó M. phaseolina con intensidad de severidad moderada se localizan al sur por la calle 12 y al poniente por la calle 28, en donde teóricamente la presencia de este patógeno sería de consecuencias menos drásticas por tener menor frecuencia de aparición y quizá por condiciones de clima muy particulares. La presencia de este hongo tuvo mayor impacto en este ciclo debido a que la temperatura máxima diaria estuvo por arriba de 32 ºC con mayor frecuencia (Figura 2). Se ha mencionado que M. phaseolina tiene mayor virulencia bajo condiciones de estrés de sequía aunado a condiciones de clima caliente (Gupta y Sharma, 2015; Mayek et al., 2002). El Sistema Nacional Argentino de Vigilancia y Monitoreo de Plagas menciona que la infección de este patógeno es favorecida por condiciones que producen estrés de las plantas, en general por temperaturas altas (28 a 35 ºC) y baja humedad edáfica o sequía, especialmente durante el período reproductivo de las plantas.
En cuanto a los índices de riesgo de F. oxysporum, este junto con M. phaseolina son los de mayor distribución en los suelos de esta región, con presencia alta en alrededor de 86 696 ha que representan el 57.1% del total del área agrícola de la Costa de Hermosillo (Figura 5), con distribución desde la parte suroeste hacia el oriente afectando la parte central de la región, además de presencia alta al noroeste de la región y al norte de la carretera Hermosillo-Bahía de Kino, se ubicó dentro del rango moderado alrededor de 53 857 ha (35.5%), en zonas localizadas al oriente, sureste y noreste de la región y el 7.4% de la superficie que corresponde a 11 267 has, se ubicaron en el nivel de bajo localizado básicamente al centro y poniente de la región.
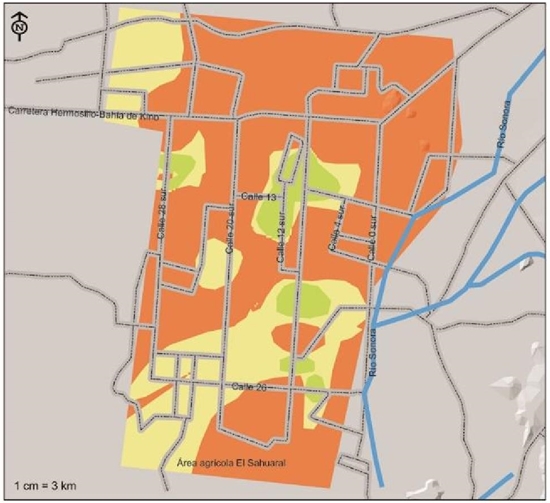
Figura 5 Índices de severidad de presencia de Fusarium oxisporum f. sp. ciceris, patógeno asociado a las pudriciones de raíz del garbanzo, aislado e identificado en la Costa de Hermosillo, Sonora.
En un trabajo similar realizado en la región agrícola de Maharashtra, India en la que se siembran 756 mil ha con garbanzo y tomando muestras tanto de variedades criollas como mejoradas, Nikam et al. (2007), obtuvieron resultados que indicaron la presencia de F. oxysporum causando daño al cultivo a través de diversas localidades desde 9.15 hasta 16.5 % de los campos muestreados. Pande et al., (2015) señalaron que la marchitez del garbanzo causada por F. oxysporum es la enfermedad más extendida y destructiva en la India; mientras que, en España, Landa et al. (2001) mencionaron que el desarrollo de esta enfermedad es mayor a 25 ºC en comparación con 20 y 30 ºC
En la Figura 6, se observa la distribución de F. solani en la región agrícola de la Costa de Hermosillo, de acuerdo a los índices de riesgo ponderado, este patógeno está menos distribuido comparado con M. phaseolina y F. oxysporum, las áreas con mayor presencia se localizan al sur suroeste de la Costa de Hermosillo y la región del Sahuaral, entre las calles 4 y 28, y algunos focos distribuidos alrededor de la calle 13, de este a oeste. Se consideran dentro del índice de severidad alta, con un 29.5% de la superficie que corresponde a aproximadamente 44 765 ha; en 41 093 ha que corresponden a 27.1% de la superficie, estas se consideran con índice de riesgo moderado en donde la incidencia de la enfermedad se esperaría sea menos severa, se encuentran las áreas que comprenden la región del centro entre las calles 0 y 28 sur, además de una región comprendida al sureste dentro de la región del Sahuaral. Los suelos con índice de severidad baja se localizaron del centro de la región hacia el norte comprendiendo una superficie total de 65 962 ha (43.4%).
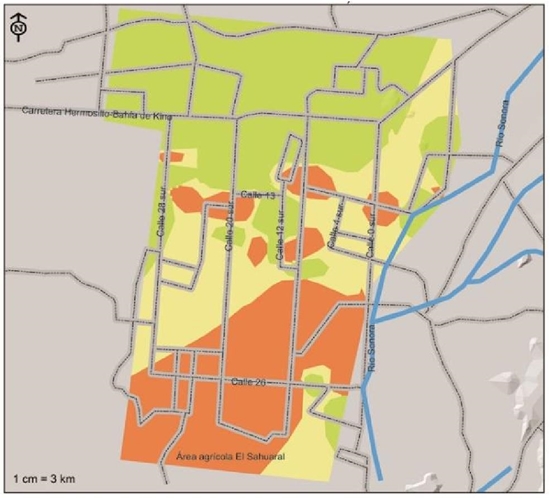
Figura 6 Índices de severidad de presencia de Fusarium solani, patógeno asociado a las pudriciones de raíz del garbanzo aislado e identificado en la Costa de Hermosillo, Sonora.
Rhizoctonia solani, de acuerdo a los índices de riesgo mostrados en la Figura 7, este patógeno se localiza con un alto índice de riesgo al suroeste de la región por la calle 26 entre las calles 12 y 4, y al noroeste por la carretera a Bahía de Kino entre las calles 20 y 36 norte, correspondiendo esta distribución a una superficie de 34 106 ha que equivale a 22.5% del total. Con índice de riesgo moderado, se detectó el 25.1% de los suelos que corresponden a una superficie de 38 129 ha localizadas básicamente al sur de la región hasta adentrarse en la región del Sahuaral. Se detectó un bajo índice de riesgo en suelos de una franja que va del poniente en la calle 28 hasta el noreste de la calle 4 pasando por el centro en una superficie mayor de 79 585 ha que representa el 52.4%.
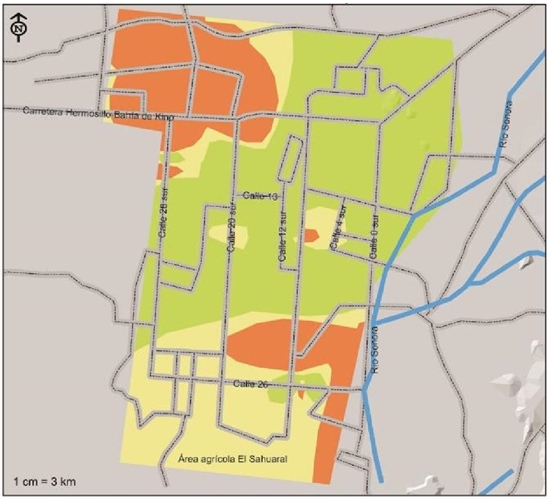
Figura 7 Índices de severidad de presencia de Rhizoctonia solani, patógeno asociado a las pudriciones de raíz del garbanzo aislado e identificado en la Costa de Hermosillo, Sonora.
Las áreas con presencia de solo uno o máximo dos especies de hongos asociados a la fusariosis vascular y pudriciones de raíz, serían las más adecuadas para sembrar garbanzo considerando: la especie presente, la resistencia de la variedad a utilizar, y la oportunidad y costo de un control cultural. La nutrición de la planta determina en gran medida su resistencia o susceptibilidad a las enfermedades, su estructura histológica y morfológica o propiedades, y la virulencia o habilidad de los patógenos para sobrevivir (Huber y Haneklaus, 2007); así, una adecuada nutrición para el cultivo puede contribuir a disminuir el riesgo de daño por enfermedades. En las áreas con mayor número y densidad de patógenos causantes de las pudriciones de la raíz, la rotación de cultivos, preferentemente con cereales que no sean afectados por estos, por tres o cuatro años sería una práctica adecuada. Al considerar que uno de los patógenos de mayor presencia fue M. phaseolina, cuyo daño es por condiciones de sequía y temperaturas altas (Gupta y Sharma, 2015; Mayek et al., 2002), se deben considerar fechas de siembra o variedades con ciclo de cultivo corto que eviten la coincidencia de la etapa reproductiva del cultivo con la presencia de esos estreses ambientales. En la actualidad, en esta región la mayoría de las siembras se realizan en el mes de enero con alta probabilidad de ocurrencia de temperaturas superiores a 30 °C desde finales de marzo.
Conclusiones
Durante el ciclo otoño-invierno 2012-13, en distintas proporciones y combinaciones, se identificaron a cuatro especies de patógenos causando daño en la raíz del garbanzo en la Costa de Hermosillo, en orden de abundancia estas fueron: Macrophomina phaseolina, Fusarium oxysporum f. sp. ciceris, Fusarium solani y Rhizoctonia solani, las dos últimas en la misma proporción.
En el 74.3% de la superficie agrícola de la Costa de Hermosillo, que corresponde a 112 866 ha, se aislaron e identificaron a las especies Macrophomina phaseolina y Fusarium oxysporum f. sp. ciceris, con potencial patogénico de riesgo de medio a alto de causar daño al cultivo de garbanzo.
El patógeno de mayor distribución potencial en cuanto a superficie en la región de la Costa de Hermosillo fue Macrophomina phaseolina en 105 572 hectáreas que representan el 69.5% de la superficie del área de estudio.











 texto em
texto em