Introducción
El melón Cantaloupe es un fruto apreciado por su aroma y sabor los cuales son determinantes para la calidad sensorial y comercial del producto (Kourkoutas et al., 2006). El aroma y sabor del melón son atribuidos a su contenido de compuestos aromáticos volátiles en la pulpa, que incluyen ésteres y alcoholes (Aubert et al., 2005), aunque en algunas variedades de melón se han determinado hasta 240 compuestos por medio de técnicas de cromatografía de gases (Kourkoutas et al., 2006).
Entre los compuestos aromáticos más abundantes en este fruto se encuentran ésteres como el etilbutanoato, etilcaproato, y 3-hexil 2-butanoato, y en menor medida derivados azufrados, aldehídos y alcoholes (Obando-Ulloa et al., 2010). Por otro lado, el melón Cantaloupe tiene una vida de anaquel corta de 10-15 días (Suslow et al., 2002), por lo cual es requerida la evaluación de métodos de conservación que contribuyan a mantener la calidad sensorial de este fruto durante periodos de almacenamiento más largos, como lo es la aplicación de cubiertas o películas.
Las cubiertas (soluciones y emulsiones) a base de polímeros comestibles como polisacáridos, proteínas o lípidos han sido aplicadas sobre diversos productos vegetales (Bonilla et al., 2013). La aplicación de películas sobre el melón tiene el potencial de reducir la pérdida de humedad (Reyes et al., 2016), firmeza (Reyes et al., 2017), y tasa de respiración del producto (Reyes et al., 2016). Asimismo, las cubiertas comestibles protegen al producto contra daños mecánicos, oxidativos y microbiológicos, además mejoran la apariencia y la pérdida de aroma del fruto (Genskowsky et al., 2015).
El mayor beneficio del uso de películas y cubiertas es que pueden ser consumidos junto con el producto alimenticio en que están aplicadas, pudiendo dichas películas ser enriquecidas con compuestos que aporten benéficos para la salud o que mejoren las propiedades sensoriales del alimento cubierto (Perdones et al., 2012). Algunos polisacáridos utilizados para preparación de cubiertas comestibles son el alginato de sodio, carragenina y la carboximetilcelulosa (Hamzah et al., 2013; Tavassoli-Kafrani et al., 2016).
La hidroxipropilmetilcelulosa (HPMC) es un polímero derivado de la celulosa usado en la formulación de películas, el cual ha sido probado en diversos vegetales, resultando en menor daño por frío, conservación de la firmeza y menor pérdida de peso en dichos productos (Reyes et al., 2017). Además, las películas comestibles retrasan el proceso de maduración de las frutas (Reyes et al., 2016) por lo que, si las cubiertas pueden disminuir la actividad de las enzimas pécticas, como la pectinmetilesterasa, el fruto mantendrá por más tiempo la firmeza de sus tejidos.
El objetivo de este trabajo fue evaluar el afecto de la aplicación de una película de HPMC-Parafina sobre la concentración de compuestos aromáticos y la actividad de la PME del melón Cantaloupe.
Materiales y métodos
Muestras experimentales
Se utilizaron frutos de melón Cantaloupe (Cucumis melo L. var. reticulates) recolectados en Ceballos, Durango (coordenadas geográficas latitud 26.526 y longitud -104.129) en etapa pre climatérica (25 a 27 días después de polinización) de acuerdo con el método publicado por Nishiyama et al. (2007). Los frutos se seleccionaron en estado de madurez tres cuartos desprendido, de tamaño y dimensiones similares (frutos de 1.2 a 1.5 kg libres de daños físicos). El proceso de producción fue riego por goteo.
Materiales y reactivos
La HPMC (C56H108O30) fue donada por Colorcon (México). Los siguientes reactivos fueron adquiridos de Sigma-Aldrich (St Louis MI, EUA) Metabisulfito de sodio, sorbato de potasio, monoestearato de propilenglicol, D-metilo de ácido poligalacturónico, Tris, sulfato de amonio, dodecil sulfato de sodio, Triton X-100, azul de bromotimol y estándares de etilbutirato, etilcaproato, butilacetato, benzilalcohol y metilbutanol. Se empleó parafina grado reactivo Analítika (Monterrey, Nuevo León, México).
Tratamientos
Los melones recolectados se seleccionaron libres de daños físicos y contaminación microbiana aparente. Se lavaron con agua clorada a 200 ppm de hipoclorito de sodio, y distribuidos aleatoriamente en dos lotes: tratamiento control (sin aplicación de película), y película (frutos cubiertos con la película HPMC-parafina). La preparación y aplicación de la película de HPMC-parafina se describió previamente en Meza et al. (2013). Todos los frutos se almacenaron luego en un frigorífico a 8 ±2 ºC con humedad relativa de 80 ±4% durante 20 días. Posteriormente, los melones se analizaron cada cuatro días a lo largo del periodo de estudio (0, 4, 8, 12, 16 y 20 días). Los análisis practicados fueron concentración de etilbutirato, etilcaproato, butilacetato, benzilalcohol, metilbutanol y la actividad de la pectinmetilesterasa (PME) llevados a cabo por triplicado. Los tratamientos (control y película) se repitieron ocho veces y cada repetición contenía 24 melones.
Análisis de compuestos volátiles
El análisis se desarrolló con el método propuesto por Aubert et al. (2005) con algunas modificaciones. Una muestra compuesta de 125 g de melón de cada una de las repeticiones de los tratamientos se mezcló con 125 ml de galato de n-propilo (10 mM) y triturada en una mezcladora por 2 min, posteriormente, homogeneizada por un min con el ultraturrax. La mezcla se centrifugó (4 500 rpm, 20 min, 4 ºC) y se recolectó el sobrenadante.
Para llevar a cabo las pruebas de porcentaje de recuperación, se prepararon soluciones de 5 estándares de compuestos volátiles presentes en el melón; estas soluciones se prepararon a 40 ppm en diclorometano. Posteriormente, 150 ml de la solución de estándares (conteniendo etilbutirato, etilcaproato, butilacetato, benzilalcohol y metilbutanol) o el extracto obtenido de la pulpa de melón, fueron extraídos tres veces con 50 ml de diclorometano (3 x 15 min) bajo agitación constante a una temperatura de 4 ºC. Posteriormente, la mezcla se concentró hasta 8 ml usando un equipo kuderna-danish a 70 ºC. Los 8 mL se colocaron en un microkuderna y concentrados hasta 1 mL a 45 ºC. El concentrado se inyectó en un cromatógrafo de gases HP 6820 con detector de ionización en flama y una columna capilar DB-5 de 30 x 0.25 x 0.25 (Supelco, PA, EUA).
Las condiciones del cromatógrafo fueron de 250 ºC en el inyector, 250 ºC en el detector; la columna se sometió a un programa de 35 ºC de temperatura inicial con rampa de 5 ºC por min hasta alcanzar 150 ºC, la temperatura final se mantuvo por 10 min. Las lecturas del cromatógrafo se registraron y analizaron con el software Agilente Cerity NDS y comparadas con una curva de calibración de estándar de los compuestos mencionados. Los resultados se reportaron como mg kg-1 de fruto fresco.
Preparación de la muestra para la actividad de pectinmetilesterasa
El análisis se llevó a cabo con el método descrito por Lamikanra y Watson (2004) con algunas modificaciones. Se utilizaron rebanadas del centro de la fruta (ecuador) de medidas aproximadas de 80 x 30 x 2 mm de cada tratamiento. A 40 g de rebanadas de melón se les agregó 80 mL de buffer de Tris (pH 7.8, 0.05 M) y se homogenizó en una mezcladora por 2 min para después ser centrifugada a 4 ºC y 4 800 G durante 30 min. El sobrenadante se mezcló con sulfato de amonio de manera de obtener una concentración del mismo de 60% y se colocó en un congelador a -18 ºC por 1 h. La mezcla fue entonces centrifugada a 4 ºC y 4 800 G por 1 h. El sobrenadante fue descartado y los residuos se homogenizaron en 4 ml de Tris por 1 min. La mezcla se centrifugó a 4 ºC y 4 800 G por 1.5 h. El sobrenadante fue la muestra para ensayo de la actividad enzimática.
Actividad de la pectinmetilesterasa
La prueba se realizó con una modificación del método propuesto por Lamikanra and Watson (2003). Una solución de éster D-metilo de ácido poligalacturónico (0.1%) se preparó en una solución de NaCl 0.4 M. Se usó como indicador azul de bromotimol 0.01% en un buffer de fosfato de potasio. Antes de cada reacción, la solución péctica (2.5 mL) era ajustada a un pH de 7.5 con NaOH 2 M. A la solución péctica se le adicionó el azul de bromotimol (0.2 mL), 0.1 mL del extracto enzimático y se agitó en vórtex. La muestra se leyó a una absorbancia a 620 nm en 20 y 80 s para determinar la velocidad de la reacción. Los resultados se reportaron en actividad enzimática relativa donde 100% de actividad era de muestras de melón antes de tratamientos.
Diseño experimental y análisis estadístico
Se usó un diseño factorial con dos factores: tiempo de almacenamiento (0, 4, 8, 12, 16 y 20 días) y aplicación de película (sin y con película), y se llevaron a cabo ocho repeticiones por tratamiento. Los resultados de las variables evaluadas se analizaron mediante análisis de varianza. La diferencia entre medias de tratamientos se realizó por la prueba de comparación múltiple de diferencia mínima significativa de Fisher (DMS de Fisher) con un nivel de significancia de 0.05, usando el programa estadístico SAS versión 8 (SAS Institute Inc., 2005).
Resultados y discusión
Compuestos volátiles
Se presentaron diferencias significativas en las concentraciones de etilbutirato, etilcaproato y butilacetato entre los melones sin y con película (p≤ 0.05). Se observó que, en los melones con película, las concentraciones de etilbutirato y etilcaproato presentaron un aumento súbito a los 4 días de almacenamiento (Figura 1 y 2), mientras tanto la cantidad de butilacetato tuvo aumento repentino hasta los 8 días (Figura 3).
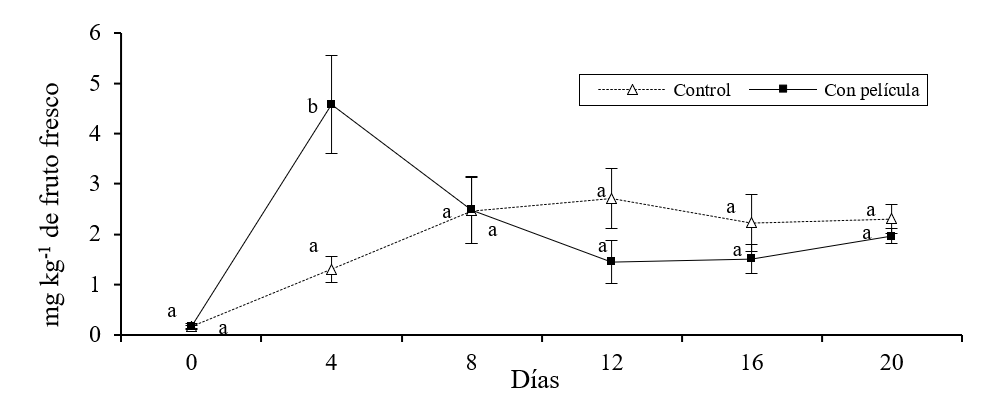
Figura 1 Concentración de etilbutirato (mg kg-1 de solido fresco) en melones con y sin película almacenados durante 20 días en refrigeración. Barras sobre la media de los resultados representa ±desviación estándar (n= 4). Diferentes literales indican diferencia significativa, por LSD de Fisher (p≤ 0.05), entre melones con y sin película durante el tiempo de almacenamiento.
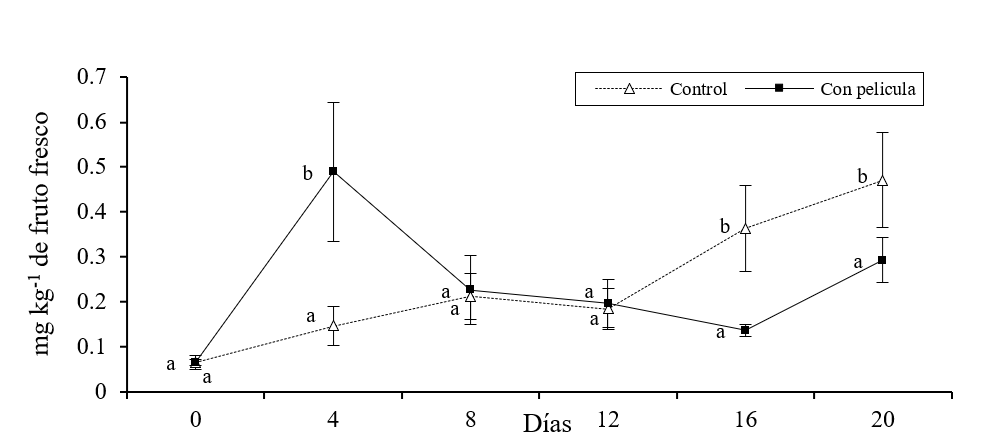
Figura 2 Concentración de etilcaproato (mg kg-1 de solido fresco) en melones con y sin película almacenados durante 20 días en refrigeración. Barras sobre la media de los resultados representa ±desviación estándar (n= 8). Diferentes literales indican diferencia significativa, por LSD de Fisher (p≤ 0.05), entre melones con y sin película durante el tiempo de almacenamiento.
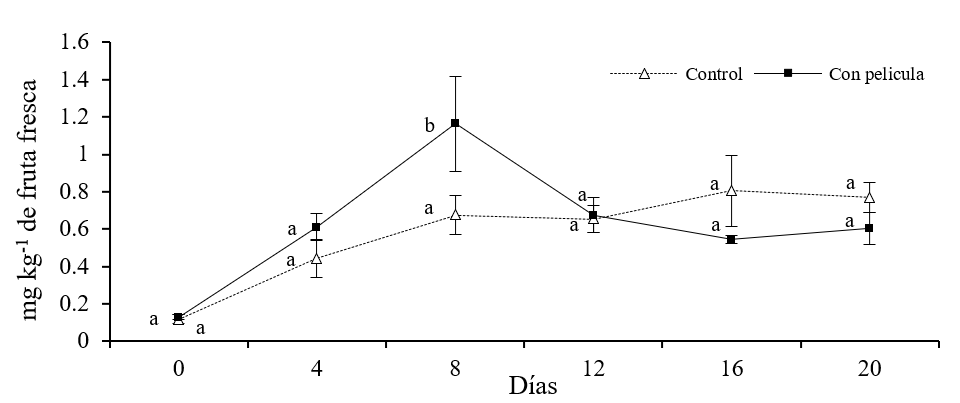
Figura 3 Concentración de butilacetato (mg kg-1 de solido fresco) en melones con y sin película almacenados durante 20 días en refrigeración. Barras sobre la media de los resultados representa ±desviación estándar (n= 8). Diferentes literales indican diferencia significativa, por LSD de Fisher (p≤ 0.05), entre melones con y sin película durante el tiempo de almacenamiento.
La concentración de estos compuestos fue significativamente menor (p≤ 0.05) en los frutos control durante los periodos de tiempo mencionados. Asimismo, los melones sin cubierta presentaron un aumento gradual en la concentración de los ésteres analizados a lo largo del periodo de estudio. Además, los resultados obtenidos en el estudio mostraron que la concentración de los compuestos alcohólicos monitoreados no tuvo cambios (p> 0.05) entre los diferentes tratamientos durante el almacenamiento. Resultados similares se han encontrado al cubrir fresas con una película de quitosán (Almenar et al., 2009) y mango con carnauba (Dang et al., 2008), los autores citados consiguieron aumentar la concentración de aromas con el uso de estas cubiertas.
Diversos estudios han demostrado que la producción o síntesis de compuestos aromáticos en frutas y vegetales (especialmente de tipo éster) están directamente relacionados con la madurez y la presencia y concentración de etileno (Günther et al., 2015; Li et al., 2016), por lo que el rápido aumento observado en la cantidad de los compuestos ésteres puede estar relacionado con la concentración relativamente alta de etileno encontrada en el interior de los melones cubiertos con la película de HPMC-parafina, reportada con anterioridad (Meza et al., 2013). La presencia de esta hormona activa enzimas como lipasas, alcohol aciltransferasa y alcohol acetiltransferasa, las cuales promueven una mayor síntesis de compuestos ésteres responsables de aromas y sabores en frutas y vegetales (Hui et al., 2010. En contraste, se observó que las concentraciones de alcoholes, presentes en manzana, no fueron afectados por la inhibición de síntesis de etileno (Dandekar et al., 2004).
Actividad de la pectinmetilesterasa (PME)
La actividad de PME fue menor en los melones con cubierta durante el periodo de 8 a 16 días de almacenamiento (p≤ 0.05) (Figura 4). Los frutos con película presentaron una actividad relativa de 25% (donde 100% es la actividad relativa de los frutos sin tratamiento al tiempo inicial) a los 8 días de almacenamiento; mientras que las muestras sin película tuvieron actividad relativa mayor a la inicial de hasta ~122% en el periodo de 12-16 días. Ha sido reportado que el uso de cubiertas comestibles puede disminuir la actividad enzimática de los vegetales al promover la formación de atmosferas modificadas internas (Meza et al., 2013), lo cual puede retardar su proceso de maduración (Reyes et al., 2016).
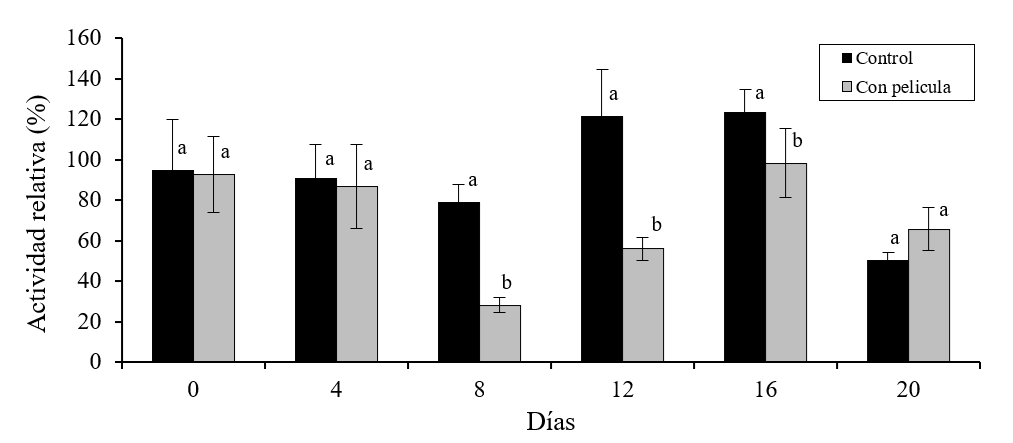
Figura 4 Actividad relativa de la pectinmetilesterasa en pulpa de melón tratado con una cubierta polimérica y almacenado por 20 días en refrigeración. Barras sobre la media de los resultados representa ±desviación estándar (n= 8). Diferentes literales indican diferencia significativa, por LSD de Fisher (p≤ 0.05), entre melones con y sin película durante el tiempo de almacenamiento.
La función de la PME es iniciar el cambio y degradación estructural de las pectinas, lo que afectará directamente en la disminución de la firmeza del vegetal (Giovane et al., 2004). La síntesis de aromas y los cambios de textura durante la maduración y senescencia de las frutas tiene una cierta correlación debido a los cambios en la estructura celular (Dos-Santos et al., 2013).
Algunas investigaciones concuerdan que los aromas pueden estar atrapados o ligados en la estructura celular formado por polisacáridos, principalmente pectinas (Bezman et al., 2003; Savary et al., 2006; Harker y Johnston, 2008), y probablemente cambios estructurales puedan afectar la liberación o acumulación de aromas en el tejido del fruto, por lo que frutos con menores cambios estructurales, cambios promovidos por enzimas como la PME, podrían contener mayor cantidad de compuestos aromáticos.
Conclusiones
La aplicación de la película a base de HPMC-parafina aceleró la síntesis de compuestos ésteres en melón durante etapas tempranas de almacenamiento en refrigeración. Asimismo, esta película disminuyó la actividad de la PME, lo cual puede disminuir cambios estructurales en los tejidos del fruto y consecuentemente mejorar la retención de compuestos volátiles.











 texto en
texto en 


