Introducción
México ocupa el décimo lugar como productor de sandía [Citrullus lanatus (Thunb.) Matsum. & Nakai] a nivel mundial (FAOSTAT, 2016). No obstante, el potencial productivo de México se ve disminuido, debido principalmente a la presencia de enfermedades transmitidas a través del suelo (ETTS) como Fusarium oxysporum f. sp. niveum, nematodos y el virus de la mancha necrótica del melón (MNSV). Este último ha causado graves pérdidas en la producción de sandía, debido a que ocasiona la muerte repentina de la planta antes o durante la cosecha, incrementando su patogenicidad cuando se asocia con el hongo vector Olpidium bornovanus (Guirado et al., 2009).
Este virus ataca cultivos de pepino (Cucumis sativus L.), melón (Cucumis melo L.) y sandía, en países como España, Túnez, Brasil, Guatemala, Honduras, Panamá, Estados Unidos y en México en los estados de Sinaloa y Colima (Herrera‐Vásquez et al., 2010). Para incrementar la producción y hacer más rentables los cultivos, en México se ha optado por utilizar plantas injertadas para la producción de cultivos como melón, tomate (Solanum lycopersicum L.) y pimiento (Capsicum annuum L.) (García-Rodríguez, 2010; Ricárdez-Salinas et al., 2010; Osuna-Ávila et al., 2012). En sandía se reportan incrementos en la producción de hasta 115% cuando se utilizan plantas injertadas en suelos infestados con MNSV (Huitrón-Ramírez et al., 2009).
A pesar de las ventajas conocidas sobre el uso de plantas injertadas, también existen inconvenientes, algunas combinaciones de variedades y portainjertos pueden provocar modificaciones en la textura, el color, el tamaño del fruto, el contenido de azúcares, así como una mayor incidencia de fisiopatías (Davis y Perkins-Veazie, 2005; Crinò et al., 2007; King et al., 2010).
Las sandías suelen ser injertadas sobre híbridos interespecíficos de Cucurbita maxima Duchesne x Cucurbita moschata Duchesne, debido a su vigorosa raíz y a su resistencia a ETTS; sin embargo, varios autores han reportado que los frutos de sandía de plantas injertadas con estos portainjertos tienden a poseer un pH menor, mayor firmeza de pulpa, variación en tamaño y un sabor insípido (Colla et al., 2006; Davis et al., 2008; Kyriacou et al., 2016). Por esto, algunos productores manifiestan cierto rechazo a adoptar esta técnica, debido principalmente a los parámetros de calidad con los que el fruto debe cumplir para poder ser exportado a Estados Unidos de América.
En sandía se busca uniformidad en el tamaño, con poca variación y de consistencia firme. El contenido de azucares debe ser superior a 8%, y se considera de muy buena calidad cuando supera 10% (USDA, 2006). Los portainjertos de Citrullus lanatus var citroides (sandía silvestre) han demostrado ser resistentes a los nematodos (Meloidogyne spp.) y a la mayoría de las ETTS (Thies et al., 2010; Thies et al., 2015), sin afectar los parámetros de calidad del fruto (Huitrón-Ramírez et al., 2007); no obstante, se desconoce si son resistente al MNSV.
Por estos motivos, es esencial disponer de portainjertos para sandía que mantengan los estándares de calidad habituales en el mercado y que brinden resistencia a ETTS. El objetivo de esta investigación fue evaluar el rendimiento y la calidad de sandías injertadas sobre portainjertos comerciales de híbridos interespecíficos y compararlos con portainjertos de sandía silvestre en suelos infestados de forma natural con MNSV asociado con Olpidium bornovanus.
Materiales y métodos
Los experimentos se realizaron en el rancho “Las Carmelitas”, localizado en el estado de Colima, México (19.16° latitud norte, 103.38° longitud oeste) en una parcela a campo abierto. El experimento 1 se realizó en la temporada otoño-invierno 2011-2012 y el experimento 2 se realizó en la temporada otoño-invierno 2012-2013. Para ambos experimentos se consultaron las temperaturas máximas y mínimas (Figura 1) de la región con la ayuda de la red de estaciones del INIFAP (INIFAP, 2013).
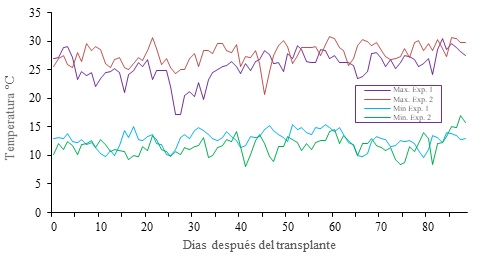
Figura 1 Temperaturas máximas y mínimas a lo largo del cultivo para el experimento 1 (2011-2012) y experimento 2 (2012-2013).
El suelo de las parcelas experimentadas estaba infestado de forma natural con el virus de la mancha necrótica del melón (MNSV) asociado con el hongo vector Olpidium bornovanus, el cual fue identificado en el Laboratorio de Fitopatología de la Universidad de Almería, España previo a la realización del experimento, y corroborado posteriormente por el laboratorio de Fitopatología del Centro Universitario de Ciencias Biológicas y Agropecuarias (CUCBA) de la Universidad de Guadalajara. La textura del suelo es franco arenoso con 3.44% de materia orgánica, pH de 5.2, y conductividad eléctrica (CE) en el extracto de saturación de 0.9 dS m-1. En los dos experimentos se realizaron aplicaciones de fertilizante de fondo 0N-34.8P-72.8K (superfosfato y sulfato de potasio). Adicionalmente, a lo largo del ciclo se agregó, mediante el sistema de riego, 187N-14.2P-176K.
Material vegetal. Para el experimento 1 y experimento 2 se utilizó la variedad de sandía (Citrullus lanatus) triploide “Mielheart” del tipo mini, y como polinizador la sandía diploide “Minipool”. Los híbridos interespecíficos de Cucurbita maxima×Cucurbita moschata “RS-841” y “Ercole”, adicionalmente se utilizaron los portainjertos de sandías silvestres (Citrullus lanatus var citroides) “Robusta”, “RS0272” y “RS1833” para el experimento 1, generándose así un total de cinco tratamientos. En el experimento 2 no fue posible la utilización de los portainjertos de sandía silvestre “RS0272” y “RS1833” debido a su desaparición del mercado, por lo que únicamente se utilizaron los portainjertos “RS-841”, “Ercole” y “Robusta”. En ambos experimentos se utilizó el portainjertos “RS-841” como control, debido a que este portainjerto se utiliza en la región para producir sandías de la variedad Mielheart. Las plántulas se injertaron por el método de aproximación utilizando el método descrito por Lee (1994). El sustrato que se utilizó para germinar y desarrollar la planta fue una mezcla de perlita y peat-moss a una proporción de 2:1 (v/v).
Manejo del cultivo. En los dos experimentos las plantas injertadas de sandías se plantaron a una distancia de 0.7 m sobre la cama y a 3.6 m entre camas. Las camas de plantación se cubrieron con plástico de polietileno plata/negro para acolchar. El riego fue por goteo, para ello se utilizó una cintilla con separación de goteros de 45 cm y un gasto de 1.2 L h-1 (Rain Bird; California, Estados Unidos de América). Para cada tratamiento se hicieron cuatro repeticiones, para un total de 20 parcelas experimentales para el experimento 1, y 12 para el experimento 2. Cada unidad experimental se conformó por 5 camas de cultivo, con un ancho de 18 m y una longitud de filas de 10 m, dando un total de 180 m2 por parcela.
El trasplante se realizó entre 14 y 17 días después del injerto, con una distribución de 2:1 entre las sandías triploides/diploides sobre la misma fila (Huitrón-Ramírez et al., 2009). El control de maleza se hizo de forma manual y se utilizaron productos químicos para el control de plagas (imidacloprid, abamectina, cipermetrina) y enfermedades (clorotalonil, boscalid+ pyraclostrobina). Para una adecuada polinización se utilizaron abejas (Apis mellifera), las cuales se introdujeron a la parcela 30 días después del trasplante, utilizando 4 colmenas ha-1.
Determinación de calidad y rendimiento. La cosecha la realizó personal especializado, el cual cosechó únicamente frutas con estándares de calidad aceptables para el mercado. Se realizó un conteo de todos los frutos comercializables de la variedad Mielheart, de los cuales se seleccionaron cinco frutos por cada parcela experimental, por corte (cuatro cortes en cada experimento); posteriormente, se pesaron en una báscula (Mettler, Toledo Wildcat 3009; DF, México) para estimar el rendimiento y la producción total. Con el fin de medir los atributos de calidad, se hicieron determinaciones en tres frutos representativos (por cosecha), a los cuales se les midió el contenido total de sólidos solubles, firmeza, calibre, forma y grosor de corteza. Los sólidos solubles se midieron a partir del jugo de la fruta con un refractómetro digital (Atago Pal-1; Tokio, Japón).
Se usó un penetrómetro (Bertuzzi FT-011; Milán, Italia) para determinar la firmeza de la pulpa del fruto, para esto se partió el fruto por la mitad, y se hicieron tres penetraciones, una en el centro del fruto y dos más en la zona perimetral de la pulpa, aproximadamente a 2 cm de la corteza del fruto, obteniendo tres lecturas, de las cuales se calculó el promedio. Se utilizó una cinta métrica para determinar el perímetro ecuatorial y longitudinal; para la forma se dividió el perímetro ecuatorial entre el perímetro longitudinal y por último se midió el grosor de corteza con un vernier digital. Al final del ciclo se estimó un porcentaje de supervivencia de las plantas para valorar la resistencia de los portainjertos al MNSV.
Análisis estadístico. Se utilizó un diseño de bloques al azar. En ambos experimentos cada bloque contó con un total de 72 plantas (48 triploides y 24 diploides). Los datos no normales fueron transformados por diversos procedimientos sugeridos por la transformación Box-Cox, las medias se compararon con la prueba LSD de Fisher. El análisis estadístico se realizó con el programa informático Minitab 16 (Minitab Inc., 2010).
Resultados y discusión
En los experimentos 1 y 2, la mayoría de las plantas injertadas sobre los portainjertos de las sandías silvestres (C. lanatus cv. citroides) se marchitaron después de la primera cosecha, ocasionando la muerte de éstas (Figura 2). Los síntomas observados en las plantas injertadas sobre las sandías silvestres corresponden a una infección ocasionada por MNSV, los cuales han sido descritos y reportados para sandía y otras cucurbitáceas (Komuro, 1972; Moya et al., 2009). Más de 80% de estas plantas presentaron necrosis en los tallos y numerosas manchas pequeñas necróticas por todo el follaje.
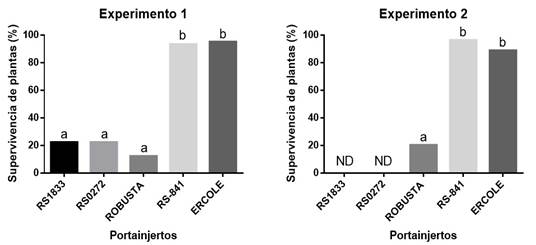
Figura 2 Taza de supervivencia (%) de plantas de sandía injertadas sobre portainjertos de híbridos interespecíficos de Cucurbita máxima x Cucurbita moschata (“RS-841” y “Ercole”) y portainjertos de sandía silvestre (“RS1833”, “RS0272” y “Robusta”) en suelos infestados con MNSV asociado con O. bornovanus.
La presencia de Olpidium bornovanus se confirmó por medio de observación microscópica. Las infecciones ocasionadas por MNSV pueden ser asintomáticas en plantas jóvenes, así que los síntomas pueden aparecer repentinamente durante la etapa de maduración del fruto y puede causar daños que llegan a 100% de las plantas cuando existe la presencia del hongo vector O. bornovanus (Kwak et al., 2015). Los portainjertos de C. lanatus cv. citroides han sido utilizados de forma comercial debido a su alta compatibilidad con variedades de sandías, altos rendimientos, resistencia a nematodos (Meloidogyne spp.) y algunos patógenos como Fusarium oxysporum f. sp. niveum (Huitrón-Ramírez et al., 2007; Thies et al., 2010; Thies et al., 2015), pero son muy susceptibles al MNSV.
Rendimiento. Se observó diferencia estadística en ambos experimentos en el peso medio del fruto (PUF) entre los portainjertos de híbridos interespecíficos de C. maxima×C. moschata y los portainjertos de sandía silvestre (Cuadro 1). El PMF de sandías normalmente incrementa cuando se injerta sobre portainjertos de sandía silvestre en suelos sin la presencia del MNSV y su hongo vector O. bornovanus (Rodríguez et al., 2008). Por su parte, Bekhradi et al. (2011), observaron que el peso de los frutos de sandía no se ve afectado por el tipo de portainjertos que se use.
Cuadro 1 Parámetros de rendimiento en sandías injertadas con diferentes portainjertos.
| Tratamientos | Frutos por planta | PMF (kg) | Rendimiento (t ha-1) |
| Experimento 1 (2011-2012) | |||
| RS1833 | 1.6 a | 1.4 a | 12.1 a |
| RS0272 | 1.7 a | 1.7 a | 13.5 a |
| Robusta | 1.9 a | 1.4 a | 13.5 a |
| RS-841 | 5.1 b | 2.4 b | 49.5 b |
| Ercole | 5.2 b | 2.3 b | 51.9 b |
| Significancia | *** | *** | *** |
| Experimento 2 (2012-2013) | |||
| Robusta | 0.9 a | 2.4 a | 9 a |
| RS-841 | 3.8 b | 3.4 b | 52 b |
| Ercole | 3.7 b | 3.4 b | 50 b |
| Significancia | *** | *** | *** |
PMF= peso medio del fruto; ***= significativo a p≤ 0.001. Letras diferentes indican diferencia significativa a p< 0.05.
De igual forma, Alan et al. (2007) no reporta diferencia en el PMF en un cultivo a campo abierto en el que comparó tres tipos de portainjertos y un control sin injertar. No obstante, la presencia de patógenos como el MNSV puede reducir el peso y tamaño del fruto en cultivares no resistentes (Huitrón-Ramírez et al., 2009). En los dos experimentos de este estudio, los portainjertos de sandía silvestre produjeron menor cantidad de frutos, con diferencia estadística en comparación con los portainjertos de los híbridos interespecíficos.
Algunos autores han atribuido un mayor desarrollo de los frutos de sandía al vigoroso sistema radical de algunos portainjertos, como es el caso de los portainjertos de C. maxima×C. moschata, porque estos absorben agua y nutrientes de forma más eficiente e incrementan la tolerancia de las plantas injertadas a factores bióticos y abióticos (Rouphael et al., 2008; Rouphael et al., 2012; Borgognone et al., 2013). Se pudo observar en este estudio, que el rendimiento de las plantas injertadas sobre “RS-841” y “Ercole” sobrepasó a las plantas injertadas sobre sandía silvestre por 430% en el experimento 1 y por 578% en el experimento 2.
Las plantas injertadas en los portainjertos de sandía silvestre comenzaron a marchitarse unos días antes de la primera cosecha en ambos experimentos, lo que redujo el desarrollo del fruto. Mientras que las plantas injertadas sobre “RS-841” y “Ercole” permanecieron sanas durante el desarrollo del fruto y la etapa de maduración; estos portainjertos permitieron al fruto lograr un estado óptimo de maduración (Figura 3). Las plantas infestadas con MNSV suelen sufrir un drástico descenso en el rendimiento en comparación con las plantas injertadas sobre híbridos interespecíficos de C. maxima×C. moschata (Huitrón-Ramírez et al., 2009). De igual forma en este estudio las plantas injertadas sobre sandías silvestres fueron de un rendimiento menor que las plantas injertadas sobre “RS-841” y “Ercole”.

Figura 3 Desarrollo de plantas de sandía injertadas en suelos infestados con MNSV. Plantas de sandías injertadas sobre “Robusta” (C. lanatus cv. citroides) antes (A) y durante la maduración del fruto afectado por el MNSV (B). Plantas de sandía injertadas sobre “RS-841” (C. maxima×C. moschata) antes (C) y durante la maduración del fruto (D).
Calidad del fruto. En el experimento 1 y 2, se detectaron diferencias estadísticas en la firmeza de la pulpa del fruto (Cuadro 2) entre los tratamientos con portainjertos de híbridos interespecíficos y las sandías silvestres. La utilización de distintos portainjertos puede generar variabilidad en la firmeza del fruto (Bruton et al., 2009). En la mayoría de los casos, la firmeza del fruto beneficia a los productores de sandía, ya que los frutos con mayor firmeza incrementan su vida de anaquel. Adicionalmente, el contenido de sólidos solubles (SS) es uno de los aspectos más importantes en la calidad del fruto, debido a que la presencia de azúcares es responsable del dulzor del fruto (Sánchez-Rodríguez et al., 2012).
Cuadro 2 Parámetros de calidad en sandía injertada.
| Tratamientos | Firmeza (kg) | SS (°Brix) | GC (mm) | PE (cm) | PL (cm) | Forma PE/PL |
| Experimento 1 (2011-2012) | ||||||
| RS1833 | 2.7 a | 9.8 a | 11 b | 46.7 a | 48.9 a | 0.98 |
| RS0272 | 2.8 a | 9.6 a | 10.6 b | 48.8 a | 50.7 a | 0.96 |
| Robusta | 2.7 a | 9.7 a | 10.7 b | 48.1 a | 49.4 a | 0.97 |
| RS-841 | 3.2 b | 10.3 b | 9.9 a | 52.7 b | 54.4 b | 0.97 |
| Ercole | 3.2 b | 9.9 a | 10.7 b | 52.2 b | 53.3 b | 0.98 |
| Significancia | ** | *** | *** | *** | *** | ns |
| Experimento 2 (2012-2013) | ||||||
| Robusta | 2.68 a | 9.7 a | 10.6 b | 48 a | 49.4 a | 0.96 |
| RS-841 | 3.16 b | 10.3 b | 9.9 a | 53 b | 54.3 b | 0.96 |
| Ercole | 3.14 b | 9.9 a | 10.7 b | 52 b | 53.3 b | 0.95 |
| Significancia | * | * | ** | *** | *** | ns |
SS= sólidos solubles; GC= grosor de corteza; PE= perímetro ecuatorial; PL= perímetro longitudinal. Los símbolos ns, *, **, ***= no significativo, significativo a p≤ 0.05, 0.01, 0.001, respectivamente.
El tratamiento con el portainjertos “RS-841” mostró el mayor contenido de SS en ambos experimentos, registrando diferencia significativa con respecto a los demás tratamientos, incluso con respecto al portainjertos “Ercole”. No obstante, la mayoría de los autores afirman que el contenido de SS no parece ser alterado por el uso de diferentes tipos de portainjertos (Rouphael et al., 2008; Han et al., 2009; Bekhradi et al., 2011; Miceli et al., 2016). La corteza de los frutos de “RS-841” fue significativamente más delgada en los dos experimentos.
Una corteza más gruesa puede estar asociada a una reducción en el contenido de pulpa para el consumidor. Mientras que las sandías con una corteza muy delgada son más susceptibles a sufrir daños mecánicos durante el empaque y transporte (Alexopoulos et al., 2007). Por esto, la preferencia en el grosor de corteza puede variar dependiendo del propósito para el que los frutos estén destinados. No se encontró variación en la forma del fruto en ninguno de los dos experimentos.
Es notable que los resultados previamente mencionados mostraron variación entre los dos experimentos estudiados. En el experimento 2, se observó una mayor mortalidad en el tratamiento con el portainjertos de “Robusta”, así como un incremento en la severidad de los síntomas del MNSV, con respecto al Experimento 1. Kido et al. (2008) indican que los síntomas del MNSV aumentan cuando la temperatura es inferior a 20 °C, y la propagación viral y diseminación incrementan a temperaturas superiores a 25 °C.
No obstante, bajo las condiciones en las que se establecieron los experimentos no era posible determinar si la oscilación en la temperatura era responsable por el incremento en la severidad de la infección del MNSV. En cambio, en las variables de calidad se pudo apreciar que el portainjertos “RS-841” mostró características superiores en comparación con los otros portainjertos. Özmen et al. (2015) observó un fenómeno similar cuando comparó distintos ciclos de sandías injertadas, estos autores mencionaron que el rendimiento no fue afectado por la variación estacional. No obstante, es bien conocido que los portainjertos pueden tener efectos sobre la calidad, aunque en la mayoría de los casos suele ser perjudicial, a excepción del tamaño del fruto (Lee, 1994).
Conclusiones
Los portainjertos de los híbridos interespecíficos son una excelente opción para la producción de sandía “Mielheart” en suelos infestados con el virus de la mancha necrótica del melón (MNSV) y su hongo vector Olpidium bornovanus. Adicionalmente, estos portainjertos producen frutos con estándares de calidad aceptables para el mercado de los Estados Unidos de América. Los portainjertos de sandías silvestres no deben ser utilizados en suelos infestados con el MNSV porque son muy susceptibles a este virus y pueden ocasionar pérdidas considerables en el rendimiento. No obstante, bajo otras condiciones, los portainjertos de sandías silvestres pueden ser muy útiles, debido a su alta resistencia a plagas como los nematodos y a otros patógenos que se presentan en el suelo. La calidad del fruto fue afectada cuando se utilizaron portainjertos de sandía silvestre en suelos infestados con MNSV.











 texto en
texto en 


