Introducción
La floricultura es una industria global en los países en vías de desarrollo y desarrollados; el volumen del comercio mundial se estima en un valor de más de 100 billones de dólares por año (African Bussiness Magazine, 2012). En México, la floricultura es una actividad de importancia económica, existiendo en el país alrededor de 2.2 mil hectáreas cultivadas de gladiolo (Escalante et al, 2006). Dicho cultivo es afectado por diferentes tipos de plagas y enfermedades, entre las principales enfermedades fúngicas, destaca la roya transversal, originada por el agente causal Uromyces transversalis (Thümen) G. Winter, misma que fue reportada oficialmente en México, en noviembre de 2004 (CESAVEM, 2005; Rodríguez et al, 2006).
En el Estado de México se siembran alrededor de 800 ha; sin embargo, el rendimiento y calidad de la flor son afectados por enfermedades como la "royatransversal" ocasionando pérdidas mayores a 90% de la producción (CESAVEM, 2005; Schubert et al, 2006). Para el manejo y control de esta enfermedad, en el Estado de México, se han aplicado diversas estrategias basadas principalmente en el uso de fungicidas químicos sintéticos, favoreciendo la aparición de hongos fitopatógenos resistentes, por lo que se requieren nuevos productos para el manejo de enfermedades (Vásquez et al, 2013).
La SAGARPA (2005); CESAVEM (2005); CESVMOR (2006), recomiendan el uso de fungicidas como Azoxystrobin®, Trifloxystrobin + Oxycarboxin®, Amistar® 50 y Epoxiconazol®, para controlar la enfermedad a partir de la detección del primer síntoma (pústula), teniendo mayor efectividad la aplicación el Oxycarboxin+Tebuconazole. En las últimas décadas, se han incrementado estudios dirigidos a implementar métodos biológicos con efecto potencial en el control de enfermedades, debido a la reciente tendencia
a utilizar alternativas menos perjudiciales al ambiente (Flores et al, 2013). Una estrategia innovadora para el manejo de plagas y enfermedades de plantas de importancia agrícola, es el control biológico, mediante microorganismos antagonistas al patógeno (Whipps, 2001; Harman, 2006).
Dentro del control biológico existe el empleo de enemigos naturales (introducidos o manipulados), cuyo conocimiento de su efectividad y de su mecanismo de acción es esencial para el manejo y el desarrollo de estrategias en la implementación de una agricultura sostenible (Torres et al, 2008). El uso de hongos antagonistas nativos adaptados a las condiciones de manejo del cultivo, puede dar mejores resultados en la reducción del ataque del patógeno, pero es necesario evaluarlos antes de su recomendación. Debido a lo anterior, la presente investigación tuvo como objetivo experimentar y evaluar la eficiencia antagónica en condiciones in vitro, de seis cepas de los hongos Cladosporium sp. (ClGl), Alternaria sp. (AltGl), Aspergillus sp. (AspGl) y Trichoderma sp. (TrZA, TrJi y TrPi), contra la roya transversal (Uromyces transversalis), así como evaluar el porcentaje de infección en cinco municipios (Villa Guerrero, Zumpahuacán, Malinalco, Jocotitlán e Ixtlahuaca) de la zona florícola del Estado de México, para establecer si la utilización de micoparásitos como controladores de enfermedades, constituye una alternativa eficaz para la sustitución del control químico sintético.
Materiales y métodos
Muestreo. En el periodo de julio a diciembre de 2013 se realizaron 15 muestreos de plantaciones comerciales de gladiolo con roya (Uromyces transversalis), distribuidos en cinco municipios que conforman parte de la zona florícola del Estado de México; Villa Guerrero, Zumpahuacán, Malinalco, Jocotitlán e Ixtlahuaca. El muestreo del cultivo llevo a cabo durante las etapas de floración, cosecha y postcosecha. De cada muestreo se colectaron 15 hojas al azar.
Evaluación de severidad. Se eligieron 12 hojas de plantas al azar de cada parcela muestreada, determinando la severidad de la enfermedad mediante una escala a nivel foliar adaptada de Núñez y Romero (1980) (Cuadro 1).
Cuadro 1 Escala de severidad para la evaluación del nivel de daño de Uromyces transversalis en hojas de gladiolo.

Nivel de daño. Se calculó empleando la fórmula: P= [Σ (n * v)/ cat. mayor * N] * 100, de Towsand y Heuberger (T y H); donde: p= °/o de infección; Σ= sumatoria; n= número de plantas por categoría; v= valor numérico de cada categoría; cat. mayor= categoría mayor; N= número de plantas por muestra.
Aislamiento e identificación de hongos antagonistas. De hojas infectadas por U. transversalis en gladiolo, Puccinia horiana en crisantemo, Phragmidium mucronatum en rosa, y de hojas de clavel y de chile manzano infectadas con Cladosporium sp, se identificaron bajo microscopio estereoscópico hongos antagonistas colocados sobre los hongos fitopatógenos de cada cultivo, empleando claves taxonómicas para hongos imperfectos (Barnett y Hunter, 1972) y fueron sembrados en medio de cultivo de papa-dextrosa-agar (PDA marca Bioxon) acidificado con ácido láctico 25% (pH de 5.5); los aislamientos se incubaron entre 5 -7 días a 26 °C ± 2 °C para la esporulación de los hongos. Debido a su fácil y rápido crecimiento, además de sus características de micoparasitar a otros hongos (Quiroz et al., 2008), se emplearon tres cepas de Trichoderma sp, aisladas de jitomate (TrJi), pino (TrPi) y otra de zacate con avena (TrZA).
Se tomó un disco de crecimiento de 5 mm de cada colonia con un sacabocado estéril y se transfirieron a cajas de Petri con PDA para obtener cultivos uniformes. Las cepas de los hongos antagonistas fueron preparadas bajo dos diluciones a partir de una caja de Petri colonizada, la cual se licuo y aforo en agua destilada a 600 y 300 mL. El licuado obtenido fue vertido en garrafas de plástico con capacidad de 750 mL, a las que se les agregó Aceite micro-refinado de aceite de soya (EPA) y surfactante penetrante en solución acuosa (Inex-A). Asimismo, se determinaron las unidades formadoras de colonia (UFC) de cada preparación, cuantificadas mediante Cámara de Neubauer.
Pruebas de antagonismo in vitro. Siguiendo la metodología modificada de Hsiang et al. (2004), se realizaron cortes transversales con navaja de afeitar en el microscopio estereoscópico de hojas de gladiolo con pústulas de U. transversalis de 3X7 cm aproximadamente. Cada corte se depositó sobre una base plástica desinfectada con hipoclorito de sodio (NaClO). Se colocó en cada corte empleando una micropipeta 0.7 uL de la suspensión de UFC de cada antagonista sobre cada una de las pústulas, contando previamente el número total de estas. Una vez vertida la gota de UFC, se pasaron los cortes del tejido junto con las bases plásticas en cajas de Petri con medio agar-agua acidificado con ácido láctico 25%, incubados por 5 días bajo cámara de germinación a una temperatura de 25 °C ± 2 °C. La colonización de los antagonistas se observó cada 24 h, bajo estereomicroscópio.
Porcentaje de colonización. La evaluación final fue considerada a los 5 días, cuando el patógeno cubrió totalmente la pústula y el tejido del cultivo mantuviera turgencia, empleando la fórmula: (%) colonización= (núm. de pústulas colonizadas/ núm. de pústulas totales) X 100, adaptada de la fórmula de Phillips y Hayman (1970).
Microscopía. Se realizaron montajes temporales de cortes de los crecimientos fúngicos exitosos de los antagonistas sobre las pústulas de U. transversalis. Los cortes se tiñeron con azul de algodón al 0.5% y fueron fotografiados en un microscopio compuesto con el software Pixel Pro Versión 1.1.0.
Análisis estadístico. Con la información de las variables de estudio obtenidas, con un modelo de bloques completamente al azar, se realizaron los análisis de varianza de acuerdo al modeló que contempla el diseño utilizado (Littell et al., 1996), y cuando la prueba de F de los análisis de varianza resulto significativa, se procedió a realizar la prueba de medias utilizando para esto, la diferencia mínima significativa honesta (DMSH) de la prueba de Tukey (p≤ 0.05) (Palaniswamy y Palaniswamy, 2006).
Resultados y discusión
Distribución y severidad de la enfermedad. De la evaluación de severidad de las plantaciones de gladiolo muestreados en 15 cultivos comerciales de los municipios de Zumpahuacán, Jocotitlán, Malinalco, Villa Guerrero e Ixtlahuaca se obtuvo un grado de infección que varío de 22% en Villa Guerrero a 91.7% en Malinalco (Cuadro 2). La enfermedad se detectó en las etapas de floración, cosecha y poscosecha, sin tener algún registro en plantaciones jóvenes.
Estadísticamente, se observaron efectos significativos (p≤ 0.05) en el porcentaje de daño de los 5 municipios evaluados, siendo el municipio de Malinalco el que presento mayor porcentaje de infección (Cuadro 3).
Cuadro 3 Porcentaje de infección en hojas de Gladiolo por U. transversalis por municipio.

† Medias con la misma letra no son estadísticamente diferentes (Tukey, 0.05)
De acuerdo a la altitud de los municipios, es evidente la diferencia porcentual en el grado de infección por roya. Si bien, la zona florícola de Villa Guerrero ocupa la mayor superficie del cultivo para venta nacional y extranjera (Aquino y Ríos, 2010), también es el municipio de mayor uso de fungicidas, insecticidas y herbicidas sintéticos que a la par con buenas prácticas de manejo del cultivo pudieran explicar el bajo (%) de infección en comparación al resto de los municipios, que se anteceden con menor tiempo de introducción del gladiolo para su producción. Además la reciente introducción del cultivo a los municipios de Malinalco y Jocotitlán, así como el uso de fungicidas sintéticos podría favorecer la aparición de hongos fitopatógenos resistentes, tal como lo menciona Vásquez et al. (2013).
En las observaciones de campo se notó que algunas de estas plantaciones se encontraban deficientemente manejadas por los productores. De lo cual se asume que si la enfermedad no se combate oportunamente, puede ocasionar la pérdida total del cultivo, tal como los registros de Schubert et al. (2006). Aquino y Ríos (2010) y el CESAVEM (2007), quienes reportan a Ixtlahuaca y Jocotitlán como municipios aparentemente libres de roya. Sin embargo de acuerdo a los resultados obtenidos, estos municipios presentaron un porcentaje de infección mayor a 50%.
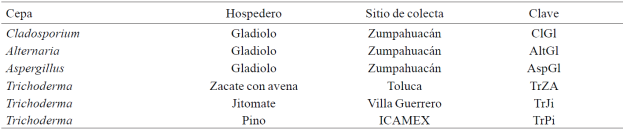
Aislamiento e identificación de hongos antagonistas. De las muestras de las localidades de Villa Guerrero (3 cepas) y Zumpahuacán (5 cepas), se obtuvieron ocho aislamientos de hongos antagonistas asociados a roya. El total de cepas de hongos antagonistas empleados fueron diez, cinco cepas del género Cladosporium sp, una del género Aspergillus sp, otra de Alternaria sp. y tres del género Trichoderma sp. Estos resultados concuerdan con lo encontrado por García et al. (2005), quienes obtuvieron cepas nativas de Cladosporium, de la parte foliar de crisantemo infectado por Puccinia horiana. Los ecosistemas agrícolas contienen gran cantidad y diversidad de microorganismos benéficos Duffy et al. (2003), por lo que no es raro que se hayan aislado hongos antagonistas de todas las muestras de flores y hojas colectadas. El efecto inhibitorio de los hongos antagónicos hacia los patógenos, se midió con el crecimiento de los primeros, a partir de este análisis se seleccionaron únicamente seis cepas para proceder a la evaluación de la interacción antagónica in vitro (Cuadro 4).
Cuadro 4 Aislamientos de hongos antagonistas identificados por planta hospedera y localidad muestreada.
Los antagonistas utilizados para biocontrol de enfermedades son generalmente saprófitos, debido a su facilidad de adaptación al medio, su alta capacidad de competencia por nutrientes frente a otros microorganismos, su versatilidad y fácil manipulación. El hongo Cladosporium ha sido empleado como agente de biocontrol de la roya blanca (Puccinia horiana) del crisantemo, obteniendo una reducción de severidad en condiciones de invernadero de 41% y 84%, afectando la producción y liberación de basidiosporas (García et al., 2005). El género Trichoderma ha sido reportado como agente de biocontrol de diversos hongos patógenos, principalmente del suelo, debido a su amplia distribución y alto rango de hospedantes (Howell, 2006; Aquino et al., 2007; Hoyos et al., 2008; Quiroz et al., 2008).
Pruebas de antagonismo in vitro. Se observaron efectos altamente significativos (p≤ 0.05) entre los tratamientos de TrPi y las cepas ClGl y AspGl, en las diluciones de 300 mL. De las seis cepas probadas, TrPi invadió claramente el mayor número de pústulas. Los tratamientos de la dilución de 600 mL, no presentaron diferencias estadísticas, sin embargo las cepas AltGl, TrZA y TrPi presentaron un porcentaje de colonización superior a 50% (Cuadro 5). Pese a la mayor cantidad de UFC en la cepa de Aspergillus sp. (Cuadro 6), esta no influyó en su eficiencia biológica representada en el porcentaje de colonización. La cepa nativa AltGl presentó igual porcentaje de colonización, en ambas diluciones. Sin embargo, al no presentar diferencias en el porcentaje de colonización en las cepas empleadas bajo una dilución de 600 mL, todas las cepas son susceptibles a utilizarse con un porcentaje de eficacia promedio de 51.2%, y en general la preparación de las cepas antagonistas de la roya transversal será más eficiente a una dilución de 300 mL.
Cuadro 5 Porcentaje de colonización (efectividad biológica) de dos concentraciones de UFC de seis hongos antagonistas sobre U. transverslis.
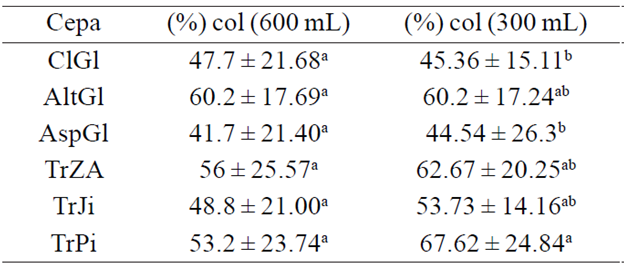
Medias con la misma letra no son estadísticamente diferentes (Tukey, 0.05).
La capacidad antagónica de algunas cepas de hongos hacia hongos fitopatógenos se puede definir con base en la destrucción total o parcial de las poblaciones de patógenos (Cook y Baker, 1983). Esta capacidad es el resultado de la agresividad del antagonista y de la susceptibilidad del patógeno (Paul, 1999). Respecto a los cortes transversales de los crecimientos fúngicos sobre las pústulas Sempere y Santamarina (2008), mencionan que la capacidad antagónica se hace evidente por la variación observada con respecto a la selectividad de algunas cepas de hongos. En las observaciones microscópicas de las zonas de colonización, las seis cepas evaluadas, produjeron variaciones como deshidratación, degradación y deformación de uredias y urediosporas.
Los cortes de las pústulas indicaron que las seis cepas antagonistas desarrollaron micelio dentro de las pústula de U. transverslis sugiriendo que los hongos actúan como hiperparásitos en las uredias (Figura 1), lo cual concuerda con García et al. (2005), con Cladosporium, quienes mencionan que aun cuando las observaciones microscópicas indicaron que Cladosporium actúa como un hiperparásito, no se descarta la posibilidad de que en el antagonismo de este hongo se involucren otros mecanismos, como la producción de antibióticos, metabolitos tóxicos y enzimas. Varios de los microorganismos utilizados como agentes de control biológico producen metabolitos secundarios que afectan el crecimiento o germinación mediante la producción de antibióticos y/o enzimas que degradan pared celular (Assante et al, 2004), por lo que sería recomendable realizar estudios de investigación con las cepas que se evaluaron en la presente investigación.
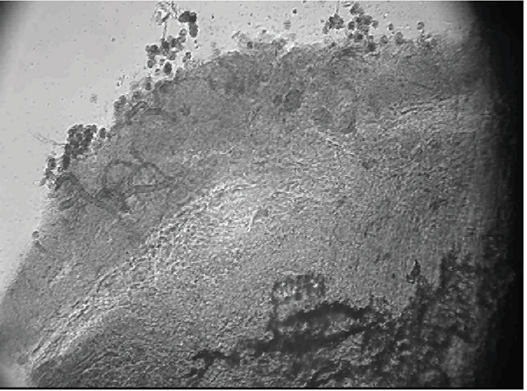
Figura 1 Observación en microscopio compuesto de la invasión de Trichoderma de Pino (TrPi) en el tejido y ureidas de U. transverslis a los cinco días de incubación (40X).
Spiegel y Chet (1998); Hermosa et al. (2000); Rey et al. (2000), han descrito los mecanismos por lo que las cepas del género Trichoderma sp, desplazan a fitopatógenos, presentándose en esta evaluación el parasitismo directo. Los resultados obtenidos sugieren que las cepasAltGl, TrFCA y TrPi, actuaron como los más eficientes antagonistas de la roya transveral (U. transversalis) en condiciones de laboratorio, sin embargo, será conveniente determinar si en condiciones de invernadero y de campo, prevalece su establecimiento y eficiencia biológica en varios municipios. Es necesario complementar la investigación con un enfoque polifásico que comprenda no solo características morfológicas, sino también bioquímicas y moleculares de las cepas de estudio de acuerdo con lo establecido por Arrúa et al. (2012).
Conclusiones
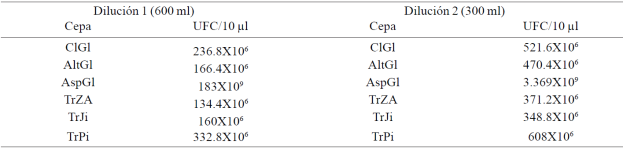
La roya transversal por Uromyces transversalis se encuentra distribuida en los cultivos comerciales de gladiolo de cinco municipios de producción florícola del estado de México con una severidad de 22 a 91.7%. Por otra parte, los hongos antagonistas asociados a la roya transversal son: Cladosporium sp., Alternaria sp y Aspergillus sp. La inoculación in vitro de las pústulas de Uromyces transversalis con los aislamientos TrPi (608X106mL-1 UFC), TrZA(371.2X106 mL-1 UFC) y AltGl (470.4X106 mL-1 UFC), presentaron la mayor colonización de pústulas de roya cuyos valores de acuerdo a las cepas fueron de 67.6, 62.6 y 60.2%, en condiciones controladas de 25 °C ± 2 °C durante cinco días. Asimismo, se observó que el modo de acción de los hongos antagonistas fue por hiperparasitismo.











 texto en
texto en