Introducción
El selenio es un elemento esencial para los humanos pero calificado como no esencial para las plantas. Sin embargo, en presencia de selenio en el sustrato o aplicado por aspersión foliar las plantas lo acumulan en sus tejidos, sirviendo como fuente primaria de este elemento en la alimentación (Broadley et al., 2006). En la mayoría de los suelos del mundo la concentración de selenio es baja, de 0.01 a 2 mg kg-1 con una media de 0.4 mg kg-1, aunque pueden encontrarse en suelos denominados seleníferos concentraciones de hasta 1 200 mg kg-1de Se (Fordyce, 2005). Se considera que el selenio es esencial en los humanos por su papel como cofactor de enzimas relacionadas con el metabolismo antioxidante (Rayman, 2008). En las plantas el selenio también ejerce un efecto positivo en la capacidad antioxidante, actuando más efectivamente este elemento en forma de selenito que en forma de selenato (Cartes et al., 2005). En México los estudios acerca de la relación entre el selenio y la calidad nutricional de los alimentos en términos de su capacidad antioxidante son pocos y por ello el objetivo de este trabajo fue documentar el efecto de las aplicaciones de selenio en plantas de lechuga, verificando el crecimiento de las plantas, la composición mineral de las hojas y la capacidad antioxidante de los extractos celulares foliares. Lo anterior bajo la hipótesis de que la aplicación de este elemento modificará el balance redox celular, aumentando la capacidad antioxidante de los tejidos de la planta.
Materiales y métodos
El presente trabajo se llevó a cabo en la Universidad Autónoma Agraria Antonio Narro (UAAAN), en Saltillo, Coahuila, México, en condiciones de invernadero, teniendo una temperatura y humedad relativa promedio de 17.8 °C y 68% respectivamente. Se utilizaron semillas de lechuga (Lactuca sativa) de la variedad Great Lakes, estas se colocaron en charolas germinadoras de 200 cavidades utilizando como sustrato peat moss y perlita para germinación. Transcurridos 40 días después de la siembra las plántulas se trasplantaron a macetas de polietileno de 20 L usando como sustrato una mezcla de peat moss y perlita con una proporción de 70:30 v: v. Los tratamientos consistieron en aplicaciones foliares de selenio en concentración de 0, 5 y 10 mg L-1 a los 15, 30 y 45 días después del trasplante. Como fuente de selenio se utilizó selenito de sodio (Na2SeO3, Sigma Aldrich, USA) sin mezclarlo con coadyuvantes.
Se colectaron las hojas con madurez fisiológica de tres plantas por cada tratamiento a los 20 y 35 días después del trasplante (ddt), estas fueron molidas y se obtuvo el extracto fresco foliar en donde se determinó el potencial de óxidoreducción (ORP) (mV), usando un potenciómetro HI9818501 (HANNA, Inc., USA),usando la técnica descrita por Benavides-Mendoza et al. (2002). La actividad catalasa (EC 1.11.1.6) se cuantificó igualmente en las hojas con madurez fisiológica a los 35 días después del trasplante (ddt) siguiendo la técnica de Ramos et al. (2010).
Se utilizó un espectrofotómetro UV-Vis Biomate 5 (Thermo Electron, USA) en 590 nm y los resultados se expresaron en mM de consumo de H2O2 min-1 proteínas totales-1 (mg/g). El peso fresco de las partes aéreas y de la raíz se determinó a los 50 ddt tomando tres plantas completas por cada tratamiento. Estas se lavaron cuidadosamente y se separó la raíz del tallo y hojas a la altura de la corona. Los pesos fueron medidos con una balanza Adventurer Pro (OHAUS, Inc., USA). Posteriormente las mismas muestras fueron colocadas en una estufa deshi dratadora marca Robertshawa a 60 ºC durante 72 h para luego ser pesadas en una balanza analítica Pionner (OHAUS, Inc., USA). Sobre las muestras secas se determinó la concentración de minerales en las hojas.
Para el nitrógeno total se usó la técnica de micro Kjelhdal (AOAC, 1980a), mientras que para el fósforo se utilizó un método espectrofotométrico (AOAC, 1980b), el K, Ca, Mg, Na, Fe, Mn, Cu y Zn fueron medidos por medio de un espectrofotómetro de absorción atómica de la marca Varían AA-1275 siguiendo la técnica de Fick et al. (1976). Para la determinación del selenio se hizo primero la digestión de 0.5 g de muestra seca en ácido nítrico concentrado hasta que se eliminó toda la parte orgánica usando un espectrofotómetro de emisión atómica por plasma IRIS ADVANTAGE (THERMO JARRELL, USA). El diseño estadístico fue de bloques completos al azar con tres repeticiones. El análisis de los datos consistió en análisis de varianza y pruebas de medias de Tukey y se llevó a cabo con el programa SAS versión 6.0 (SAS Institute, 2001).
Resultados y discusión
La aplicación de selenio foliar presentó un efecto sustancial sobre el potencial de óxido-reducción (ORP) (Figura 1). Los valores de ORP indican la capacidad antioxidante, es decir, la capacidad del sistema bajo análisis de ceder electrones en comparación con un electrodo de hidrógeno (Benavides et al., 2002). Mientras más bajo sea el valor de ORP mayor capacidad de ceder electrones y funcionar como antioxidante.
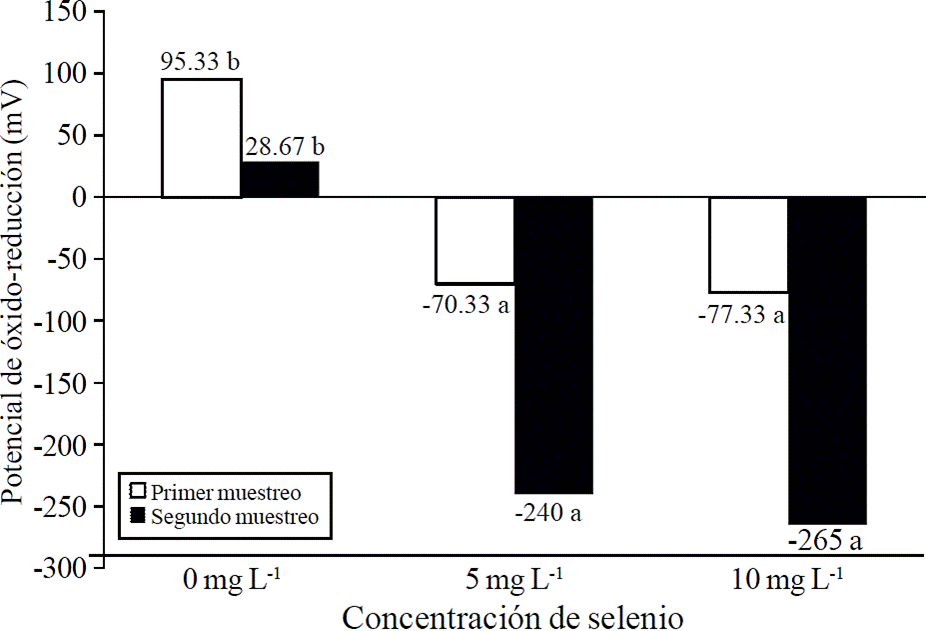
Figura 1 Promedio y desviación estándar del potencial de óxido reducción (ORP en mV) en el extracto fresco de plántulas de lechuga a las cuales se les aplicó selenio en forma de selenito de sodio. Las barras con distinta literal indican diferencia según Tukey (p≤ 0.05).
Este resultado se relaciona posiblemente con una mayor actividad enzimática antioxidante, la cual se sabe aumenta en presencia de ciertas concentraciones de selenio (Freeman et al., 2010). Lo anterior parece confirmarse por los resultados obtenidos con la actividad catalasa foliar (Figura 2) que mostró una tendencia positiva y significativa al aplicarse selenio a las plantas. Estos resultados son similares a los obtenidos por Lingan et al. (2005) que también reportaron un efecto positivo del selenio sobre la actividad catalasa.
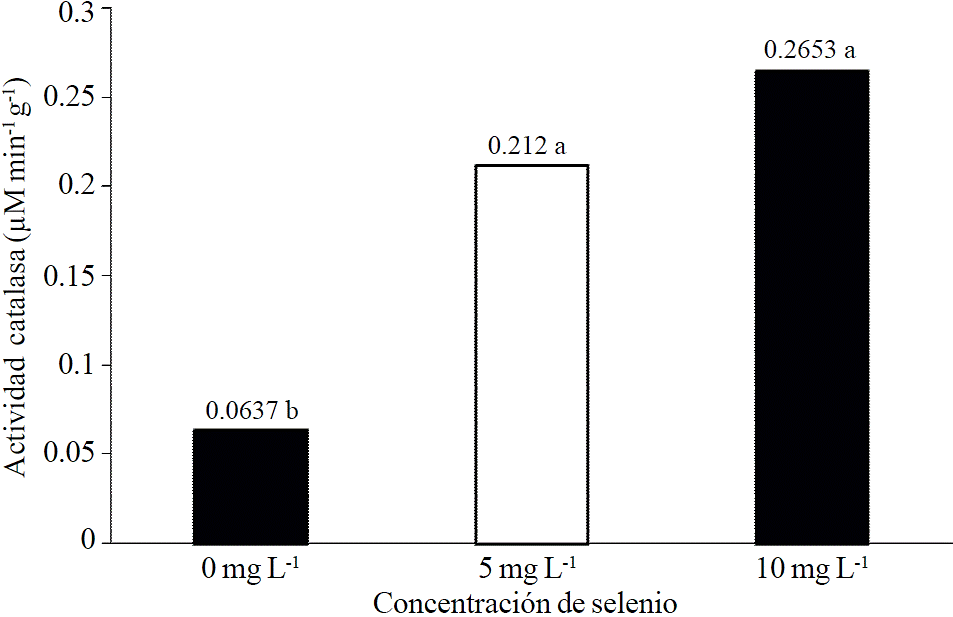
Figura 2 Promedio y desviación estándar de la actividad catalasa en plántulas de lechuga a las cuales se les aplicó selenio en forma de selenito de sodio. Las barras con distinta literal indican diferencia según Tukey (p≤ 0.05).
Es probable que el efecto del selenio sobre el potencial antioxidante no se asocie con una mayor actividad fotosintética y tal vez ello explique la ausencia de diferencias en el peso fresco y seco de la raíz y las hojas de las plantas de lechuga en este estudio (Cuadro 1). Becvort et al. (2012) obtuvieron resultados análogos aplicando selenio en tomate, obteniendo un aumento significativo en el estado antioxidante pero sin observar diferencias en los pesos frescos y secos de frutos y raíz entre los distintos tratamientos.

¥Promedios seguidos de distintas literales son estadísticamente diferentes según Tukey (P≤0.05).
Cuadro 1 Efecto de la aplicación foliar de selenio sobre los pesos frescos y secos de plantas de lechuga.
En cuanto al contenido de minerales en las plantas de lechuga (Cuadro 2) únicamente se encontraron diferencias en el contenido de nitrógeno y fósforo al aplicar selenio. Nowak et al. (2002) también encontraron un incremento en el contenido de nitrógeno con la aplicación de selenito a plantas de trigo. Los datos obtenidos en cuanto al P coinciden con Wu y Huang (2004), quienes encontraron un incremento de este elemento en plantas de trébol cuando se aplicaron cantidades bajas de selenito aplicando al sustrato 0, 10, 20 y 30 mg kg-1. Respecto a la concentración del selenio se encontró en mayor cantidad en el tratamiento de 10 mg kg-1, Kápolna et al. (2009) incrementaron la concentración radical de selenio de 0.045 a 2.0 μg g-1 en peso seco al aplicar 100 mg L-1 de selenio por aspersión foliar. Estos datos coinciden con los de Smrkolj et al. (2006) quienes indican la necesidad de llevar a cabo aspersiones repetidas si el objetivo es la acumulación de selenio.
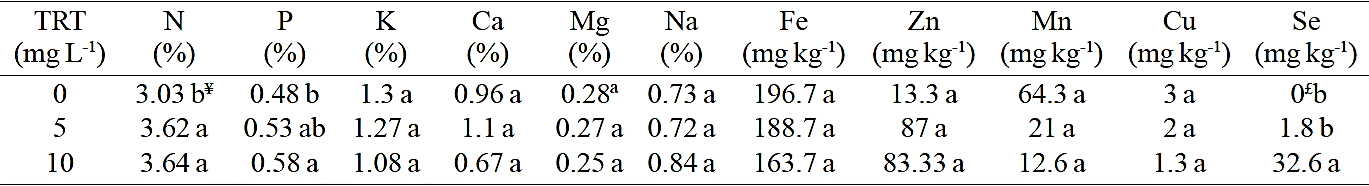
TRT=Tratamiento. ¥Promedios seguidos de distintas literales son estadísticamente diferentes según Tukey (P≤0.05). £Se consideró un valor de cero en la concentración de Se cuando no fue detectado.
Cuadro 2 Efecto de la aplicación foliar de selenio sobre la concentración de minerales en hojas de lechuga.
Conclusiones
La aplicación de selenio en forma foliar indujo un mayor estatus antioxidante en las plantas de lechuga, aumentando la concentración de N y P foliar pero sin modificar la concentración de otros elementos ni la biomasa.
La aplicación foliar de selenio puede usarse como una herramienta para elevar la calidad nutricional de la lechuga en términos de antioxidantes.











 texto en
texto en 


