Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias agrícolas
versión impresa ISSN 2007-0934
Rev. Mex. Cienc. Agríc vol.1 no.2 Texcoco abr./jun. 2010
Artículos
Diversidad genética, patogénica y morfológica del hongo Colletotrichum gloeosporioides (Penz.) de Michoacán, México*
Genetic, pathogenic and morphological diversity of fungi Colletotrichum gloeosporioides (Penz.) from Michoacan, Mexico
Víctor Montero Tavera1§, José Luciano Morales García2, Mario Martín González Chavira1, José Luis Anaya López1, Tarsicio Corona Torres3 y Amanda Gálvez Mariscal4
1 Campo Experimental Bajío. INIFAP. Carretera Celaya-San Miguel de Allende, km 6.5. Celaya, Guanajuato, México. A. P. 112. C. P. 38110. Tel. 01 461 6115323. (mgchavira@msn.com), (jose.luis.al@hotmail.com). §Autor para correspondencia: montero.victor@inifap.gob.mx.
2 Campo Experimental Uruapan, INIFAP. Av. Latinoamericana 1101, colonia Revolución, Uruapan, Michoacán. C. P. 60150. Tel. 01 452 5237392. (cefapuru@prodigy.net.mx).
3 Instituto de Recursos Genéticos y Productividad. Colegio de Posgraduados. Carretera México-Texcoco, km 36.5. Montecillo, Texcoco, Estado de México. Tel. 01 55 58045957. (tcoronat@colpos.mx).
4 Facultad de Química. UNAM. Ciudad Universitaria, Distrito Federal, México. Tel. 01 55 56166816. (galvez@unam.mx).
* Recibido: mayo de 2009
Aceptado: enero de 2010
Resumen
El hongo Colletotrichum gloeosporioides, es el agente causal de antracnosis y representa la principal limitante para la cosecha de frutos con calidad comercial de aguacate Hass (Persea americana). La diversidad genética poblacional de este hongo se ha estudiado en diversas partes del mundo, pero en México se desconoce su estructura poblacional y particularmente los componentes de su diversidad. Se determinó la diversidad genética, patogénica y morfológica de 21 cepas monoconidiales de Colletotrichum gloeosporioides de Michoacán, México. La diversidad genética se estimó por medio del polimorfismo de ADN amplificado al azar y por la determinación de los perfiles de isoenzimas de cada cepa monoconidiales. La diversidad patogénica se midió mediante la capacidad invasiva de pulpa de aguacate y por la tasa de crecimiento in vitro. La diversidad morfológica in vitro se determinó por la comparación de caracteres del micelio de cada cepa monoconidiales. Los resultados mostraron alta diversidad de Colletotrichum gloeosporioides con un índice de variabilidad genética de 0.3031 y los estimadores más precisos fue el polimorfismo de ADN amplificado al azar (índice de variabilidad genética igual a 0.344) y perfiles de isoenzimas (índice de variabilidad genética igual a 0.35). Las características típicas fueron micelio blanco, consistencia algodonosa, colonia blanca, crecimiento de micelio al azar e hifas cortas en el borde de crecimiento. No se encontró relación entre la patogenicidad medida como capacidad invasiva de pulpa y la velocidad de crecimiento in vitro. Los análisis de agrupamiento establecieron que las relaciones entre cepas se dan principalmente con base en la localidad de origen y de manera secundaria, en el síntoma producido en el fruto.
Palabras clave: Persea americana, análisis de agrupamiento, isoenzimas, RAPD.
Abstract
The fungi Colletotrichum gloeosporioides, is the agent that causes anthracnose and the main limitation to the harvest of commercial quality Hass avocado (Persea americana). The genetic diversity of the population of this fungus has been studied in several parts of the world, yet in Mexico, its population structure, and especially the components of its diversity, are unknown. The genetic, pathogenic and morphological diversity was determined for 21 monoconidial strains of Colletotrichum gloeosporioides from Michoacán, Mexico. The genetic diversity was estimated by means of random amplified DNA polymorphism, and by determining the profiles of isoenzymes of each monoconidial strain. Pathogenic diversity was measured with the invasive capacity of avocado pulp and the growth rate in vitro was determined by comparing the characteristics of the mycelia of each monoconidial strain. Results showed a high diversity of Colletotrichum gloeosporioides with a genetic variability index of 0.3031, and the most accurate estimator was the random amplified DNA polymorphism (genetic variability index= 0.344) and isoenzyme profile (genetic variability index= 0.35). The typical characteristics were white mycelia, cotton-like consistency, white colony, random mycelia growth and short hyphae on the growth border. There was no relation between the pathogenicity measured as the invasive capacity of the pulp and this growth rate in vitro. The group analyses determined that the relations between the strains are established based mainly on the origin and, in a secondary manner, on the symptom in the fruit.
Key words: Persea americana, cluster analysis, isoenzymes, RAPD.
INTRODUCCIÓN
En México el cultivo del aguacate (Persea americana cv. Hass) es muy importante para la economía nacional, debido a que se mantienen en promedio 118 000 hectáreas sembradas con producción anual promedio de 1 150 000 t y rendimiento de 10.5 t ha–1 y exportaciones hasta de 260 000 t (Colín, 2009). El estado de Michoacán cuenta con el 90% de la superficie nacional sembrada, siendo el primer productor en el ámbito mundial; los municipios más importantes de la franja aguacatera del estado son: Peribán, Uruapan, Tancítaro, San Juan Nuevo, Tacámbaro, Ario de Rosales, Tingüindín, Zitácuaro, Atapan, Salvador Escalante y Ziracuaretiro. Uno de los factores más importantes que limitan la producción, abatiéndola hasta 70%, es la presencia de enfermedades fungosas; de las cuales, la más importante por el daño económico que causa es la antracnosis, que se reconoce por diversos síntomas tales como cuarteaduras, manchas y viruela.
La antracnosis se caracteriza por presentar lesiones oscuras y hundidas, circulares o elipsoidales, con grandes cantidades de esporas formando masas compactas de color salmón, naranja o rosadas. El agente causal de esta enfermedad es el hongo ascomiceto Colletotrichum gloeosporioides (Binyamini y Schiffmann-Nadel, 1972). En Michoacán la antracnosis se presenta en todos los municipios productores de aguacate y ataca al aguacate desde la etapa de formación de frutos hasta su traslado, almacenaje y comercialización (Morales y Vidales, 1994). La entrada del hongo al fruto puede producirse antes de la maduración y manifestar los daños cuando éste madura, fenómeno que es posible ya que la muerte celular no es una condición necesaria para la patogénesis por C. gloeosporioides (Nesher et al., 2008); además este proceso es modulado por el pH de la pulpa (Yakob et al., 2000) y la actividad de los genes que codifican para la MAPK cinasa (Zhao et al., 2007 ) y pectato liasa (Yakob et al., 2000).
La caracterización genética y morfológica del género Colletotrichum se ha intentado realizar desde hace mucho tiempo; así, Smith (1990) caracterizó morfológica, cultural y patogénicamente las especies de Colletotrichum aisladas de fresa, estas especies incluyeron C. fragariae, C. gloeosporioides y C. acutatum. Maas (1983) pudo diferenciar a C. gloeosporioides, C. fragariae, C. coccodes, C. trifolii, C. dematium, G. cingulata y Gloeosporium spp. con base en la virulencia de cada aislamiento. McDonald y McDermott (1993), consideran que los marcadores electroforéticos como las proteínas o isoenzimas estiman de manera muy precisa la estructura genética de las poblaciones; sin embargo, afirman que muchas especies de hongos poseen muy poca variación isoenzimática.
A pesar de lo anterior, Morales (1996) logró separar aislamientos de C. gloeosporioides con base en diferentes sistemas isoenzimáticos, aunque no logró obtener buena resolución para ninguna deshidrogenasa. Lenné y Burdon (1990) encontraron seis patotipos de C. gloeosporioides asociados a diferentes patrones isoenzimáticos. Bailey y Jeger (1992) reportaron un estudio de variación genética en aislados de C. gloeosporioides obtenidos de aguacate, papaya, plátano y mango, confirmando que hay alta variación entre aislamientos del mismo cultivo y en el mismo país, sin embargo algunos aislamientos procedentes de diferentes cultivos fueron similares. Mills et al. (1992) reportaron alta diversidad en esta especie aislada de aguacate, mediante el empleo de patrones de restricción con las enzimas Hind III y Bam I e hibridizados con el plásmido pMY60 usado como sonda. Sreenivasaprasad et al. (1992) utilizó RFLP en DNA ribosómico y mitocondrial de C. gloeosporioides aislados de fresa y encontraron que no había variación entre aislamientos.
Ante el presente panorama y considerando la importancia económica y agronómica del aguacate en México, se realizó el presente trabajo con el objetivo de estimar la diversidad genética del hongo C. gloeosporioides de Michoacán, para establecer las relaciones genéticas entre cepas de diferentes localidades del área productora de aguacate Hass. Se probó la hipótesis que la adaptación al manejo para el control de enfermedades fungosas en las huertas comerciales de aguacate, que incluye el uso de un alto número de productos químicos (fungicidas) y la plasticidad genética de su ciclo de vida y reproductivo confiere a C. gloeosporioides alta variabilidad genética. El conocimiento de este atributo aportará elementos para un control más adecuado de la antracnosis del aguacate.
MATERIALES Y MÉTODOS
Material biológico
El presente estudio se realizó en 2005, para lo cual se colectaron tres frutos de aguacate variedad Hass por cada una de tres parcelas con los síntomas representativos producidos por Colletotrichum gloeosporioides: antracnosis típica, antracnosis-cuarteaduras, manchas superficiales y viruela. El muestreo se hizo al azar en cada tipo de síntoma en ocho municipios de la franja aguacatera de Michoacán (Los Reyes, Peribán, San Juan Nuevo, Tacámbaro, Tancítaro, Uruapan, Ziracuaretiro y Zirosto).
En total se muestrearon 24 parcelas y 288 frutos, obteniendo un aislado por cada fruto, este tamaño de muestra se definió con base en la capacidad de análisis del laboratorio y en investigaciones reportadas previamente en la literatura científica (Kelemu et al., 1999). Las parcelas muestreadas se distribuyeron formando una diagonal a través de la superficie plantada de cada municipio. Para obtener el material biológico micelial, se hicieron aislamientos a partir de frutos con cada tipo de síntoma en un medio de cultivo papa-dextrosa-agar (PDA) al 4% en cajas petri de 100 mm de diámetro, siguiendo la técnica de Morales (1996).
A los dos días de crecimiento se reaislaron los diferentes hongos en nuevos subcultivos para obtener aislamientos puros. Cuando estos llenaron la caja y habían esporulado, se hicieron preparaciones temporales con lactofenol azul, para observarse al microscopio compuesto y proceder a su identificación mediante el uso de las claves dicotómicas especializadas de Hanlin (1998); Barnett y Hunter (1998).
De los cultivos puros se obtuvieron aislamientos monoconidiales de la siguiente manera: se sometieron a luz continua durante ocho días para obtener abundante esporulación; posteriormente a cada caja de petri, se le agregaron 10 mL de agua destilada estéril y la superficie del hongo se removió con una espátula para liberar los conidios; el preparado obtenido se consideró como suspensión madre para preparar diluciones sucesivas en proporción 1:10. Los cultivos monoconidiales se obtuvieron con una solución diluida en un factor de 10-8. De 60 aislamientos monoconidiales se seleccionaron 21, por ser representativos de cada tipo, por los síntomas y características morfológicas.
Diversidad morfológica
Para la caracterización morfológica de las cepas monoconidiales (MC), se cultivaron en un medio papa-destrosa-agar (PDA) en una incubadora a 28 ºC. Los caracteres considerados fueron los siguientes: color, consistencia y tipo de crecimiento del micelio; dirección y longitud de las hifas del borde del cultivo; color y forma del cultivo; color del centro del cultivo; presencia de anillos concéntricos, manchas radiales y estrías. Las mediciones se llevaron a cabo cuando cada MC llenó la caja de cultivo.
Diversidad patogénica
Se determinó mediante la estimación de la capacidad invasiva de pulpa y la velocidad de crecimiento in vitro. Para estudiar la capacidad invasiva de pulpa de aguacate se colectaron en el municipio de Uruapan, frutos seleccionados con base a uniformidad de tamaño, madurez fisiológica (tres cuartos de madurez) y contenido de materia seca (23%). En cada una de tres repeticiones, se obtuvieron inóculos de las cajas petri conteniendo el medio PDA con sacabocados de 7 mm de diámetro y se insertaron en tres perforaciones equidistantes practicadas con el mismo sacabocados en un fruto de aguacate Hass.
Los frutos inoculados se mantuvieron ocho días en charolas cubiertas con plástico, para formar una cámara húmeda en condiciones ambientales, después se pesó la pulpa infectada por cada inóculo. Con fines estadísticos los pesos promedio de pulpa invadida, se distribuyeron en una escala de cuatro categorías: el tipo I tuvo un rango de 1 a 3.9 g, tipo II de 4 a 6.9 g, tipo III de 7 a 9.9 g, y el tipo IV de 10 a 12.5 g. Para medir la velocidad de crecimiento in vitro se sembraron las 21 MC en cajas petri con PDA y se incubaron a 28 ºC en oscuridad total.
Diariamente se midió el diámetro de la colonia con un calibrador tipo vernier, con el objetivo de encontrar la tasa diaria de crecimiento en diámetro y en área, así como el crecimiento acumulado por día. Las mediciones se detuvieron cuando el MC con mayor velocidad de crecimiento llenó la caja petri. Para el análisis de los resultados se consideró una escala de tres categorías de acuerdo al diámetro final alcanzado por cada MC: el tipo I se asignó un rango de 4 a 6 cm, tipo II de 6.7 a 9.3 cm, y el tipo III de 9.4 a 12 cm.
Diversidad genética
Se llevó a cabo mediante el análisis de zimogramas isoenzimáticos y por medio de amplificación de fragmentos de polimorfismo de ADN amplificado al azar (RAPD). Los zimogramas isoenzimáticos se obtuvieron por electroforesis en gel horizontal de almidón al 12%; las enzimas consideradas fueron malato deshidrogenasa, alcohol deshidrogenasa, glutamato deshidrogenasa, catalasa, isocitrato deshidrogenasa, esterasa, fosfatasa ácida y transaminasa glutámico oxaloacética.
Para obtener la muestra que se usó en la electroforesis las 21 MC, se cultivaron en 100 mL de medio líquido papa-dextrosa. La preparación de este medio se hizo hirviendo 200 g de papas frescas picadas en 500 mL de agua destilada durante 10 min, posteriormente la solución obtenida se filtró a través de manta de cielo estéril, se agregaron 20 g de dextrosa y se aforó a 500 mL. El medio se distribuyó en porciones de 100 mL dentro de matraces de 250 mL y en cada uno se colocaron tres rodajas de 7 mm de diámetro de cada MC. Los matraces se mantuvieron a 28 ºC y con agitación orbital de 200 rpm.
Cuando el micelio llenó el matraz, se filtró a través de manta de cielo estéril y se exprimió para eliminar la máxima cantidad de medio posible. La masa de micelio obtenida se congeló con nitrógeno líquido y se liofilizó a -50 ºC con presión de vacío de 10 mBar. Las muestras liofilizadas se molieron finamente en un molino para café hasta obtener un polvo muy fino y se guardaron a -20 ºC hasta su uso. La preparación de los geles y las condiciones generales de la electroforesis fueron establecidas por Stuber et al. (1988).
La extracción de ADN genómico, se realizó a partir de polvo liofilizado siguiendo el método de Raeder y Broda (1985) modificado por Sreenivasaprasad et al. (1992). La PCR se realizó usando 20 iniciadores decámeros de Operon Technologies Inc. Las reacciones de amplificación en volúmenes de 20 µL, se prepararon a las concentraciones finales siguientes: ADN genómico (40 ng), iniciador (10 µM), Taq polimerasa (1 unidad), dNTP's (200 µM cada uno), MgCl2 (2 mM) y buffer 10X (2µL).
Para la amplificación se usó el termociclador Ericomp Delta Cycler II, el programa de amplificación estuvo compuesto por un ciclo inicial de desnaturalización de 7 min a 94 ºC, tres ciclos de 94 ºC durante 1 min, 36 ºC por 1 min y 72 ºC por 2 min; 36 ciclos de 94 ºC durante 10 s, 40 ºC por 20 s y 72 °C durante 2 min; y un ciclo de extensión final de 72 ºC por 5 min. Los productos amplificados se separaron por electroforesis en geles de agarosa al 1.5% aplicando un voltaje de 5V/cm.
Análisis estadístico
Los datos de los experimentos morfológicos de isoenzimas RAPD, patogénico y velocidad de crecimiento; se codificaron en formato binario de presencia/ausencia, incluyendo los caracteres cuantitativos que por su distribución normal se categorizaron en rangos y se consideró la presencia/ausencia en cada uno de estos.
La codificación se hizo de acuerdo a los lineamientos establecidos por Crisci y López (1983); con este procedimiento se formó una matriz de ceros y unos, que se consideró como la matriz de datos originales, a partir de la cual se calcularon distancias genéticas mediante el programa de cómputo numerical taxonomy system (NTSYS) (Rohlf, 1993) y usando el algoritmo de Rogers y Tanimoto (1960).
Con la nueva matriz se realizaron análisis de agrupamiento, que generaron dendrogramas con el método Neighbor Join Tree, para conocer las relaciones de semejanza entre todos los monoconidiales; también se calculó el índice de variabilidad genética (IVG), propuesto por Montero et al. (1998), para calcular la diversidad genética con base en caracteres.
Este índice se utilizó para uniformizar las estimaciones de variabilidad; además se hizo un análisis de componentes principales que se complementó con la correlación de pearson y coeficientes de determinación, con el objeto de encontrar las variables que poseen la mayor varianza acumulada, para explicar de manera general la distribución de la variabilidad de C. gloeosporioides, además de identificar las variables características que lo describen.
RESULTADOS Y DISCUSIÓN
Diversidad morfológica
El análisis de componentes principales (ACP), demostró amplia variabilidad en los caracteres morfológicos ya que los primeros ocho presentaron una proporción acumulada que explica la variabilidad observada en 81.5%, lo que indica que la varianza estadística observada, se distribuye en varios componentes incrementando el número de variables requeridas para cubrir la diversidad morfológica observada.
El análisis de coeficientes de determinación, demostró que las variables mínimas que describen la diversidad de Colletotrichum gloeosporioides son: presencia de anillos concéntricos (varianza acumulada igual a 0.2152), presencia de manchas radiales (0.2055), consistencia algodonosa del micelio (0.2870), centro gris muy oscuro (0.2057), forma del borde de crecimiento (0.2415), velocidad de crecimiento tipo II (0.3171) y III (0.2438), capacidad invasiva de pulpa tipo I (0.2097) y III (0.2793).
El análisis de agrupamiento originó el dendrograma que se muestra en la Figura 1A, en la que se observa que el MC 57, se separa completamente del resto a una distancia mayor de 0.36. A distancia un poco mayor de 0.24 se forman los grandes grupos I y II, con el grupo I formado por monoconidiales de Uruapan; a distancia aproximada de 0.24 el grupo II, se subdivide en los subgrupos 2A y 2B, en el 2A dos de los MC son de Uruapan y en el 2B se observan tres MC que producen viruela, cuatro que producen manchas superficiales y dos producen antracnosis. Por lo tanto, la distribución general del dendrograma se manifiesta con base en la localidad de colecta del hongo y los síntomas que produce.
El análisis de correspondencia determinó por medio del cálculo de la distancia al centroide, que las variables características (distancia menor o igual a 1) de este hongo fueron: micelio blanco de consistencia algodonosa, color de colonia blanca, crecimiento de micelio al azar e hifas del borde de crecimiento cortas que crecen al azar. Por otra parte, las variables más raras (mayor distancia al centroide) fueron: micelio blanco cremoso, colonia blanco grisácea, colonia blanco cremosa, micelio adsorbido al medio de cultivo y centro de la colonia de color amarillo-naranja.
Los caracteres morfológicos in vitro resultaron buenos descriptores de la diversidad de C. gloeosporioides, sobre todo en conjunción con la caracterización molecular; sin embargo, pocos trabajo en esta especie han puesto tal nivel de atención en ello (Morales, 1996 y 2000); limitándose a la medición de características básicas como la tasa de crecimiento in vitro. Álvarez et al. (2004) caracterizaron 54 aislados de C. gloeosporioides de Annona muricata, obteniendo como resultado únicamente tres tipos de colonia.
Diversidad patogénica
En la Figura 2, se observa una amplia variabilidad patogénica entre cepas; el análisis de correlación entre las variables demostró que la patogenicidad en aguacates, es un evento independiente a la velocidad de crecimiento en medios de cultivo. La MC 62 presenta la mayor cobertura final en medios de cultivo, pero es de patogenicidad media. La MC 54 es de baja cobertura en caja petri, pero es altamente patogénico. Finalmente se observó que el cuarto día de cultivo in vitro, la velocidad de crecimiento presenta una caída con respecto a los días anteriores y posteriores, este fenómeno coincide con el inicio de la producción masiva de conidios, lo cual sugiere una mayor inversión energética a favor de la reproducción.
La patogenicidad es una característica que se usa comúnmente, para diferenciar aislamientos de especies de Colletotrichum y los resultados presentados concuerdan con las investigaciones de Freeman et al. (1996), en la cual analizaron la patogenicidad de aislados de C. gloeosporioides de aguacate y almendro por medio de la patogenicidad en fruto y encontraron que los aislados de aguacate presentaban mayor variabilidad, ya que eran capaces de infectar a ambas especies con diversos patrones de severidad.
Del mismo modo, Casarrubias et al. (2003) encontraron diversidad patogénica entre aislados de C. gloeosporioides de fruto de papaya procedentes de Veracruz, Chiapas y Campeche y propusieron que esta característica se puede correlacionar con grupos obtenidos en un dendrograma, realizado con datos de marcadores moleculares RAPD. Resultados similares reportan Rojas et al. (2008) en aislamientos de mango.
Diversidad bioquímica
Los ocho sistemas enzimáticos definieron 17 loci y 44 alelos. Se consideró un locus como cada una de las zonas de actividad en el zimograma de cada enzima, un alelo fue cada una de las bandas de actividad enzimática detectadas en cada locus.
Un zimograma típico se muestra en la Figura 3, se observa que las ocho enzimas estudiadas cuatro fueron deshidrogenasas (malato deshidrogenasa, glutamato deshidrogenasa, alcohol deshidrogenasa e isocitrato deshidrogenasa); las cuales, Morales (1998) consideraban de difícil resolución para C. gloeosporioides.
La enzima isocitrato deshidrogenasa presentó un patrón de dos bandas asociadas a cada alelo, las demás presentaron una banda por cada alelo.
Los valores característicos del ACP tuvieron dos comportamientos: los dos primeros CP fueron altos con proporción de 22.95% y 15.44% y los siguientes seis tuvieron valores bajos (9.74%, 8.49%, 7.6%, 6.76%, 4.98% y 3.98%).
Estos componentes principales presentaron una proporción acumulada de 79.8%; dado que este porcentaje es alto se puede concluir, al igual que para el análisis de componentes principales de los datos morfológicos, la varianza al interior de cada componente es pequeña y que hay muchos alelos importantes en la descripción de la variabilidad de este hongo.
Por lo tanto, se concluye que el hongo C. gloeosporioides, presenta una gran diversidad de tipos. Estos resultados concuerdan con Bonde et al. (1991) quienes demostraron que los patrones isoenzimáticos fueron más diversos en C. gloeosporioides que en C. acutatum y C. fragariae aislados de fresa.
A partir de la matriz de los vectores característicos, se hizo un análisis de coeficientes de determinación y varianza acumulada y se encontró que el conjunto mínimo de bandas de isoenzimas, que describen la variabilidad isoenzimática total observada son: Mdh2-1, Mdh3-2, Mdh3-3, Adh1-1, Adh2-1, Cat2-1, Idh1-1, Est1-4, Est4-1, Acp1-3 y Got1-1.
Con el análisis de correspondencia se encontró que los alelos más comunes y que presentan la distancia más corta al centroide son Mdh3-2, Idh1-1, Idh2-3, Est1-4, Est2-1, Est4-1 y Acp1-3. Por otra parte, las variables más raras (las que tienen mayor distancia con respecto al centroide) son: Idh1-2, Idh2-1, Est1-1, Acp1-1 y Acp2-1.
En el dendrograma de la Figura 1B se observa que el MC 56, se separa completamente de los demás, los cuales forman dos grandes grupos, en el primero de ellos se observa una gran preponderancia de los MC de Uruapan y en el segundo se encuentran cuatro de los cinco MC, que producen viruela formando parejas. En general, se puede describir que al igual que los análisis morfológicos el agrupamiento se manifiesta primariamente con base en la localidad de colecta y después en los síntomas producidos.
Diversidad por RAPD
Para este análisis de diversidad genética se seleccionaron los cuatro iniciadores que detectaron mayor variabilidad, los cuales definieron 93 bandas: el iniciador OPB06 presentó 18 bandas; OPQ09 38, OPA09 25 y OPV06 12 bandas. Productos de amplificación típicos se observan en la figura 3B.
La matriz de valores característicos del ACP mostró una distribución continua de los componentes principales (CP), ya que el CP1 representa 19% de la variabilidad total, CP2 16.3%, CP3 11.3%; CP4 8.2% y el CP5 6.7%. Con los primeros siete CP se explica 73.6% de la variabilidad total y con los primeros once CP explican 89%; al igual que en los análisis con caracteres morfológicos e isoenzimáticos demuestra la amplia variabilidad exhibida por C. gloeosporioides.
Mediante la aplicación de coeficientes de determinación y varianza acumulada se encontró, que los loci que mejor describen la variabilidad total observada son: OPB06.3, OPB06.8, OPB06.10, OPB06.11, OPQ09.14, OPQ09.18, OPQ09.28, OPQ09.30, OPQ09.31, OPQ09.33, OPQ09.35, OPQ09.36, OPQ09.37, OPA09.06, OPA09.14, OPA09.15, OPA09.18, OPA09.20, OPA09.23 y OPV06.05. En cambio los loci característicos de este hongo, de acuerdo al análisis de correspondencia, son: OPB06.11, OPB06.13, OPB06.14, OPB06.15, OPQ09.07, OPQ09.12, OPQ09.18, OPQ09.19, OPQ09.24 y OPA09.11. Por otra parte, los loci más raros (de frecuencia baja y distancia al centroide igual o mayor a 12) son: OPB06.07, OPB06.16, OPQ09.14, OPQ09.28, 09Q09.33, OPQ09.35, OPQ09.36 y OPQ09.37.
En la Figura 1C puede observarse la formación de grupos por localidad, ya que el grupo I contiene siete de los monoconidiales procedentes de Uruapan. En el grupo II hay tres monoconidiales procedentes de Uruapan que causan manchas superficiales, pero los monoconidiales de zirosto causantes de viruela se agrupan estrechamente, asimismo los monoconidiales procedentes de Tacámbaro y Peribán que causan antracnosis se unen estrechamente en el subgrupo IA. La distribución de este dendrograma es similar, como en el caso de los análisis morfológicos y de isoenzimas, con base en la localidad y síntomas producidos.
Los estimadores estadísticos usados en este estudio confirman la amplia variabilidad genética de C. gloeosporioides; esta característica ha sido reportada en diferentes ocasiones, aunque en México sólo se ha realizado el trabajo de Morales (1996 y 2000). En el estado de Michoacán esta amplia variabilidad genética, puede ser ocasionada por el intenso intercambio de germoplasma de aguacate en forma de plantas recién injertadas o frutos; esto puede suceder porque la gran mayoría de los viveros se encuentra en Uruapan y de aquí se distribuyen plantas a las otras localidades.
Por otra parte, el municipio de Uruapan es el lugar donde se concentra la producción de aguacate para ser comercializada y principalmente se envía a la ciudad de México y Guadalajara; este intenso tráfico propicia un intercambio de germoplasma del hongo que se encuentra como infección latente (sin síntomas visibles) en plantas y frutos. Además se debe considerar la capacidad de C. gloeosporioides para reproducirse sexualmente, siendo además una especie heterotálica que incluye la meiosis como un tipo de reproducción y por consiguiente el entrecruzamiento de segmentos cromosómicos, y junto con las mutaciones, es la mayor fuente de variabilidad de este hongo, cuya fase sexual Glomerella cingulata, es ampliamente reconocida.
Otra posible fuente de variabilidad genética, es la transferencia intergenérica de genes ribosómicos reportada por Xie et al. (2008) y de cromosomas supernumerarios (He et al., 1998); también se distribuye por la dispersión por esporas, que facilita el intercambio de material genético a distancias considerables pudiendo abarcar diferentes localidades.
Índice de variabilidad genética
En el Cuadro 1 se observan los valores de los índices de variabilidad genética (IVG), obtenidos con cada categoría de datos; en la cual, se observa que con los caracteres morfológicos se estima una magnitud menor de diversidad que con isoenzimas y RAPD. El valor del IVG para las bandas RAPD fue de 0.344 (Cuadro 1); cuyo valor es aproximadamente igual al encontrado mediante análisis isoenzimáticos (0.35); esto indica que ambos sistemas son igualmente predecibles en la detección y descripción de la diversidad genética de C. gloeosporioides.
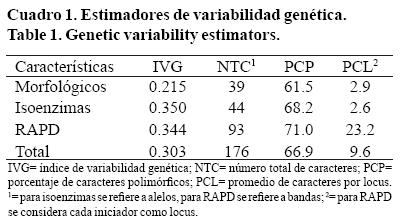
Adicionalmente se calcularon el porcentaje de caracteres polimórficos (PCP) y número promedio de caracteres por locus. El PCP fue 71% en RAPD; 68.2% en isoenzimas y 61.5% en caracteres morfológicos, lo cual proporciona una estimación de la amplia variabilidad genética exhibida por este hongo. Se han reportado múltiples trabajos que demuestran la alta variabilidad genética de esta especie estimada mediante diversas herramientas moleculares.
Álvarez et al. (2004) usaron amplificación aleatoria de microsatélites y PCR-RFLP, técnicas con las que detectaron variabilidad genética usando sólo un iniciador microsatélite y digestión con ocho enzimas de restricción. Los dendrogramas que obtuvieron definieron agrupamientos principalmente por localidad de colecta y patogenicidad de cepas. Casarrubias et al. (2003) estudiaron la variabilidad genética de C. gloeosporioides aislados de Carica papaya procedente de Veracruz, Campeche y Chiapas y obtuvieron dendrogramas que definen grupos por localidad de colecta. Resultados similares se obtuvieron en aislados de Arachis pintoi (Kelemu et al., 2000) y mango (Rojas et al., 2008).
CONCLUSIONES
Se concluye que C. gloeosporioides es un hongo genéticamente variable, ya que todos los estimadores relacionados con la diversidad genética considerados en este estudio presentan valores altos.
Los patrones isoenzimáticos y de fragmentos RAPD, son mejores estimadores de la variabilidad genética que los caracteres morfológicos; sin embargo, existe complementariedad entre todos ellos.
Las relaciones genéticas que se establecen entre las diferentes cepas monoconidiales están influenciadas por la localidad de origen y por los síntomas que producen.
AGRADECIMIENTOS
Los autores agradecen al CONACyT por la beca No. 11384 otorgada a Víctor Montero Tavera.
LITERATURA CITADA
Álvarez, E.; Ospina, C. A.; Mejía, J. F. y Llano, G. A. 2004. Caracterización morfológica, patogénica y genética del agente causal de la antracnosis (Colletotrichum gloeosporioides) en guanábana (Annona muricata) en el Valle de Cauca. Fitopatol. Colom. 28:1-8. [ Links ]
Bailey, A. J. and Jeger, J. M. 1992. Colletotrichum: biology, pathology and control. British Society for Plant Pathology. CAB. International. 388 p. [ Links ]
Barnett, L. H. y Hunter, B. B. 1998. Illustrated general of imperfect fungi. The American Phytopathological Society. St. Paul. Minnesota, USA. 219 p. [ Links ]
Binyamini, N. and Schiffmann-Nadel, M. 1972. Latent infection in avocado fruit due to Colletotricum gloeosporioides. Phytopathology. 62:592-294. [ Links ]
Bonde, M. R.; Peterson, G. L. and Maas, J. L. 1991. Isozyme comparisons for identification of Colletotrichum species pathogenic to strawberry. Phytopathology. 81:1523-1528. [ Links ]
Casarrubias, C. U.; González, C. M. M.; Cruz, H. A.; Cárdenas, S. E.; Nieto, A. D. y Guevara, G. R. G. 2003. Variabilidad genética de Colletotrichum gloeosporioides aislados de frutos de papaya (Carica papaya L.) mediante el uso de marcadores moleculares RAPD. Rev. Mex. Fitopatol. 21:338-345. [ Links ]
Colín, M. 2009. Comercialización de aguacate, inmune a la crisis. México líder en producción y ventas. México libre. URL: http://www.mexicolibre.com.mx/content/view/432712/28/. [ Links ]
Crisci, J. V. y López, M. F. 1983. Introducción a la teoría y práctica de la taxonomía numérica. O. E. A. Serie de biología. Monografía. Núm. 26. Washington DC, USA. [ Links ]
Freeman, S.; Kattan, T. and Shabi, E. 1996. Characterization of Colletotrichum gloeosporioides isolates from avocado and almond fruits with molecular and pathogenicity tests. Appl. Environ. Microbiol. 62:1014-1020. [ Links ]
Hanlin, T. R. 1998. Illustrated genera of Ascomycetes. Vol. I. Am. Phytopathol. Soc. USA. 118-119 pp. [ Links ]
He, C.; Rusu, G. A.; Poplawski, M. A.; Irwin, J. A. G. and Manners, M. J. 1998. Transfer of a supernumerary chromosome between vegetatively incompatible biotypes of the fungus Colletotrichum gloeosporioides. Genetics. 150:1459-1466. [ Links ]
Kelemu, S.; Skinner, Z. D.; Badel, L. J.; Moreno, X. C.; Rodríguez, X. M.; Fernández, D. C.; Charchar, J. M. and Chakraborty, S. 1999. Genetic diversity in south american Colletotrichum gloeosporioides isolates from Stylosanthes guianensis, a tropical forage legume. Eur. J. Plant. Pathol. 105:261-272. [ Links ]
Kelemu, S.; Muñoz, F. y Rodríguez, X. M. 2000. Diversidad genética y patogénica de los aislamientos de Colletotrichum gloeosporioides que infectan la leguminosa forrajera Arachis pintoi. Pasturas tropicales. 22:16-21. [ Links ]
Lenné, J. M. and Burdon, J. J. 1990. Preliminary study of virulence and isozymic variation in natural populations of Colletotrichum gloeosporioides from Stylosanthes guianensis. Phytopathology. 80:728-731. [ Links ]
Maas, J. C. 1983. Pathogenicity and gel electrophoretic protein pattern comparisons among strawberry anthracnose fungi. Phytopathology. 73:838-843. [ Links ]
McDonald, B. A. and McDermott, J. M. 1993. Population's genetics of plant pathogenic fungi. Electrophoretic markers give unprecedented precision to analyses of genetic structure of populations. BioScience. 43(5):311-319. [ Links ]
Mills, P. R.; Hodson, A. and Brown, A. E. 1992. Molecular differentiation of Colletotrichum gloeosporioides isolates infecting tropical fruits. In: Colletotrichum: biology, pathology and control. Bailey, A. J. and Jeger, J. M. 1992. CAB. International. 388 p. [ Links ]
Montero, T. V.; Montalvo, H. L.; García, M. J. L.; Azpiroz, R. H. S.; Peña, L. A. y Gálvez, M. A. 1998. Estimación de la variabilidad genética intrapoblacional mediante el uso de fragmentos de ADN amplificados al azar. Agric. Téc. Méx. 24(1):83-89. [ Links ]
Morales, J. L. 1996. Caracterización cultural, morfológica, patogénica y molecular de Colletotrichum gloeosporioides Penz. causante de la antracnosis del aguacate de Michoacán. Tesis de maestría. Colegio de Postgraduados. Montecillo, Texcoco, Estado de México. 96 p. [ Links ]
Morales, J. L. 2000. La antracnosis (Colletotrichum gloeosporioides Penz.) y la roña (Sphaceloma perseae Jenk) del aguacate de Michoacán, México: epidemiología, predicción y caracterización. Tesis de Doctor en Ciencias. Colegio de Postgraduados. Montecillo, Texcoco, Estado de México. 137 p. [ Links ]
Morales, G. J. L.; Montero. T. V.; Azpiroz, R. H. S. y Gálvez, M. A. 1998. Caracterización molecular de Colletotrichum gloeosporioides en aguacate Hass procedente de Michoacán, México. XVII Congreso de la Sociedad Mexicana de Fitogenética. Memoria. 345 p. [ Links ]
Morales, G. J. L. y Vidales, A. F. 1994. Enfermedades del aguacate en Michoacán. CIPAC. INIFAP. SARH. Folleto para productores. Núm. 24. 1-6 pp. [ Links ]
Nesher, I.; Barhoom, S. and Sharon, A. 2008. Cell cycle and cell death are not necessary for appressorium formation and plant infection in the fungal plant pathogen Colletotrichum gloeosporioides. BMC. Biology. 6:9-15. [ Links ]
Perkins, D. D. 1987. Mating-type switching in filamentous ascomycetes. Genetics. 115:215-216. [ Links ]
Raeder, U. and Broda, P. 1985. Rapid preparation of DNA from filamentous fungi. Lett. Appl. Microbiol. 1:17-20. [ Links ]
Rogers, D. J. and Tanimoto, T. T. 1960. A computer program for classifying plants. Science. 132:1115-1118. [ Links ]
Rohlf, J. F. 1993. NTSYS-PC. Numerical taxonomy and multivariate analysis system. Version 1.80. Department of Ecology and Evolution State University of New York. Stony Brook, New York, USA. [ Links ]
Rojas, M. R. I.; Zavaleta, M. E.; Nieto, A. D. and Acosta, R. M. 2008. Virulence and genetic variation isolates of Colletotrichum gloeosporioides Penz. and Sacc. on mango (Manguifera indica) cv. Haden. Rev. Mex. Fitopatol. 26:21-26. [ Links ]
Smith, B. J. 1990. Morphological, cultural and pathogenic variation among Colletotrichum species isolated from strawberry. Plant Dis. 74(1):69-76. [ Links ]
Sreenivasaprasad, S.; Averil, E. B. and Mills, P. R. 1992. DNA sequence variation and interraliotionship among Colletotrichum species causing strawberry anthracnose. Phys. Mol. Plant. Pathol. 41:265-281. [ Links ]
Stuber, C. W.; Wendel, J. F.; Goodman, M. M. and Smith, J. M. 1988. Techniques and scoring procedures for starch gel electrophoresis of enzymes from maize (Zea mays L.). North Carolina State University. Raleigh, NC, USA. Technical bulletin. Num. 286. [ Links ]
Xie, J.; Fu, Y.; Jiang, D.; Li, G.; Li, B.; Hsiang, T. and Peng, Y. 2008. Intergeneric transfer of ribosomal genes between two fungi. BMC. Evol. Biol. 8:72-87. [ Links ]
Yakob, N.; Kobiler, I.; Dinoor, A. and Prusky, D. 2000. pH regulation of pectate lyase secretion modulates the attack of Colletotrichum gloeosporioides on avocado fruits. Appl. Environ. Microbiol. 66:1026-1030. [ Links ]
Zhao, X.; Mehrabi, R. y Xu, R. 2007. Mitogen-activated protein kinase pathways and fungal pathogenesis. Eukaryotic cell. 6:1701-1714. [ Links ]














