Introducción
Los tumores del estroma gastrointestinal (GIST) son el tipo más común de tumores mesenquimatosos del tracto gastrointestinal; representan del uno al 3% de las neoplasias malignas gastrointestinales,1 con prevalencia de 15-20 casos/millón, cifra que se ha ido incrementando a medida que la inmunohistoquímica ha facilitado su diagnóstico.2 Actualmente se considera que podría haber hasta 10,000 nuevos casos anualmente.3 Se presentan en pacientes de 20 a 98 años, con una media de 62.9 años, sin diferencia de géneros;4 los factores de riesgo relacionados son la neurofibromatosis tipo I y dos síndromes tumorales, la tríada de Carney y el síndrome de tumor del estroma gastrointestinal familiar.5
Son más frecuentes en estómago (50%), intestino delgado (25%), colon y recto (10%).6 Los síntomas son habitualmente inespecíficos e incluyen saciedad precoz, distensión abdominal, hemorragia, anemia u obstrucción intestinal; presentan patrón definido de metástasis al hígado y/o la cavidad abdominal, con innumerables nódulos en el peritoneo. Raramente metastatizan a los ganglios linfáticos; la diseminación extraabdominal es rara.
Respecto al tratamiento, la cirugía es de elección para los GIST. Sólo 50% de los pacientes permanecen libres de recurrencia por cinco o más años.7 Antes de 2001, la cirugía era la única modalidad de tratamiento; en aproximadamente 50% de los pacientes, la resección no era posible y la supervivencia media oscilaba entre 10 y 23 meses.8 Con el advenimiento de los inhibidores de tirosina cinasa, como el imatinib,9 la supervivencia se ha modificado. A partir del reporte inicial de un paciente con GIST rápidamente progresivo, quien mostró una respuesta dramática al mes de iniciar tratamiento con imatinib, varios trabajos han confirmado la utilidad de este agente.10 En un estudio fase I de 35 pacientes con GIST11 que recibieron imatinib a dosis de 400 a 1,000 mg diariamente, se reportaron 18 respuestas parciales y 11 pacientes con enfermedad estable por periodos prolongados (> 36 meses). La duración óptima del tratamiento con imatinib en pacientes que responden aún es desconocida. En una investigación francesa que aleatorizó pacientes con GIST avanzado que no tuvieron progresión de la enfermedad después de un año de tratamiento con imatinib, se valoró la continuidad del tratamiento versus la interrupción hasta la progresión de la enfermedad; el estudio fue cerrado prematuramente debido a la evidencia de que el riesgo de progresión fue más alto cuando se pausó la terapia, lo que corroboró que la interrupción de imatinib resulta en una rápida progresión en la mayoría de los pacientes con GIST avanzado, por lo que no es recomendable la suspensión del tratamiento a menos que exista toxicidad significativa.12,13 Con el objetivo de dar a conocer en nuestro medio la frecuencia de adherencia a imatinib en pacientes con GIST y los factores que influyen en ella, realizamos la presente comunicación.
Material y métodos
Con un protocolo avalado por los Comités de Investigación y Ética en Investigación en Salud de la institución y con apego a los criterios éticos definidos por la Declaración de Helsinki, se desarrolló un estudio transversal prospectivo en una muestra no probabilística (casos consecutivos) de pacientes de la institución (pública) con diagnóstico de GIST que cumplieran los siguientes criterios de inclusión: a) mayores de 18 años (independientemente del género), con reporte histopatológico confirmatorio de GIST en cualquier etapa clínica; b) en tratamiento con imatinib como adyuvante. Como criterio de exclusión: quienes no aceptaron participar en el estudio. Criterio de eliminación: aquéllos que respondieron menos del 80% del cuestionario específico. Los participantes otorgaron su consentimiento informado y respondieron el cuestionario de Morisky-Green/Batalla, que consta de un apartado de datos generales y siete reactivos específicos sobre apego al tratamiento farmacológico. Para los cuatro primeros reactivos, cuando se obtuvo una respuesta negativa, a cada una se otorgó el valor de +1, y para cada respuesta positiva, un valor de -1. Para los últimos tres reactivos, en donde se obtuvo una respuesta positiva, cada una tuvo un valor de -1 y cada respuesta negativa, de +1; de esa manera, la sumatoria algebraica otorgó un valor de +1, lo cual representó apego al tratamiento; cualquier resultado < 1 o > 1 se consideró como no apego al tratamiento. Se utilizó el programa SPSS v. 12 para la construcción de la base de datos y el análisis estadístico, empleando frecuencias simples de las variables estudiadas y análisis bivariado, con medición de cada una de las variables consideradas como factores que influyeron en el apego al tratamiento.
Resultados
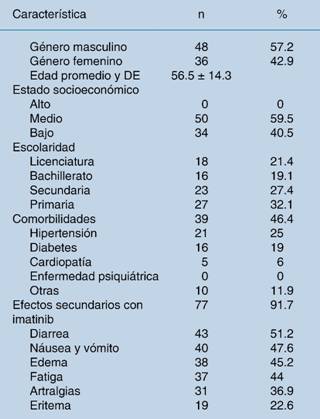
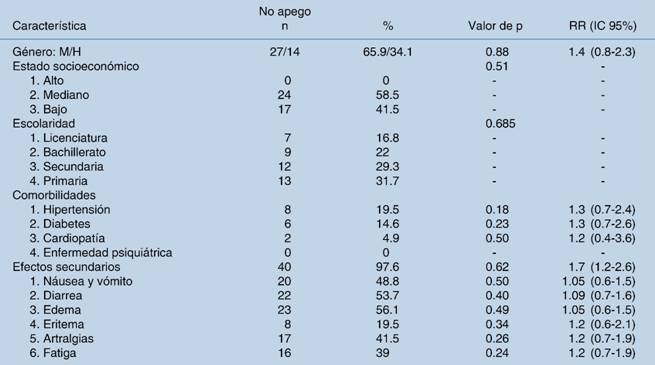
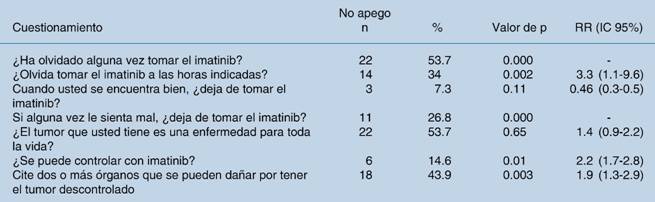
Se identificaron 84 pacientes que cumplieron los criterios de inclusión, 48 masculinos (57.2%) y 36 femeninos (42.9%), con edad promedio y DE de 56.5 ± 14.3; sus características demográficas se muestran en el Cuadro 1. De ellos, 41 pacientes (48.8%) mostraron falta de apego al tratamiento. De acuerdo con el cuestionario utilizado, los factores que determinaron el no apego al tratamiento fueron: a) olvido de tomar el medicamento, en 53.7% (n = 22); b) olvido de tomarlo a las horas indicadas, en 34% (n = 14); c) no tomarlo cuando le sentaba mal, en 26.8% (n = 11) ; d) desconocimiento de que el GIST se puede controlar con imatinib, en 14.6% (n = 6), y e) desconocimiento sobre los órganos que se pueden dañar por tener un GIST sin control, en 43.9% (n = 18) (Cuadro 2). No se encontró relación entre factores generales (género, estado socioeconómico, escolaridad, comorbilidades o efectos secundarios) y la falta de apego al tratamiento (Cuadro 3). En el análisis de regresión logística bivariado, sólo la variable “Olvidó tomar el medicamento” presentó relación con la falta de apego, con significancia estadística (p = 0.001). Cuando se analizó la relación entre el tiempo de apego y el tiempo tomando el fármaco, no se halló ninguna relación estadísticamente significativa; sin embargo, se observó la tendencia siguiente: mayor tiempo de toma de imatinib entre los pacientes con apego, 22.2 ± 20.8, en comparación con 17.1 ± 17.2 en los pacientes sin adherencia al tratamiento.
Cuadro 2: Factores que determinan el no apego al tratamiento con imatinib de pacientes con GIST,de acuerdo al cuestionario de apego de Morisky-Green/Batalla.
Discusión
Las terapias orales se han vuelto más frecuentes en oncología: ofrecen la ventaja de poder autoadministrarse en casa. Sin embargo, la evidencia sugiere que la adherencia al tratamiento oral en cáncer se encuentra muy lejos de lo óptimo.14
Al analizar la relación entre la farmacocinética del imatinib y la respuesta al tratamiento, se ha determinado que existe relación entre los niveles en suero del fármaco y la respuesta al mismo, por lo que se ha concluido que una adecuada exposición al fármaco es importante para mantener una respuesta terapéutica.15 En un estudio de 58 pacientes con GIST, los resultados indican que una concentración más alta de imatinib (expresada en AUC: área debajo de la curva) es un predictor significativo de respuesta (p = 0.026).16),(17 Debido a que el tratamiento requiere de administración diaria, el mantener una adecuada adherencia tiene significancia en pacientes con GIST, ya que su interrupción se asocia con pérdida de la remisión y progresión de la enfermedad en corto tiempo. Todas las investigaciones realizadas de adherencia al tratamiento con imatinib se han llevado a cabo en pacientes con leucemia mielocítica crónica, incluyendo algunos con GIST. Los estudios de adherencia al tratamiento (definida como la dosis tomada versus la dosis prescrita) con imatinib, tanto en pacientes con GIST como en aquéllos con leucemia mieloide crónica, reportan altas tasas de no adherencia. Tsang y sus colaboradores18 reportan que la adherencia fue de 75%; sólo en la mitad de los pacientes fue de 100%. Los factores relacionados a la no adherencia fueron edad avanzada (mayor de 51 años), género femenino, alto número de medicamentos concomitantes y complicaciones vinculadas con la enfermedad o el tratamiento.
Al momento no se han realizado estudios donde se valore la adherencia al tratamiento con imatinib en una población específica de pacientes con GIST. Al respecto, la medición de las concentraciones séricas de imatinib es el estándar de oro para evaluar el apego al tratamiento; sin embargo, no es un recurso regularmente disponible, por lo que su aplicación es limitada. Por eso, se ha recurrido a cuestionarios de valoración indirecta del cumplimiento terapéutico;19 entre los más utilizados se encuentra el de Morisky-Green,20 que es breve y fácil de aplicar, tiene alta especificidad, alto valor predictivo positivo y escasos requisitos de nivel sociocultural para su comprensión; sus desventajas son que subestima al buen cumplidor y sobrestima el no cumplimiento, tiene baja sensibilidad y bajo valor predictivo negativo. Para compensar estas desventajas, se combina con el cuestionario de Batalla,21 que es breve, comprensible, económico, fácil de aplicar y cuenta con buena sensibilidad; sus desventajas son que tiende a sobrestimar el cumplimiento y tiene baja especificidad. Ambos cuestionarios han sido previamente validados en diferentes enfermedades crónicas; se ha propuesto su uso combinado como método más práctico para valorar el cumplimiento terapéutico e intentar obtener un conocimiento del cumplimiento lo más exacto y cercano a la realidad.
En este estudio se utilizó el cuestionario de Morisky-Green/Batalla. En nuestro medio, encontramos que aproximadamente 50% de los casos no tienen apego al tratamiento; el factor más importante es el olvido de tomar el medicamento. Al correlacionar la falta de apego con las comorbilidades, no se encontró una relación estadísticamente significativa con enfermedades psiquiátricas. La falta de entendimiento sobre la importancia de tomarlo depende en mucho de la explicación médica que sensibilice al paciente sobre la relevancia del fármaco en su evolución. También existe falta de interés o motivación por parte de paciente, pues no se encontró relación entre los efectos secundarios del medicamento y la falta de apego. Por lo anterior, es posible que se encuentren implicados otros factores de índole emocional. Cuando se analizó el nivel de escolaridad y la falta de apego al tratamiento, no hubo correlación alguna, así como tampoco con el estado socioeconómico.
Dado que la relación médico-paciente es un binomio, creemos que la falta de apego al tratamiento de este grupo de pacientes se debe, principalmente, a dos factores: a) el inadecuado razonamiento del paciente debido al nivel de estrés al que está sometido al recibir información sobre el estado y pronóstico de su enfermedad y el tratamiento a seguir, y b) la manera de emitir la información por parte del médico, por lo que consideramos que la información debe proporcionarse de manera completa e insistente, y entregarla, además, por escrito.
Por lo anterior, consideramos que el tener acceso a una línea telefónica de orientación para el paciente y/o un folleto informativo sobre la enfermedad y la importancia del apego al tratamiento ayudarán a elevar el porcentaje de adherencia en pacientes con GIST.
Por último, de acuerdo con los estudios realizados por Blay, Adenis12 y sus respectivos grupos,13 podemos esperar que en prácticamente 50% de los pacientes del presente estudio se presente una rápida progresión en la mayoría de aquéllos con GIST avanzado.











 nueva página del texto (beta)
nueva página del texto (beta)