Introducción
Mielofibrosis es una entidad hematológica maligna que se encuentra englobada en los síndromes mieloproliferativos de cromosoma Philadelphia negativos.1
Esta entidad se caracteriza por la expansión clonal de una célula madre pluripotente, la cual origina una proliferación predominante de precursores de megacariocíticos y granulocíticos en la médula ósea. Durante el desarrollo de la enfermedad, las citoquinas liberadas por megacariocitos, histiocitos y monocitos clonales provocan un depósito reactivo de tejido fibroblástico policlonal en médula ósea, provocando fibrosis, neoangiogénesis y osteosclerosis, provocando disminución en la producción del tejido hematopoyético normal y da pie a la hematopoyesis extramedular, especialmente a nivel esplénico.2
La mielofibrosis post-trombocitemia esencial (TE) y la post-policitemia vera (PV), caracterizadas por la aparición de datos clínicos compatibles con mielofibrosis, así como por un aumento de la fibrosis medular, se presentan en pacientes de edad avanzada, mayores de 60 años, con predominio en hombres, presencia de mutación en el gen JAK2 y múltiples comorbilidades, razón por la cual son más susceptibles a presentar efectos adversos a ciertos medicamentos; se considera que el tratamiento de elección es por medio de trasplante de “stem cells”, pero pocos de los pacientes son candidatos aptos para este procedimiento.1-3
La mielofibrosis se considera poco frecuente debido a su baja incidencia de 1.5 casos por cada 100,000 habitantes. El diagnóstico de este padecimiento se hace por exclusión. Es una enfermedad de etiología desconocida, de la cual se pueden sospechar como factores predisponentes la exposición previa a radiaciones ionizantes y a tóxicos industriales como el benzeno o tolueno; en algunos estudios se han identificado casos en pacientes con antecedentes heredofamiliares de esta entidad.4
La causa de muerte en este grupo de pacientes se da principalmente por falla de la médula ósea, infecciones, progreso de mielofribrosis a leucemia mieloide aguda o eventos trombohemorrágicos; una vez hecho el diagnóstico, el promedio de supervivencia de estos pacientes es de 3-5 años.1
Caso clínico
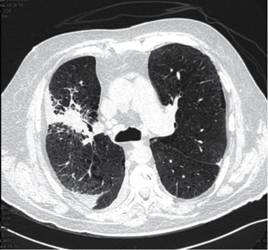
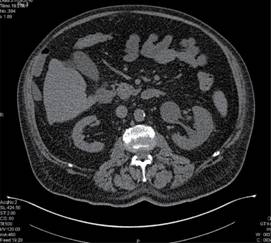
Paciente masculino de 64 años de edad, con antecedentes de importancia de hipertensión arterial sistémica, enfermedad pulmonar obstructiva crónica, hiperuricemia de larga evolución y enfermedad renal crónica de reciente diagnóstico. Se presenta al Servicio de Urgencias con cuadro gastrointestinal, fiebre, dificultad respiratoria con saturación de 70% al aire ambiente y disminución de volúmenes urinarios. Se realizan estudios de laboratorio en los cuales se hace evidente falla multiorgánica caracterizada por anemia y trombocitopenia; en el frotis sanguíneo se reportan mieloblastos y blastos, 5% en sangre periférica, con reacción leucoeritroblástica, elevación de enzimas hepáticas, elevación de azoados con anuria, persistencia de saturación de oxígeno baja (70-85%) a pesar de haberse proporcionado oxígeno suplementario por puntas nasales y posteriormente tienda facial a 10 L/min. Se decide realizar las TAC tóraco-abdominal con las siguientes alteraciones descritas en las Figuras 1, 2 y 3.
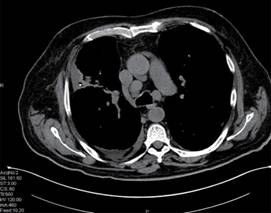
Figura 2: Adenopatías supraclaviculares derechas, axilares bilaterales a nivel de cadena mamaria interna derecha, periaórticas con pérdida de su morfología.
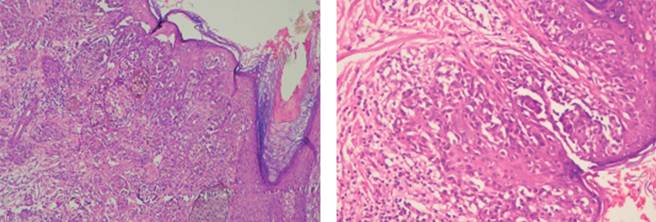
Se decide manejo integral por medio del departamento de hematología; se realiza biopsia de hueso y aspirado de médula ósea (AMO: médula ósea con hiperplasia de la serie eritroide y fibrosis reticulínica grado 3) (Figura 4) y se hacen varias transfusiones (4 paquetes globulares durante su estancia hospitalaria) por parte del Servicio de Neumología; se efectúa broncoscopia con toma de biopsias de masa localizada en bronquio de lóbulo apical posterior de pulmón derecho con resultado de patología final de adenocarcinoma pulmonar y del Servicio de Urología, realizando ureteroscopia y colocación de catéteres doble J, sin especificar la causa de la obstrucción ureteral. Debido al manejo integral que se proporciona, el paciente se mantiene estable durante su estancia intrahospitalaria.
Discusión
Dentro del grupo de las enfermedades malignas de la médula ósea se incluye mielofibrosis primaria (MFP), leucemia mieloide crónica, trombocitemia esencial (TE), policitemia vera (PV), leucemia neutrofílica crónica, leucemia eosinofílica crónica, mastocitosis sistémica. Como se comentaba anteriormente, tanto la trombocitemia esencial como la policitemia vera son capaces de evolucionar hacia estados mielofibróticos; estas tres entidades (MFP, TE, PV) se engloban en el término mielofibrosis.1
La mielofibrosis se caracteriza por hiperproliferación de la médula ósea con dismielopoyesis y megacariocitos hipolobulados, fibrosis, citopenias o citosis, y esplenomegalia progresiva.4
Las manifestaciones son variables e incluyen anemia progresiva, leucopenia o leucocitosis, leucoeritroblastosis, trombocitopenia o trombocitosis, y hematopoyesis multiorgánica extramedular que se manifiestan principalmente como hepatoesplenomegalia sintomática.4 En casos avanzados, los pacientes presentan una variedad de síntomas como consecuencia de la esplenomegalia, dentro de los cuales destaca: dolor, saciedad temprana, infarto esplénico, hipertensión portal y disnea; además presentan síntomas asociados a falla medular progresiva, hipertensión pulmonar, transformación leucémica y muerte prematura.5
Los hallazgos de laboratorio incluyen anemia con niveles de hemoglobina < 10 g/dL en más del 50% de los pacientes, encontrando en el frotis de sangre periférica anisocitosis, poiquilocitosis, dacriocitos, entre otros.6 Los valores de plaquetas y glóbulos blancos son variables, y dependen de la progresión de la enfermedad; es frecuente encontrar elevación de fosfatasa alcalina, deshidrogenasa láctica e hiperuricemia.
El aspirado de médula ósea es difícil de realizar dadas las características fibróticas; los principales hallazgos son hiperplasia megacariocítica y neutrofílica; sin embargo, no son diagnósticos. La biopsia de médula ósea es necesaria para demostrar la fibrosis, asociada a hiperplasia megacariocítica y osteoesclerosis. Se debe realizar en forma rutinaria la búsqueda de mutaciones genéticas, principalmente JAK2, BCR-ABL, MPL.2
En 2008, la OMS definió los criterios diagnósticos para mielofibrosis primaria basados en una combinación de características clínicas, morfológicas, citogenéticas y moleculares.3 Para establecer el diagnóstico se requieren tres criterios mayores y dos menores (Figura 5).
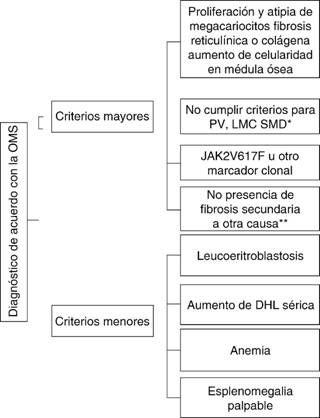
*PV = policitemia vera, LMC = leucemia, mieloide crónica, SMD = síndrome mielodisplástico, **infección, enfermedades inflamatorias, metástasis, etc.
Figura 5: Diagnóstico para mielofibrosis.
Existen muchas causas de fibrosis de médula ósea que se deben considerar antes de establecer el diagnóstico de mielofibrosis primaria.
El grado de fibrosis de la médula ósea puede dificultar la distinción entre causas como metaplasia mieloide agnogénica (MMA), mielofibrosis aguda y síndromes mielodisplásicos con mielofibrosis. En la MMA, datos como hiperplasia de los tres linajes, esplenomegalia marcada, mieloptisis y niveles elevados de DHL apoyan el diagnóstico. En la mielofibrosis aguda, los pacientes habitualmente presentan síntomas constitucionales severos, fiebre, pancitopenia pero sin organomegalia o mieloptisis en sangre periférica.4 En cambio, en el síndrome mielodisplásico con mielofibrosis las manifestaciones son variables y pueden semejar la mielofibrosis aguda o la metaplasia mieloide angiogénica. En el aspirado de médula ósea en las tres patologías se observa fibrosis reticulínica e hiperplasia megacariocítica; sin embargo, la presencia de osteoesclerosis nos debe orientar hacia MMA, mientras que las otras dos entidades mencionadas tienden a presentar dispoiesis de los tres linajes.3 La presencia de diseritropoyesis en ausencia de esplenomegalia sugiere un síndrome mielodisplásico.7 Por otro lado, en las tres patologías puede existir un número desproporcionado de blastos, ya sea en sangre periférica o en médula ósea; sin embargo, es mucho más frecuente en mielofibrosis aguda.4
La determinación del cromosoma Philadelphia (Ph) nos orienta hacia el diagnóstico de leucemia mieloide crónica.
Se deben descartar aquellas patologías que constituyen el grupo de neoplasias mieloproliferáticas crónicas Ph negativas: mielofibrosis primaria, policitemia vera y trombocitemia esencial. La policitemia vera se caracteriza por un incremento de los glóbulos rojos, mientras que para realizar el diagnóstico diferencial de mielofibrosis primaria de trombocitemia esencial se debe valorar la morfología de la médula ósea, el grado de fibrosis, esplenomegalia y la presencia de leucoeritroblastosis en sangre periférica; esta última clásica de mielofibrosis primaria.5,6
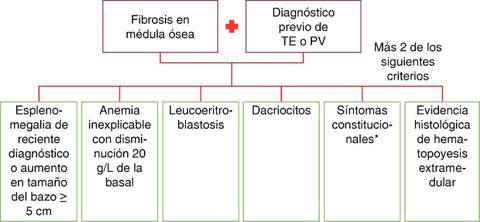
Existen formas de mielofibrosis secundaria, entre ellas las otras dos neoplasias mieloproliferativas mayores, metaplasia mieloide post-policitemia y metaplasia mieloide post-trombocitemia. El grupo internacional para la investigación y tratamiento de mielofibrosis (IWG-MRT por sus siglas en inglés) clarificó los criterios diagnósticos de estas dos entidades y fue adoptado por la OMS (Figura 6).2,9 Otras causas hematológicas incluyen leucemia de células peludas, linfoma y mieloma múltiple. En las formas de mielofibrosis no hematológicas se encuentra la invasión metastásica de la médula ósea, enfermedades autoinmunes (lupus eritematoso sistémico, esclerodermia, enfermedad del tejido conectivo, polimiositis), hiperparatiroidismo secundario, entre otras.9
Conclusiones
Se han realizado avances significativos en el abordaje y entendimiento de la mielofibrosis y su fisiopatología, lo cual lleva a nuevos enfoques terapéuticos; la identificación del gen JAK2 y el desarrollo de tratamientos de primera elección como los inhibidores de la JAK2 que ya se encuentra aprobada por la FDA, mejoran la calidad de vida y las expectativas de tratamiento. Debido a que se trata de una enfermedad o grupo de entidades poco comunes se espera en el futuro próximo que se ahonde en la investigación del manejo y terapias incluyendo la combinación de las terapias ya conocidas y así mejorar los resultados en los tratamientos.











 nueva página del texto (beta)
nueva página del texto (beta)