Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista odontológica mexicana
versión impresa ISSN 1870-199X
Rev. Odont. Mex vol.18 no.2 Ciudad de México abr./jun. 2014
Trabajos originales
Estomatotoxicidad bucal inducida por quimioterapia
Blanca Leticia Martínez Goyri,* María Elena Cruz Ramos, § Enrique Echevarría y PérezII
* Exresidente de la Especialidad de Prótesis Maxilofacial, División de Estudios de Postgrado e Investigación. Facultad de Odontología, UNAM. Hospital General de México, Servicio de Oncología, Unidad de Oncología Bucodentomaxilofacial.
§ Cirujano Dentista adscrito al Servicio de Oncología. Hospital General de México.
II Profesor Titular de Prótesis Maxilofacial, División de Estudios de Postgrado e Investigación. Facultad de Odontología, UNAM.
RESUMEN
El objetivo principal de este estudio fue determinar el tipo de lesiones bucales más frecuentes en las pacientes con cáncer de mama tratadas con quimioterapia en el Hospital General de México, y establecer en qué condiciones se presentan dichas manifestaciones. Se realizó una revisión de expedientes entre los años de 1994 y 1999, estableciendo los criterios de inclusión y exclusión. De un total de 405 que fueron considerados, se incluyeron en la muestra 327 expedientes. De ellos, la incidencia de estomatotoxicidad se presentó en 122 casos, 89 de los cuales presentaron una sola manifestación bucal, 19 presentaron dos, y 14 pacientes reportaron más de dos. La relación entre la estirpe histológica del tumor se refleja presentándose en el canalicular infiltrante, lobular y otros (p < .005). Los esquemas de tratamiento con quimioterapia fueron integrados con: 5-fluoracilo, adriamicina, ciclofosfamida y metotrexato (p < .005). La dosis y estomatotoxicidad se relacionaron con p < .005.
Palabras clave: Estomatotoxicidad, mucositis, xerostomía, sialorrea.
INTRODUCCIÓN
El cáncer es una enfermedad cronico degenerativa que actualmente se presenta con mayor incidencia debido al aumento en el promedio de vida de la población. Representa la segunda causa de defunción en nuestro país y se caracteriza por el crecimiento anárquico de las células, lo que da origen a tumores con capacidad de diseminarse, principalmente por vía linfática y hematógena. Su tratamiento es multidisciplinario, pues puede ser local en el área afectada y sistémico, por medio de la quimioterapia.1
El cáncer de la glándula mamaria tiene una alta incidencia en la población femenina. Aproximadamente el 6% de las defunciones suceden por lesiones en esta entidad anatómica. Este tipo de cáncer se considera como una enfermedad sistémica que localmente es tratada con cirugía y radioterapia, pero su control sistémico se realiza con quimioterapia; ello representa un avance importante, pues impacta favorablemente en el 25 y 50% de la población afectada. 2-4
Su pronóstico y protocolo de tratamiento dependen de dos elementos principalmente: la estirpe histológica y el estadio clínico. Éstos son considerados para establecer un esquema, dosis terapéutica y número de ciclos programados.
DOSIFICACIÓN
La dosis de quimioterapia que se suministra al enfermo con cáncer es calculada y administrada por el especialista, quien establece los esquemas que se refieren a los medicamentos seleccionados y a los ciclos que corresponden al número de tratamientos.
En términos generales, puede decirse que las dosis se basan en la superficie corporal o peso del paciente (miligramos/m2 de superficie o miligramos/ peso en kilogramos). En los estadios clínicos avanzados se aplican dosis altas y un mayor número de ciclos, lo que induce más manifestaciones tóxicas en general.5
De acuerdo con la literatura consultada, entre el 40 y 60% de los pacientes portadores de cáncer son tratados sistémicamente, y el 40% presenta toxicidad bucal, aun sin estar involucrada la región cervicofacial en la lesión primaria.6,7
La mucositis se presenta por una disminución en la tasa de renovación del epitelio basal, que se adelgaza y presenta úlceras en tejidos blandos, principalmente en los no queratinizados, como la mucosa bucal y labial y las superficies ventrales y laterales de la lengua. La severidad varía por el esquema empleado, dosis y condiciones bucales previas a la terapia.
Casi todos los quimioterápicos producen algún grado de estomatotoxicidad. En la experiencia clínica de algunos autores, los antimetabolitos, el metotrexato, 5-fluoracilo, doxorrubicina, bleomicina, dactinomicina, daunorrubicina y ciclofosfamida representan los agentes causales más frecuentes. Cuando se agregan funciones hepáticas y renales alteradas, el riesgo aumenta como resultado del metabolismo reducido, que disminuye la excreción de los medicamentos. Ante estas circunstancias, las estomatitis son más severas y perdurables. Las concentraciones hísticas y sanguíneas de los cito-tóxicos retrasan la reepitelización, por lo que a medida que se van administrando los diversos ciclos propuestos, la probabilidad de manifestarse es cada vez mayor.8,9
Debido a la gran incidencia de cáncer mamario en México y a la necesidad de aplicación de sus tratamientos, los estadios tan avanzados en que se presenta la mayoría de estas pacientes ocasionan manifestaciones estomatológicas que pueden atenuarse y, en algunos casos, evitarse si son tratadas odontológicamente antes, durante y después de su tratamiento de quimioterapia10-12
MÉTODOS
Se efectuó un estudio retrospectivo y descriptivo revisando los expedientes clínicos de entre 1994 y 1999 de las pacientes con diagnóstico de cáncer mamario que fueron tratadas en el Servicio de Oncología del Hospital General de México mediante interconsultas en las unidades de tumores mamario, quimioterapia y prótesis maxilofacial.
CRITERIOS DE EXCLUSIÓN
De los expedientes estudiados se excluyeron:
1) Las pacientes con enfermedades propias de la cavidad bucal, con manifestaciones previas al tratamiento de quimioterapia.
2) Las pacientes con enfermedades sistémicas y manifestaciones estomatológicas como la diabetes mellitus o síndrome de inmunodeficiencia adquirida.
3) Aquellas pacientes sometidas a radioterapia en cabeza y cuello previamente al tratamiento de quimioterapia.
CRITERIOS DE INCLUSIÓN
Se incorporaron los expedientes de todas las pacientes con diagnóstico de cáncer de mama que fueron atendidas desde su inicio en las unidades de quimioterapia y prótesis maxilofacial del Hospital General de México.
Se registraron las siguientes variables:
1. Tipo de lesión por búsqueda específica.
2. Aparición de las lesiones bucales con relación al esquema de quimioterapia.
Los expedientes fueron explorados con una hoja de recolección de datos que incluyó edad, sexo, diagnóstico histopatológico, estadio clínico, esquema de quimioterapia, grupo estomatológico y búsqueda específica de lesiones.
El análisis de los resultados se realizó de acuerdo con los métodos de estadística descriptiva:
• T de student para las variables continuas.
• χ2 para las no continuas (se anexan las estadísticas).
RESULTADOS
Se realizó una revisión de expedientes entre 1994 1999, seleccionando de ellos 405 expedientes de pacientes con diagnóstico de cáncer mamario, incluyendo sólo 327 en este estudio, que cumplieron con los criterios de inclusión.
El rango de edad correspondiente a las pacientes con cáncer de mama fue de 26 años la más joven y de 76 la mayor, con una media de 42 años y un rango de 50 años (Figura 1).

En el análisis histopatológico se obtuvieron los siguientes datos: 297 pacientes presentaron diagnóstico de carcinoma canalicular infiltrante, 22, diagnóstico de carcinoma lobular, y 8 fueron incluidas en el grupo de otros (papilar, medular) (Figura 2). Asimismo, de los expedientes revisados se obtuvo como resultado que 101 pacientes se encontraban en estadio clínico II, 155 en estadio III y 71 pacientes en estadio IV (Figura 3).


De acuerdo con el esquema que recibieron estas pacientes durante su tratamiento, se obtuvo lo siguiente: 206 pacientes recibieron 5-fluoracilo, ciclofosfamida y doxorrubicina (FAC); 84 fueron tratadas con adriamicina y ciclofosfamida (ACII); 30 se sometieron a la ciclofosfamida, metotrexato y 5-fluoracilo (CMF). Sólo tres pacientes recibieron 5-fluoracilo más metotrexato (5FU + MTX). Respecto a los esquemas adriamicina (A), 5-fluoracilo (5FU), A + 5FU, platino y navelvine (PL + NV), éstos se aplicaron en un solo caso cada uno (Figura 4).

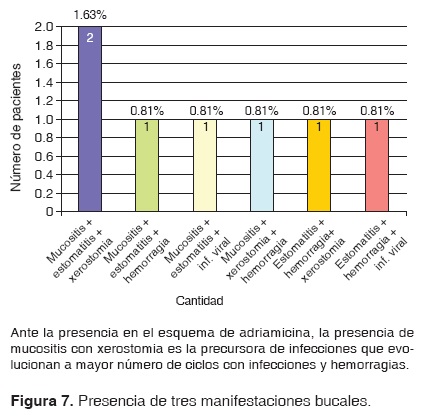
De los 327 expedientes incluidos en este estudio, 122 pacientes presentaron manifestaciones estomatológicas, lo cual representa el 37.31% de nuestra población. De los mismos, 89 experimentaron una sola manifestación bucal durante su tratamiento de quimioterapia, 19 mostraron dos manifestaciones diferentes y 14 pacientes tuvieron más de dos manifestaciones estomatológicas. (Figuras 5 a 8)(6, 7).



El análisis estadístico fue desarrollado utilizando el paquete diseñado para este propósito. De la base de datos se incluyeron en este análisis las siguientes variables:
1. Dentro del diagnóstico histopatológico, se estudió la relación:
a) Canalicular infiltrante versus lobular
b) Canalicular infiltrante versus otros
La comparación estadística en ambos casos resulta significativa con una p < .005.
Otro factor analizado fue:
2. Los diferentes esquemas de quimioterapia, comparando en este caso:
a) FAC versus ACII
b) FAC versus CMF
Resultando en ambos una p < .005 (estadísticamente significativo).
Finalmente, fueron valorados los siguientes factores:
3. Las manifestaciones estomatológicas:
a) Para identificar la cantidad de manifestaciones presentes, comparando:
- 1 versus 2 (manifestaciones)
- 1 versus 3 (manifestaciones)
b) Para determinar el tipo de manifestaciones presentes, comparando:
- Mucositis versus sialorrea
- Mucositis versus xerostomía
- Mucositis versus infecciones micóticas
En estos casos se obtuvo una p < .005, lo que nos indica resultados estadísticamente significativos.
DISCUSIÓN
De acuerdo con la literatura consultada, el promedio de edad de las pacientes con cáncer mamario se reportó entre los 43 a 53 años. En nuestra revisión, se obtuvo una media de 42 años, lo que indica una tendencia a presentarse en mujeres más jóvenes; en la población en general, representó el 90.82% de nuestra población.13,14
Como diagnóstico histopatológico de nuestras pacientes, esta revisión reporta al carcinoma canalicular infiltrante como el más frecuente (91 por ciento) de la muestra, así como un estadio avanzado (III y IV) en la mayoría de los casos, lo que representa 69.12%. Estos datos se apoyan en el Primer Consenso Nacional sobre Tratamiento del Cáncer Mamario, mismo que reporta que en nuestro país el 50% de las pacientes recibe su diagnóstico en esta etapa tan avanzada; por ello, es imprescindible la utilización de quimioterapéuticos para aumentar sus posibilidades de supervivencia.15,16
Los tratamientos sistémicos de quimioterapia dirigen su efecto principalmente sobre las células cancerosas, lo que impide su crecimiento y multiplicación, pero actúan también sobre aquellas células corporales que se dividen rápidamente, como lo son las de la médula ósea, las del aparato digestivo, el sistema reproductor, los folículos pilosos y la piel.17
Nuestros hallazgos confirman los estudios en los que se reporta principalmente a los esquemas de quimioterapia que incluyen tanto a la adriamicina como a la ciclofosfamida y el 5-fluoracilo, como los esquemas que han mostrado una mayor efectividad en el tratamiento del carcinoma mamario y, por tanto, los de mayor utilización en países del tercer mundo, ya que sus costos son accesibles.11,15
Los datos de la literatura especializada confirman que una de las reacciones secundarias de la quimioterapia son las manifestaciones estomatológicas. En esta revisión, el 100% de las pacientes recibió poliquimioterapia o, por lo menos, alguna de las drogas reportadas como asociadas con manifestaciones estomatológicas.18
Los esquemas a que estuvieron sujetas nuestras pacientes fueron: CMF, FAC, ACII, A, 5FU, 5FU + MTX, PL + NV y 5FU + A).
Los resultados confirman lo establecido en estudios previos, que mencionan entre las manifestaciones estomatológicas causadas por quimioterapia a la mucositis como manifestación común y potencialmente seria.
De un total de 122 pacientes, 91 presentaron mucositis sola o asociada con otras manifestaciones, lo que representó el 54.09% de nuestra población, de acuerdo con la Escala de Evaluación de Mucositis Oral (OMAS) desarrollada en 1996 por un equipo de médicos especialistas oncólogos y expertos en la evaluación y estadística del dolor.
La mucositis se divide en los siguientes grados:
a) Grado 0. En donde no hay partes afectadas.
b) Grado 1. Boca adolorida y eritema.
c) Grado 2. Presencia de eritema y úlceras, pero el paciente puede alimentarse a base de sólidos.
d) Grado 3. Boca adolorida y ulcerada, lo cual sólo le permite dieta líquida.
e) Grado 4. En donde la alimentación oral es imposi-ble.10,19-26
Coincidiendo con algunos autores, los quimiotera-péuticos que causan principalmente la mucositis son: 5FU, metotrexato, doxorrubicina, bleomicina, dactinomicina, daunomicina, ciclofosfamida, vincristina, citosina-arabinosido, cisplatino y leocovorin.10,23,26,27
La manifestación que ocupó el segundo lugar en esta revisión fue la estomatitis, ya que se presentó sola o asociada con otras manifestaciones en 33 de las 122 pacientes (26.95%).
Dreizen y colaboradores mencionan al metotrexato (antagonista del ácido fólico) como uno de los causantes de esta manifestación, debido a una deficiencia de ácido fólico, lo que interfiere en la producción y maduración de las células epiteliales y lleva a una atrofia o extinción de las papilas linguales y formación de úlceras, que a su vez causan una deficiencia nutricional al paciente por el dolor que provocan.19,27,36-39
Otros autores han demostrado que el 5FU (antagonista metabólico del uracilo) es causante también de la estomatitis, pues produce deficiencia de timina, lo que interfiere en la síntesis del ácido nucleico y se refleja en una rápida división celular por un desequilibrio en el crecimiento y muerte celular, causando ulceración y descamación epitelial.19,26,28 Ello nos permite establecer que la presente revisión demuestra que la hemorragia gingival es otra de las manifestaciones constantes en estos pacientes, pues ésta fue observada en nueve individuos, aunque asociada siempre con alguna otra manifestación. Es producida principalmente por la vincristina, citosina-arabinosido y prednisona; se genera por trombocitopenia inducida por la droga y por coagulación intravascular diseminada, sobre todo en pacientes con niveles plaquetarios de 20,000 a 50,000 por mm3.
Estos medicamentos alteran la síntesis y maduración de las células sanguíneas provocando leucopenia, trombocitopenia y anemia, privando al sistema inmune de protección. La mielosupresión puede precipitar el sangrado espontáneo del periodonto y agudizar la enfermedad periodontal crónica, así como los problemas pulpares.19,29,30
Otra manifestación común en nuestras pacientes revisadas fue la xerostomía, pues la misma se encontró en 27 de 122 pacientes, lo que representa el 22.05% de nuestra población; esta cifra coincide con la literatura especializada.
La xerostomía se presenta como efecto secundario o agregado a la mucositis, ya que hay una reducción (cantidad y calidad) del flujo salival a partir del segundo día de tratamiento; además, existe atrofia hacinar, necrosis celular, degeneración y fibrosis de la glándula salival, lo que provoca disminución del flujo salival y su pH, así como de la capacidad buffer de la saliva. Todo esto acelera el deterioro periodontal y favorece la aparición de caries dental.
Esta disminución de enzimas, minerales y proteínas salivales afecta directamente al órgano dental en su remineralización, y por otra parte, se ven afectadas la dicción, masticación y deglución del paciente.14,30-35
Existen reportes que indican a la ciclofosfamida, doxorrubicina y vincristina como causantes de infecciones virales; esto se confirma en nuestro estudio, en donde ocho pacientes (7.32%) de la muestra presentaron infecciones virales, siempre asociadas con otras manifestaciones, durante su tratamiento.
De acuerdo con William Carl y asociados,28 esta manifestación se presenta porque las drogas interfieren con el crecimiento y la maduración celular de la mucosa oral, lo que reduce el tejido que sirve como barrera para este tipo de infecciones. Esto mismo es apoyado por Dreizen y colaboradores,19 quienes sugieren también que se presentan infecciones micóticas además de las virales; sin embargo, en nuestra revisión se encontró sólo a dos pacientes con infecciones micóticas; esto representó un porcentaje mínimo de nuestra población (1.63%). Estas infecciones son causadas por la alteración de la saliva y la flora bucal provocada principalmente por la prednisona, vincristina, doxorrubicina y metotrexato.10,21,22
Otra enfermedad de manifestación frecuente, la sialorrea, se menciona en algunos otros estudios, pero en esta revisión sólo se encontró en un paciente, representando el 0.81% de la población total estudiada. Los autores reportan que se presenta antes de la xerosto-mía, lo cual podría explicar que es común reportar esta última y no valorar adecuadamente la presencia de la sialorrea en estas pacientes.29
El presente estudio de las manifestaciones de estomatotoxicidad inducida por el tratamiento con quimioterapia del cáncer mamario establece la necesidad de protocolizar el tratamiento simultáneo entre el oncólogo y estomatólogo especializado.
Un buen cuidado bucal es crítico durante los tratamientos de quimioterapia, ya que de esta manera se podrán evitar estas manifestaciones e, incluso, reducir el grado de su afección sin impedir al paciente alimentarse o retrasar su tratamiento de quimioterapia. La prevención de las manifestaciones estomatológicas reportadas en este trabajo muestra la importancia de realizar al paciente un examen bucal minucioso antes de la quimioterapia.
CONCLUSIONES
1. Las manifestaciones estomatológicas por quimioterapia en pacientes con cáncer mamario se presentan principalmente cuando se aplican esquemas a base de 5FU, adriamicina y ciclofosfamida.
2. Las manifestaciones estomatológicas más frecuentes en las pacientes incluidos en este estudio fueron la mucositis, estomatitis, xerostomía y las infecciones virales y micóticas.
3. Con base en los resultados, se puede sugerir que todas las pacientes tratadas con quimioterapia deben recibir un tratamiento odontológico antes, durante y después de su tratamiento de quimioterapia. Basándonos en un estudio radiográfico del paciente, podemos elaborar un plan de tratamiento en el cual se tomen en cuenta las medidas preventivas y se incluyan tratamientos convencionales programados. Debe darse una especial atención a la población con las características de nuestro estudio, ya que normalmente ésta es afectada por los problemas periodontales, con vigilancia específica en el control de la placa bacteriana y en las aplicaciones tópicas de flúor.
PROPUESTA
Resulta de enorme relevancia eliminar las enfermedades dentales y periodontales (caries, placa dentobacteriana y cálculo dentario), así como las obturaciones en mal estado, antes de que el paciente inicie su tratamiento de quimioterapia.
Por lo anterior, es primordial efectuar un diagnóstico temprano y un tratamiento adecuado de infecciones virales y micóticas, para evitar infecciones generalizadas al paciente.
Requerimos también de un estudio amplio en cuanto a esta población y otras tratadas con quimioterapia, lo que nos permitirá conocer las alteraciones que se presentan en la calidad enzimática de la saliva y las alteraciones que en la estructura del esmalte se presentan y que afectan la calidad de vida de la población con una supervivencia del cáncer cada día más amplia.
REFERENCIAS
1. López-Ríos O, Tovar-Guzmán V, Lazcano-Ponce E, Hernández-Ávila M. La epidemia de cáncer de mama en México ¿Consecuencias de la transición demográfica? Salud Pública. 1997; 39: 259-265. [ Links ]
2. Boring C, Squires T, Tong T. Cancer around the world, 19861988. Cancer statistics. Cancer J. Clin. 1992; 42: 19-38. [ Links ]
3. Atlanta American Cancer Society. Cancer facts and figures. 1991: 9. [ Links ]
4. Dirección General de Estadística y Evaluación. Secretaría de Salud. Daños a la salud. Boletín de información estadística. 1992; 12. [ Links ]
5. Peterson D, Sonis S. Oral complications of cancer chemotherapy. The Hague: Ed. Martinus Nijhoff Publishers; 1983. pp. 11-12. [ Links ]
6. Wahlin YB, Matsson L. Oral mucosal lesions in patients with acute leukemia and related disorders during cytotoxic therapy. Scand J. Dent Res. 1988; 96 (2): 128-136. [ Links ]
7. Hou GL, Tsai CC. Oral manifestations of agranulocytosis associated with methimazole therapy. J Periodontol. 1998; 59 (4): 244-248. [ Links ]
8. Dreizen M. Oral complications of cancer therapies. Description and incidence of oral complication. NCI Monog. 1990; 9: 11-15. [ Links ]
9. Simard-Savoie S. Oral manifestations in the patient taking anti-neoplastic medication. The role of the dentist. J. Dent Que. 1989; 26: 51-53. [ Links ]
10. Carl W. Oral complications of local and systemic cancer treatment. Curr Opin Oncol. 1995; 7: 320-324. [ Links ]
11. De Vita SH, Helman SA, Rosenberg S. Principles and practice of oncology. 5th edition. Philadelphia: Lippincott Williams & Wilkins; 1997. pp. 2705-2725. [ Links ]
12. National Cancer Institute monographs. Consensus development conference on oral complications of cancer therapies: diagnosis, prevention and treatment. Bethesda: National Institutes of Health; 1990. [ Links ]
13. Hernández-Muñoz GA. Avances en mastología. 2a. ed. Caracas Venezuela: Editorial Cromotip; 1990. pp. 147-155. [ Links ]
14. Frykberg. Management of in situ and minimally invasive breast carcinoma. J. Surgery. 1994; 18: 45-57. [ Links ]
15. Fernández-Ci et al. Anomalías del desarrollo mamario. En: Patología Mamaria. Barcelona: Salvat Editores; 1982. pp. 475-477. [ Links ]
16. Cárdenas J. Primer Consenso Nacional sobre Tratamiento del Cáncer Mamario. Colima, México; Septiembre, 1994. Disponible en: http://www.consensocancermamario.com/documentos/Folleto-Consenso-Nacional-1-Revision.pdf [ Links ]
17. Simon AR, Roberts MW. Management of oral complications associated with cancer therapy in pediatric patients. Journal of Dentistry for Children. 1991; 58: 384-388. [ Links ]
18. Peterson D, Sonis S. Oral complications of cancer chemotherapy. The Hague: Martins Nijhoff Publishing; 1983. pp. 113-149. [ Links ]
19. Dreizen S. Oral complications of cancer therapies. Description and incidence of oral complications. NCI Monogr. 1990; 9: 11-15. [ Links ]
20. Gordon B, Spadinger A, Hodges E, Ruby E, Stanley R, Coccia P. Effect of granulocyte macrophage colony stimulating factor on oral mucositis after hematopoietic stem cell transplantation. Journal of Clinical Oncology. 1994; 12 (9): 1917-1922. [ Links ]
21. O'Sullivan E, Duggal MS, Bailey CC, Curzon MEJ. Changes in the oral microflora during cytotoxic chemotherapy in children being treated for acute leukemia. Oral Surgery, Oral Medicine, Oral Pathology. 1993; 76 (sppl. 2): 161-168. [ Links ]
22. Bunetel L, Martine B, Rennes F. Oral pathoses caused by candida albicans during chemotherapy update on development mechanisms. Oral Surgery, Oral Medicine, Oral Pathology. 1996; 82 (2): 161-165. [ Links ]
23. Chi KH, Chen CH, Chan WK, Chow KC, Chen SY, Yen SH et al. Effect of granulocyte-macrophage colony stimulating factor on oral mucositis in head and neck cancer patients after cisplatin, fluoracil and leucovorin chemotherapy. Journal of Clinical Oncology. 1995; 13 (supl. 10): 2620-2628. [ Links ]
24. Barash A, Peterson D, Tanzer J, D'ambrosio J, Nuk K, Schubet M et al. Helium-neon lasser affects on conditioning induced oral mucositis in bone marrow transplantation patients. Cancer. 1995; 76 (12): 2550-2556. [ Links ]
25. Epstein J, Frances LWW. The efficacy of oral sucralfate suspention in prevention of oral mucositis due to radiation therapy. Int J Radiat Oncol Biol Phys. 1994; 28 (3): 693-698. [ Links ]
26. Osaki T, Elisaku V, Kazunori Y, Josui H, Yetsuya Y. Prophyla-sis of oral mucositis associated with chemoradiotherapy of oral carcinoma by azelastine hydrochloride with other antioxidants. Head and neck. 1994; 16: 331-339. [ Links ]
27. Fidler P, Loprizi Ch, Fallon J, Leitch J, Lee J, Hayes D et al. Prospective evaluation of a chamomile mouthwash for prevention of 5-FU induced oral mucositis. Cancer. 1996; 77 (3): 522-525. [ Links ]
28. Grandisher W. Docetaxel como tratamiento nedyuvante en pacientes con estadio III de cáncer de mama. Oncology. 1997; 8: 15-18. [ Links ]
29. William CW Lawrence S. Management of oral mucositis during local radiation and systemic chemotherapy: A study of 98 patients. J. Prosthetic Dent. 1991; 66 (sppl 3): 361-369. [ Links ]
30. Rosenberg S. Atención bucal de los pacientes bajo quimioterapia. "Care of the mouth". Manual de Oncología. 1989. pp. 227-237. [ Links ]
31. Peterson D. Oral toxicity of chemotherapeutic agents. Semin Oncol. 1992; 19 (5): 478-491. [ Links ]
32. Overhoster CD, Peterson DE. Infection in acute nolynphocytic leukemia prevalence of acute exacervations. Arch Inter Med.1982; 142: 51-54. [ Links ]
33. Ramos de la RC. Manifestaciones orales en pacientes con carcinoma mamario bajo tratamiento de quimioterapia con esquemas a base de adriamicina [Tesis]. México: Hospital General de México; 1999. p. 20. [ Links ]
34. Díaz-Rubio E. Monografías clínicas en oncología: efectos secundarias de la quimioterapia antineoplásica. Vol. II. Barcelona: S. A. Ediciones; 1990. [ Links ]
35. Lockhart PB, Soriss T. Alterations in the oral mucosa caused by chemotherapeutic agents. J. Dental Surgery Oncology. 1981; 7: 15. [ Links ]
36. Lynch M et al. Medicina bucal de Burkcet. la. ed. México: Ed. Mc Graw-Hill Interamericana; 1996. [ Links ]
37. Scully C, Macfarlane TW. Orofacial manifestations of childhood malignancy:clinical and microbiological findings during remission. ASDJ Dent Child. 1983; 50: 121-125. [ Links ]
38. Williams MC, Martin MV. A longitudinal study of the effects on the oral mucosa of treatment for acute childhood leukemia. Inter J Paed Dent.1992; 2: 73-79. [ Links ]
39. Wimenga ANM, Vandergraff WTA, Spijkervet FLK, Times W, Tinner-Bosscha H, Slviter MJ et al. A new in vitro assay for cuan-titation of chemotherapy induced mucositis. British Journal of Cancer. 1997; 76: 1062-1066. [ Links ]
 Dirección para correspondencia:
Dirección para correspondencia:
Enrique Echevarría y Pérez
E-mail: eechevarriayperez@hotmail.com
Nota
Este artículo puede ser consultado en versión completa en http://www.medigraphic.com/facultadodontologiaunam











 texto en
texto en 


