INTRODUCCIÓN
La elevación del piso de seno maxilar con injertos óseos es uno de los procedimientos quirúrgicos utilizado para la reconstrucción del segmento maxilar posterior edéntulo atrófico previo a la colocación de una prótesis fija soportada por implantes endoóseos.
Desde finales de los años 60, Linkow 1 reportó la elevación de la membrana sinusal para la colocación de implantes de navaja. En 1976, Tatum 2 describió un procedimiento utilizando una técnica Caldwell-Luc modificada para tener acceso al seno maxilar e injertarlo con hueso sintético. En 1980, Boyne y James 3 corroboraron esta técnica pero utilizando hueso de la cresta iliaca. Misch en 1987, 4,5 propuso diferentes modalidades de tratamiento con base en la cantidad de hueso remanente entre el piso del seno maxilar y el reborde alveolar, clasificando los senos atróficos en SA1, SA2, SA3 y SA4,(¶) dando parámetros para la colocación simultánea o tardía de implantes endoóseos según fuera el caso. Desde entonces, se han descrito varias técnicas para este procedimiento regenerativo,6,7 y se ha sugerido colocar implantes simultáneamente a la elevación de piso de seno cuando existe un mínimo de 4 a 5 mm de hueso; con menos de esta cantidad se ha recomendado colocarlos en un segundo tiempo quirúrgico.8,9
Los materiales seleccionados para ser injertados deben proveer soporte a largo plazo para los implantes endoóseos.10 Estos injertos son utilizados solos o combinados en diferentes proporciones y en la actualidad incluyen: aloinjertos, materiales aloplásticos, xenoinjertos e injertos autólogos extra e intraorales; siendo estos últimos los más seguros, efectivos y predecibles.11-(26), (12), (13), (14), (15), (16), (17), (18), (19), (20), (21), (22), (23), (24), (25) Estos materiales también se mezclan con factores de crecimiento o proteínas óseas.27-(40), (28), (29), (30), (31), (32), (33), (34), (35), (36), (37), (38), (39
El papel de los factores de crecimiento en la cicatrización de las heridas fue descrito por Knighton y Hunt en los 80;41),(42 y por Marx en los 90.43 Este último desarrolló un método para obtener dichos factores mediante el centrifugado de sangre, al que llamó plasma rico en plaquetas (PRP). El PRP es un concentrado plaquetario autólogo (1'000,000 plaquetas/uL), es un material seguro, no transmite enfermedades infectocontagiosas 44,45 y puede ser obtenido a través de diversos métodos de concentración plaquetaria.46)-(51), (47), (48), (49), (50 Una vez en contacto con trombina y cloruro de calcio, las plaquetas liberan factores de crecimiento como el derivado de las plaquetas, transformante-B, endotelial vascular y epitelial, entre otros, los cuales son media dores biológicos naturales que regulan la proliferación, diferenciación y quimiotaxis celular, así como también la síntesis de matriz extracelular.43,(52),53 El PRP ha mostrado ser efectivo en la regeneración ósea, acelerando los tiempos de osificación, así como de oseointegración de los implantes, reduciendo el tiempo total de tratamiento en casi el 50% (de 18 a 10 meses).28
El propósito de este reporte es presentar un caso clínico en el cual se rehabilitaron 2 zonas maxilares posteriores atróficas edéntulas con prótesis fijas implantosoportadas, realizando la elevación bilateral de piso de seno maxilar, injertando hueso autólogo y aloinjerto combinados con PRP, con la colocación simultánea y tardía de implantes endoóseos, resaltando los beneficios clínicos observados con el tratamiento regenerativo.
REPORTE DEL CASO CLÍNICO
Una paciente de 55 años de edad acudió a la Clínica de Periodoncia de la División de Estudios de Postgrado e Investigación, Facultad de Odontología, de la Universidad Nacional Autónoma de México, referida por el Departamento de Prótesis Bucal, para realizar un tratamiento que incluyó la elevación de piso de seno maxilar bilateral con el fin de colocar implantes endoóseos en las zonas maxilares posteriores. Radiográficamente los senos maxilares se observaron neumatizados (Figura 1), por lo que existía una dimensión vertical insuficiente del reborde óseo, pero con una relación interarcada adecuada. De acuerdo con la clasificación de Misch los senos fueron clasificados como SA2 (1 etapa: regeneración ósea y colocación simultánea de implantes) y SA3 (2 etapas: regeneración ósea y colocación tardía de implantes) derecho e izquierdo respectivamente, por lo cual se elaboró el siguiente plan de tratamiento:
PLAN DE TRATAMIENTO
FASE QUIRÚRGICA EN 2 ETAPAS
Primera etapa:
Elevación bilateral de piso de seno maxilar, utilizando hueso autólogo intraoral y aloinjerto mezclados con PRP.
Colocación inmediata de 2 implantes endoóseos en la zona edéntula superior derecha.
Segunda etapa: 5 meses después
Fase protésica: 10 meses después
PROCEDIMIENTO QUIRÚRGICO
Preparación del PRP
En este procedimiento se utilizó el sistema Platelet Concentrate Collection System (PCCS, Implant Innovations, Inc. Palm Beach Gardens, FL 33410), sistema aprobado por la FDA. Antes de la cirugía se recolectaron 54 mL de sangre del paciente con una jeringa hipodérmica de 60 mL, con 6 mL de anticoagulante (citrato de dextrosa), tomada de la vena mediana cubital, depositándose en un contenedor plástico para su procesamiento.
Concentración plaquetaria: El contenedor fue sometido a un doble centrifugado a 3,000 rpm:
1ero: 4 minutos (fase de separación de los elementos celulares).
2do: 13 minutos (obtención del concentrado plaquetario).
Se obtuvieron aproximadamente de 7 a 8 mL de PRP (Figura 2), el cual se homogenizó presionando el contenedor ligeramente con la yema de los dedos.
Obtención y preparación del injerto óseo:
Se tomó hueso autólogo de las tuberosidades maxilares de ambos lados, así como también de un torus mandibular unilateral del lado izquierdo, de aproximadamente 8 mm de diámetro. A estas tomas se añadieron 5 g de aloinjerto (hueso congelado liofilizado) con el fin de aumentar el volumen. Se obtuvo un total de 8 cc de injerto óseo en una proporción de 2:1 (aloinjerto: autoinjerto) y se agregaron 4 cc de PRP sin activar con el fin de hidratarlo. Este total fue dividido en 2 porciones iguales, una para cada seno.
Elevación de piso de seno maxilar
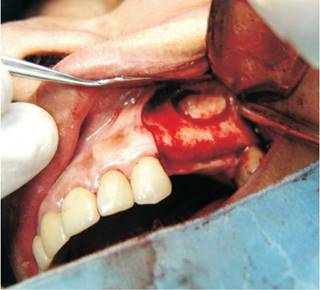
De acuerdo con la técnica descrita por Boyne y posteriormente por Woo y Garg,3,(6),7 primero se realizó una incisión horizontal ligeramente palatina sobre el reborde alveolar, extendiéndola más allá del borde anterior y posterior del seno maxilar con una incisión liberatriz anterior distal al canino. La pared lateral del maxilar fue expuesta al levantar superiormente el colgajo mucoperióstico de espesor total hasta la base del hueso malar. Se demarcó una ventana oval de 10 x 15 mm (acceso tipo Cadwell-Luc) (Figura 3), con una fresa de bola # 8 de baja velocidad, irrigando con suero fisiológico. Con un instrumento romo, la ventana ósea fue fracturada y completamente liberada del maxilar sin perforar la membrana sinusal; ésta fue despegada y proyectada medial y superiormente, liberándola de las paredes anterior, media y posterior del seno maxilar.
Una vez elevada la membrana sinusal, se procedió a preparar los lechos quirúrgicos para los implantes de acuerdo con la guía quirúrgica previamente elaborada. Una porción del injerto óseo con PRP fue activada con 2 gotas de trombina bovina (1,000 u de trombina bovina/1 mL de cloruro de calcio). Una vez que el injerto tomó una consistencia gelatinosa (Figura 4) se procedió a introducirlo al seno. Ya injertado el seno maxilar derecho en un 50%, procurando llenar primero la zona medial, se colocaron los implantes endoóseos y se terminó de llenar el seno maxilar con el injerto. Finalmente se elaboró una membrana de fibrina autóloga utilizando 1 cc de PRP, la cual fue colocada sobre la pared lateral del maxilar cubriendo el injerto y la ventana ósea. El colgajo fue reposicionado en su lugar utilizando una sutura absorbible (ácido poliglicólico 4-0 VYCRIL®). El seno maxilar izquierdo fue elevado con la misma técnica pero no se llevó a cabo la colocación de implantes. Se realizaron revisiones clínicas postquirúrgicas a los 4 días y a las 1, 3 y 4 semanas. La sutura fue retirada 1 semana después a la intervención quirúrgica (Figura 5).

Figura 5 Radiografía panorámica. 1 mes después de la primera cirugía, se observa ganancias en altura de los rebordes alveolares regenerados con injertos óseos.
Después de 5 meses se realizó la segunda etapa quirúrgica colocando 2 implantes endoóseos en la zona edéntula izquierda, de acuerdo a una guía quirúrgica previamente fabricada y siguiendo el protocolo establecido. La sutura fue retirada 7 días después y se realizaron revisiones clínicas postquirúrgicas a los 7, 15 y 30 días (Figura 6). El tratamiento farmacológico en ambas etapas quirúrgicas incluyó: Amoxicilina (750 mg c/12 h/8 días) e ibuprofeno (400 mg c/6 h/5 días), comenzado 24 horas antes de cada intervención quirúrgica.

Figura 6 Radiografía panorámica a los 10 meses del inicio, con la colocación de 2 implantes del lado izquierdo.
Los 4 implantes colocados fueron de la marca 3i Osseotite (Parallel-Walled Implants, Implant Innovations, Inc Palm Beach Gardens, FL 33410), dos de 4 mm de diámetro por 15 mm de largo en la zona de premolares y dos de 5 mm de diámetro por 15 mm de largo en la zona de molares.
A los 10 meses del inicio del tratamiento y habiéndose realizado un seguimiento radiográfico y clínico del caso, se programó el descubrimiento de los 4 implantes para la colocación de los tornillos de cicatrización. Utilizando el protocolo quirúrgico establecido para esta fase, se retiraron los tornillos tapas y se colocaron los tornillos de cicatrización, de 4 x 3 mm y de 5 x 3 mm, en los implantes anteriores y posteriores respectivamente. Los cuidados postoperatorios incluyeron paracetamol 500 mg 1 tableta c/8 h por 5 días y la aplicación de gel de clorhexidina 2 veces al día.
La fase protésica fue realizada en el Departamento de Prótesis de la División de Estudios de Postgrado e Investigación, Facultad de Odontología, de la Universidad Nacional Autónoma de México de acuerdo al plan de tratamiento.
RESULTADOS
En la primera etapa quirúrgica la preparación del PRP fue un procedimiento sencillo y limpio y la cantidad obtenida fue suficiente para el procedimiento regenerativo. El PRP al combinarlo con el injerto óseo facilitó su manipulación al momento de ser introducido al seno maxilar. En las revisiones posteriores a la intervención quirúrgica, a los 4 y 7 días después del procedimiento, los bordes de las heridas de los colgajos se observaron afrontados, sin signos de dehiscencia ni de inflamación. La paciente no refirió ninguna molestia sinusal a lo largo del tratamiento, así como tampoco se observaron signos de inflamación ni de dolor en las zonas tratadas. En una radiografía panorámica tomada una semana después de la cirugía se observó un aumento en la dimensión vertical del reborde de 12 mm del lado derecho y de 13 mm del lado izquierdo.
Pasados 10 meses, durante la colocación de los tornillos de cicatrización, no se percibió movilidad de los implantes y a las pruebas de percusión se percibieron sonidos sólido-sordos. El paciente no refirió dolor, no se observó salida de material purulento ni signos de inflamación y radiográficamente no se observaron sombras radiolúcidas peri-implantares.
A través de un seguimiento durante los 28 meses posteriores a las elevaciones de piso de seno, se mantuvo el resultado exitoso, con base en las revisiones clínicas y controles radiográficos realizados cada 6 meses, parámetros clínicos que se consideran como criterios de éxito para los implantes oseointegrados.(65) En la última revisión de control, 28 meses, se observó una ganancia de hueso regenerado de 11 mm del lado derecho y de 12 mm del lado izquierdo, el hueso injertado se observó de la misma densidad que el hueso perisinusal en ambos sitios. Se perdió 1 mm de cresta ósea peri-implantar sólo en los implantes distales (Figura 7). Clínicamente se realizaron pruebas de movilidad y percusión sobre las prótesis y la paciente no refirió dolor, así como tampoco molestias sinusales hasta la última revisión.
DISCUSIÓN
Existen varios procedimientos de reconstrucción ósea del segmento maxilar posterior edéntulo atrófico; uno de ellos es la elevación del piso del seno maxilar, el cual tiene por objetivo aumentar sólo la dimensión vertical del reborde óseo. De acuerdo al diagnóstico y análisis radiográfico y de modelos montados en articulador de las zonas edéntulas se determinó realizar elevaciones de seno maxilar bilaterales para la posterior colocación de implantes de suficiente longitud.9 Este caso era ideal, ya que la relación inter-arco no estaba alterada y sólo estaba disminuida la dimensión ósea vertical. En los últimos 25 años el procedimiento de elevación del piso del seno maxilar con injertos óseos ha ido evolucionando por la introducción de diversos materiales, incluyendo la utilización de factores de crecimiento desde 1998 43 incrementando su tasa de éxito significativamente. Al controlar las diferentes variables 7 la morbilidad es baja y las complicaciones postoperatorias pueden ser tratadas fácilmente.7,10
La técnica quirúrgica utilizada en este caso clínico, abordaje a través de la pared lateral del seno maxilar, está indicada cuando la altura del reborde óseo es menor a 4 mm y se desea incrementarla para la colocación de implantes de una longitud mínima de 10 a 13 mm, por lo que se requiere injertar el seno en suficiente cantidad para cubrir esta necesidad,5-(7),9 además de también considerar la longitud de las brechas edéntulas para realizar este procedimiento.
La colocación de implantes endoóseos, simultánea a la elevación de piso de seno, es realizada siempre y cuando se pueda obtener una estabilidad primaria del implante dentro del reborde óseo residual. La cantidad de hueso remanente, tanto en sentido vertical como horizontal, va a proporcionar la estabilidad primaria que un implante requiere para aumentar su tasa de éxito.5-10),(66) En el lado derecho, puesto que se tenía una altura ósea por arriba de los 4 mm, se pudieron colocar y estabilizar los implantes en el mismo acto quirúrgico, mientras que en el lado izquierdo, con una menor altura del reborde, se decidió colocarlos en un segundo acto quirúrgico posterior, aunque existen re portes que sugieren que aun en rebordes de altura mínima pueden ser colocados simultáneamente si se logra estabilizarlos.54),(55 El éxito del procedimiento no depende de la colocación inmediata o en un segundo tiempo quirúrgico de los implantes, sino de su estabilidad primaria.8)-(10),(54),(56
Diversos tipos de injertos han sido utilizados en la elevación de piso de seno, encontrándose que los sustitutos óseos, aloinjertos, xenoinjertos y materiales aloplásticos -utilizados solos o combinados con autoinjertos en diferentes proporciones- son igual 11)-(26 o mayormente9 efectivos si se comparan con los autoinjertos solos. Utilizar sustitutos óseos disminuye la necesidad de otros sitios quirúrgicos.8 En este caso, debido a la magnitud del procedimiento, se utilizó una mezcla aloinjerto-autoinjerto intraoral en una proporción de 2:1, con la cual se obtuvo la cantidad suficiente y necesaria para realizar el procedimiento bilateralmente. Los autoinjertos intraorales son osteogénicos, osteoinductivos y osteoconductivos, además de tener una menor tasa de reabsorción que los extraorales, los cuales podrían obtenerse en mayor cantidad, pero a expensas de procedimientos quirúrgicos adicionales y con posible riesgo de falla por neumatización del seno.8,57 La mezcla utilizada en el presente caso resultó ser exitosa para el resultado final del tratamiento, ya que en ambos sitios se obtuvo estabilidad de la rehabilitación implanto-soportada 28 meses después del procedimiento.
Existe una gran controversia en cuanto a la utilidad del PRP en la cicatrización de heridas e injertos. Algunos estudios indican que el PRP puede incrementar la regeneración ósea cuando se combina con autoinjertos particulados combinados con sustitutos óseos,44),(58)-(60), (59 pero otros estudios no han encontrado un valor biológico con su utilización.61)-(63), (62 Weibrich 46,47 comparó los niveles de factores de crecimiento en PRP obtenidos por dos protocolos diferentes: el PCCS 1 y el Cura-san y concluyó el PCCS 1 obtuvo niveles más altos en el conteo del concentrado plaquetario y un contenido más alto de factores de crecimiento. Además de ser un sistema aprobado por la FDA.
Aun con estos antecedentes, las observaciones de este caso permiten afirmar que el PRP tuvo una gran utilidad clínica, ya que al mezclarlo con los injertos óseos se obtuvo un material a manera de masilla, de una consistencia el cual permitió una fácil y rápida manipulación al momento de rellenar la cavidad formada en el piso de seno, evitando que el injerto se dispersara fuera de su lugar, de manera irregular, dentro del sitio quirúrgico aun antes, durante y después de la colocación de los implantes y favoreciendo una densidad uniforme del injerto. Con la utilización del PRP, también se ha reportado un resultado clínico muy favorable en la cicatrización de los tejidos blandos de las heridas quirúrgicas en términos de un menor tiempo para lograr el cierre completo y de menores complicaciones postquirúrgicas como dehiscencias o fenestraciones;10 como pudo ser observado en este caso, puesto que no se tuvieron contratiempos durante la fase de cicatrización y aparentemente ésta ocurrió en un menor tiempo, aun en ausencia de algún otro sitio que sirviera como control para hacer comparaciones.
Una ventaja principal que brinda el PRP es el menor tiempo para realizar la exposición de los implantes. Un estudio previo mostró que implantes con una estabilidad primaria comprometida requerían un mayor tiempo de cicatrización antes de ser cargados protésicamente; los implantes son normalmente expuestos después de 9 meses.28 En este caso clínico el uso de PRP permitió que este periodo de exposición se redujera en un 50% sin comprometer el resultado final del tratamiento.
CONCLUSIÓN
La elevación bilateral de piso de seno maxilar, utilizando aloinjerto y autoinjerto óseo en proporción 2:1 con plasma rico en plaquetas, resultó ser un procedimiento exitoso, el cual sirvió como un importante coadyuvante en la cicatrización de tejidos duros y blandos y permitió la colocación simultánea y tardía de implantes endoóseos para la rehabilitación protésica implanto-soportada. El resultado del tratamiento fue exitoso a 28 meses y se redujo en un 50% el tiempo total del proceso.











 nova página do texto(beta)
nova página do texto(beta)