Introducción
Es muy importante para la formación de recursos humanos de los futuros profesionistas concientizarlos sobre la relevancia del control de todo tipo de procesos en particular del de Limpieza ya que es una posible fuente de contaminación cruzada, si no se siguen las medidas de bioseguridad.
Las interacciones con el medio ambiente, el desarrollo tecnológico, las actividades sociales y económicas, degradan los ecosistemas; en años recientes los procedimientos de limpieza han tomado gran importancia y se deben de aplicar de acuerdo a las Buenas Prácticas de Fabricación(BPF)1,2 y por medio de un protocolo de validación del procedimiento de limpieza, es útil la determinación de la toxicidad aguda que pudiese tener el residuo y para lo cual se pueden utilizar diferentes modelos biológicos.1,2,3,4,5
El arsenal de los productos de limpieza es muy basto e incluye bio-controladores, inactivadores, detergentes, sanitizantes y desinfectantes; se miden visualmente, sensorialmente, macroscópicamente y microscópicamente; para determinar la bioseguridad se requierede la máxima eficacia en sus programas de limpieza. La adecuada elección del producto de limpieza (detergente y/o sanitizante) a emplear se basan en los datos técnicos: características físicas y químicas, ingredientes y riesgos tanto físicos como en salud, datos de reactividad, síntomas de sobre-exposición, precauciones para su uso y seguridad así como procedimientos de primeros auxilios, justificación científica de su uso, así como conocer la superficie de aplicación, la cual debe estar libre de residuos de materiales y grasa; se debe considerar también la dureza del agua, el pH y su temperatura. Se utiliza el producto según las especificaciones del fabricante de acuerdo a la ficha técnica del producto sanitizante seleccionado (concentración, tiempo de aplicación, frecuencia de uso) y después de su aplicación se enjuaga con abundante agua, de acuerdo con las exigencias de las normas y protocolos vigentes. La eficacia en los proceso de limpieza e higiene depende de que se haya hecho la adecuada elección del producto de limpieza, la temperatura, la dureza y el pH del agua utilizada, tiempo de contacto del producto y su forma de aplicación (concentrado, solución, espuma, inyección, aspersión, vaporizado, rociado, inmersión recirculación, restregado, trapeado, limpiado, etc.) se debe realizar un monitoreo ambiental para asegurar que no quedó ningún residuo visible en el equipo y área de trabajo una vez aplicados los procedimientos de limpieza.1,6
En un modelo educativo integral es muy importante concientizar a los alumnos en proceso de formación en la licenciatura en QFB de la UAM-Xochimilco, la relevancia de esta temática desde el punto de vista de la eficacia del proceso mismo de limpieza así como de la protección ecológica que se debe de prever.
El proceso estandarizado de sanitización (POES)
Es un sistema integral y continuo, consistente en la reducción del número de microorganismos a un nivel que no signifique contaminación nociva del producto elaborado, pero que se ajuste a los límites aceptados, sin disminuir su calidad mediante el empleo de agentes químicos (productos de limpieza: sanitizantes) además de utilizar los métodos higiénicamente satisfactorios aplicando los reglamentos de condiciones ambientales y sanitarias en el lugar de trabajo.3,7 El operador deberá portar el uniforme y ropa de trabajo adecuada (guantes, lentes de seguridad) para dicho fin.8
De manera general en las operaciones de limpieza se deben de considerar varios puntos para la elección delos productos de limpieza: Ser específico para el lugar de trabajo donde será aplicado, debe tener una buena actividad desengrasante, el detergente seleccionado es seguro (biodegradable) tanto para las personas como para los animales; se deben seguir las instrucciones de uso indicadas por el fabricante, hay que saber si interfiere con la actividad del desinfectante, es necesario saber si se puede aplicar con el actual equipo con mínimas modificaciones, saber si dejará residuos o no; debe ser alcalino. Es mejor sí posee acción espumante.9
Además se busca que los productos químicos de limpieza sean ecológicos y estén certificados. Lo cual no significa que sean seguros; por lo tanto hay que tratar de seleccionar los menos peligrosos, para los usuarios (alumnos en un laboratorio de enseñanza, hasta los operadores en las áreas industriales).10
Etapas del proceso de sanitización
Adecuada elección del agente sanitizante.
Enjuague del área de trabajo, con lo que se consigue la eliminación de la suciedad excesiva de las instalaciones.
Limpieza, con la aplicación de detergentes con el fin de eliminar la suciedad adherida a las superficies.
Aclarado, para la eliminación de las sustancias detergentes y sanitizantes empleadas en la limpieza.
Aplicación de sustancias desinfectantes para la destrucción de la carga microbiana.
Aclarado final para la eliminación de los residuos de los desinfectantes aplicados anteriormente.9
Se deben cambiar los productos de limpieza elegidos para evitar que se desarrolle resistencia bacteriana y evitar contaminaciones cruzadas.
La diferencia entre un desinfectante y un sanitizante está determinada por la concentración y dilución utilizadas del producto, por ejemplo un yodoforo a 25 ppm se considera que actúa como sanitizante, mientras que a 75 ppm se considera como desinfectante; por lo tanto él desinfectante debe tener una mayor capacidad para matar bacterias patógenas en comparación con la de un sanitizante (debe ser capaz de eliminar en 30 segundos, el 99.99 % de las bacterias patógenas de prueba; pero no destruye esporas o virus).11,12,13 Para eliminar las esporas se emplean agentes químicos o medios físicos (remoción mecánica, calor seco o calor húmedo).
El sanitizante más adecuado ofrece una buena esterilización, sin dañar otras formas de vida, no es corrosivo y es barato; desafortunadamente, los sanitizantesy desinfectantes ideales no existen. Debido a su naturaleza química los sanitizantes, desinfectantes, son potencialmente perjudiciales (incluso tóxicos) para los animales y los seres humanos, por lo tanto deben ser tratados con el cuidado apropiado, la mayoría de los envases que los contienen traen las instrucciones necesarias de seguridad, que deben leerse en su totalidad antes de usar el producto.
La mayoría de los materiales con poder bactericida (germicidas) contienen benzoato de denatonio que es un catión de amonio cuaternario, comercialmente llamado Bitrex, una sustancia amarga diseñada para desalentar su ingestión, como una medida de seguridad añadida.
Los desinfectantes y sanitizantes que se utilizan en espacios cerrados no deben mezclarse con otros productos de limpieza porque pueden generar vapores al ocurrir reacciones químicas secundarias, por lo que se sugiere trabajar en un área ventilada y así disminuir el riesgo de intoxicación. Son utilizados con frecuencia en hospitales, clínicas dentales, cocinas y cuartos de baño, en industrias del ramo alimentario, en la Industria Químico Farmacéutica, etc., para matar microorganismos infecciosos.
La elección de la solución sanitizante o desinfectante que se utilizará depende de cada situación en particular. Algunos tienen un amplio espectro (matan a casi todos los microorganismos), mientras que otros tienen efecto en un espectro más reducido de microorganismos patógenos; pero se prefieren por sus otras propiedades (como no ser corrosivos ni tóxicos, o de bajo costo).
Clasificación de los sanitizantes
A través de la historia se han utilizados diferentes tipos de sanitizantes: alcohólicos, aldehídicos, halogenados, fenólicos, compuestos de amonio cuaternario.
Alcoholes: Los más comunes son el etanol y el alcohol isopropílico, que al ser más volátiles, se evaporan con rapidez; presentan un amplio poder microbicida para una mejor desinfección, no son corrosivos, pero son peligrosos ya que son inflamables y explosivos. Tienen limitada actividad residual debido a su fácil evaporación, lo que resulta en un breve contacto y tienen una limitada actividad en presencia de material orgánico. Son más eficaces en combinación con agua purificada (alcohol isopropílico al 70 % y el alcohol etílico al 62 % es más efectivo que el alcohol del 95 %). Los alcoholes no son eficaces contra hongos o esporas bacterianas.
Aldehídos: Como glutaraldehído, son buenos microbicidas, esporicidas y fungicidas, que no dejan casi residuos aunque se inactivan parcialmente en presencia de compuestos orgánicos.
Halogenuros: Como la Cloramina-T se utiliza en el tratamiento de agua potable en lugar del cloro, ya que produce un menor número de subproductos derivados de la desinfección. Mantiene su acción antibacteriana incluso después de que el cloro se haya agotado.
Cloro e Hipocloritos: El cloro se utiliza comúnmente en el hogar para la desinfección de los tinacos, cisternas, baños, patios, drenajes. Los hipocloritos de sodio, de calcio y las soluciones de hipobromito también se utilizan, sobre todo como aditivos en las albercas evitando el crecimiento de algas, bacterias y los malos olores.
Yodo: Se utiliza como antiséptico para la piel en raspones y cortadas.
Fenólicos: Son los ingredientes activos en varios sanitizantes de uso común, en enjuagues bucales y en jabón para manos. Probablemente son el sanitizante más antiguo que se conoce, ya que fue usado por primera vez en 1865 por Joseph Lister (fundador de la medicina antiséptica y preventiva), cuando se llamaba ácido carbólico. Es corrosivo para la piel y algunas personas son sensibles a sus vapores tóxicos, existen varios tipos de derivados fenólicos como son: o-fenilfenol utilizado frecuentemente en lugar de fenol, ya que es menos corrosivo. Hexaclorofenol: es un compuesto fenólico que fue utilizado como aditivo germicida en algunos productos para el hogar, pero fue prohibido debido a la sospecha de efectos nocivos.
Quats (Compuestos de amonio cuaternario): como el cloruro de benzalconio, se ha utilizado como sanitizante de bajo nivel, es eficaz contra algunas especies de bacterias, pero no sirven contra Pseudomonas, o en esporas bacterianas. Los quats son biocidas que también matan a las algas y se utilizan como aditivos a gran escala en sistemas de abastecimiento de agua industrial para reducir al mínimo el crecimiento de gérmenes biológicos.
Empleo de sustancias fotoactivas como el dióxido de titanio (TiO2) son activadas por la presencia de luz ultravioleta, generando un efecto antimicrobiano.12,13,14
Muchos de los sanitizantes y detergentes están hechos en base a amonios cuaternarios de cuarta generación. Desengrasan, limpian, desinfectan y desodorizan en una sola etapa; debido a su alta concentración son efectivos contra bacterias y virus, por lo que se consideran como agentes biocidas, las cuales se han empleado desde hace mucho tiempo; pero solamente en fechas recientes se ha logrado crear conciencia en el público usuario, en cuestiones de higiene; por ejemplo a bajas concentraciones presentan una acción reversible en la membrana citoplasmática y por inhabilitación de la capacidad enzimática de los microorganismos.15
La Industria químico farmacéutica requiere la determinación de límites de aceptación para las diferentes sustancias utilizadas tanto en la manufactura de los medicamentos, así como de las sustancias utilizadas en los POES, tal es el caso de los agentes bio-controladores (ab-c) empleadas en los procesos industriales de limpieza, evitando de esta manera la contaminación cruzada de los medicamentos a través del límite en la dosis del residuo de los principios activos y del límite de residuo en la muestra de análisis correspondiente a los propios residuos de las sustancias empleadas en la limpieza; permitiendo que los medicamentos sean seguros y cumplan con la Norma Nacional SSA-059-2006, así como con la regulación internacional de la Food and Drug Administration de los Estados Unidos (FDA), la norma CFR21 fue dictada por la FDA y permite el uso de tecnología electrónica, así como indicadores biométricos dentro de la Industria Químico Farmacéutica, para identificar al personal que ahí labora, en la Comunidad Europea y Sistema de Calidad Farmacéutico de acuerdo con la Conferencia Internacional de Armonización (International Conference on Harmonisation, ICH Q7A)15 los fabricantes de medicamentos en la Unión Europea están obligados a establecer e implementar un sistema efectivo de aseguramiento de calidad farmacéutico, con el fin de cumplir con las "Buenas prácticas en la Fabricación". Por lo tanto se requiere evaluar la toxicidad aguda (DL50), estos procesos de limpieza deben contar con matrices de riesgo en donde se evalúen diferentes propiedades de los residuos, resultando ser la más importante "toxicidad de los residuos"; la estimación del límite de aceptación para el peor de los casos debe realizarse en base a los datos técnicos que sean justificados científicamente, de tal forma que el valor para estimar el límite de aceptación en base a la toxicidad es el valor de la DL50 obtenida de estudios de toxicidad aguda. De manera general las sustancias químicas contenidas en los productos de limpieza, detergentes y desinfectantes pueden irritar los ojos, nariz, garganta, pulmones, ocasionando problemas respiratorios o desencadenar asma, causar salpullido en la piel produciendo quemaduras o incluso causar la muerte del trabajador; por tal motivo en la actualidad se busca que estos productos sean seguros y ecológicos para evitar la contaminación de los mantos acuosos por la actividad antropogénica.1,6,16
Como trabajan los agentes antimicrobianos
Cuando una bacteria es expuesta a un sanitizante o desinfectante su estructura celular puede sufrir daños irreversibles. La pérdida permanente de la capacidad de reproducirse se denomina muerte microbiana.
En presencia de sustancias germicidas, algunas bacterias son parcialmente dañadas. Es por ello que superficies muestreadas con hisopos, inmediatamente después de ser sanitizadas proveen resultados adecuados sobre una efectiva sanitización. No obstante, dependiendo del grado y concentración de la sustancia empelada, algunas bacterias parcialmente inactivadas pueden regenerarse dentro de las siguientes 18 a 24 horas.
Una superficie aparentemente limpia y libre de bacterias puede presentar una elevada contaminación bacteriana al día siguiente y si no es verificada debidamente puede contaminar cualquier cosa que entre en contacto con dicha superficie; dañando tanto alimentos, como consultorios, material quirúrgico, clínicas, mesas de trabajo, etc. La efectividad de germicidas específicos depende de diversos factores, incluyendo el número y el tipo de microorganismo presente en la superficie a sanitizar.
Es también importante considerar que si las bacterias se encuentran en su estado vegetativo son fáciles de eliminar, pero no así si se encuentran como esporas altamente resistentes.
Así mismo, se deben tener en cuenta la presencia de restos orgánicos, sangre u otros elementos que pueden transformar en agentes contaminantes.
Los sanitizantes son sustancias que reducen el número de microorganismos a un nivel seguro, poseen propiedades germicidas o antimicrobianos y se aplican a todo tipo de superficies para destruir los microorganismos durante el proceso de sanitización.
Acción biológica de los sanitizantes
Destructores de la membrana celular: Son germicidas como el hipoclorito de sodio o ácido peracético, que son agentes altamente oxidantes y pueden causar la destrucción total de la membrana celular, matando al microorganismo se ha estandarizado su uso para acabar con distintas esporas tales como Clostridium sporogenes PA3679, Geobacillus stearothermophilus, Moorella thermoacetica/thermoautotrophica que se encuentran en suspensión sobre superficies de acero inoxidable.18
Inhibición de la alimentación bacteriana y de la eliminación de desechos: Algunos germicidas como los compuestos de amonios cuaternarios, tienen la capacidad de adherirse a lugares específicos de la membrana celular de las bacterias. Esto se debe a que los amonios cuaternarios poseen una carga positiva en solución y se adhieren a ciertas partes de la membrana celular con carga negativa. De esta manera evitan que la bacteria tome nutrientes y previene la eliminación de desechos que se acumulan dentro de su estructura.19 La célula muere por falta de nutrientes y por contaminación por los desechos acumulados en su interior.
Inactivación de enzimas críticas: Biocidas, como compuestos fenólicos, entran en la célula bacteriana y reaccionan químicamente con ciertas enzimas vitales que sustentan tanto el crecimiento, como actividades metabólicas que le proveen energía a la bacteria para poder reproducirse. Si este mecanismo no se realiza en forma completa la bacteria puede regenerarse nuevamente luego de varias horas y contaminar nuevamente la superficie.
Existen metodologías analíticas como la cromatografía de gases acoplada a espectroscopia de masas (GC-MS) que permiten la determinación de los residuos químicos, pero estos equipos son costosos y no siempre están al alcance; por lo tanto algunos modelos biológicos siguen siendo representativos y aportan suficiente información, que demuestra el riesgo en salud de una constante exposición a agentes sanitizantes que a una alta concentración causan intoxicación e incluso la muerte.
Por lo tanto estos modelos biológicos deben estar supervisados por un comité de ética para asegurar que la manipulación, daño y muerte en caso de suceder en especies animales predeterminadas por ejemplo la artemia salina y ratones; no es en vano su manipulación y sacrificio.
Las artemias salinas son animales acuáticos fáciles de conseguir y mantener, además de ser muy sensibles a los cambios de su medio ambiente, lo que los convierte en un adecuado modelo para probar la toxicidad de los agentes sanitizantes a diferentes concentraciones.
Por otro lado el modelo de los ratones nos permitió determinar de manera directa el daño que se produce en un organismo vivo por la ingesta accidental de sanitizantes, no removidos adecuadamente de las áreas y equipos de trabajo que requieren su uso.
Por lo tanto consideramos que estos modelos son económicos y representativos a nivel educativo, para concientizar sobre el riesgo sanitario del uso inadecuado de agentes sanitizantes.
Los objetivos de la presente investigación fueron:
Diseñar un modelo eco-toxicológico económico, rápido y confiable que permita orientar a los alumnos en proceso de formación de la carrera de QFB, sobre la relevancia y riesgos del proceso de limpieza, (modelo de la artemia salina).
Determinar el valor de DL50 correspondiente a la toxicidad aguda, en ratones macho NIH de aproximadamente 18 ± 5 g, para utilizarlo como un indicador acerca del criterio de aceptación para los residuos de sustancias utilizadas en los procesos de limpieza.
Crear consciencia sobre el uso adecuado de estas sustancias, tratando de evitar dañar el medio ambiente.
Material y métodos
Existe una gran cantidad de productos que se pueden utilizar en los procesos de limpieza, por lo que fue necesario hacer una revisión bibliográfica de la toxicidad de los principios activos que conforman al ab-c de la cual se partió como dosificación de inicio, para establecer de manera experimental el umbral de prueba (dosis mínima y máxima).
Cajas Petri de vidriomarca Pyrex
Pipetas de 1 mL
Jeringas desechables de polietileno de 1 y 3 mL
Jaulas de acrílico con tapa metálica para ratón acondicionadas al bioterio
Cánula de acero inoxidable para administración oral
Bebederos yalimentocomprimidopara ratones Aserrín
BalanzaOhaus "Scout Pro"
Aceite de maíz
Sanitizante 1 Detergente líquido, de respuesta rápida, 100 % biodegradable, multifuncional, pH neutro, presenta total solubilidad y micro espuma, de bajo residuo y de menor consumo de agua en los enjuagues debido a que su composición básica contiene sustancias secuestrantes y de secado rápido y 2 es un sanitizante con actividad antiviral que contiene sales bencílicas de sodio, existentes comercialmente en el mercado.
Modelo Biológico 1: Se utilizaron ejemplares adultos de artemia miden de 10 a 20 mm de longitud, se caracterizan por un cuerpo alargado con dos ojos complejos pedunculados, un aparato digestivo lineal, unas anténulas sensoriales y 11 pares de toracópodos funcionales; para el bioensayo se utilizaron 10 mL de solución salina, adicionada al agua comercial de la artemia salina, se colocaron de 2 a 4 artemias salinas en media caja petri y se le agrega 1 mL de la solución delos agentes sanitizantes en estudio: desinfectante fenólico (df) y agente bio-controlador (ab-c), se tomó el tiempo en que manifestaron algún cambio (intoxicación o muerte), se utilizó este modelo por ser accesible y muy sensible a los cambios de su entorno.
Modelo Biológico 2: Debido a que el ab-c mató más rápido a las artemias se procedió a probar sus diluciones y de manera concentrada por medio del modelo "murino clásico" para la determinación de la toxicidad aguda, determinándose la DL50 utilizando ratones macho, de la cepa NIH con un peso corporal aproximado de 18 ± 5 g, los cuales fueron pesados y marcados de manera individual y se mantuvieron bajo condiciones controladas de Bioterio (temperatura controlada 22 ± 2 °C, ciclo de luz/oscuridad 12 - 12 horas, con libre acceso al agua y alimento) de acuerdo a la norma NOM-zoo-062, al grupo testigo se le administró aceite de maíz, se distribuyeron en varios grupos (n = 4) de manera aleatoria para probar el ab-c en estudio y determinar las dosis máximas y mínimas, la cual se administró con una jeringa desechable de polietileno de 1 mL con cánula de acero inoxidable por la vía oral, a varias dosis 0.0205, 0.0103, 6.833 x 10-3, 5.12 x 10-3, 2.563 x 10-3, 1.708 x 10-3, 8.54 x 10-4. Y para la prueba de toxicidad aguda la n = 14, observado a los animales por un periodo de 24 h.
Resultados y discusión
En la Tabla 1 se muestran las propiedades químicas de los sanitizantes y desinfectantes indicando el rango de pH y la concentración en que se utilizan comúnmente en los procesos de limpieza.
Tabla 1 Propiedades químicas de los sanitizantes y desinfectantes17
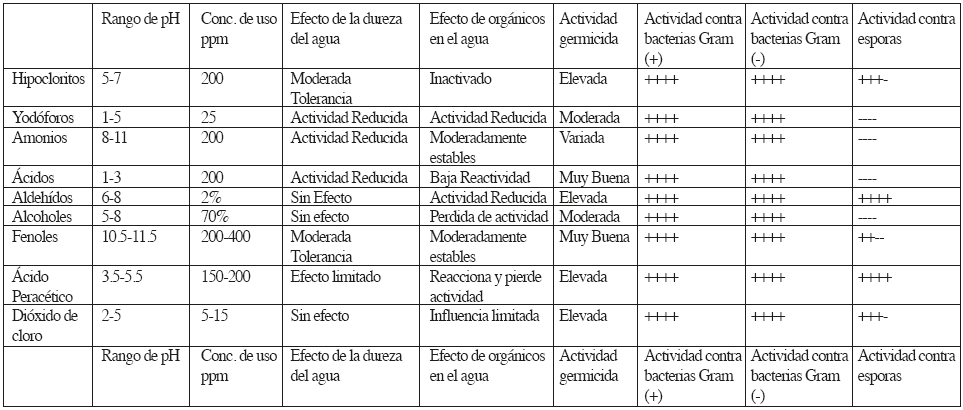
+++ Altamente efectivo, +++ Moderadamente efectivo, ++-- Lvemento efectivo, ---- Inefectivo
En dicha tabla se muestran las condiciones de uso de varias de las sustancias químicas que han sido empeladas para la sanitización y desinfección.
Respecto a los resultados experimentales planteados, en el modelo biológico 1 el ab-c mató a las artemias salinas en 12 minutos, mientras que el df mato a las artemias salinas en 15 minutos, lo cual nos indica mayor ecotoxicidad por parte del ab-c.
Existen trabajos referidos por otros autores, que demuestran la utilidad de trabajar el modelo de artemiascomo los de Pino Pérez y colaboradores; Vanhaecke P, Persoone G, ya que se dispone de un gran número de sujetos experimentales para los ensayos, son fáciles de conseguir y de mantener, se pueden utilizar tanto dentro como fuera del laboratorio. En estos estudios se monitorea la presencia de diversas sustancias que contaminan el medio ambiente y abarca desde los plaguicidas20,21 y en nuestro proyecto de investigación se estudiaron agentes sanitizantes, buscando así posibles alternativas para la solución de esta problemática ambiental (Evitar contaminaciones cruzadas y prevenir posibles daños al entorno).
Es evidente que se deben emplear los agentes sanitizantes con sumo cuidado, usando las mínimas concentraciones que eliminen microorganismos patógenos y que también sean fáciles de remover con abundante agua de las áreas y equipos de trabajo.
Al implementar el modelo biológico 2, se determinaron de manera experimental (n=4) la DL mínima que fue de 0.041g/kg y la DL máxima que fue de 0.163g/kg.
Una vez establecidas las dosis máximas y mínimas se dividió el intervalo de concentración de la sustancia en estudio (ab-c) en varias fracciones progresivas, las cuales se consideraron como las dosis de estudio para el ensayo de toxicidad aguda, manteniendo un grupo testigo y varios grupos de tratamiento con diferentes dosis de prueba (n = 14).
Las dosis de 0.0205, 0.0103, 6.833 x 10-3, mostraron ser tóxicas para los sujetos experimentales.
Así mismo se pudo demostrar experimentalmente que las concentraciones de 8.54 x 10-4, 1.708 x 10-3, 5.12 x 10-3, 2.563 x 10-3 no fueron dañinas bajo las condiciones del estudio, indicándonos claramente que al utilizar los agentes sanitizantes en forma diluida, pero en concentración adecuada eliminan la carga microbiana y limpian el área de trabajo de manera eficiente y dañan menos el medio ambiente.
En la Tabla 2 se muestran los resultados del ensayo de toxicidad aguda, el modelo de regresión mostró significancia estadística.
Conclusiones
Los sanitizantes probados experimentalmente (ab-c y df) demostraron poseer un efecto eco-toxicológico negativo ya que mataron a las artemias salinas, al utilizar el modelo biológico 1 y por lo tanto es indispensable su total remoción de las superficies de trabajo que hayan sido tratadas con estos productos y evidenciar que los agentes de limpieza deben ser lo más biodegradables posibles para ser amigables con él entorno.
Se identificó en el modelo biológico 2, la toxicidad aguda estimando un modelo de regresión que representa el 88.2 % de la variación con un P value de 0.018 (mayor a 0.05) por medio de las tablas de Probit de Fisher and Yales y se determinó el valor de la DL50 (2.4407 g/Kg con un intervalo de confianza inferior al 95 % de 1.1575 g/Kg) por medio de un método sencillo, práctico y confiable con lo cual el valor estimado podrá ser utilizado con confianza y justificado científicamente en la estimación del límite de aceptación de toxicidad para los procedimientos de Limpieza, lo cual permite establecer una bioseguridad en el uso de este tipo de productos.











 nueva página del texto (beta)
nueva página del texto (beta)



