Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias farmacéuticas
versión impresa ISSN 1870-0195
Rev. mex. cienc. farm vol.45 no.4 Ciudad de México oct./dic. 2014
Trabajo científico
Tolerabilidad del resveratrol y efectos sobre parámetros bioquímicos sanguíneos
Resveratrol Tolerability and effects on blood chemistry parameters
Pedro Lennon Sáenz Chávez, Lourdes Garza Ocañas, Christian Tadeo Badillo Castañeda, Eduardo Javier Tamez de la O, Jesús Triana Verástegui
Departamento de Farmacología y Toxicología, Facultad de Medicina, Universidad Autónoma de Nuevo León, México.
Correspondencia:
Dra. Lourdes Garza Ocañas
Departamento de Farmacología y Toxicología
Facultad de Medicina, Universidad Autónoma de Nuevo León
Madero y Dr. Aguirre Pequeño, Col. Mitras Centro
Monterrey Nuevo León, México C.P. 64460
Teléfono (81) 83485147
e-mail: logarza@live.com.mx
Fecha de recepción: 12 de enero de 2015
Fecha de recepción modificaciones: 06 de abril de 2015
Fecha de aceptación: 11 de mayo de 2015
Resumen
El resveratrol es un polifenol aislado de la uva al cual se le ha adjudicado actividad terapéutica antitumoral, incremento de longevidad, disminución de peso y protección cardiovascular. Se encuentra disponible como suplemento alimenticio y se vende sin prescripción médica. Evaluar la tolerabilidad de resveratrol, efectos adversos y efectos sobre pruebas de función hepática, renal y perfil de lípidos. Se administró resveratrol 500 mg, vía oral a 8 sujetos sanos durante 30 días y se realizó evaluación clínica, perfil bioquímico y de lípidos al inicio y final del estudio. No se observaron efectos adversos ni alteración en el perfil bioquímico ni de lípidos. El resveratrol fue bien tolerado, mostró ser seguro en dosis diarias de 500 mg, sin embargo se requieren estudios con mayor número de sujetos para confirmarlo.
Palabras clave: Resveratrol, efectos adversos, tolerabilidad, farmacovigilancia.
Abstract
Resveratrol is a grape extract polyphenol. It has been associated with antitumoral activity, weight loss, longevity and cardiovascular protection. It is available as a food supplement and sold over the counter.
Assess tolerability of resveratrol, its side effects and possible effects on lipid profiles as well as liver and kidney function. Eight healthy subjects received 500 mg of resveratrol v.o. during thirty days and clinical and blood chemistry parameters and lipid profile were evaluated at the start and at the end of the study.
There were no effects on blood chemistry or lipid profiles, and none of the subjects had adverse effects. Resveratrol was well tolerated and was safe at 500 mg daily doses. Nevertheless, studies including a larger number of subjects are needed to confirm this.
Key words: Resveratrol, Adverse effects, Tolerability, Pharmacovigilance.
Introducción
El resveratrol (trans-3,4,5-trihidroxistilbeno) es una fitoalexina polifenólica, producida por plantas en respuesta a estrés y pertenece al grupo de los fitoestrógenos. Especialmente se ha descrito la producción de resveratrol como protección contra Botrytis cinerea, hongo patógeno de muchas plantas.1 En los últimos años ha habido un auge en el ámbito de investigación de este compuesto.2 Se encuentra en el vino tinto, uvas, pistaches, nueces, cacahuates, moras, entre otros alimentos y algunas plantas como Polygonum cuspidatum. En la naturaleza puede encontrarse como trans-, cis- y dihidro-resveratrol.3 A pesar de que no hay evidencia científica adecuada respecto a sus efectos y seguridad en el humano muchas personas consumen esta sustancia por las propiedades antes mencionadas.4
Los parámetros farmacocinéticos del resveratrol son: vida media de 9.2 horas, absorción de 75 %, biodisponibilidad oral baja, menor a 1 %; la sulfatación y la glucuronización en intestino delgado parecen ser los pasos limitantes en la biodisponibilidad.5 Sus metabolitos más importantes son glucurónido y sulfato de resveratrol.6 Se metaboliza extensamente en hígado mayormente por glucuronización y sulfatación, ésta última llevada a cabo por las sulfotransferasas de fenol (SULT1A1 y SULT1E1).7 A pesar de prometedores resultados en el ámbito preclínico, el éxito en el humano se ha cuestionado, en gran parte debido a su baja biodisponibilidad, ya que se considera que muchos de los efectos benéficos no serían alcanzables en el humano a menos que se utilizara en grandes dosis, sin que se haya encontrado a la fecha un mecanismo para mejorarla.8
Son múltiples los efectos positivos del resveratrol ya demostrados en modelos in vitro y otros pocos en ensayos clínicos en humanos, a saber: efecto antiaterosclerótico y cardioprotector, efecto antiagregante plaquetario, anticáncer, antiviral, hipolipemiante, antioxidante y neuroprotector.9-12
El efecto del resveratrol en la aterosclerosis involucra múltiples vías, entre las que se destaca la disminución de la agregación plaquetaria, disminución de expresión de factor de necrosis tumoral alfa, disminución de angiogénesis, disminución de lipogénesis y aumento de lipólisis entre otros.9
En una revisión sistemática de 13 estudios del efecto del resveratrol sobre lípidos, en 5 de ellos se reportó que no hubo cambios significativos en el perfil lipídico, en el resto si hubo disminuciones en el colesterol total y triglicéridos. En 4 se reportó reducción de los niveles de LDL.9
Desde que se estableció que se requerirían cantidades abundantes de resveratrol en dosis diarias para emular los hallazgos en los modelos de investigación, se ha cuestionado la posibilidad de que esa dosis sea tóxica. En dosis administradas a 0.5 g, 1 g, 2.5 g y 5 g diariamente durante 29 días a voluntarios sanos no se reportaron efectos adversos graves. Tan sólo se reportaron efectos gastrointestinales leves con las dosis de 2.5 y 5 g.6 Se ha establecido el NOAEL (Nivel de efecto adverso no observable) en 300mg/kg/día y con dosis superiores a ésta se ha descrito neurotoxicidad, leucocitosis, anemia y deshidratación. Una dosis diaria de 5-10 g es aparentemente segura.13 Queda aún pendiente esclarecer la farmacodinamia y ensayos clínicos apropiados sobre su efectividad en humanos.14 Johnson et al realizaron estudios de toxicidad subcrónica en perros y ratas, pero la evidencia en humanos sobre estas variables aún es escasa.15 Smoliga y colaboradores realizaron una revisión de ensayos clínicos de resveratrol en humanos, la mayoría de ellos se enfocan en la biodisponibilidad del resveratrol, pocos han evaluado el efecto sobre lípidos, además en algunos estudios las dosis usadas han sido bajas 250 o 500 mg durante 3 días.16
En México el resveratrol se encuentra disponible a la venta al público, sin receta, como suplemento alimenticio, con la premisa de bajar de peso, como protector cardiovascular, antioxidante e incluso para prolongar la longevidad. La gran mayoría de la evidencia actual es en animales y es necesario realizar estudios clínicos en humanos para demostrar su seguridad y tolerabilidad. A la fecha no se ha realizado ningún estudio en población mexicana.
El objetivo de este trabajo es verificar la tolerabilidad al resveratrol administrado durante 30 días mediante evaluaciones clínicas para detectar posibles efectos adversos además de comparar los perfiles bioquímicos previo a la administración y posterior al mes de administración con el propósito de investigar posibles alteraciones a nivel de función renal, función hepática, electrólitos y lípidos.
Material y métodos
Se reclutaron 8 sujetos sanos, basados en la NOM-177-SSA1-2013 que establece que los estudios piloto con carácter exploratorio cuyo objetivo es evaluar la seguridad de un fármaco en una población específica deben realizarse en al menos 8 sujetos sanos.17 El estado de salud se determinó mediante evaluación clínica con una historia clínica, examen físico médico, signos vitales y exámenes auxiliares (biometría hemática completa, perfil bioquímico, examen general de orina, pruebas para VIH, Hepatitis B y C, Sífilis, EKG, antidoping en orina y prueba de embarazo en mujeres).
Los criterios de inclusión fueron; haber dado y firmado su consentimiento informado para participar en el estudio, de acuerdo con las Buenas Prácticas Clínicas, ser un hombre o mujer de 18 a 40 años de edad, tener un índice de masa corporal 18 a 26.9 Kg/m2, ser sujetos sanos de acuerdo a la historia médica, examen físico y valores de laboratorio clínico normales y ser sujetos que han entendido y están dispuestos a cumplir con los procedimientos del estudio, incluyendo el seguimiento y las restricciones.
Los criterios de exclusión fueron: tener una historia personal de reacciones alérgicas a medicamentos, usar cualquier medicamento que pueda modificar la respuesta a evaluar, padecer alguna enfermedad crónico-degenerativa que requiera tratamiento médico, tener problemas médicos no controlados que en opinión del investigador pudieran reducir la seguridad de su participación en el estudio, tener desórdenes neurológicos o psiquiátricos, tener resultados de laboratorio anormales como prueba de sífilis positivo, prueba de SIDA positivo, Hepatitis B o C positivo, antecedentes de exposición crónica al alcohol u otras substancias de abuso dentro del último año, tener una historia de fumador en el último trimestre, haber participado en algún otro estudio de investigación en los 60 días previos al estudio, embarazo o lactación.
Los criterios de eliminación fueron; fallar en más del 10 % de las tomas del medicamento, presentar embarazo durante el transcurso del estudio, incurrir en alguna falta a los reglamentos, iniciar tratamiento con algún medicamento, sufrir alguna condición o enfermedad grave durante el mes de estudio o la presencia de efectos adversos serios durante el estudio y baja voluntaria.
Para la realización de los exámenes de laboratorio en la etapa de pre-selección se tomó una muestra de 5 mL se sangre por venopunción por personal médico. Los exámenes de seguimiento (perfil bioquímico completo) se realizaron al concluir el estudio, en condiciones de ayuno, en el día 30 de administración de resveratrol.
El resveratrol fue proporcionado por laboratorios Senosiain S.A. de C.V. Las cápsulas conteniendo el resveratrol se prepararon en el departamento de Farmacología y Toxicología, bajo luz infrarroja (para evitar la isomerización del resveratrol) Se verificó el peso del resveratrol usando una balanza analítica calibrada de manera que cada cápsula contenía 250 mg.
Se usaron cápsulas de gel duro No. 1 y el resveratrol se encapsuló usando "The Capsule Machine" #1 de Capsule Connection, LLC.
Una vez reclutados los sujetos, se citaron para la administración diaria de resveratrol 500 mg (2 cápsulas de 250 mg) en el departamento de Farmacología y Toxicología de la Facultad de Medicina de la UANL entre 8:30 y 10:30 de la mañana, en ayuno. La administración se realizó en la presencia de uno de los investigadores médicos, con 200 mL de agua de lunes a domingo durante 30 días. Durante cada visita se interrogó a los participantes sobre la presencia de posibles efectos adversos (náuseas, vómitos, irritabilidad gástrica, dispepsia, dolor abdominal, cefalea, mareos, temblor, disnea o erupciones cutáneas entre otros). Se tomaron los signos vitales (presión arterial, temperatura, frecuencia respiratoria y pulso) en el período de selección, al iniciar el estudio y al concluirlo. Durante el mes de tratamiento se instruyó a los sujetos para que se comunicaran con el personal médico ante la sospecha de cualquier efecto adverso. La actividad física no fue restringida y se les indicó que continuaran su vida cotidiana, incluyendo rutina de ejercicio normal. Se les prohibieron alimentos altos en grasa, chocolate, almendras, uvas, frambuesas, moras y otros alimentos conocidos por contener concentraciones elevadas de resveratrol. (Figura 1)

Para analizar los resultados del perfil bioquímico y de lípidos previos y posteriores a la administración de resveratrol se usó la prueba de Kolmogorov-Smirnov y se compararon las medias usando la prueba t de Student mediante el programa estadístico SPSS. Se establecieron valores de p menores de 0.05 para determinar diferencias estadísticamente significativas.
Resultados y discusión
Este es el primer estudio en sujetos mexicanos donde se evalúa la tolerabilidad y posibles efectos adversos del uso diario de resveratrol durante 30 días El estudio se inició con 8 sujetos, 4 hombres y 4 mujeres, todos de nacionalidad y ascendencia mexicana. Edades entre 20 y 24 años, índice de masa corporal desde 20.82 hasta 26.75 Kg/m2 y con un rango de peso desde 53.3 hasta 91.1 Kg. Las características demográficas de los sujetos se muestran en la Tabla 1. Un sujeto se retiró del estudio por motivos personales y los otros 7 participantes (3 mujeres y 4 hombres) concluyeron el estudio.

Durante el mes de administración no se reportó ningún efecto adverso, el resveratrol fue bien tolerado, no se presentaron reacciones alérgicas ni alteraciones gastrointestinales, respiratorias o neurológicas.
No se observaron diferencias estadísticamente significativas en los valores iniciales y finales de signos vitales (presión arterial, temperatura, frecuencia respiratoria y pulso) manteniéndose los valores dentro de rangos normales.
Los resultados del perfil bioquímico inicial (previo a la administración de resveratrol) y posterior a la administración 500 mg diarios, vía oral, durante 30 días se muestran en las tablas 2 y 3. Al comparar los valores promedio de los parámetros de los perfiles bioquímicos iniciales y finales se observó que todos los valores estuvieron dentro de límites normales. Los valores promedio de glucosa y creatinina fueron 69.5mg/dL y 0.8 mg/dL respectivamente. No se observó alteración en las pruebas de función hepática, bilirrubinas totales proteínas totales, ni electrolitos séricos. Se observó una diferencia estadísticamente significativa entre los valores iniciales y finales de albúmina, sodio y cloro sin embargo, tanto los valores iniciales como finales se reportaron dentro de límites normales (Tabla 6).

Aunque no se observó diferencia estadísticamente significativa, hubo un incremento aparente en los valores promedio iniciales y finales de glucosa (69.5 vs 77.57mg/dL), TGO (18.5 vs 22.14 UI/L) y TGP (22.1 vs 27.4 UI/L) sin embargo todos los valores estuvieron dentro de límites normales.
En relación al perfil de lípidos todos los resultados iniciales se encontraron dentro de límites normales. Los valores promedio para colesterol, LDL, HDL, y triglicéridos fueron 135.5, 82.7, 51.86 y 62.86 mg/dL respectivamente (Tabla 4).
Al comparar los valores iniciales y finales, se observó un incremento en el colesterol (135.57 vs 139.29 mg/dL) así como una aparente disminución en triglicéridos (62.86 vs 58.57 mg/dL) y LDL (82.71 vs 80.57UI/L) sin embargo estas diferencias no fueron estadísticamente significativas, pues en ninguno de estos casos los valores de p fueron menores de 0.05 (Tabla 6). Ghanim (2010) quien realizó un estudio en sujetos sanos, administrando una dosis menor a la de este estudio (40mg diarios, vía oral durante 6 semanas) reportó una ligera disminución de colesterol, LDL y HDL sin cambios en los triglicéridos.18
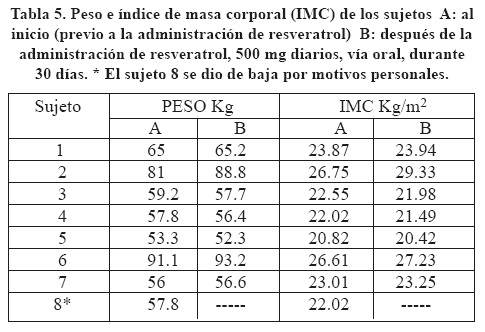
El peso e índice de masa corporal (IMC) de los sujetos se midió en la etapa de pre-selección (previo a la administración de la primera dosis de resveratrol) y al finalizar el estudio. En los sujetos 3, 4 y 5 se observó una ligera disminución de peso y del IMC en cambio los sujetos 2 y 6 tuvieron un incremento de peso y del IMC (Tabla 5). Ya que durante el mes de tratamiento se les indicó que continuaran sus rutinas ya establecidas de ejercicio (si es que las había) y siguieran su dieta como normalmente lo harían, con excepción de los alimentos elevados en resveratrol, existen muchas variables que pudieron haber influido en estos ligeros cambios en el peso corporal por lo que se consideran no concluyentes y no podrían atribuirse al tratamiento recibido.
En las comparaciones de los perfiles bioquímicos, existen algunas tendencias que debieran ser consideradas en futuros estudios con un mayor número de sujetos como el incremento en los valores promedio de glucosa (a pesar de haber sido estadísticamente no significativo) que contrasta con lo publicado por Brasnyo et al quienes tras administrar 5 mg de resveratrol por vía oral 2 veces al día durante 4 semanas a pacientes diabéticos observaron una disminución en los valores de glucosa y en la resistencia a la insulina postprandial.19 Así mismo el aparente aumento en los valores de TGO (p=0.054) y calcio (p=0.052) con valores de p que podrían indicar una tendencia a ser significativos si el número de sujetos del estudio fuera mayor.
En general el tratamiento con resveratrol durante 30 días no alteró el perfil de lípidos, las pruebas de función renal ni hepática. Lo publicado por Haneke en cuanto a la seguridad del resveratrol concuerda con los resultados de este estudio, ya que no se reportaron efectos adversos en ninguno de los sujetos.13
Actualmente se tiene escasa información sobre el uso de resveratrol en humanos, lo cual seguramente cambiará en el futuro cercano ya que en una búsqueda realizada en la página de Clinical Trials, www.clinicaltrials.gov se encontró que actualmente hay 15 ensayos clínicos registrados involucrando el uso de resveratrol en sujetos sanos. 20 De estos estudios, 14 están reportados como completos, solo de uno se reporta que hay resultados (los cuales no se muestran) y para todos aún está pendiente la publicación de dichos resultados por lo que por ahora no es posible hacer comparación de los mismos con los resultados obtenidos en este estudio.
Conclusiones
El uso diario de resveratrol 500 mg por vía oral durante 30 días no produjo ningún efecto adverso y fue bien tolerado por todos los sujetos. No se observaron alteraciones en los parámetros bioquímicos sanguíneos relacionados con función renal, hepática y electrolitos ni en el perfil de lípidos sin embargo se requieren estudios con mayor número de sujetos para confirmarlo.
Agradecimientos
Los autores agradecen al Dr. Juan Pablo Senosiain Peláez por la aportación del resveratrol.
Referencias
1. Adrian M, Jeandet P. Effects of Resveratrol on the ultrastructure of Botrytis cinerea conidia and biological significance in plant/pathogen interactions. Fitoterapia. 2012 Dec; 83(8):1345-50 [ Links ]
2. Baur JA, Sinclair DA, Therapeutic potential of resveratrol: the in vivo evidence. Nat Rev Drug Discov. 2006; 5; 493-505. [ Links ]
3. Anisimova NY, Kiselevsky MV, Sosnov A, Sadovnikov SV, Stankov IN, Gakh AA, Trans, cis and dihidro-resveratrol: a comparative study. Chem Cent J. 2011; 5(1)88. [ Links ]
4. Vang O, Ahmad N, Baile C, et. al. What is new for and old molecule? Systematic review and recommendations on the use of resveratrol. Plos One. 2011; 6 (6); e19881. [ Links ]
5. Walle T, Bioavailability of Resveratrol. Ann N.Y. Acad Sci. 2011; 1215; 9-15. [ Links ]
6. Brown VA, Patel KR, Viskaduraki M et. al. Repeat Dose Study of Resveratrol in Healhy Volunteers; Safey, Pharmacokinetics and Effect on he Insulin-like Growth Factor Axis. Cancer Res 2010; 15:9003-9011. [ Links ]
7. Neves AR, Lucio M, Lima JL, Reis S. Resveratrol in medicinal chemistry: a critical review of its pharmacokinetics, drug delivery and membrane interactions. Curr Med Chem. 2012; 19(11):1663-81. [ Links ]
8. Santos AC, Veiga F, Ribeiro AJ. New delivery systems to improve the bioavailability of resveratrol. Expert Opin Drug Deliv. 2011 Aug; 8(8):973-90. Epub 2011 Jun 14. [ Links ]
9. Ramprasath VR, Jones PJH, Anti-atherogenic effects of Resveratrol. Eur J Clin Nutr. 2010; 64; 660-668. [ Links ]
10. Gnoni GV, Paglialonga G, Resveratrol inhibits fatty acid and triacylglycerol synthesis in rat hepatocytes. Eur J Clin Invest. 2009; 39 (3); 211-218. [ Links ]
11. Frombaum M, Le Clanche S, Bonnefont-Rousselot D, Borderie D. Antioxidant effects of resveratrol and other stilbene derivatives on oxidative stress and NO bioavailability: potential benefits to cardiovascular diseases. Biochimie. 2012 Feb; 94(2):269-76. [ Links ]
12. Tyagi S, Singh, Sharma A, Aggarwal G, et. al. Clinical and Medical Applications of Resveratrol: A review. Int J Pharm Sci Rev Res. 2010; 3-1; 49-52. [ Links ]
13. Haneke K, Toxicological Summary for trans-Resveratrol. Rev Tox Lit. 2002; 501-36-0. [ Links ]
14. Patel KR, Scott E, Brown VA, Gescher AJ, Stewad WP, Brown K, Clinical Trials of Resveratrol. Ann. N. Y. Acad Sci. 2011; 1215: 161-169. [ Links ]
15. Johnson WD, Morrisey, Usborne AL, Kapetanovic I, Crowell JA, Muzzio M, McCormick DL; Subchronic oral toxicity and cardiovascular safety pharmacology studies of resveratrol, a naturally occurring polyphenol with cancer preventive activity; Food Chem Toxicol. 2011 December ; 49(12): 3319-3327 [ Links ]
16. Smoliga JM, Baur JA, Husenblas HA; Resveratrol and Health - A comprehensive Review of Human Clinical Trials. Mol. Nutr. Food Res. 2011, 55, 1129-1141 [ Links ]
17. Norma Oficial Mexicana NOM-177-SSA1-2013. Que establece las pruebas y procedimientos para demostrar que un medicamento es intercambiable. Diario Oficial de la Federación. (20-09-2013). [ Links ]
18. Ghanim H, Sia CL, Abuaysheh S, et al. An antiinflammatory and reactive oxygen species suppressive effects of an extract of Polygonum cuspidatum containing resveratrol. J Clin Endocrinol Metab. 2010; 95:E1-E8. [ Links ]
19. Brasnyó P, Molnár GA, Mohás M, et al. Resveratrol improves insulin sensitivity, reduces oxidative stress and activates the Akt pathway in type 2 diabetic patients. Br J Nutr. 2011; 106:383-389. [ Links ]
20. National Institutes of Health. Clinical Trials [homepage en internet] US National Library of Medicine. c1993 [actualizada 26 Noviembre 2012; consultado Octubre 2014]. Disponible en: https://clinicaltrials.gov/ [ Links ]














