Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias farmacéuticas
versión impresa ISSN 1870-0195
Rev. mex. cienc. farm vol.42 no.1 Ciudad de México ene./mar. 2011
Secciones
¿Qué sabe Ud. acerca de... la vía de administración transdérmica?
What do you know about... transdermal drug delivery?
Dra. Adriana Ganem Rondero
Laboratorio de Posgrado en Tecnología Farmacéutica, Facultad de Estudios Superiores Cuautitlán, UNAM.
Preguntas
1. ¿Qué ventajas ofrece la vía transdérmica sobre otras rutas de administración?
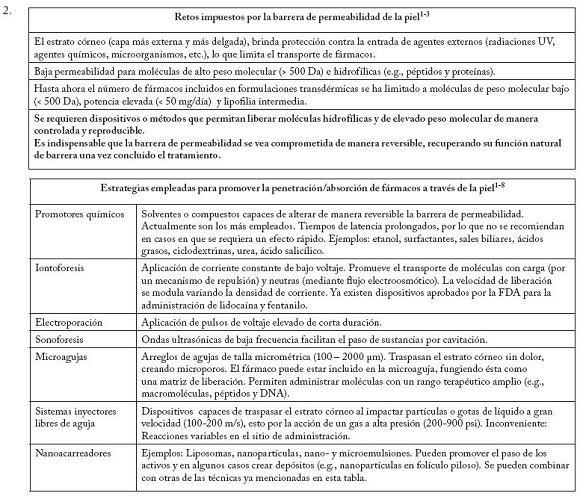
2. ¿Qué retos representa y a qué estrategias se ha recurrido para vencerlos?
3. ¿Qué fármacos se encuentran disponibles en el mercado como sistemas de liberación transdérmica?
4. ¿Es posible la toma de muestras de fluidos biológicos a través de la piel?
5. ¿Qué se espera en el futuro de la vía administración transdérmica?
Respuestas

3.
• Clonidina (hipertensión)
• Escopolamina (mareo, náusea y vómito)
• Estradiol (reemplazo hormonal)
• Lidocaína y tetracaina (parche iontoforético para anestesia local)
• Lidocaína y epinefrina (sistema iontoforético para anestesia local)
• Lidocaína (anestésico)
• Metilfenidato (hiperactividad, déficit de atención)
• Nitroglicerina (angina de pecho)
• Nicotina (tratamiento para dejar de fumar)
• Acetato de noretisterona y estradiol (reemplazo hormonal)
• Norelgestromina/etinilestradiol (anticonceptivo)
• Oxibutinina (vejiga hiperactiva)
• Rivastigmina (tratamiento de Alzheimer)
• Rotigotina (tratamiento de Parkinson)
• Selegilina (depresión)
• Testosterona (disfunción eréctil, deficiencia hormonal)
• Fentanilo (opióide potente disponible en forma de parche pasivo y sistema iontoforético)
• Buprenorfina (opioide potente)
4. Hasta ahora la toma de muestras de sangre se realiza mediante una punción. No obstante, lo doloroso que esto puede resultar y el riesgo de infección, han motivado la propuesta de diversas técnicas que hagan posible realizar muestreos de manera no invasiva o poco invasiva para la determinación in situ (empleando biosensores enzimáticos), de la concentración plasmática de fármacos o de alguna sustancia endógena que permita realizar un diagnóstico. En este sentido, se ha recurrido al uso de la iontoforesis, que como ya se mencionó, consiste en aplicar una pequeña corriente eléctrica. Debido a la simetría de este método, es posible no sólo administrar fármacos a través de la piel, sino extraer compuestos hacia la superficie, proceso que se conoce como "iontoforesis reversa". El mecanismo de extracción de especies incluye la electromigración de aquellas especies con carga hacia el electrodo de polaridad opuesta y el flujo electroosmótico para las moléculas neutras, aportando una estimación de la concentración del analito durante el tiempo de muestreo. Sus aplicaciones pueden ser múltiples, desde el monitoreo terapéutico de fármacos (e.g., litio empleado en el tratamiento de transtornos bipolares), hasta el control de concentraciones de fenilalanina en fenilcetonúricos, urea en pacientes con disfunción renal y de glucosa en diabéticos. En este último caso, la FDA aprobó en el año 2001 el sistema denominado "Glucowatch", basado en el principio de la iontoforesis reversa, el cual permite la determinación de niveles de glucosa. Aunque este sistema presenta todavía algunos inconvenientes que deben ser mejorados, es un gran paso hacia el desarrollo de estos dispositivos.
Las microagujas huecas también se han propuesto como sistemas para el muestreo de fluidos biológicos haciendo uso de la acción capilar. Diversos estudios muestran su utilidad para la determinación de niveles de glucosa, hormonas o algunos agentes terapéuticos.
5. Administración efectiva a través de la piel de macromoléculas hidrofílicas (e.g., proteínas).
Desarrollo de sistemas activos cada vez más efectivos, por ejemplo, microelectromecánicos (microelectromechanical systems, MEMS) para la administración activa y controlada de fármacos.
Combinación de sistemas activos (e.g., iontoforesis, electroporación) con nanoacarreadores (e.g., liposomas, nanopartículas, microemulsiones).
Sistemas autoprogramables. Un ejemplo de ello sería un dispositivo que permitiera la determinación de niveles de glucosa en sangre (como lo realiza el Glucowatch que se basa en el principio de la iontoforesis reversa), y que si estos son elevados, automáticamente liberara insulina hasta alcanzar niveles normales de glucosa.
Uso de la terapia fotodinámica para el tratamiento de afecciones de la piel y para liberación sistémica.
Referencias
1. Akomeah F.K. 2010. Topical dermatological drug delivery: Quo vadis? Current Drug Deliv, 7:283-296. [ Links ]
2. Brand R.M., Iversen P.L. 2000. Transdermal delivery of antisense compounds. Adv Drug Deliv Rev, 44: 51-57. [ Links ]
3. Orive G., Gascón A.R., Hernández R.M., Domínguez-Gil A., Pedraz J.L. 2004. Techniques: New approaches to the delivery of biopharmaceuticals. TRENDS in Pharmaceutical Sciences, 25 (7): 382-287. [ Links ]
4. Allevato M. 2007. Sistemas terapéuticos transdérmicos. Act Terap Dermatol, 30:154-165. [ Links ]
5. Arora A., Prausnitz M.R., Mitragotri S. 2008. Microscale devices for transdermal drug delivery. Int J Pharm, 364:227-236. [ Links ]
6. Cázares-Delgadillo J. Balaguer-Fernández C., Calatayud-Pascual A., Ganem-Rondero A., Quintanar-Guerrero D., López-Castellano A.C., Merino V., Kalia Y.N. 2010. Transdermal iontophoresis of dexamethasone sodium phosphate in vitro and in vivo: Effect of experimental parameters and skin type on drug stability and transport kinetics. Eur J Pharm Biopharm, 75:173-178. [ Links ]
7. Nava-Arzaluz M.G., Calderón-Lojero I., Quintanar-Guerrero D., Villalobos-García R., Ganem-Quintanar A. 2011. Microneedles as transdermal delivery systems: Combination with other enhancing strategies. Current Drug Deliv, In press.
8. Domínguez-Delgado C.L., Rodríguez-Cruz I.M., Escobar-Chávez J.J., Calderón-Lojero I.O., Quintanar-Guerrero D., Ganem A. 2011. Preparation and characterization of triclosan nanoparticles intended to be used for the treatment of acné. Eur J Pharm Biopharm, In press.
9. Rabah E. 2007. Opioid analgesic: New way of transdermal administration. Boletín ACHED, 47:30-34. [ Links ]
10. Rao G., Guy R.H., Glikfeld P., LaCourse W.R. , Leung L., Tamada J., Potts R.O., Azimi N. 1995. Reverse iontophoresis: non invasive glucose monitoring in vivo in humans. Pharm Res, 12:1869-1873. [ Links ]
11. Tierney M.J., Tamada J.A., Potts R.O., Jovanovic L., Garg S., Cygnus Research Team. 2001. Clinical evaluation of the GlucoWatchR biographer: a continual, non-invasive glucose monitor for patients with diabetes. Biosens Bioelectron 16:621-629. [ Links ]
12. Delgado-Charro M.B., Guy R.H. 2003. Transdermal reverse iontophoresis of valproate: a non-invasive method for therapeutic drug monitoring. Pharm Res, 20:1508-1513. [ Links ]
13. Degim I.T., Ilbasmis S., Dundaroz R., Oguz Y. 2003. Reverse iontophoresis: a non-invasive technique for measuring blood urea level. Pediatr Nephrol, 18:1032-1037. [ Links ]
14. Sieg A., Guy R.H., Delgado-Charro M.B. 2004. Electroosmosis in transdermal iontophoresis: Implications for noninvasive and calibration-free glucose monitoring. Biophys J, 87:3344-3350. [ Links ]
15. Leboulanger B., Guy R.H., Delgado-Charro M.B. 2004. Reverse iontophoresis for non-invasive transdermal monitoring. Physiol Meas, 25:35-50. [ Links ]
16. Leboulanger B., Aubry J-M., Bondolfi G., Guy R.H., Delgado-Charro M.B. 2004. Lithium monitoring by reverse iontophoresis in vivo. Clin Chem, 50:2091-2100. [ Links ]
17. Wascotte V., Leboulanger B., Guy R.H., Delgado-Charro M.B. 2005. Reverse iontophoresis of lithium: electrode formulation using a thermoreversible polymer. Eur J Pharm Sci, 59:237-240. [ Links ]
18. Mudry B., Guy R.H., Delgado-Charro M.B. 2006. Prediction of iontophoretic transport across the skin. J Control Release, 111:362-367. [ Links ]














