Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista mexicana de ingeniería química
Print version ISSN 1665-2738
Rev. Mex. Ing. Quím vol.10 n.3 Ciudad de México Dec. 2011
Materiales
Interacción goma de mezquite–quitosano en la interfase y su influencia en la estabilidad de emulsiones múltiples W1/O/W2
Interaction of mesquite gum–chitosan at the interface and its influences on the stability of multiple emulsions W1/O/W2
J.P. Pérez–Orozco1*, E. Barrios–Salgado1, A. Róman–Guerrero2 y R. Pedroza–Islas3
1 Instituto Tecnológico de Zacatepec, Departamento de Ingeniería Química y Bioquímica, Calzada Tecnológico No. 27, Col. Centro, Zacatepec, Morelos 62780, México. *Autor para la correspondencia. E–mail: jppoebs@gmail.com TelJFax: (734) 3432110/ (734) 34 34141.
2 Universidad Autonóma Metropolitana–Iztapalapa, Departamento de Biotecnología, San Rafael Atlixco 186, Vicentina, México DF 09340, México.
3 Universidad Iberoamericana, Departamento de Ingeniería y Ciencias Químicas, Prolongación Reforma 880, Lomas de Santa Fé, México DF 01210, México.
Recibido 13 de Abril 2011.
Aceptado 12 de Julio 2011.
Resumen
En este trabajo se estudió el efecto de las interacciones entre la goma de mezquite (GM) y quitosano (Q) sobre las propiedades interfaciales de las películas adsorbidas en la interfase agua–aceite de Canola, y su influencia en las propiedades reológicas, estructurales y estabilidad de emulsiones aceite–en–agua (O/W) y agua–en–aceite–en–agua (W1/O/W2). Los resultados interfaciales mostraron la existencia de una interacción asociativa (del tipo electrostática) entre ambas macromoléculas a un pH 3.8, influenciada por la concentración relativa de los biopolímeros y características de la fase oleosa. La viscosidad aparente interfacial y las propiedades interfaciales de fluencia–capacitancia de las películas adsorbidas se incrementaron con la mezcla polimérica de composición 10%GM–0.4%Q. El complejo electrostático (10%GM–0.4%Q) proporcionó la menor tasa de coalescencia y las propiedades reológicas exhibieron un mayor carácter elástico con ligera dependencia respecto al tiempo de envejecimiento de la emulsión O/W, así como brindo una mayor estabilidad al sistema múltiple W1/O/W2.
Palabras clave: viscosidad aparente interfacial, propiedades interfaciales de fluencia–capacitancia, propiedades viscoelásticas, polielectrolitos, complejo electrostático.
Abstract
In this work, the effect of interaction between mesquite gum (GM) and chitosan (Q) on the interfacial properties of adsorbed layer in the water–Canola oil interface, and their influence in the rheological properties, structure and stability of emulsions oil–in–water (O/W) and water–in–oil–in–water (W1/O/W2), were studied. The interfacial results showed that there is an associative (electrostatic) interaction between both macromolecules at the pH 3.8, influenced by she biopolymer concentration ratio and oil phase characteristic. The interfacial apparent viscosity and the interfacial creep–compliance properties of adsorbed layer were increases when using 10%GM–0.4%Q. The electrostatic complex (10%GM–0.4%Q) gave the minor coalescence kinetics and their rheological properties exhibited a mayor elastic character with litile dependence regarding the aging time of emulsion O/W, and provided greater stability for the multiple system W1/O/W2.
Keywords: interfacial apparent viscosity, interfacial creep–compliance properties, viscoelastic properties, polyelectrolytes, electrostatic complex.
1 Introducción
Las emulsiones múltiples son sistemas dispersos complejos en los que la fase dispersa es una emulsión, y están caracterizados por tener una baja estabilidad termodinámica. Cada uno de los glóbulos en estos sistemas contiene uno o más compartimentos de una fase, la cual está separada de una fase químicamente similar, a través de una membrana o película de una fase diferente e inmiscible; es por ello que también suele dárseles el nombre de membranas dobles. Los dos tipos más comunes de estos sistemas son las emulsiones de agua–aceite–agua (W1/O/W2) y aceite–agua–aceite (O1/W/O1) (Muschiolik, 2007).
Las emulsiones múltiples W1/O/W2 tienen un gran potencial de aplicación en la industria farmacéutica, cosmética, agrícola, alimentaria y ambiental; pues pueden ser usadas como medios de separación de sustancias contaminantes, encapsulación y liberación controlada de productos probióticos (Pimentel–González, D. y col. 2009), en la protección oxidativa de sabores y colorantes (Rodríguez–Huezo y col., 2004; Cho y Park, 2004), encapsulamiento de fármacos (Lindenstruth y Muller, 2004), o para generar nuevos alimentos de bajo contenido calórico (Lobato–Calleros y col., 2009). También existen reportes de la implementación de estos sistemas en la elaboración de películas y/o recubrimientos comestibles (Murillo Martínez y col. 2011).
Sin embargo, la inherente inestabilidad de las emulsiones W1/O/W2 que se asocia a la complejidad estructural de estos sistemas, sigue limitando su aplicación. Existen varios factores que afectan la estabilidad de una emulsión W1/O/W2. Entre los cuales tenemos: El método de preparación, naturaleza de los materiales entrampados, el volumen de las fases, la concentración y tipo de emulsionantes, los electrolitos presentes en el sistema y todos los ingredientes adicionados en la fase acuosa externa (Özer y col., 2000; Su y col., 2008). La eficacia y eficiencia en la aplicación de las emulsiones múltiples está íntimamente ligada al uso de emulsionantes como surfactantes, biopolímeros, copolímeros, entre otros, que son utilizados para proveer estabilidad cinética y mantener su estructura por un período de tiempo largo. Las interacciones entre éstas moléculas que se adsorben en las interfases fluidas tiene un papel importante en la estructura, estabilidad, propiedades reológicas y funcionales de éstos sistemas (Laplante y col, 2005).
La reología de corte de las moléculas adsorbidas en interfases fluidas gas–líquido o líquido–líquido proporciona información sobre las interacciones inter e intramoleculares presentes que están ligadas a los procesos dinámicos de las interfases fluidas. El comprender éstas interacciones es de gran relevancia en una gran variedad de aplicaciones técnicas, especialmente en la formulación de sistemas coloidales que están conformados por un gran número de interfases, como son las espumas y emulsiones, en particular las emulsiones múltiples (Krägel y Derkatch, 2010). Para realizar estudios de reología interfacial de corte se han sugerido varios métodos y dispositivos, cuya sensibilidad y rango de medición varían según el método propuesto. En nuestro trabajo previo (Pérez–Orozco y col., 2004) se evaluaron las propiedades de fluencia–capacitancia (creep–compliance) y viscosidad interfacial de corte de películas de goma de mezquite (GM) y quitosano (Q) adsorbidas en la interfase aceite Mineral–agua mediante la modificación de un reometro convencional; se encontró que el incremento de las interacciones electrostáticas Coulómbicas entre las cargas negativas de GM y las positivas del Q, y la fuerza de la interacción son influenciadas por la concentración relativa de las macromoléculas y el tiempo de envejecimiento de las películas.
La GM es el exudado en forma de lágrima de color ámbar producida por árboles de Prosopis spp., químicamente es una sal neutra de un polisacárido ramificado de naturaleza acídica formado por un núcleo de residuos de β–D–galactosa, constituyendo un esqueleto de uniones (1–3) y ramificaciones (1–6) conteniendo L–arabinosa (formas cíclicas de piranosa y furanosa), L–ramnosa, β–D–glucuronato y 4–o–metil–β–D–glucuronato como azucares simples y cadenas laterales de oligosacáridos. La goma de mesquite obtenida de Prosopis laevigata contiene una pequeña fracción de proteína (2.7 ± 0.06%) ligada a la parte central de la estructura primaria de carbohidratos, su estructura está compuesta por una mezcla compleja de al menos cinco fracciones distintas con diferentes composiciones químicas (Román–Guerrero y col., 2009). Varias investigaciones han reportado que la GM es un excelente agente encapsulador de aceites esenciales dentro de un amplio intervalo de actividades acuosas (0.108–0.743 a 35 °C), y un agente emulsionante y estabilizante de colorantes naturales (Perez–Alonso y col., 2003; Beristain y col., 2001, 2002; Rodríguez–Huezo y col., 2004).
El Q, por otra parte, es la forma N desacetilada de la quitina de la que se obtiene tras sustituir los grupos acetamido por grupos amino, es un polisacárido catiónico de alto peso molecular, químicamente está constituido de unidades de glucosamina parcialmente desacetilado (2 amino–2 deoxi–D–glucosa), es biodegradable, no tóxico y soluble en soluciones ácidas, que posee actividad microbiana, funguicida, bactericida y nematicida (Coma y col, 2002). Su peso molecular tiene un intervalo de 10,000 a 1,000,000 g/mol (Fredheim y Christensen, 2003). En los últimos años, el Q ha recibido un interés especial debido a su capacidad de formar complejos polielectrolitos (Espinosa–Andrews y col., 2008). Cuando éstos complejos son con un biopolímero que posee actividad superficial, pueden ser usados como agentes emulsionantes y estabilizantes mediante la formación de membranas alrededor de las gotas de emulsiones O/W (Ogawa y col., 2004).
El objetivo del presente trabajo es determinar el efecto de las interacciones del complejo goma de mezquite–quitosano sobre las propiedades reológicas interfaciales, y evaluar su influencia sobre la estructura, propiedades reológicas y estabilidad de emulsiones sencillas O/W y múltiples W1/O/W2.
2 Metodología
2.1 Materiales
Goma de mezquite (Prosopis laevigata), recolectada en forma de lágrima en el estado de San Luis Potosí y purificada según Vernon–Carter y col. (1996). Quitosano de peso molecular medio y 79% de grado de desacetilación, adquirido en Sigma–Aldrich Química, S.A. de C.V. (Toluca, Edo. Méx.).
GrinstedPGR (Poliglicerol ésterde ácido recinoleico), proporcionado por Danisco Cultor Mexicana, Jalisco, Mex. Aceite de Canola, proporcionado por Unilever de México S.A. de C.V. Tultitlán, Edo. Mex. ácido acético, comprado en J.T. Baker, S.A. de C.V. (Xalostoc, Edo. Mex.). Agua destilada con una tensión superficial de 72 ± 0.4 mN m–1 a 25 °C.
2.2 Preparación de las soluciones de biopolímeros
Se prepararon soluciones al 10% (p/p) de GM y diferentes concentraciones de Q (0.2, 0.4, 0.6, 0.8 y el 1.0% p/p), disueltas en 1.0 % (p/p) de ácido acético. Las soluciones fueron mezcladas durante dos horas en un agitador magnético Corning PC–420D a 320 rpm y temperatura ambiente antes de formar la interfase. El pH de las soluciones fue de 3.8, aproximadamente.
2.3 Reología interfacial
La caracterización de las interacciones entre la GM y Q en la interfase agua–aceite de Canola se realizó mediante la medición de la viscosidad aparente interfacial (ηint) y propiedades de fluencia–capacitancia (Creep–compliance) utilizando la metodología propuesta por Pérez–Orozco y col. (2004). Para ello, se utilizó un reómetro Paar–Physica MCR 300 (Anton–Paar, Messtechnik, Stuttgart, Alemania) con una geometría tipo bicono de 15 mm de radio (Rb) y doble ángulo de 10°. La temperatura de medición fue de 25°C, y se controló utilizando un baño refrigerante de acrílico con un radio interno (Rc) de 27 mm y una profundidad de 34 mm. Para formar la interfase se adicionó 30 mL de la solución de biopolímeros sobre el baño refrigerante, el bicono se bajó lentamente hasta ubicarse en la interfase agua–aire, posteriormente, se formó la interfase agua–aceite adicionando 30 mL de aceite de Canola.
2.3.1 Medición de la viscosidad aparente interfacial
Se hizo girar el bicono a una velocidad angular constate (Ω) de 1.27 x 10–3 rad/s; se midió el ángulo de desplazamiento en función del tiempo (θ(t)) y el momento de fuerza (M) necesario para mantener dicha velocidad. Con los valores obtenidos en la región de equilibrio del momento de fuerza aplicado se calculó la viscosidad aparente interfacial (ηint), la deformación de la interfase (γint) y el esfuerzo de cizalla interfacial (σint) mediante las siguientes expresiones:



donde r es la posición radial en la interfase con Rb < r < Rc y Ωt = θ(t) es el ángulo de desplazamiento del bicono determinado por el equipo (Pérez–Orozco y col., 2004).
2.3.2 Medición de las propiedades de fluencia–capacitancia interfaciales
Después de 24 h de formada la interfase agua–aceite de Canola, se aplicó un momento de fuerza constante de 0.5 μNm durante 15 min, y posteriormente se aplicó un momento de fuerza de magnitud cero (15 min). Se midió el ángulo de desplazamiento y se evaluó la deformación y esfuerzo de cizalla interfacial cada 10 s, con estos valores se calculó la capacitancia del sistema, mediante la expresión (Sherman, 1969):

2.4 formulación y caracterización de las emulsiones aceite–en–agua (O/W)
Se formularon emulsiones O/W utilizando las soluciones de GM–Q como fase continua y aceite de Canola como fase dispersa con una fracción en peso ( ) de 0.2. La fase oleosa fue adicionada a la mezcla de polímeros poco a poco hasta tener una dispersión homogénea. Las emulsiones se homogenizaron usando un homogenizador Silverson L4R (Silverson Machines, Ltd., Waterside, Chesham. Bucks., Inglaterra) a 5800 rpm durante 20 minutos a temperatura ambiente.
) de 0.2. La fase oleosa fue adicionada a la mezcla de polímeros poco a poco hasta tener una dispersión homogénea. Las emulsiones se homogenizaron usando un homogenizador Silverson L4R (Silverson Machines, Ltd., Waterside, Chesham. Bucks., Inglaterra) a 5800 rpm durante 20 minutos a temperatura ambiente.
2.4.1 Determinación de la cinética de coalescencia en las emulsiones O/W
Se determinó el diámetro promedio volumétrico de los glóbulos de las emulsiones utilizando un analizador de tamaño y distribución de partículas Malver MasterSize 2600 (Malvern Instruments, Worcs, Inglaterra), y se calculó la tasa de coalescencia específica (Kc) considerando que la velocidad de coalescencia en las emulsiones sigue una cinética de primer orden (Sherman, 1969):

con

la cual relaciona el número de gotas de la fase dispersa a un tiempo (Nt) con el número inicial de gotas de fase dispersa (No),  es la fracción volumétrica de la fase dispersa y D4.3 es el diámetro promedio volumétrico (μm) a un tiempo t(s).
es la fracción volumétrica de la fase dispersa y D4.3 es el diámetro promedio volumétrico (μm) a un tiempo t(s).
2.4.2 Propiedades reológicas de las emulsiones O/W
Las pruebas fueron realizadas en el reómetro Paar–Physica MCR 300 utilizando una geometría de doble gap con una relación de radios de 1.035, y una temperatura de 25°C controlada con sistema Peltier. Se evaluaron los módulos de pérdida (G') y almacenamiento (G'') aplicando un barrido de frecuencia de 0.01–10 Hz con una deformación constante de 0.3% dentro de la región viscoelástica lineal (localizada por debajo del 1% para todas las formulaciones). Se aplicó un barrido de esfuerzo de cizalla de 0.1–100 Pa y se obtuvieron las curvas de flujo.
2.4.3 Medición del potencial Zeta
Las emulsiones O/W fueron diluidas 1:10 mL en una solución acuosa al 1 % de ácido acético y se inyectaron en la cámara de un instrumento de medición de tamaño de partícula y movilidad electroforética (ZEM3500, Zetasizer Nano ZS, Malvern Instruments, Worchesire, Inglaterra).
2.5 formulación y caracterización de la emulsión W1/O/W2
Se formularon emulsiones W1/O/W2 por el método de las dos etapas, seleccionando la relación de biopolímeros que brindó las mejores condiciones de estabilidad en los análisis previos. La emulsión interna agua–en–aceite (W1/O) se homogenizó a 5800 rpm durante 20 min. con una  W/O de 0.2 utilizando una concentración de 8% de Grinsted como agente emulsionante lipofílico. La emulsión múltiple se obtuvo adicionando lentamente la emulsión primaria a la solución acuosa de biopolímeros, y ésta se homogenizó a 5000 rpm durante 10 min, la
W/O de 0.2 utilizando una concentración de 8% de Grinsted como agente emulsionante lipofílico. La emulsión múltiple se obtuvo adicionando lentamente la emulsión primaria a la solución acuosa de biopolímeros, y ésta se homogenizó a 5000 rpm durante 10 min, la  W/O/W fue de 0.2.
W/O/W fue de 0.2.
Se determinó el diámetro promedio volumétrico superficial (D3,2) para las gotas internas y el diámetro promedio volumétrico (D4,3) para los glóbulos externos usando un sistema de análisis de imágenes (Microscopio óptico Olimpus BX 45, cámara digital Olimpus C–3030 y software Image–pro plus versión 4.5) y aplicando las ecs. (7) y (8).


donde ni es la gota i, y di es el diámetro de la gota i.
3 Resultados y discusión
3.1 Reología interfacial de los complejos GM–Q
La Fig. 1 muestra el comportamiento de la ηint vs tiempo de envejecimiento de las películas de GM–Q adsorbida en la interfase agua–aceite de Canola. Todas las películas mostraron un incremento en ηint, hasta llegar a un punto en el cual la viscosidad ya no varía debido a que los rearreglos intramoleculares alcanzan un equilibrio en la interfase. Este equilibrio de estructural de la película se alcanzó después de 12 h. Los valores de ηint indican la existencia de una interacción sinérgica entre los polielectrolitos que depende de su concentración relativa. Las películas formadas con las soluciones de 10%GM–0.2%Q y 10%GM–0.4%Q tienen valores de ηint mayores que la formada con la solución de 10%GM, indicando un incremento en la capacidad y velocidad de adsorción de los biopolímeros en la interfase agua–aceite de Canola. Al incrementar la concentración de quitosano la capacidad de adsorción de los complejos formados se ve disminuida, y por ende, se presenta un disminución en la valor de ηint.
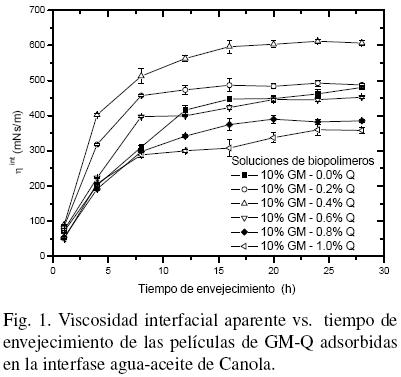
Un comportamiento similar fue presentado por la adsorción de estas macromoléculas en la interfase agua–aceite Mineral (Perez–Orozco, y col., 2004), en la que al aumentar la concentración de Q la densidad de carga neta de la solución de biopolímeros empieza a ser menos negativa, indicando una interacción del tipo electrostática entre los biopolímeros. A concentraciones de 0.2% y 0.4% (p/p) de Q, la interacción de este con la GM permite la formación de complejos (coacervados) solubles que difunden más rápidamente y se adsorben en la interfase agua–aceite; la mayor interacción complejo–complejo presente en la película adsorbida da como resultado un aumento en la resistencia a la deformación. La solución con una concentración de 10%GM–0.6%Q presentó una neutralización en su densidad de carga neta, incrementando la formación de complejos electrostáticos y disminuyendo los sitios hidrofílicos, lo que provoca una disminución del valor de ηint a valores aproximados a los obtenidos por la goma pura. A concentraciones de 10%GM–0.8%Q y 10%GM–1.0%Q, la mayor cantidad de moléculas de Q disponibles para interactuar con la GM provoca que los sitios hidrofílicos de ésta disminuyan, y, por consecuencia, ésta se contrae y sufre un apantallamiento, disminuyendo al máximo la adsorción de biopolímeros en la interfase agua–aceite, lo que da como resultado que los valores de ηint sean menores que los obtenidos por la GM. Para una misma relación de biopolímeros, los valores de ηint de la película de GM–Q adsorbida en la interfase agua–aceite de Canola son mayores que aquellos reportados por Pérez–Orozco y col. (2004) en la interfase agua–aceite Mineral, este incremento en la ηint es el resultado de la mayor interacción de los complejos GM–Q con los residuos hidrofílicos correspondientes a los grupos carboxílicos de los ácidos oleico, linoleico y linolénico que constituyen el aceite de Canola (Bayourthe y col., 2000; Mariya y Nikolay, 2002).
En la Fig. 2 se muestra el comportamiento de las propiedades de fluencia–capacitancia de las películas de biopolímeros adsorbidas en la interfase agua–aceite de Canola, a partir de las diferentes formulaciones a un tiempo de envejecimiento de 24 h, excepto el de las concentraciones de 0.8 y 1.0% de Q, cuyos valores de capacitancia (J(t)), aunque presentaron un comportamiento viscoelástico, salieron del intervalo de medición. Los datos experimentales se ajuntaron al siguiente modelo con un tiempo de relajación:


donde J0 es la capacitancia instantánea, Jm es la capacitancia de relajación, tm es el tiempo de relajación y JN es la capacitancia newtoniana. Los valores de los parámetros del modelo se reportan en la Tabla 1. Los datos muestran que la adición de Q a concentraciones de 0.2 y 0.4 incrementa el valor del módulo elástico instantaneo (E0 = 1/J0), debido a la existencia de un mayor número de entrecruzamientos y enredos moleculares, que a su vez, le confieren una mayor rigidez e incrementa las fuerzas de cohesión de la película de de complejos GM–Q adsorbida en la interfase (Borbas y col., 2003). Los parámetros de la región de relajación como son el mó dulo elástico de relajación (Em= 1/Jm) y tiempo de relajación (tm) proporcionan una medida sobre la complejidad y diversidad de los enlaces en la estructura interfacial (Lobato–Calleros y col., 2000). Las películas adsorbidas en la interfase con una concentración menor o igual a 0.4% de Q presentaron mayores valores de Em y tm (Tabla 1) como resultado de una mejor orientación de los complejos adsorbidos (Ducel y col., 2005).
La región de equilibrio para evaluar la viscosidad interfacial newtoniana (ηN = t/JN) es caracterizada por el rompimiento de los entrecruzamientos que unen la estructura interfacial, y como el tiempo requerido para su reacomodo es mayor que el tiempo de prueba trae como consecuencia que exista un flujo de corte a través de la interfase (Martin y col., 2002). El comportamiento en los valores de ηN presentados en la Tabla 1 corroboran los resultados obtenidos en las curvas de ηint (Fig. 1), mayores valores en la viscosidad interfacial newtoniana, que presenta un máximo en 0.4% Q, son indicativo de la existencia de una mayor fuerza de cohesión entre los complejos absorbidos en la interfase, y por ende de una mayor resistencia al flujo.
3.2 Interacciones de los complejos GM–Q en la emulsión O/W
En la Fig. 3 se muestra la variación en el tamaño promedio volumétrico (D4,3) de los glóbulos de la emulsión O/W, en función del tiempo de envejecimiento. Como se puede observar la adición del Q disminuye el diámetro de los glóbulos de la emulsión. El sistema que presentó el menor diámetro fue el formulado con la relación de 10%GM–0.2%Q, seguido de las emulsiones con 10%GM–0.4%Q y 10%GM–0.6%Q. Para las concentraciones de 10%GM–0.8%Q y 10%GM–1.0%Q no fue posible la formulación de la emulsión debido a la formación de complejos insolubles que tienden a sedimentarse en la fase acuosa. Este comportamiento en D4,3 se puede fundamentar en el hecho de que el complejo electrostático GM–Q interactúa fuertemente con la fase oleosa. Debido a esto, durante la formación de las emulsiones la rapidez de adsorción del complejo GM–Q en las interfases formadas es mayor que la rapidez de adsorción de la GM, como consecuencia de, por un lado, un mayor reacomodo de la GM en la interfase, y por otro, la posible interacción de los grupos amino del Q con las residuos polares del aceite de Canola, todo ello promueve un incremento de la actividad superficial del complejo que se ve reflejado en una disminución del tamaño del glóbulo del sistema disperso. La disminución en D4,3 en las emulsiones O/W presenta un máximo a 0.2% Q, posteriormente existe un ligero incremento del glóbulo de la emulsión, mientras este último sufre una neutralización en su densidad de carga negativa (aproximadamente a 0.4%Q) hasta presentar un cambio de signo –"overcharging" (Ogawa y col., 2003) a concentraciones de 0.6%Q (ver Fig. 4). Los valores de las tasas de coalescencia específica (KC) reportados en la Tabla 2 permiten inferir que los sistemas son estables (Sherman, 1969).



La Fig. 5 muestra el comportamiento viscoelástico de las emulsiones recién formuladas, la prueba se realizó dejando reposar 30 min la emulsión en el reó metro. Las emulsiones formuladas con una concentración de 0 a 0.4% Q exhibieron un mayor carácter elástico que viscoso, y presentaron una ligera dependencia en los módulos viscoelásticos con respecto a la frecuencia, los cuales tuvieron una pequeña disminución al aumentar esta ultima. La poca dependencia de G' respecto a la frecuencia se debe a la fuerte adsorción del complejo GM–Q en la interfase agua–Aceite de Canola que aumenta las fuerzas de van der Waals, así como a la existencia de una mayor interacción intergota que disminuye la movilidad del sistema (Blijdenstein y col., 2004).

La emulsión formada con 10%GM–0.6%Q presentó un comportamiento totalmente diferente con propiedades viscoelásticas altamente dependiente de la frecuencia. A frecuencias mayores de 0.1 Hz, G' fue menor que G'', indicando que en este intervalo de frecuencia la emulsión es predominantemente viscosa en su naturaleza (Fig. 5). Dicho comportamiento probablemente se deba a que los complejos electrostáticos no adsorbidos forman una región de agotamiento alrededor de las gotas de la emulsión que induce una atracción débil de las fuerzas intergota, provocando una mayor movilidad en el sistema que da como resultado una alta dependencia de G' con respecto a la frecuencia, y que, a altas frecuencias, esta movilidad le proporcione a la emulsión un mayor carácter viscoso.
El comportamiento de la viscosidad vs velocidad de cizallamiento de las emulsiones aceite–en–agua se muestra en la Fig. 6. Los sistemas fueron ajustados al modelo de Ostwald–de Waele (τ = k( )n). Las formulaciones con concentraciones de 0–0.4% Q, exhibieron un comportamiento Newtoniano en la viscosidad; mientras que los sistemas con 0.6% Q reflejan un comportamiento mas reoadelgazante, tal como lo indica el factor de flujo (n) obtenido del modelo ajustado. La viscosidad de las emulsiones permaneció prácticamente igual con el tiempo de envejecimiento, lo cual confirma que la tasa de coalescencia (Tabla 2) de los sistemas es relativamente baja, y los bajos valores obtenidos para el potencial Zeta reportados en la Fig. 4 indican que la estabilidad de las emulsiones es provocada por efectos estéricos y no por electrostáticos.
)n). Las formulaciones con concentraciones de 0–0.4% Q, exhibieron un comportamiento Newtoniano en la viscosidad; mientras que los sistemas con 0.6% Q reflejan un comportamiento mas reoadelgazante, tal como lo indica el factor de flujo (n) obtenido del modelo ajustado. La viscosidad de las emulsiones permaneció prácticamente igual con el tiempo de envejecimiento, lo cual confirma que la tasa de coalescencia (Tabla 2) de los sistemas es relativamente baja, y los bajos valores obtenidos para el potencial Zeta reportados en la Fig. 4 indican que la estabilidad de las emulsiones es provocada por efectos estéricos y no por electrostáticos.

3.3 Formulación y caracterización de la emulsión W1/O/W2
De acuerdo a los análisis previos, se utilizó la mezcla de 10%GM–0.4%Q para formar la emulsión múltiple (W1/O/W2) y se comparó con una emulsión que solo contenía GM. La Fig. 7 muestra la relación entre el D3,2/D4,3 del glóbulo interno y externo respectivamente. Como podemos observar, la presencia de complejos electrostáticos entre la GM y Q en la formulación de la emulsión W1/O/W2 genera la formación de una membrana polimérica que se adsorbe alrededor de los glóbulos externos de la emulsión, la cual brinda un mayor control del transporte difusivo de agua entre la fase acuosa interna y externa provocados por los gradientes osmóticos. De igual forma, se ven disminuidos los fenómenos de floculación y coalescencia, por lo que el sistema presentó una alta estabilidad, reflejada en la no variación en la relación D3,2 D4,3 durante el tiempo de envejecimiento (30 días). La Fig. 8 confirma los resultados descritos previamente, los diámetros de los glóbulos internos y externos permanecieron sin variación a los días 1, 15 y 30 (Fig. 8d, e, f) de formulada la emulsión, y la morfología presentada por el sistema fue del tipo C (Florence y Whitehill, 1981).

La ausencia de Q en la formulación de la emulsión múltiple originó un incremento en los mecanismos de desestabilización del sistema, que puede atribuirse a la débil adsorción de la película polimérica (GM) en la interfase aceite–agua externa. Este fenómeno provocó una ligera coalescencia tanto en los glóbulos internos como externos; y un ligero transporte de agua entre las fases acuosas interna y externa que es posible observar bajo el microscopio. Lo anterior se reflejo en el incremento de la relación D3,2/D4,3 (Fig. 7) y en el cambio de la morfología del sistema, pasando del tipo C (Fig. 8a) al tipo A y B con el tiempo (Fig. 8b y c). Efectos similares han sido reportados por Benichou y col. (2007), quienes demostraron que el uso de complejos poliméricos formados con aislado de proteína de leche y goma xantana, permite la obtención de emulsiones dobles W/O/W con diámetros menores y una mayor estabilidad comparadas con las emulsiones obtenidas al 5%(p/p) del aislado de proteína.
Las curvas de flujo de las emulsiones W1/O/W2 recién formadas se muestran en la Fig. 9. La ausencia de Q provocó que el sistema disperso exhibiera un comportamiento reoadelgazante como consecuencia de la deformación aplicada. Los glóbulos de la emulsión son afectados por la acción de dos fuerzas opuestas cuando son sometidos a un flujo de corte estacionario macroscópico (Pal, 1996), las cuales están dadas por: (1) el esfuerzo viscoso de magnitud ηc , el cual que tiende a deformar en forma longitudinal los glóbulos (ηc es viscosidad de la fase continua, y es la velocidad de corte) y (2) el esfuerzo de magnitud σ/R que tiende a minimizar la energía superficial y por lo tanto, trata de mantener los glóbulos en forma esférica (σ es la tensión interfacial y R es el radio de los glóbulos). Cuando se incrementa la magnitud de la velocidad de cizallamiento, los glóbulos de las emulsiones empiezan a elongarse en un grado mayor en la dirección del flujo, dando como resultado una disminución en la viscosidad del sistema (carácter reoadelgazante, n < 1). Este comportamiento de las emulsiones es el resultado del incremento de los mecanismos de floculación y coalescencia del sistema. El sistema múltiple formulado en presencia de Q mostro un comportamiento de flujo Newtoniano, lo cual es indicativo de que los glóbulos de la emulsión presentan una mayor resistencia a los esfuerzos de flujo, como consecuencia de la adsorción de la película polimérica en la interfase externa agua–aceite, la cual brinda una mayor elasticidad a los glóbulos y en consecuencia, una mayor estabilidad contra los mecanismos de floculación y coalescencia.
, el cual que tiende a deformar en forma longitudinal los glóbulos (ηc es viscosidad de la fase continua, y es la velocidad de corte) y (2) el esfuerzo de magnitud σ/R que tiende a minimizar la energía superficial y por lo tanto, trata de mantener los glóbulos en forma esférica (σ es la tensión interfacial y R es el radio de los glóbulos). Cuando se incrementa la magnitud de la velocidad de cizallamiento, los glóbulos de las emulsiones empiezan a elongarse en un grado mayor en la dirección del flujo, dando como resultado una disminución en la viscosidad del sistema (carácter reoadelgazante, n < 1). Este comportamiento de las emulsiones es el resultado del incremento de los mecanismos de floculación y coalescencia del sistema. El sistema múltiple formulado en presencia de Q mostro un comportamiento de flujo Newtoniano, lo cual es indicativo de que los glóbulos de la emulsión presentan una mayor resistencia a los esfuerzos de flujo, como consecuencia de la adsorción de la película polimérica en la interfase externa agua–aceite, la cual brinda una mayor elasticidad a los glóbulos y en consecuencia, una mayor estabilidad contra los mecanismos de floculación y coalescencia.

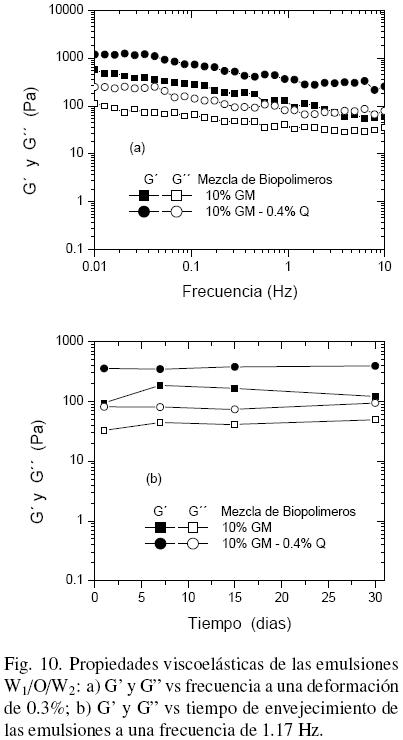
La Fig. 10a muestra los módulos G' y G'' de las emulsiones múltiples W1/O/W2. Podemos apreciar que el carácter elástico predominó sobre el carácter viscoso (G' > G''). La presencia de Q en el sistema da como resultado un aumento en el carácter elástico (un incremento en G'). Este comportamiento se mantuvo constante respecto al el tiempo de envejecimiento de la emulsión (Fig. 10b). La mayor estabilidad presentada por el sistema W1/O/W2 formulado con el complejo 10%GM–0.4%Q está en estrecha relación con las propiedades de adsorción del complejo en la interfase agua–aceite. El comportamiento reológico de los sistemas emulsionados (O/W y W1/O/W2) es gobernado por la capacidad que tiene el complejo GM–Q de formar una película adsorbida continua y homogénea alrededor de las gotas de aceite. Las características estructurales de la película adsorbida pueden ser determinadas mediante el análisis de sus propiedades reológicas interfaciales: un mayor módulo elástico interfacial y una mayor viscosidad interfacial son el resultado de la formación de una película rígida y homogénea, como consecuencia de una mejor orientación de las moléculas en la interfase, y estas propiedades juegan un papel importante para el control de los mecanismos de desestabilización de los sistemas dispersos (emulsiones y espumas).
Conclusiones
La viscosidad aparente interfacial y propiedades de fluencia–capacitancia de las películas de GM–Q adsorbidas en la interfase agua–aceite de Canola fueron afectadas por la concentración relativa de ambas macromoléculas. Los complejos formados con 10%GM y concentraciones de Q de 0.2, 0.4 y 0.6%Q exhibieron una mayor capacidad de adsorción en la interfase en comparación con la GM pura. Los valores de ηint , E0, Em, y ηN se ven maximizados cuando la película de biopolímeros adsorbida en la interfase está formada por los complejos obtenidos a partir de 10%GM–0.4%Q, lo que es indicativo de la existencia de una mejor orientación molecular y mayores fuerzas de cohesion en la película. La presencia de un mayor número de cargas positivas en el sistema, a concentraciones de 0.8 y 1% de Q, origina una neutralización y encogimiento de los complejos GM–Q formados, disminuyendo la cantidad de sitios hidrofílicos, y por ende, su solubilidad, dando como resultado una disminución en la capacidad de adsorción del complejo GM–Q.
El uso de un polisacárido catiónico, p.e. el Q, en combinación con un hidrocoloide aniónico con mayor actividad superficial, tal es el caso de la GM, da origen a la formación de complejos electrostáticos en soluciones acuosas, cuya interacción tiene un beneficio significativo en la estabilidad de emulsiones O/W. La mayor capacidad de adsorción en las interfases agua–aceite de los complejos GM–Q mejora la estabilidad y homogeneidad de la distribución de tamaño de los glóbulos de las emulsiones O/W, y provoca una disminución en el D4,3. Al presentarse una neutralización en la carga neta de la película de biopolímeros (10%GM–0.4%Q) adsorbida alrededor de las gotas de la emulsión O/W, el sistema exhibe un comportamiento newtoniano, un mayor carácter viscoelástico (con G' > G'') y una menor tasa de coalescencia; bajo estas condiciones, la GM y el Q interactúan fuertemente formando complejos que se adsorben en las interfases agua–aceite de Canola y estabilizan la emulsión O/W mediante efectos estéricos.
Finalmente, podemos mencionar que existe una estrecha relación entre las propiedades reológicas interfaciales evaluadas en la interfase agua–aceite de Canola y las propiedades reológicas y estabilidad de la emulsión O/W. Un mayor módulo elástico interfacial y una mayor viscosidad aparente interfacial son el resultado de la formación de una película rígida y homogénea, como resultado de una mejor orientación de las moléculas en la interfase; esto permite tener un mejor control sobre los mecanismos de desestabilización en los sistemas dispersos. Los resultados de los análisis realizados en la interfase y en las emulsiones O/W se utilizaron para seleccionar la mezcla de biopolímeros 10%GM–0.4%Q, la cual permitió la formación de complejos electrostaticos que al adsorberse en la interfase externa aceite–agua de la emulsión múltiple W1/O/W2, le confieren una mayor estabilidad, manteniendo las propiedades reológicas y estructurales con variaciones mínimas durante el tiempo de envejecimiento (30 días) de la emulsión.
Referencias
Bayourthe, C., Enjalbert, F. y Moncoulon R. (2000). Effects of different forms of canola oil fatty acids plus canola meal on milk composition and physical properties of butter. Journal of Dairy Science 83, 890–896. [ Links ]
Benichou, A., Aserin, A. y Garti, N. (2007). W/O/W double emulsions stabilized with WPI–polysaccharide complexes. Colloids and Surfaces A: Physicochemical Engineering Aspects 294, 20–32. [ Links ]
Beristain, C. I., Azuara, E. y Vernon–Carter, E. J. (2002). Effect of water activity on the stability to oxidation of spray–dried encapsulated orange peel oil using mesquite gum (Prosopis juliflora) as wall material. Journal of Food Science 67, 206–211. [ Links ]
Beristain, C.I., García, H.S. y Vernon–Carter, E.J. (2001). Spray–dried cardomom essential oil mesquite (Prosopis juliflora) gum. Lebensmittel Wissenschaft und Technologie 34, 398–401. [ Links ]
Blijdenstein, T.B.J., van der Linden, van Vliet, T. y van Aken, G.A. (2004). Scaling behavior of delayed memixing, rheology, and microstructure of emulsions flocculated by depletion and bridging. Langmuir 20, 11321–11328. [ Links ]
Borbas, R., Murray, B.S. y Kiss, E. (2003). Interfacial shear rheological behaviour of proteins in three–phase partitioning systems. Colloids and Surfaces A: Physicochemical Engineering Aspects 213, 93–103. [ Links ]
Cho, Y.H. y Park, J. (2003). Evaluation of process parameters in the O/W/O multiple emulsion method for flavor encapsulation. Journal of Food Science 68, 534–538. [ Links ]
Coma, V., Martial–Gros, A., Garreau, S., Copinet, A., Salin, F. y Deschamps, A. (2002). Edible antimicrobial films based on chitosan matrix. Journal of Food Science 67, 1162–1169. [ Links ]
Ducel, V., Richard, R., Popineau, Y. y Boury, F. (2005). Rheological interfacial properties of plant protein–arabic gum coacervates at the oil–water interface. Biomacromolecules 6, 790–796 [ Links ]
Espinosa–Andrews, H., Lobato–Calleros, C., Loeza–Corte, J.M., Beristain, C.I., Rodríguez–Huezo. M.E. y Vernon–Carter, E.J. (2008). Quantification of the composition of gum arabic–chitosan coacervates by HPLC. Revista Mexicana de Ingeniería Química 7(3), 293–298. [ Links ]
Florence, A.T. y Whitehill, D. (1981). Some features of breakdown in water–in–oil–in–water multiple emulsions. Journal of Colloid and Interface Science 79, 243–256. [ Links ]
Fredheim, G.E. y Christensen, B.E. (2003). Polyelectrolyte complexes: Interactions between lignosulfonate and chitosan. Biomacromolecules 4, 232–239. [ Links ]
Girard, M., Tuergeon, S.L. y Paquin, P. (2002). Emulsifying properties of whey protein–carboxymethylcellulose complexes. Journal of Food Science 67, 113–119. [ Links ]
Krägel, J y Derkatch, S.R. (2010). Interfacial shear rheology. Current opinion in colloid & interface science 15, 246–255. [ Links ]
Laplante, S., Turgeon, S.L. y Paquin, P. (2005). emulsion stabilizing properties of various chitosans in the presence of whey protein isolate. Food Hydrocolloids 19,425–434. [ Links ]
Lindenstruth, K. y Muller, B.W. (2004). W/O/W multiple emulsions with diclofenac sodium. European Journal of Pharmaceutics and Biopharmaceutics 58, 621–627. [ Links ]
Lobato–Calleros, C., Recillas–Mota, M.T., Espinosa–Solares, T., Alvarez–Ramirez, J. y Vernon–Carter, E.J. (2009). Microstructural and rheological properties of low–fat stirred yoghurts made with skim milk and multiple emulsions. Journal of Texture Studies 40(6), 657–675. [ Links ]
Mariya M. y Nikolay J. (2002). Creating a yield stress in liquid oils by the addition of crystallisable modifiers. Journal of Food Engineering 51, 235–237. [ Links ]
Martin, A.H., Grolle, K., Bos, M.A., Cohen, M.A. y van Vliet, T. (2002). Network forming properties of various proteins adsorbed at the air/water interface in relation to foam stability. Journal of Colloid and Interface Science 254, 175–183. [ Links ]
Murillo–Martínez, M.M., Pedroza–Islas, R., Lobato–Calleros, C., Martínez–Ferez, A. y Vernon–Carter, E.J. (2011). Designing W1/O/W2 double emulsions stabilized by protein–polysaccharide complexes for producing edible films: Rheological, mechanical and water vapor properties. Food Hydrocolloids 25, 577–585. [ Links ]
Muschiolik, G. (2007). multiple emulsions for food use. Current Opinion in Colloid & Interface Science 12, 213–220. [ Links ]
Ogawa, S., Decker, E.A. y McClements, D.J. (2004). Production and characterization of O/W emulsions containing droplets stabilized by lecithin–chitosan–pectin. Journal of Agricultural and Food Chemistry 52, 3595–3600. [ Links ]
Osés, J., Fabregat–Vázquez, M., Pedroza–Islas, R., Tomas, S.A., Cruz–Orea, A. y Maté, J.I. (2009). Development and characterization of composite edible films based on whey protein isolate and mesquite gum. Journal of Food Engineering 92, 56–62. [ Links ]
Özer, Ö., Muguet, V., Roy, E, Grossiord, J.L. y Seiller, M. (2000). Stability study of W/O/W viscosified multiple emulsions. Drug Development and Industrial Pharmacy 26(11), 1185–1189. [ Links ]
Pal, R. (2000). Linear Viscoelastic Behavior of multiphase dispersions. Journal of Colloid and Interface Science 232, 50–63. [ Links ]
Pérez–Alonso, C., Báez–González, J. G., Beristain, C. I., Vernon–Carter, E.J. y Vizcarra–Mendoza, M. G. (2003). Estimation of the activation energy of carbohydrate polymers blends as selection criteria for their use as wall material for spray–dried microcapsules. Food Carbohydrates 53, 197–203. [ Links ]
Pérez–Orozco, J.P., Beristain, C.I., Espinosa–Paredes G., Lobato–Calleros, C. y Vernon–Carter, E.J. (2004). Interfacial shear rheology of interacting carbohydrate polyelectrolytes at the water–oil interface using an adapted conventional rheometer. Carbohydrate Polymers 57, 45–54. [ Links ]
Pimentel–González, D.J., Campos–Montiel, R.G., Lobato–Calleros, C., Pedroza–Islas, R. y Vernon–Carter, E.J. (2009). Encapsulation of Lactobacillus rhamnosus in double emulsions formulated with sweet whey as emulsifier and survival in simulated gastrointestinal conditions. Food Research International 42, 292–297. [ Links ]
Rodríguez–Huezo, M.E., Pedroza–Islas, R., Prado–Barragán, L.A., Beristain, C.I. y Vernon–Carter, E.J. (2004). Microencapsulation by spray drying of multiple emulsions containing carotenoids. Journal of Food Science 69, 351–359. [ Links ]
Román–Guerrero, A., Orozco–Villafuerte, J., Pérez–Orozco, J.P., Cruz–Sosa, F., Jiménez–Alvarado, R. y Vernon–Certer, E.J. (2009). Application and evaluation of mesquite gum and its fractions as interfacial film formers and emulsifiers of orange peel–oil. Food Hydrocolloids 23, 708–713. [ Links ]
Sherman, P. (1969). General properties of emulsions and their constituents. In P. Sherman (Ed.), emulsion Science. London, England: Academic Press. 217–351. [ Links ]
Su, J., Flanagan, J. y Singh H. (2008). Improving encapsulation efficiency and stability of water–in–oil–in–water emulsions using a modified gum arabic (Acacia (sen) SUPER GUM TM). Food Hydrocolloids 22, 112–120. [ Links ]
Vernon–Carter, E.J., González, E.E. y Jarquin, H. (1996). Rheological properties of mesquite and arabic gum films at the oil–water interface. Theoretical and Applied Developments in Rheology 51–62. [ Links ]














