Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.69 no.2 México mar./abr. 2012
Caso clínico
Osteopetrosis, calcificación más allá del sistema óseo. Reporte de un caso
Osteopetrosis — calcification beyond the skeletal system. A case report
Patricia Mejía Osuna,1 Jesús Santos-Guzmán,2 Luis Villela,1 Enrique Javier Cedillo-Alemán,1 Adrián García3
1 Cátedra de Hematología y Cáncer, Escuela de Medicina TEC de Monterrey Instituto Tecnológico de Estudios Superiores de Monterrey (ITESM)
2 Cátedra de Terapia Celular, Escuela de Medicina TEC de Monterrey Instituto Tecnológico de Estudios Superiores de Monterrey (ITESM)
3 Jefe de Traumatología de la Clínica 21, Instituto Mexicano del Seguro Social; Monterrey, Nuevo León, México
Autor de correspondencia:
Dr. Jesús Santos-Guzmán
Correo electrónico: jsg@itesm.mx
Fecha de recepción: 28-06-11.
Fecha de aceptación: 11-11-11.
Resumen
Introducción. La osteopetrosis se presenta por una falla en la apoptosis de los osteoclastos, que producen un hueso altamente calcificado pero con mayor fragilidad. Al acumularse calcio en los espacios de los huesos largos destinados a la hematopoyesis, predomina la hematopoyesis secundaria. Con el tiempo se producen visceromegalias y pancitopenias. Es una enfermedad genética con baja incidencia y poca prevalencia en México.
Caso clínico. Se trata de un paciente de sexo femenino de 12 años que inició con dolor en los huesos largos durante su niñez temprana de manera recurrente presentaba múltiples fracturas e infecciones; se mantenía en tratamiento con analgésicos y restricción de calcio. Se le considera como candidata para un trasplante de médula ósea, que no se ha realizado.
Conclusiones. La osteopetrosis es una enfermedad poco común y compleja. Actualmente, no existe un tratamiento médico efectivo, por lo que es necesario un abordaje multidisciplinario. El trasplante de médula ósea constituye una alternativa viable para el tratamiento de algunos casos de osteopetrosis severa.
Palabras clave: osteopetrosis, calcio, osteoclasto, anemia, trasplante de médula ósea.
Abstract
Background. Osteopetrosis represents a lack of apoptosis in osteoclastic activity, producing a highly calcified but fragile bone due to excess of calcium. Excess calcium deposited in the medullary compartment leads to bone expansion, producing a predominant secondary hematopoiesis accompanied by significant visceromegaly and pancytopenia. Osteopetrosis is a genetic disease with a low prevalence and incidence in Mexico.
Case report. We report the case of a 12-year-old female who presented with bone pain in the lower extremities at an early age. A radiological diagnosis of ostepetrosis was made, and the condition was complicated by multiple fractures and infections. The patient was treated with dietary modifications and analgesics and was considered to be a candidate for hematopoietic stem-cell transplant.
Conclusions. Osteopetrosis is a rare and complex disease without any current effective medical treatment, necessitating a multidisciplinary approach. Hematopoietic stem-cell transplantation offers a promising alternative treatment for certain cases of severe osteopetrosis.
Key words: osteopetrosis, calcium, osteoclast, anemia, hematopoietic stem-cell transplant.
INTRODUCCIÓN
La osteopetrosis o enfermedad de huesos de mármol (también conocida como enfermedad de Albers-Schönberg) se refiere a un grupo de desórdenes hereditarios raros del esqueleto caracterizado por el incremento de la densidad ósea en las radiografías.1 Es una enfermedad causada por la deficiente función o pobre desarrollo de los osteoclastos; resulta en la alteración del proceso de resorción ósea y provoca una variedad de cuadros clínicos que dependen del tipo primario del que se trate. Puede clasificarse en tres tipos: a) osteopetrosis autosómica recesiva maligna (también conocida como clásica) caracterizada por osteoclerosis, fracturas, talla corta, neuropatías compresivas y falla hematológica debida a la alteración en el desarrollo de la médula ósea; b) osteopetrosis autosómica recesiva intermedia; y c) osteopetrosis autosómica dominante (también llamada enfermedad de Albers-Schönberg), que se presenta con mayor frecuencia en adultos y con un espectro muy heterogéneo, desde asintomática hasta fatal (en casos raros).2
CASO CLÍNICO
Paciente femenino de 12 años de edad sin antecedentes prenatales, perinatales o antecedentes heredofamiliares de importancia. Como antecedentes patológicos ha presentado faringitis, otitis, infección de vías urinarias bajas, conjuntivitis y episodios de caries dental, así como giardiasis intestinal, con una frecuencia esperada para las niñas de su edad. A los 3 años presentó pie valgo; el traumatólogo le recomendó el uso de zapatos ortopédicos por el dolor en extremidades inferiores (no se reportó alteración en la distribución de calcio óseo).
A los 6 años, las imágenes radiológicas de los huesos largos permitieron que se hiciera el diagnóstico de osteopetrosis porque presentaba hiperosificación. Subsecuentemente, se encontraron valores séricos elevados de fósforo (42.9 mg/dL vs normal 0.6-12.5mg/dL). El calcio sérico se ha mantenido normal a través del tiempo. Desde los 7 años, la paciente ha reportado dolor en huesos largos y, a veces, en articulaciones, sin datos de artritis, inflamación o deformidad, aunque presentó fracturas en las costillas 6, 7 y 8 (costado izquierdo). La paciente se manejó con la restricción de calcio en la dieta y analgésicos. A pesar del tratamiento, ha presentado repetidas fracturas, sobre todo en las extremidades; también, infecciones ocasionales de los aparatos respiratorio y gastrointestinal.
A los 9 años presentó fractura y deformidad del antebrazo y la muñeca derechos; a los 10 años, solo infecciones de vías respiratorias no complicadas; a los 11 años, colecistitis que requirió colecistectomía (sin complicaciones); a finales del mismo año, fractura traumática en la región del peroné derecho, por el golpe de otro niño. A principios del año siguiente, mientras portaba la férula de yeso en la fractura anterior, se cayó y se fisuró el peroné contralateral; después, sufrió también fisura en la muñeca derecha, que sanó con órtesis de yeso. Posteriormente, padeció una infección de vías aéreas superiores, que tomó una semana en alcanzar su resolución.
Durante los 11 y 12 años de edad ha padecido esplenomegalia y pancitopenia, pero no ha requerido transfusiones, solamente la reposición oral de hierro y vitaminas. También ha presentado migrañas de manera frecuente. La curva de su crecimiento no se ha visto afectada por la enfermedad. A sus 12 años mide 156 cm y pesa 46.6 kg (dentro del percentil 50 para su edad). Presentó varicela no complicada pero, debido a la pancitopenia y neutropenia severa, requirió manejo intrahospitalario. Ocasionalmente, la paciente ha presentado mareos y cefaleas, por lo que se han evaluado, por medio de una tomografía axial computarizada (TAC) de cráneo simple, las estructuras intracraneales y propias del oído interno para descartar neuropatías compresivas. Se encontró únicamente esclerosis ósea generalizada en la bóveda craneana, la base del cráneo y la región del peñasco, con aumento de la densidad y el grosor de las estructuras óseas. La TAC de oídos también mostró aumentada la densidad de la platina del estribo a nivel de la ventana oval; sin embargo, las estructuras del oído interno, la caja timpánica y el contenido se observaron normales, sin cambios con respecto a estudios previos. Tambien se realizó Holter de electrocardiograma de 24 horas para descartar un origen neurocardiogénico de los síntomas antes mencionados. En la actualidad se encuentra en un proceso de evaluación para someterla al trasplante de médula ósea.
DISCUSIÓN
Las manifestaciones que presentan los pacientes con osteopetrosis son muy variables y directamente proporcionales al grado de disfunción de los osteoclastos. La forma clásica se manifiesta con supresión medular, que conlleva anemia, trombocitopenia y complicaciones infecciosas graves, frecuentemente fatales durante la infancia. Esto, a diferencia de las formas menos severas, que cursan con un espectro muy variable de presentaciones clínicas, dentro de las que destacan malformaciones y fracturas frecuentes debido a fragilidad anormal en los huesos. El caso que presentamos posee características de mayor concordancia con el tipo de osteopetrosis autosómica dominante porque se observa que predominan manifestaciones esqueléticas, y no manifestaciones neonatales severas. A su vez, el tipo autosómico dominante de esta enfermedad se subdivide en los tipos I y II, basándose principalmente en el patrón radiológico del esqueleto axial. El tipo I presenta mayor afección de la bóveda craneal y escasa de la columna vertebral, a diferencia del tipo II, que se caracteriza por el engrosamiento y la esclerosis de las placas vertebrales terminales brindando la apariencia de "vértebra en sándwich" o ruggerjersey. También se han observado diferencias en los estudios (por ejemplo, el fosfato sérico es menor en el tipo I y la fosfatasa alcalina es mayor en el tipo II). Ello sugiere diferencias en el metabolismo óseo entre los dos tipos, e incluso diferencias clínicas, como mayor riesgo de fracturas en el tip II.3 En este caso, nos basamos principalmente en los patrones radiográficos para clasificar el cuadro como tipo II, dentro del patrón de osteopetrosis autosómica dominante (enfermedad de Albers-Schönberg) (Figura 1).
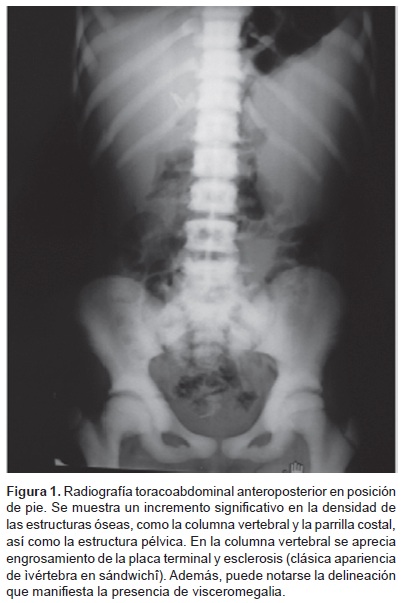
Los problemas ortopédicos que se presentan con mayor incidencia en las formas intermedias y autosómicas dominantes incluyen, además de fracturas, coxa vara, deformación en varus de los huesos largos, artritis degenerativa de las rodillas y caderas y ostiomielitis mandibular y de huesos largos. Los sitios comunes de fracturas son los huesos largos de los brazos y de las piernas, particularmente el cuello del fémur, el tercio superior de la diáfisis del fémur y el tercio superior de la tibia, la parte posterior de las costillas y el proceso acromial.4
Muchos niños con osteopetrosis se ubican por debajo del percentil 10 en las tablas de crecimiento, y algunos presentan enanismo grave. Este retardo en el crecimiento puede relacionarse a un efecto secundario de la terapia con esteroides, pero también es consecuencia de la enfermedad por sí misma ya que, al afectarse la resorción, se altera el ciclo completo de remodelación ósea, con consecuencias negativas sobre la formación del hueso. No obstante, a pesar de los padecimientos ortopédicos que afectan a la paciente del caso, su curva del crecimiento se ha conservado dentro de los límites normales.5 Por otra parte, la deficiente función de los osteoclastos puede causar alteraciones en la homeostasis del calcio; esta se puede manifestar como hipocalcemia sintomática en los primeros meses de vida, en las formas severas, a pesar de la alta reserva de calcio corporal total, ya que los osteoclastos disfuncionales muestran resistencia a la estimulación hormonal. Con el tiempo, estos niveles de calcio sérico se normalizan, probablemente debido a la acción de otros órganos mediadores de la homeostasis del calcio (intestino o riñón) en respuesta a los niveles elevados de 1,25(OH)2-Vitamina D.6 En el caso que se reporta, no se documentaron desbalances del calcio sérico. La base del cráneo, los huesos de las coanas y la mandíbula son comúnmente afectados, lo que ocasiona que la respiración sea ruidosa (snuffling) y la obstrucción de la vía aérea superior. Esto coloca a los pacientes en riesgo de apnea obstructiva del sueño que, en combinación con la anemia y la restricción del movimiento de la pared, pueden proveer las condiciones necesarias para que se desarrolle hipertensión pulmonar, además del incremento de infecciones respiratorias altas y bajas, que también pueden contribuir a una falla respiratoria.
Las manifestaciones de mayor severidad con potencial riesgo para la vida del paciente son principalmente la pancitopenia, la sepsis y la osteomielitis. La falla medular se produce por la acumulación de calcio, con la subsecuente compensación extramedular que se manifiesta clínicamente con hepatoesplenomegalia, rasgo prominente a la exploración física de la paciente de este caso. Todos los pacientes se encuentran también en riesgo de problemas de dentición y caries dentales severas.7 Se han reconocido anormalidades en los linfocitos y en la producción de inmunoglobulinas que predisponen a una mayor frecuencia y severidad de diversas infecciones.8 Este conjunto de manifestaciones resulta en el deterioro importante en la calidad de vida o el final de la misma a causa de las posibles complicaciones.
Debido a su complejidad y baja prevalencia, no existe en la actualidad un tratamiento médico único efectivo para este padecimiento. Por esta razón, el manejo y el tratamiento de los pacientes con esta enfermedad deben ser multidisciplinarios.9 Su abordaje se puede dividir en dos grandes grupos: el manejo sintomático de las complicaciones y el manejo médico de la enfermedad.
Dentro del manejo sintomático, las complicaciones —como las múltiples fracturas y artritis— deben ser tratadas por un cirujano ortopedista experimentado, por la fragilidad de los huesos y las frecuentes complicaciones secundarias.10 Conviene detectar y prevenir la atrofia del nervio óptico con evaluaciones oftalmológicas periódicas que incluyan la evaluación con potenciales evocados. Los problemas dentales son alteraciones comunes, por lo que la vigilancia odontológica y una adecuada higiene dental forman parte integral en el manejo de estos pacientes.11
Actualmente, el manejo médico de la enfermedad se puede evaluar en tres modalidades: 1) el tratamiento farmacológico y la restricción en la dieta; 2) el trasplante de médula ósea y 3) la terapia genética.
El tratamiento con corticosteroides, la restricción de calcio y la administración de calcitriol e interferón gamma son las principales opciones para el tratamiento médico de la osteopetrosis. En los niños con requerimiento continuo de transfusiones, los esteroides a dosis bajas pueden considerarse para reducir la frecuencia de las mismas, ya que incrementan el número de eritrocitos y plaquetas circulantes.12 Los pacientes con una dieta restringida en calcio y altas dosis de calcitriol experimentan una disminución en la densidad ósea; la restricción de calcio en la dieta crea un estado que facilita la absorción de calcio y el calcitriol estimula la resorción de hueso por medio de la activación de los osteoclastos o su diferenciación.13 El tratamiento a largo plazo con interferón gamma ha demostrado aumentar la resorción ósea, la hematopoyesis y la función de los leucocitos.14 En nuestra paciente se ha utilizado únicamente la restricción de calcio en la dieta, que ha sido la terapia con mayor eficacia de las mencionadas previamente. Sin embargo, basados en las manifestaciones hematológicas que presenta la paciente, también debiera considerarse como opción el tratamiento con bifosfonatos, los cuales se utilizan actualmente en el tratamiento de varios desórdenes del metabolismo óseo, principalmente osteogénesis imperfecta, osteitis de Paget, osteoperosis del adulto y algunos casos de osteopetrosis.15 De igual forma, con base en el mismo aspecto de afección de médula ósea presente en este caso, se justifica la consideración de la paciente como candidata a trasplante de médula ósea. Con este procedimiento se han obtenido buenos resultados en casos similares.16
La historia del trasplante de médula ósea como tratamiento para la osteopetrosis comenzó con los experimentos elaborados por Walker DG, en los que demostró que la osteopetrosis murina puede ser revertida con HSCT (Hematopoietic Stem Cell Transplantation).17 Actualmente el HSCT está reservado para formas severas de osteopetrosis (osteopetrosis autosómica recesiva), debido a la alta morbilidad y mortalidad asociadas. Las complicaciones incluyen rechazo, reconstrucción hematopoyética retrasada, enfermedad venosa oclusiva, hipertensión pulmonar y crisis hipercalcémicas.18 La HSCT no altera el resultado en los subtipos de osteopetrosis asociados con la neuropatía primaria en lugar de la compresión, los asociados a ciertas mutaciones genéticas (CLCN7 y OSTM1), así como las formas que son causadas por la ausencia de osteoclastos más que por su mal funcionamiento.19 En los casos cuando se justifica la realización de un trasplante de médula ósea, la evaluación previa al trasplante engloba un amplio número de estudios específicos para la enfermedad, incluyendo biometría hemática completa, inmunoglobulinas, inmunofenotipo de linfocitos de sangre periférica, fosfatasa alcalina, lactato deshidrogenasa, calcio, fósforo, pH urinario y sanguíneo; adicionalmente, deben tomarse radiografías de tórax, de cabeza y de una extremidad, TAC o RM de cabeza y las exploraciones neurológica, oftalmológica y otorrinolaringológica detalladas. El trasplante de médula ósea aún presenta numerosos y serios riesgos. Una gran proporción deja secuelas, por lo que el trasplante se reserva para las formas severas de la enfermedad, con exclusión de algunos subtipos específicos. Se requiere una evaluación previa extensiva, incluyendo determinar el subtipo genético, y un análisis cuidadoso para determinar si esta opción es la apropiada y si representa el mejor manejo de este padecimiento.20
En las formas autosómicas dominantes, al igual que la heterogenicidad de sus manifestaciones, el tratamiento es sumamente variable; puede ir desde las terapias más sencillas, como la restricción de calcio en la dieta, los nuevos agentes que han demostrado un impacto positivo en el curso de la enfermedad, como el interferón gamma, hasta la innovadora terapia genética, que se encuentra todavía en experimentación, como posible alternativa en los casos que no responden a las terapias convencionales.
Siempre debe realizarse un balance cuidadoso entre los beneficios y los riesgos potenciales de estos tratamientos, así como atenderse y prevenirse las potenciales y significativas complicaciones de esta multifacética enfermedad.
REFERENCIAS
1. Tolar J, Teitelbaum SL, Orchard PJ. Osteopetrosis. N Engl J Med 2004;351:2839-2849. [ Links ]
2. Del Fattore A, Cappariello A, Teti A. Genetics, pathogenesis and complications of osteopetrosis. Bone 2008;42:19-29. [ Links ]
3. Stoker DJ. Osteopetrosis. Semin Musculoskelet Radiol. 2002;6:299-305. [ Links ]
4. Gupta R, Gupta N. Femoral fractures in osteopetrosis: case reports. J Trauma 2001;51:997-999. [ Links ]
5. Iacobini M, Migliaccio S, Roggini M, Taranta A, Werner B, Panero A, et al. Apparent cure of a newborn with malignant osteopetrosis using prednisone therapy. J Bone Miner Res 2001;16:2356-2360. [ Links ]
6. Hermey DC, Ireland RA, Zerwekh JE, Popoff SN. Regulation of mineral homeostasis in osteopetrotic (op) rats. Am J Physiol 1995;268(2 Pt 1):E312-E317. [ Links ]
7. de Baat P, Heijboer MP, de Baat C. Osteopetrosis. Classification, etiology, treatment options and implications for oral health. Ned Tijdschr Tandheelkd 2005;112:497-503. [ Links ]
8. Villa A, Vezzoni P, Frattini A. Osteopetroses and immunodeficiencies in humans. Curr Opin Allergy Clin Immunol 2006;6:421-427. [ Links ]
9. Stark Z, Savarirayan R. Osteopetrosis. Orphanet J Rare Dis 2009;4:5. [ Links ]
10. Landa J, Margolis N, Di Cesare P. Orthopaedic management of the patient with osteopetrosis. J Am Acad Orthop Surg 2007;15:654-662. [ Links ]
11. Lam DK, Sándor GK, Holmes HI, Carmichael RP, Clokie CM. Marble bone disease: a review of osteopetrosis and its oral health implications for dentists. J Can Dent Assoc 2007;73:839-843. [ Links ]
12. Askmyr MK, Fasth A, Richter J. Towards a better understanding and new therapeutics of osteopetrosis. Br J Haematol 2008;140:597-609. [ Links ]
13. Key L, Carnes D, Cole S, Holtrop M, Bar-Shavit Z, Shapiro F, et al. Treatment of congenital osteopetrosis with high-dose calcitriol. N Engl J Med 1984;310:409-415. [ Links ]
14. Key LL Jr, Rodriguiz RM, Willi SM, Wright NM, Hatcher HC, Eyre DR, et al. Long-term treatment of osteopetrosis with recombinant human interferon gamma. N Engl J Med 1995;332:1594-1599. [ Links ]
15. Allgrove J. Biphosphonates. Arch Dis Child 1997;76:73-75. [ Links ]
16. Kaplan FS, August CS, Fallon MD, Dalinka M, Axel L, Haddad JG. Successful treatment of infantile malignant osteopetrosis by bone-marrow transplantation. J Bone Joint Surg Am 1988;70:617-623. [ Links ]
17. Walker DG. Control of bone resorption by hematopoietic tissue. The induction and reversal of congenital osteopetrosis in mice through use of bone marrow and splenic transplants. J Exp Med 1975;142:651-663. [ Links ]
18. Driessen GJ, Gerritsen EJ, Fischer A, Fasth A, Hop WC, Veys P, et al. Long-term outcome of haematopoietic stem cell transplantation in autosomal recessive osteopetrosis: an EBMT report. Bone Marrow Transplant 2003;32:657-663. [ Links ]
19. Ballet JJ, Griscelli C, Coutris C, Milhaud G, Maroteaux P. Bonemarrow transplantation in osteopetrosis. Lancet 1977;310:1137. [ Links ]
20. Steward CG. Hematopoietic stem cell transplantation for osteopetrosis. Pediatr Clin North Am 2010;57:171-180. [ Links ]














