Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Boletín médico del Hospital Infantil de México
versão impressa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.69 no.2 México Mar./Abr. 2012
Artículo de investigación
Prevalencia de polimorfismos del receptor de vitamina D en pacientes pediátricos mexicanos con enfermedad renal crónica
Prevalence of vitamin D receptor gene polymorphisms in Mexican children with chronic kidney disease
Elba Onelida Medina-Hernández,1 Benjamín Antonio Rodríguez-Espino,1 Ana María Hernández-Sánchez,1 Lourdes Matilde Ortiz-Vázquez,1 Perla Oropeza,1 Daniel Díaz,1 Rubén Aldana-Vergara,1 Francisco Velásquez-Forero,1 Olynka Vega,2 Ricardo Correa-Rotter,2 Mara Medeiros1
1 Laboratorio de Investigación en Nefrología y Metabolismo Mineral Óseo, Hospital Infantil de México Federico Gómez
2 Departamento de Nefrología, Instituto Nacional de Ciencias Médicas y la Nutrición Salvador Zubirán, México D.F., México
Autor de correspondencia:
Dra. Mara Medeiros
Correo electrónico: medeiro.mara@gmail.com
Fecha de recepción: 09-03-12.
Fecha de aceptación: 27-03-12.
Resumen
Introducción. La posible influencia de los diferentes polimorfismos del receptor de vitamina D sobre la regulación del eje calcio-hormona paratiroidea -vitamina D es particularmente importante en pacientes con enfermedad renal crónica, ya que cursan con trastornos en el metabolismo mineral óseo. El objetivo del trabajo fue describir la frecuencia de los polimorfismos rs7975232 (ApaI), rs731236 (TaqI) y rs1544410 (BsmI) en el receptor de vitamina D y su relación con el calcio, el fósforo, la fosfatasa alcalina y la hormona paratiroidea en pacientes pediátricos con enfermedad renal crónica.
Métodos. Se incluyeron 31 pacientes con enfermedad renal crónica. Se tomaron muestras de sangre a cada uno para la determinación de marcadores bioquímicos y muestras de ADN para la genotipificación del gen del receptor a vitamina D utilizando el método de la reacción en cadena de la polimerasa y restricción enzimática.
Resultados. La edad promedio de los pacientes fue de 15.6 ± 3.6 años. Para ApaI, fueron homocigotos AA siete pacientes (22.58%); Aa, 18 pacientes (58.06%) y AA, seis pacientes (19.35%). Para BsmI, 14 pacientes fueron BB (45.16%) y 17 pacientes fueron Bb (54.83%). Los pacientes BB tuvieron calcio sérico mayor que los Bb (p = 0.04). Para TaqI, fueron TT 19 pacientes (61.3%); Tt, once pacientes (35.48%) y uno, tt (3.22%). Aquellos con alelo t (Tt o tt) presentaron concentraciones de calcio sérico significativamente más bajas que el homocigoto TT.
Conclusiones. Se reportaron las frecuencias de genotipos y alelos del receptor de vitamina D en niños mexicanos. Se obtuvieron valores de calcio sérico más elevados en aquellos con alelo BB o TT.
Palabras clave: receptor vitamina D, polimorfismos, trasplante renal, calcio sérico, enfermedad renal crónica.
Abstract
Background. The possible influence of vitamin D receptor (VDR) gene polymorphisms on the regulation of the calcium–parathyroid hormone–vitamin D axis is particularly important in end-stage renal disease (ESRD) patients due to alterations in bone mineral metabolism. The aim of the study was to describe the frequency of VDR gene polymorphisms rs7975232 (ApaI), rs731236 (TaqI), rs1544410 (BsmI) and their relationship with serum calcium, phosphate, alkaline phosphatase and parathyroid hormone in children with ESRD.
Methods. Thirty one patients were included in the study. Blood samples were drawn for biochemical determinations and DNA extraction. VDR genotypes were analyzed as restriction fragment length polymorphisms using ApaI, BsmI and TaqI.
Results. Mean age of the patients was 15.6 ± 3.6 years. For ApaI, seven patients were AA (22.58%), 18 patients were Aa (58.06%) and six patients were aa (19.35%). For BsmI, 14 patients were BB (45.16%) and 17 were Bb (54.83%). Patients who were homozygous for BB had higher serum calcium concentrations than Bb patients (p = 0.04). For TaqI, 19 patients were TT (61.3%), 11 were Tt (35.48%) and one was tt (3.22%). Those with t allele (Tt or tt) had serum calcium concentrations significantly lower than TT patients.
Conclusions. Genotype and allele frequency of the VDR gene is reported in Mexican patients with ESRD. Those with BB or TT genotype had higher serum calcium concentrations.
Key words: vitamin D receptor, gene polymorphism, renal transplantation, serum calcium, end-stage renal disease.
INTRODUCCION
La enfermedad renal crónica (ERC) tiene efectos múltiples sobre el metabolismo mineral óseo desde etapas iniciales de la enfermedad.1 Esta entidad se conoce como alteraciones minerales y óseas-enfermedad renal crónica (CKD-MBD, por su siglas en inglés), y se manifiesta con una o más de las siguientes características: 1) alteraciones en el metabolismo del calcio, fósforo, vitamina D y hormona paratiroidea (PTH), 2) alteraciones en la histología, crecimiento lineal o fuerza del hueso y 3) calcificaciones vasculares o de tejidos blandos.1 La magnitud de la afección ósea tiende a asociarse con la gravedad y duración de la enfermedad renal. De no tratarse estas alteraciones en forma oportuna durante la edad pediátrica, se presenta la detención del crecimiento con o sin deformidades óseas.2 La principal causa de muerte en pacientes con enfermedad renal crónica son las afecciones cardiovasculares, tanto en niños como en adultos.3 El tratamiento de la CKD-MBD influye en la progresión del daño vascular.3-5
En la homeostasis de calcio y fósforo en el organismo participan la glándula paratiroidea, el intestino, el riñón y el hueso, que es el principal reservorio de calcio y fósforo del organismo.6
La vitamina D existe como ergocalciferol (vitamina D2) cuando se produce en plantas o colecalciferol (vitamina D3), en tejidos animales.7 Ambas son biológicamente inactivas (pro-hormonas), por lo que deben hidrolizarse en el hígado en los carbonos 25. Ya hidrolizadas, dan origen a la 25-hidroxivitamina (25(OH)D3), que es el metabolito más abundante de la vitamina D.8 La 25(OH)D3, cuando es transformada en 1,25 dihidrocolecalciferol o calcitriol (vitamina D activa), puede desempeñar su papel fisiológico como hormona.9 Esto ocurre principalmente en los túbulos renales proximales por acción de la enzima 1 α hidroxilasa (CYP27B1). Los efectos del calcitriol son regulados por la unión a su receptor esteroide nuclear específico, llamado receptor de la vitamina D (VDR). El VDR se encuentra en diferentes células del organismo, tanto en renales como en otros tejidos blanco que incluyen glándula paratiroidea, hueso, corazón, intestino, células endoteliales, linfocitos, megacariocitos, neumocitos, entre otros.10-12
El complejo calcitriol-VDR se transloca al núcleo y forma un heterodímero con el receptor X retinoico, que se une a los elementos de respuesta de la vitamina D y estimula la transcripción de diversos genes. En el hueso, la activación del VDR aumenta la expresión del factor de crecimiento de fibroblastos (FGF23) y estimula la resorción de los depósitos óseos de calcio, en la glándula paratiroidea bloquea la transcripción del gen de la PTH; en el intestino aumenta la absorción de calcio.6 También se ha reportado que modula la transcripción de genes que modifican histonas.13
El gen del VDR se localiza en el cromosoma 12 (12q13.11). Tiene 11 exones y 4 regiones polimórficas.14,15 Las mutaciones deletéreas en el gen VDR ocasionan raquitismo resistente a calcitriol, una rara enfermedad monogénica.16 También se conocen varios polimorfismos de este, que son detectados por enzimas de restricción: BsmI (para rs1544410), ApaI (para rs7975232) y TaqI (para rs731236).17 Estos polimorfismos están ubicados en la región 3' del intrón 9 y exón 10 del gen VDR (Ensembl: ENSG00000111424).
La posible influencia de los polimorfismos del gen que codifica para el VDR sobre la regulación del eje calcio–hormona paratiroidea (PTH)–vitamina D es particularmente importante en pacientes con ERC, en quienes se han descrito alteraciones, tanto en el contenido paratiroideo de VDR como en su funcionalidad, que modifican la actividad transcripcional de este gen.15
La información disponible sobre la influencia de estos polimorfismos y la densidad ósea varía según la serie consultada. En el caso de BsmI, el alelo silvestre se asocia con valores mayores de masa ósea.17
Se ha reportado que, en pacientes en hemodiálisis, los homo y heterocigotos para el alelo b presentan mayores niveles de PTH que los homocigotos BB,18 y que los portadores BB requieren menos paratiroidectomías.19
Los polimorfismos del VDR también se han asociado con enfermedades autoinmunes, como la esclerosis múltiple y diabetes mellitus tipo 1, y otras adquiridas como hipertensión, cáncer; también con la remineralización y la densidad ósea.14,16,20-22
El objetivo del trabajo fue describir la frecuencia de los polimorfismos rs7975232 (ApaI), rs731236 (TaqI) y rs1544410 (BsmI) en el VDR y su relación con algunos marcadores bioquímicos (PTH, fósforo, calcio sérico) en niños con ERC.
MÉTODOS
Pacientes. Se invitó a participar a los pacientes pediátricos23 con enfermedad renal crónica terminal (ERCT) en espera de trasplante renal, atendidos en el Departamento de Nefrología, durante el periodo de noviembre de 2009 a febrero de 2011. El estudio fue aprobado por las comisiones de ética e investigación del Hospital Infantil de México Federico Gómez. Se obtuvo el consentimiento/ asentimiento informado de todos los pacientes participantes y sus tutores.
Se realizó un examen clínico y se tomaron muestras de sangre para la determinación de la hormona paratiroidea intacta (PTHi), calcio sérico corregido para la cifra de albúmina, fósforo sérico, fosfatasa alcalina total y fracción ósea. También se obtuvo otra muestra de sangre periférica (3ml) en un tubo con EDTA, para la obtención de ADN. Para esto se utilizó el kit comercial QIAamp DNA blood mini kit (Qiagen, Hilden, Alemania) de acuerdo con las recomendaciones del fabricante. La determinación de la concentración del ADN se realizó con el espectrofotómetro NanoDrop 1000. Se prepararon soluciones de trabajo con una concentración de ADN de 100ng en 1µl de agua.
Para el análisis de los genotipos se emplearon los métodos de la reacción en cadena de la polimerasa y los polimorfismos de longitud del fragmento de restricción enzimática (PCR-RFLP). Se empleó la base de datos de NCBI dbSNP Build 13524 para la localización y secuencia de los polimorfismos de un sólo nucleótido (SNP): rs7975232, rs731236 y rs1544410 (región 3' del intrón 9 y exón 10 del gen VDR).
Oligonucleótidos para la PCR. El diseño de los cebadores se realizó con el programa Primer3©.25,26 Para el diseño se utilizó como referencia la secuencia del gen VDR (ENSG00000111424) de ENSEMBL©,27 del European Bioinformatics Institute (EBI), del European Molecular Biology Laboratory (EMBL) y del Wellcome Trust Sanger Institute (WTSI) (Cuadro 1).
Endonucleasas de restricción para los RFLP. Se emplearon las enzimas ApaI (rs7975232) y TaqI (rs731236) de los kits FastDigest® de Fermentas (Thermo Fisher Scientific Inc.) y BsmI (rs1544410) de New England Biolabs, Inc (Cuadro 2).
Para la resolución de los productos de digestión se realizó la electroforesis en gel de agarosa al 3.5% en amortiguador Tris 1M/Borato 0.9M/EDTA 0.01M (TBE1X), con un marcador de peso molecular de 100 pb (GeneRuler™ de Fermentas, Thermo Fisher Scientific Inc.) (Figuras 1 y 2).
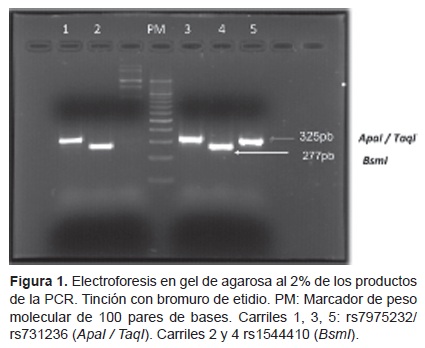
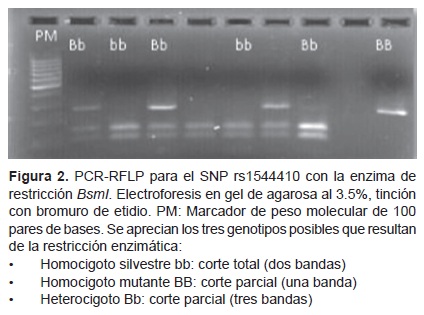
Análisis estadístico. Se registró la frecuencia y porcentaje de cada uno de los polimorfismos. La evaluación del equilibrio de Hardy Weinberg se realizó con χ2·28 Esta prueba se recomienda aplicar siempre que se realizan estudios de polimorfismos genéticos, ya que permite identificar si la muestra es representativa. La proporción de los genotipos de una población se mantendrá constante si el tamaño de la muestra es apropiado; si no existen mutaciones, no se introducen ni se pierden genes, y no ocurre selección de genotipos.
La comparación de los valores de calcio, fósforo, fosfatasa alcalina total y fracción ósea por genotipo para ApaI y TaqI se evaluó con la prueba de Kruskal Wallis. En el caso de BsmI, se empleó la prueba de Mann Whitney o t de Student, según la distribución de los valores, comparando homocigotos BB con heterocigotos.
RESULTADOS
Se incluyeron 31 pacientes pediátricos con ERCT. La edad promedio fue de 15.6 ± 3.6 años (Cuadro 3).

En cuanto al genotipo, para el SNP rs7975232 (enzima ApaI) fueron homocigotos mutantes AA siete pacientes (22.58%); heterocigotos, 18 pacientes (58.06%); y homocigotos silvestres AA, seis pacientes (19.35%). Se encontró χ2 =0.82 (Cuadro 4). Los pacientes homocigotos mutantes (AA) para este SNP mostraron cifras mayores de PTH, comparados con los pacientes homocigotos silvestres (AA); sin embargo, no hubo significancia estadística. Tampoco hubo diferencias en las concentraciones de calcio, fósforo y fosfatasa alcalina (Cuadro 5).

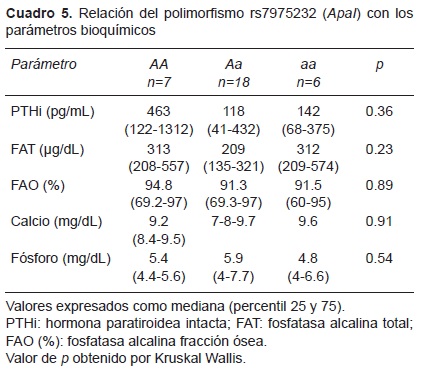
Los genotipos observados para el SNP rs1544410 (enzima BsmI) fueron las siguientes: homocigotos mutantes BB, 14 pacientes (45.16%) y heterocigotos, 17 (54.83%). No se encontraron homocigotos bb (Cuadro 4). Los pacientes BB mostraron concentraciones mayores de calcio sérico promedio (9.4 ±1.3 mg/dL) comparadas con el genotipo Bb, con concentraciones de calcio de 8.3 ± 1.38 mg/dL (p = 0.04). No se encontraron diferencias entre las otras variables estudiadas (Cuadro 6).
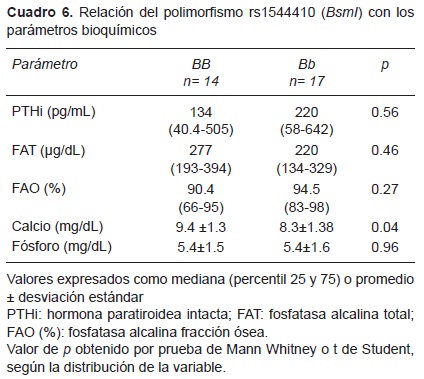
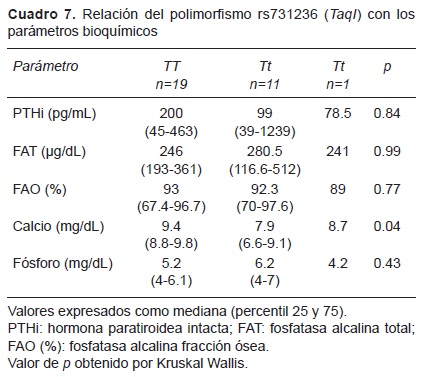
Los genotipos para el SNP rs731236 (enzima TaqI) fueron homocigotos mutantes TT, 19 pacientes (61.3%); heterocigotos, 11 pacientes (35.48%) y homocigotos silvestres, solo un caso (3.22%) (Cuadro 4). Los individuos con el alelo t presentaron concentraciones de calcio sérico significativamente menores que los homocigotos TT (Cuadro 7).
DISCUSION
Las frecuencias de los polimorfismos del VDR encontradas en niños mexicanos con ERCT difieren de lo reportado para otras poblaciones étnicas. En el caso de ApaI, se ha reportado para la población caucásica 37% AA, 39% aa y 23% Aa, mientras que 58% de los pacientes de nuestro estudio fueron heterocigotos.29
Yokoyama y colaboradores estudiaron 129 pacientes japoneses y encontraron que el polimorfismo ApaI muestra una asociación negativa con la progresión del hiperparatiroidismo. Los niveles de PTH en el grupo aa fueron casi el doble de los de los grupos AA y Aa (p ≤ 0.04).30 Nosotros no encontramos diferencias en los parámetros bioquímicos estudiados en los niños mexicanos, según el genotipo de ApaI.
El genotipo BB está reportado en el 15% de la población caucásica mientras que en la japonesa, en 1-2% solamente.17 En nuestro estudio encontramos el genotipo BB en 45% y el genotipo Bb (55%), que fue predominante. Ningún paciente presentó el alelo silvestre. Consideramos que pudo deberse a que el tamaño de la muestra fue pequeño, ya que, en un estudio previo, realizado en 197 mujeres mexicanas en diálisis por Ávila y colaboradores, se reportó una frecuencia del genotipo bb de 64%. Las mujeres con el alelo B tuvieron más osteopenia que aquellas con el alelo silvestre.31
En un estudio realizado por Sainz y colaboradores, en cien niñas sanas, prepúberes, americanas con ascendencia mexicana, con un rango de edad de entre 6.7 y 11.7 años, que fueron reclutadas en escuelas de Los Ángeles, California, se encontró que los genotipos más comunes fueron Aa (55%), Bb (42%) y TT (54%). Los genotipos aa y bb fueron más frecuentes que AA y BB (24% y 21%, 44% y 14%, respectivamente). Esto resultó similar a lo reportado previamente en una población de Francia y en personas de ascendencia europea en Australia y Estados Unidos. Las niñas con genotipo mutante aa o bb tuvieron mayor densidad ósea que aquellas homocigotas para el alelo silvestre AA o BB.32
Los genotipos más frecuentes hallados en pacientes pediátricos mexicanos con ERCT fueron los siguientes: para el SNP rs7975232 (ApaI), el genotipo heterocigoto Aa en 58%; para el SNP rs1544410 (BsmI), el genotipo heterocigoto Bb en 55%; y para el SNP rs731236 (Taql), el genotipo homocigoto mutante TT en 61%.
Los pacientes con genotipo homocigoto mutante BB para el SNP rs1544410 presentaron niveles de calcio sérico significativamente mayores que aquellos con genotipo Bb.
Los pacientes con el alelo silvestre t para el SNP rs731236 (Tt o tt) presentaron niveles de calcio significativamente menores que aquellos con genotipo mutante TT.
AGRADECIMIENTOS
El proyecto recibió apoyo de Fondos Federales HIM/2010/006.
El alumno Daniel Díaz Barriga recibió apoyo de la beca PUIS-UNAM.
REFERENCIAS
1. Moe S, Drüeke T, Cunningham J, Goodman W, Martin K, Olgaard K, et al. Definition, evaluation, and classification of renal osteodystrophy: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2006;69:1945-1953. [ Links ]
2. Klaus G, Watson A, Edefonti A, Fischbach M, Rönnholm K, Schaefer F, et al. Prevention and treatment of renal osteodystrophy in children on chronic renal failure: European guidelines. Pediatr Nephrol 2006;21:151-159. [ Links ]
3. Moe SM, Chen NX. Mechanisms of vascular calcification in chronic kidney disease. J Am Soc Nephrol 2008;19:213-216. [ Links ]
4. Hruska KA, Choi ET, Memon I, Davis TK, Mathew S. Cardiovascular risk in chronic kidney disease (CKD): the CKD-mineral bone disorder (CKD-MBD). Pediatr Nephrol 2010;25:769-778. [ Links ]
5. Bover J, Cozzolino M. Mineral and bone disorders in chronic kidney disease and end-stage renal disease patients: new insights into vitamin D receptor activation. Kidney Int Suppl 2011;1:122-129. [ Links ]
6. Mejía N, Roman-García P, Miar AB, Tavira B, Cannata-Andía JB. Chronic kidney disease—mineral and bone disorder: a complex scenario. Nefrologia 2011;31:514-519. doi:10.3265/Nefrologia.pre2011.Jun.10926. [ Links ]
7. Reichel H, Koeffler HP, Norman AW. Production of 1 alpha,25- dihydroxyvitamin D3 by hematopoietic cells. Prog Clin Biol Res 1990;332:81-97. [ Links ]
8. Portale AA, Miller WL. Human 25-hydroxyvitamin D-1alpha- hydroxylase: cloning, mutations, and gene expression. Pediatr Nephrol 2000;14:620-625. [ Links ]
9. Velásquez-Forero F, García P, Triffitt JT, Llach F. Prostaglandin E1 increases in vivo and in vitro calcitriol biosynthesis in rabbits. Prostaglandins Leukot Essent Fatty Acids 2006;75:107-115. [ Links ]
10. Silvagno F, De Vivo E, Attanasio A, Gallo V, Mazzucco G, Pescarmona G. Mitochondrial localization of vitamin D receptor in human platelets and differentiated megakaryocytes. PLoS One 2010;5:e8670. doi:10.1371/journal.pone.0008670. [ Links ]
11. Cozzolino M, Mazzaferro S, Messa P. New insights into the role of calcium-sensing receptor activation. J Nephrol 2011;24(suppl 18):S38-S41. doi: 10.5301/JN.2011.7760. [ Links ]
12. Haussler MR, Jurutka PW, Mizwicki M, Norman AW. Vitamin D receptor (VDR)-mediated actions of 1α,25(OH)(2)vitamin D(3): genomic and non-genomic mechanisms. Best Pract Res Clin Endocrinol Metab 2011;25:543-559. [ Links ]
13. Pereira F, Barbáchano A, Singh PK, Campbell MJ, Muñoz A, Larriba MJ. Vitamin D has wide regulatory effects on histone demethylase genes. Cell Cycle 2012;11:1081-1089. [ Links ]
14. Ranganathan P. Genetics of bone loss in rheumatoid arthritis—role of vitamin D receptor polymorphisms. Rheumatology (Oxford) 2009;48:342-346. [ Links ]
15. Jofre R. Polimorfismos del gen del receptor de la vitamina D (VDR) y función paratiroidea. Nefrología 2001;21(suppl 1):51-55. [ Links ]
16. Uitterlinden AG, Fang Y, Van Meurs JB, Pols HA, Van Leeuwen JP. Genetics and biology of vitamin D receptor polymorphisms. Gene 2004;338:143-156. [ Links ]
17. Gómez Alonso C, Naves Díiaz ML, Díaz-Corte C, Fernández Martín JL, Cannata Andía JB. Vitamin D receptor gene (VDR) polymorphisms: effect on bone mass, bone loss and parathyroid hormone regulation. Nephrol Dial Transplant 1998;13(suppl 3):73-77. [ Links ]
18. Nagaba Y, Heishi M, Tazawa H, Tsukamoto Y, Kobayashi Y. Vitamin D receptor gene polymorphisms affect secondary hyperparathyroidism in hemodialyzed patients. Am J Kidney Dis 1998;32:464-469. [ Links ]
19. Borràs M, Torregrossa V, Oliveras A, Almirall J, Marco MP, Betriu A, et al. BB genotype of the vitamin D receptor gene polymorphism postpones parathyroidectomy in hemodialysis patients. J Nephrol 2003;16:116-120. [ Links ]
20. Valdivielso JM, Fernandez E. Vitamin D receptor polymorphisms and diseases. Clin Chim Acta 2006;371:1-12. [ Links ]
21. Swapna N, Vamsi UM, Usha G, Padma T. Risk conferred by FokI polymorphism of vitamin D receptor (VDR) gene for essential hypertension. Indian J Hum Genet 2011;17:201-206. [ Links ]
22. Suh KT, Eun IS, Lee JS. Polymorphism in vitamin D receptor is associated with bone mineral density in patients with adolescent idiopathic scoliosis. Eur Spine J 2010;19:1545-1550. [ Links ]
23. American Academy of Pediatrics. Council on Child and Adolescent Health. Age limits of pediatrics. Pediatrics 1988;81:736. [ Links ]
24. Single Nucleotid Polymorphism data base. Disponible en: http://www.ncbi.nlm.nih.gov/projects/SNP/ [ Links ]
25. Rozen S, Skaletsky H. Primer3 on the WWW for general users and for biologist programmers. Methods Mol Biol 2000;132:365-386. [ Links ]
26. Primer 3 (v. 0.4.0.). Primer designer. Disponible en: http://frodo.wi.mit.edu/ [ Links ]
27. Ensembl genome browser. Disponible en: http://www.ensembl.org/index.html [ Links ]
28. Rodriguez S, Gaunt TR, Day IN. Hardy-Weinberg equilibrium testing of biological ascertainment for Mendelian randomization studies. Am J Epidemiol 2009;169:505-514. [ Links ]
29. Ingles SA, Haile RW, Henderson BE, Kolonel LN, Nakaichi G, Shi CY, et al. Strength of linkage disequilibrium between two vitamin D receptor markers in five ethnic groups: implications for association studies. Cancer Epidemiol Biomarkers Prev 1997;6:93-98. [ Links ]
30. Yokoyama K, Shigematsu T, Tsukada T, Ogura Y, Takemoto F, Hara S, et al. Apa I polymorphism in the vitamin D receptor gene may affect the parathyroid response in Japanese with end-stage renal disease. Kidney Int 1998;53:454-458. [ Links ]
31. Avila M, Prado C, Ventura MJ, Mora C, Briones D, Valdez H, et al. Vitamin D receptor gene, biochemical bone markers and bone mineral density in Mexican women on dialysis. Nephrol Dial Transplant 2010;25:2259-2265. [ Links ]
32. Sainz J, Van Tornout JM, Loro ML, Sayre J, Roe TF, Gilsanz V. Vitamin D-receptor gene polymorphisms and bone density in prepubertal American girls of Mexican descent. N Engl J Med 1997;337:77-82. [ Links ]














