Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.65 no.6 México nov./dic. 2008
Aspectos clínicos
Tratamiento farmacológico de la obesidad en niños
Pharmacological treatment of child obesity
Ninel Coyote-Estrada, América Liliana Miranda-Lora
Área de Endocrinología, Hospital Infantil de México Federico Gómez, México, D.F., México.
Solicitud de sobretiros:
Dra. Ninel Coyote Estrada, Área de Endocrinología,
Hospital Infantil de México Federico Gómez,
Dr. Márquez Núm. 162, Col. Doctores,
CP. 06720, México, D.F., México.
Fecha de recepción: 08-09-2008.
Fecha de aprobación: 09-10-2008.
Resumen
El tratamiento de la obesidad es un problema complejo, y los cambios en el estilo de vida no siempre tienen resultados satisfactorios, por lo que se han utilizado diversos fármacos para tratar de combatirla y algunos han mostrado ser efectivos. Entre estos medicamentos se encuentran aquellos que suprimen el apetito, los que incrementan el gasto energético, y los que modifican la absorción o el metabolismo de macronutrimentos. Sin embargo, algunos de ellos, a pesar de haber sido aprobados, han tenido que ser retirados del mercado debido a su asociación con efectos adversos graves. En la actualidad, de los utilizados para bajar de peso, solamente 2 de ellos se encuentran aprobados en población pediátrica: orlistat y sibutramina.
El tratamiento farmacológico no ha mostrado efectividad por sí mismo, ya que se trata de una enfermedad multifactorial que requiere involucrar la modificación de los hábitos de alimentación, incrementar la actividad física o de terapia conductual.
Aún quedan diversas interrogantes por resolver, como: seguridad de los medicamentos a largo plazo, forma de evitar la recuperación de peso secundaria a cualquiera que sea la intervención utilizada, eficacia de un fármaco sobre otro, tiempo óptimo de inicio, y la duración necesaria del tratamiento.
Debido a lo anterior, se sugiere reservar el tratamiento farmacológico a pacientes con comorbilidades asociadas, que no hayan respondido a un programa estructurado de reducción de peso, que comprendan las limitaciones y efectos adversos de los medicamentos y la necesidad de continuar con los cambios en el estilo de vida.
Palabras clave: Obesidad; tratamiento; fármacos; niños.
Abstract
The treatment for obesity is a complex problem and changes in life style not always render satisfactory results. For this reason different drugs have been used to lose weight and some of them have shown to be effective. Among these drugs, are those that suppress appetite, increase energy expenditure and others that modify nutrient absorption or metabolism. Nevertheless, some of them in spite of been approved, have been withdrawn of the market due to their association with serious and adverse effects. Nowadays, from all drugs used to lose weight, only 2 are approved for pediatric age: orlistat and sibutramine.
The pharmacological treatment has shown ineffectiveness by itself, because obesity is a multifaceted disease that requires the modification of eating habits, increase in physical activity and/or a behavior therapy. Many questions still remain to be solved: safety of long term-effect, forms to avoid subsequent weight regain after any intervention, effectiveness, optimal time of beginning and duration of treatment. In conclusion, all these issues suggest to keep the pharmacological treatment for patients with associated comorbidities and who have not responded to a structured weight loss program, and counseling to understand the limitations and drug adverse effects, as well as the need to continue with changes in life style.
Key words: Obesity; treatment; drugs; child.
Ante la epidemia de obesidad a la que nos estamos enfrentando, se han tenido que implementar múltiples estrategias para combatirla. Esto ha llevado al desarrollo de diversos medicamentos para tratar de bajar de peso; pero hasta la fecha, ninguno de estos por sí mismos pueden revertir por completo la obesidad. Sin embargo, la mercadotecnia y la charlatanería atraen a las personas para el consumo de medicamentos que se promocionan, la mayoría de ellos, como naturistas o activadores del metabolismo; sin embargo, en muchas ocasiones se desconoce su composición y los efectos indeseables que puedan llegar a producir.
Diversos medicamentos para bajar de peso pueden conseguirse sin receta y sin supervisión médica en farmacias, tiendas de autoservicios, e incluso gimnasios. Algunos autores encontraron que antes de que los pacientes acudan a atención médica para tratar la obesidad, hasta la mitad de ellos han consumido medicamentos para bajar de peso (sibutramina, metformina, remedios herbales, etc.), siendo consumidos con mayor frecuencia por el sexo femenino.1 En nuestro país no contamos con información similar, pero sabemos que todos estos medicamentos o suplementos para bajar de peso, son de fácil adquisición y probablemente el consumo de éstos sea indiscriminado, por lo que a pesar de que la mayoría no están aprobados para su uso en pacientes pediátricos, es de importancia conocer la forma en la que actúan y los efectos adversos que pueden llegar a producir.
Utilidad del tratamiento farmacológico para la obesidad
Es conocido que los cambios en el estilo de vida para controlar la obesidad pueden llegar a ser frustrantes, tanto para los pacientes como para el personal de salud encargado del tratamiento, ya que a pesar de diversos esfuerzos, existe una detención en la pérdida progresiva de peso, e incluso un efecto de "rebote" al suspender estas intervenciones. Se ha encontrado que en general las intervenciones rigurosas en los cambios del estilo de vida con una restricción calórica obligatoria, sesiones de consejería, ejercicio diario y vigilancia médica, alcanzan una reducción de peso en promedio de 6 kg durante un año, y solamente se logra el mantenimiento del mismo con vigilancia continua. En niños, se ha encontrado que las intervenciones intensivas pueden reducir el peso entre 4.3 a 7 kg durante el primer año,2 y estos resultados a largo plazo tienden a disminuir.3 Por lo anterior, se ha recurrido a la utilización de medicamentos que permitan una pérdida más eficiente.
Es importante señalar que de los fármacos utilizados en la práctica médica, ninguno ha mostrado utilidad si no se combina con cambios en los estilos de vida, ya sea mediante la modificación en los hábitos de alimentación, incremento en la actividad física, o a través de la utilización de terapia conductual; es decir, la "pildora mágica" que permite comer libremente y ocasionar una pérdida progresiva de peso no existe.
Diversos fármacos diseñados para la pérdida de peso han tenido que ser retirados del mercado posterior a su autorización, debido a su asociación con efectos adversos graves. La efedra, la fenil-propanolamina y la d-fenfluramina fueron retiradas por su asociación con alteraciones cardiovasculares (Cuadro 1).4,5
De los fármacos utilizados en la actualidad para el control de peso, se desconocen los efectos a largo plazo que se puedan presentar con el uso o con la suspensión de los mismos, ya que la mayoría de los estudios no tienen un seguimiento mayor a dos años, desconociéndose los efectos indeseables, en especial sobre el crecimiento y el desarrollo, que puedan llegar a producir y la efectividad que puedan tener para el mantenimiento de la pérdida de peso con el tiempo.6,7
Al igual que sucede con el tratamiento dietético, la fase inicial de los diversos tratamientos farmacológicos se asocia con una pérdida de peso significativa que puede variar entre 12 y 24 semanas; sin embargo, la efectividad a largo plazo solamente se ha demostrado en una pequeña proporción de pacientes, ya que la progresión de la pérdida de peso disminuye, y aún puede existir un efecto de recuperación de peso a los seis meses, siendo mayor con la suspensión del medicamento.4,8
La pérdida de peso, con cualquiera que sea la estrategia utilizada, se acompaña de reducciones en los niveles hormonales de leptina, insulina y triyodotironina, con un incremento en la sensibilidad a la insulina y a la ghrelina plasmática, llevando todos estos cambios a estimular el apetito; por otra parte, existe una disminución del tono simpático y del gasto energético, lo que promueve la lipogénesis y se facilita la recuperación de peso.2 Es decir, es la respuesta de defensa del organismo ante la disminución del aporte energético, condicionando que los mecanismos de almacenamiento de energía sean más efectivos. Por lo anterior, los cambios en el estilo de vida deben acompañar al tratamiento farmacológico y mantenerse a largo plazo.
La utilización de fármacos para el tratamiento de la obesidad aún es limitada en pediatría, y la mayoría de los autores reservan el uso de medicamentos para aquellos pacientes con obesidad extrema (considerada generalmente como un índice de masa corporal [IMC] > percentila 99 para la edad y género), falta de respuesta a tratamientos previos, con comorbilidades asociadas y que se encuentren en la adolescencia. En la actualidad, solamente dos fármacos han sido aprobados por la FDA (Food and Drug Administration) para su uso en pacientes pediátricos: sibutramina y orlistat;9 aunque en algunos países todavía se encuentran contraindicados en estas edades.10 De estos fármacos, no se ha demostrado la eficacia y seguridad a más de cuatro años en el caso de orlistat, y de dos años en el caso de sibutramina.9
A pesar de que solamente dos fármacos han sido aprobados en pacientes pediátricos, consideramos conveniente revisar otros, que a pesar de no ser seguros pueden ser consumidos sin supervisión médica, algunos más que solamente han sido aprobados en adultos, y que eventualmente se pudieran aprobar en pacientes pediátricos, y otros que se encuentran en fase de investigación.
Hay que tomar las consideraciones pertinentes para la aplicación de los resultados obtenidos por diversos estudios, ya que consideran diferentes criterios de inclusión y métodos de cointervención, y se han realizado en poblaciones que cuentan con diferentes factores genéticos y ambientales que pudieran estar asociados con distintas respuestas a los medicamentos, como ha sido señalado en algunos estudios. Debido a lo anterior, se requieren estudios que confirmen la efectividad y seguridad en nuestra población.
Clasificación de los fármacos utilizados en la obesidad
Si consideramos que el peso corporal es la consecuencia del balance que existe entre el aporte calórico y el gasto energético, podemos clasificar el tratamiento farmacológico de la obesidad de la siguiente manera (Fig. 1).11,12
I. Fármacos que disminuyen la ingesta de alimentos.
II. Fármacos que incrementan el gasto energético.
III. Fármacos que afectan el metabolismo o la absorción de nutrimentos.
Algunos de los fármacos diseñados para el manejo de la obesidad pueden actuar a través de más de uno de estos mecanismos.
I. Fármacos que disminuyen la ingesta calórica
Los fármacos que pertenecen a este grupo, incrementan la disponibilidad de neurotransmisores con actividad anorexigénica a nivel de sistema nervioso central (serotonina, noradrenalina y dopamina), ya sea incrementando la liberación o inhibiendo la recaptura de éstos (Cuadro 2).13
a) Fármacos noradrenérgicos
Son derivados de la feniletilamina, con excepción del mazindol. Incrementan la liberación de norepinefrina o bloquean su recaptura en neuronas hipotalámicas (solamente la fenilpropanolamina actúa como agonista α-adrenérgico), ocasionando un incremento en la actividad de péptidos anorexigénicos (Fig. 1). Debido a su mecanismo de acción pueden ocasionar dependencia psicológica.12 Los fármacos más representativos de este grupo comprenden:
Fentermina8
Mecanismo de acción: agente noradrenérgico que actúa como psicoestimulante y anorexigénico.
Dosis: de 10 a 30 mg en 24 horas.
Farmacocinética: se absorbe con facilidad en el tracto digestivo. Su metabolismo es complejo, involucrando desaminación oxidativa y reducción de muchos de sus metabolitos que son biológicamente activos. Se excreta principalmente por vía renal, y por ser una base débil se elimina más rápido en orina acida. Tiene una vida media de 20 horas.
Efectos secundarios: se ha reportado tolerancia y dependencia al medicamento. Ocasiona diversos efectos como: palpitaciones, taquicardia, hipertensión, dolor precordial, arritmias, discinesias, visión borrosa, euforia, temblor, insomnio, mareos, sequedad de mucosas, náuseas, vómito, diarrea, constipación y urticaria, entre otros. Existen reportes de infartos en personas que se encontraban recibiendo fentermina para la pérdida de peso, pero no se puede establecer una relación causal. Se ha reportado un riesgo de presentación de efectos adversos serios de 1.5%.14
Efectividad: promedio de pérdida de peso de 3.6 kg adicionales en comparación con placebo. Los estudios concluyen que existe pérdida de peso significativa, pero modesta en comparación con placebo.14
Contraindicaciones: no debe administrarse en conjunto o durante 14 días posteriores de la ingesta de inhibidores de la monoaminooxidasa, ya que puede ocasionar crisis hipertensivas.
Mazindol8
Mecanismo de acción: agente noradrenérgico y dopaminérgico, que actúa como anorexigénico, con estimulación directa del centro de la saciedad en el hipotálamo y la región límbica.
Dosis: 2 mg cada 24 horas.
Farmacocinética: se absorbe a una velocidad intermedia en el tracto gastrointestinal, se alcanzan concentraciones máximas de dos a cuatro horas, con una vida media de 33 a 55 horas.
Efectos secundarios: aunque ocasiona menores efectos que las anfetaminas, se ha reportado tolerancia al medicamento, con efectos similares a los descritos para la fentermina.
Efectividad: produce una pérdida de peso significativa en comparación con placebo durante 12 semanas de intervención, sin embargo, a un año de seguimiento no se han observado estas diferencias.15
Dietilpropión
Mecanismo de acción: catecolaminérgico.
Dosis: las dosis utilizadas en promedio son de 75 mg/día.
Efectos adversos: los efectos secundarios son similares a los producidos por la fentermina. Se predice un riesgo de efectos adversos serios de 1.5%.14
Efectividad: en general, se reporta una pérdida promedio de 3 kg más en comparación con placebo. Algunos estudios han concluido que el dietilpropión en combinación con intervenciones en el estilo de vida se ha asociado con un incremento modesto en la pérdida de peso.14
b) Fármacos serotoninérgicos
Incrementan la liberación de serotonina o bloquean su recaptura (Cuadro 2), favoreciendo la respuesta anorexigénica del sistema nervioso central (Fig. 2). Aquellos fármacos que estimulan la liberación de neurotransmisores pueden llevar a una depleción de los mismos, relacionándose con neurotoxicidad13 y con otros efectos adversos como la hipertensión pulmonar primaria y las alteraciones valvulares cardiacas.12 Los fármacos más representativos de este grupo comprenden:15
Fenfluramina8,16
Mecanismo de acción: agente serotoninérgico, químicamente relacionado con las aminas simpaticomimeticas.16
Dosis: se han descrito dosis de 400 a 800 mg al día.
Efectos secundarios: se han reportado síntomas similares a la intoxicación por anfetaminas con dosis desde 400 mg. En los estudios iniciales no se encontraron efectos adversos que ocasionaran suspensión del tratamiento; sin embargo, se observaron posteriormente efectos como diarrea, enfermedad valvular cardiaca e hipertensión pulmonar primaria. La suspensión abrupta del medicamento puede ocasionar mareo, náusea, sensación de "pesantez" en cabeza y cansancio.
Efectividad: los estudios han demostrado que la fenfluramina causa una pérdida de peso en pacientes obesos, significativamente mayor en comparación con placebo; pero el efecto de la reducción de peso cesa generalmente entre los 6 a 12 meses del mismo. Se ha reportado mejoría en los niveles de colesterol total, sin modificación en otros factores de riesgo metabólico. Un estudio realizado con adolescentes no mostró una diferencia significativa en comparación con placebo.17
Indicaciones: existen algunos reportes de su uso en síndrome de Prader-Willi y obesidad extrema.18 Se retiró del mercado en 1997 por su asociación con enfermedad valvular cardiaca e hipertensión pulmonar primaria.219
Dexfenfluramina8,15
Mecanismo de acción: agente serotoninérgico selectivo, dextroisómero de la d-fenfluramina racémica.
Dosis: de 15 a 60 mg dos veces al día.
Efectos secundarios: se ha reportado una incidencia significativamente mayor de fatiga, mareo, boca seca, náusea, diarrea y poliuria. Se ha observado que con el uso continuo los efectos adversos son menores en comparación con la administración intermitente. Está asociada con riesgo de hipertensión pulmonar cuando se usa por más de tres meses, aunque el riesgo absoluto permanece bajo.
Efectividad: en una revisión sistemática se re-portó una diferencia de pérdida de peso entre dexfenfluramina y placebo de 2.67 kg a favor del grupo de intervención durante un año de tratamiento. Sin embargo, se observó una recuperación del peso después de seis meses, la cual se encontró en proporción al pico de pérdida de peso. Existen otros reportes que no han mostrado diferencias en comparación con placebo a los cinco meses posteriores a la intervención.
Fluoxetina8
Mecanismo de acción: inhibidor de la recaptura de serotonina.
Dosis: las dosis utilizadas para la pérdida de peso son mayores (60 mg) de aquellas utilizadas para depresión (20 mg).14
Farmacocinética: alcanza concentraciones máximas entre seis y ocho horas, se une extensamente a proteínas plasmáticas, con concentraciones estables a las cuatro o cinco semanas. Su metabolito activo es la norfluoxetina, con una vida media de 6.4 días.
Efectos secundarios: se han reportado síntomas gastrointestinales (diarrea, náusea, vómito, disfagia, dispepsia, alteraciones del gusto), síntomas autonómicos (boca seca, sudoración, vasodilatación, escalofríos, etc.) y síndrome serotoninérgico (alteraciones en el estado mental y en la actividad neuromuscular en combinación con disfunción autonómica del sistema nervioso central).14,15
Efectividad: es un antidepresivo eficiente, sin embargo, produce una pérdida de peso modesta a pesar de la administración continua. Se ha observado una pérdida de peso significativa con la administración continua del medicamento entre las semanas 2 a 28, pero posterior a este período se observa recuperación del peso.15 En un meta-análisis se encontró que la pérdida de peso en relación a placebo fue de 0.9 a 9.1 kg en seis meses. En el seguimiento a un año, solamente la mitad de los pacientes reportaron una pérdida de peso estadísticamente significativa.14 En pacientes con diabetes mellitus tipo 2 (DM2) se ha reportado una pérdida de peso significativa entre los 3 y 12 meses de tratamiento en comparación con placebo.15
Indicaciones: depresión, trastorno obsesivo-compulsivo, bulimia nerviosa. No se ha aprobado su uso como tratamiento para la obesidad.13
Sertralina
Solamente se ha reportado un estudio con seguimiento a 54 semanas en donde no se han observado resultados concluyentes, y debido a la falta de estudios no se pueden realizar recomendaciones de este medicamento para el tratamiento de la obesidad.14
c) Otros fármacos con efecto central
Bupropión
Mecanismo de acción: inhibidor de la recaptura de noradrenalina, dopamina y en menor grado de serotonina.
Dosis: 300 a 400 mg por día.
Efectos adversos: entre los efectos adversos más frecuentemente observado se encuentran boca seca e insomnio. También se han observado incrementos no significativos en diarrea y constipación, problemas respiratorios superiores, cefalea, efectos a nivel de sistema nervioso central y síntomas abdominales.14
Efectividad: la pérdida de peso estimada en comparación con placebo es de 2.77 kg. La pérdida total de peso reportada es de 4-44 kg.
Sibutramina
Fórmula química: es una mezcla racémica de enantiómeros (+) y (-) de la ciclobutanemetanamina, con la fórmula l-(4-clorofenil)-N, N dimetil-(2-metilpropil)-hidroclorodemonohidrato20 (Fig. 3).
Mecanismo de acción: la sibutramina se comenzó a estudiar como fármaco antidepresivo, aunque no demostró ser eficaz para este objetivo.21 Es un agente de acción central con inhibición no selectiva de la recaptura de neurotransmisores, siendo más efectivo contra serotonina y norepinefrina, pero también puede bloquear la recaptura de dopamina.22
La sibutramina tiene una acción fisiológica dual, influenciado ambos lados de la ecuación del balance de energía13 (Fig. 4).
1. Reduce la ingesta incrementando la saciedad. Se ha descrito una reducción en adultos de la ingesta de 312 a 356 kcals por día. Su efecto se basa en prolongar la sensación de saciedad que se desarrolla de forma normal después de comer. Esto ocasiona además, que los pacientes terminen de comer de forma más temprana y disminuyan la ingesta de alimentos entre comidas.
2. El otro efecto de la sibutramina es su acción en el tejido adiposo pardo promoviendo la termogénesis, produciendo una pérdida adicional de peso al incrementar el gasto energético. Este efecto dual lleva a una pérdida de peso y mantenimiento de esta pérdida.13,23
Dosis: la dosis recomendada en adultos va de 10 a 15 mg/día, aunque existen reportes de dosis administradas de hasta 20 mg/día. Los estudios en pacientes adolescentes han sugerido una dosis inicial de 10 mg con incremento a 15 mg/ día si a los seis meses no existe una reducción del índice de masa corporal (IMC) en un 10%.24,25
Farmacocinética: la sibutramina es una amina terciaria que forma seis metabolitos a partir de la desmetilación hepática, de los cuales dos son farmacológicamente activos (MI y M2) y responsables de las acciones farmacológicas26 (Fig. 3). Se absorbe rápidamente después de la ingestión oral, alcanzando concentraciones máximas en una hora. Se excreta en su mayoría por orina (77%) y en menor cantidad por la bilis, permitiendo una reabsorción intestinal que ocasiona un segundo pico plasmático entre 6 y 10 horas después de administrada la dosis. Los metabolitos activos alcanzan concentraciones máximas entre tres y cinco horas, y por el reciclamiento biliar entre seis y nueve horas. La vida media total de la sibutramina es de 16 horas.27
Efectos secundarios: los efectos adversos más frecuentemente observados son secundarios a la vasoconstricción, manifestándose como boca seca, incremento en la presión arterial (promedio de 1 a 4 mm Hg de presión sistólica y de 2 a 4 mm Hg de presión diastólica),2 constipación y taquicardia (incremento promedio de cuatro latidos por minuto). También se han reportado: insomnio, mareo, ansiedad, depresión, constipación y cefalea, entre otros.9,20,25,26 Existen reportes que asocian el uso de sibutramina con ectopia ventricular y síndrome de QT alargado.26 En un estudio realizado en adolescentes, se requirió disminución de la dosis en 28% de los pacientes y suspensión del medicamento en 12%, por la presencia de hipertensión e incremento en la frecuencia cardiaca;28 sin embargo, en un estudio posterior realizado por el mismo grupo de investigación, se reportó un abandono del tratamiento hasta de 24%, pero no asociado a efectos adversos ocasionados por sibutramina.24 No se han documentado efectos adversos posteriores a la suspensión del medicamento,27 así como tampoco existe evidencia de abuso o dependencia.20 En un meta-análisis se reportó que los efectos adversos serios pueden ser de 0.15%.14
Efectividad: el estudio STORM (Sibutramine Trial on Obesity Reduction and Maintenance) concluyó que sibutramina es útil en la reducción de peso y en el mantenimiento del mismo a largo plazo; se encontró también que sibutramina disminuye el efecto de "rebote", aunque, al igual que con otros tratamientos, se sigue presentando. Los estudios han demostrado que se puede obtener una pérdida de peso exitosa cuando se combina con cambios en la alimentación y la actividad física, ya que sin estas modificaciones la pérdida de peso es pobre. Los resultados en diversos estudios son variados y dependen de los criterios de inclusión y las medidas de cointervención aplicadas. La respuesta inicial en la pérdida de peso es un predictor importante del éxito a largo plazo, de tal forma que los pacientes que pierden entre 1 y 2 kg en un mes, alcanzan una pérdida de 3.5 kg en un año, mientras que aquellos que pierden más de 3 kg en un mes, pueden tener una pérdida promedio de 10.5 kg en un año; y por el contrario, aquellos que no alcanzaron una pérdida de peso de 3 kg a los tres meses no alcanzarán una pérdida significativa a un año.11 En estudios de meta-análisis y revisiones sistemáticas, se encontró una pérdida entre 3.4 y 6 kg a cuatro meses de tratamiento, y una diferencia en la pérdida de peso de 4-45 kg en comparación a placebo entre 44 a 54 semanas de tratamiento. En general, se ha descrito que los pacientes que toman sibutramina tienen 20 ó 30% más de posibilidad de perder por lo menos 5% del peso corporal en comparación con placebo. No se han observado reducciones en los índices de morbilidad y mortalidad con el uso de sibutramina.14,20,29 Estudios en población mexicana adulta han reportando una pérdida de peso en seis meses de 7.52 kg vs 3.56 kg con placebo, y una reducción del IMC de 3.14 kg/m2 vs 1.4 kg/m2 respectivamente.25 En esta misma población se encontró que la suspensión del medicamento ocasiona una recuperación del peso pero sin alcanzar los niveles básales, y en pacientes que habían recibido previamente placebo se observó un efecto benéfico al iniciar sibutramina; sin embargo, la administración temprana de este fármaco tuvo mejores resultados.27 Se ha demostrado, por otra parte, que sibutramina puede tener un efecto benéfico en las comorbilidades asociadas como la apnea del sueño y el asma.13 Se ha descrito una disminución en los factores de riesgo asociados con el síndrome metabólico, con disminución de la grasa visceral, mejoría en el perfil lipídico, disminución de la hemoglobina glucosilada y del ácido úrico. También se ha encontrado que sibutramina es efectiva en alcanzar una pérdida de peso en pacientes adultos con DM2, pero ésta ocurre más lentamente en comparación con pacientes no diabéticos.30
Diversos estudios han demostrado su eficacia en pacientes adolescentes, en quienes el IMC disminuye en promedio 2.9 kg/m2 y el peso en 8.4 kg en comparación con placebo.9,24,31 La combinación de sibutramina con terapia conductual en adolescentes, ha reportado una disminución del peso en los primeros seis meses de 7.8 kg vs 3.2 kg en el grupo placebo, con una reducción del IMC de 8.5 vs 4%, respectivamente. Sin embargo, nuevamente, al igual que lo reportado en diversos tratamientos para la obesidad, se observó una ganancia de 0.8 kg entre los 6 y 12 meses, a pesar de continuar el tratamiento.15,28 En adolescentes, también se han observado efectos benéficos de sibutramina sobre factores de riesgo cardiometabólico, disminuyendo los niveles postprandiales de insulina, la resistencia a la insulina y mejorando el perfil lipídico.24 Se realizó un estudio para valorar la eficacia y seguridad de 46 adolescentes mexicanos obesos, con un seguimiento a seis meses. Se observó una pérdida de peso promedio de 7.3 kg vs 4.3 kg en el grupo de placebo, en la circunferencia de cintura de 8 vs 3.8 cm y de IMC de 9.2 vs 5.2%, respectivamente; concluyendo que sibutramina, aunada a un programa de dieta y ejercicio, es efectivo y generalmente bien tolerado en la población de estudio.32
Indicaciones: aunque en los estudios citados previamente, se ha utilizado sibutramina en pacientes desde los 13 años de edad, las recomendaciones actuales por la FDA limitan su uso a mayores de 16 años,9 sin extender el tratamiento a más de dos años,4 y suspenderlo si no existe respuesta al tratamiento en un año. A pesar de haber sido aprobado su uso en pacientes pediátricos, la mayoría de los investigadores concuerdan en que se requiere de más estudios para determinar la seguridad y eficacia a largo plazo de sibutramina en adolescentes.4
Contraindicaciones: pacientes con trastornos mayores de alimentación o que estén tomando inhibidores de la monoaminoxidasa u otros supresores centrales del apetito.4,20 No debe administrarse en pacientes con historia de enfermedad arterial coronaria, insuficiencia cardiaca congestiva, disritmias, infarto, daño renal severo, disfunción hepática severa, y en aquellos con hipersensibilidad a la fórmula. Deberá utilizarse con cautela en pacientes con hipertensión arterial, glaucoma de ángulo cerrado y aquéllos con historia de convulsiones o desórdenes bipolares.21
Interacciones farmacológicas: no deberá administrarse junto con fármacos que incrementen la frecuencia cardiaca y la presión arterial. Dado que se metaboliza por la citocromo P450, se deberá evitar administrar de forma concomitante con fármacos que compitan por esta enzima (ej. ketoconazol, eritromicina y cimetidina).21
Rimonabant
Mecanismo de acción: inhibidor del receptor de canabinoides 1 (CB1). El sistema de endocanabinoide es un neuromodulador que participa en varios procesos fisiológicos, incluyendo la regulación del balance energético y la secreción adipocitaria. Se encuentran involucrados mecanismos centrales y periféricos, cuyas acciones están mediadas por dos subtipos de receptores CB1 y CB2. El receptor CB1 está localizado en cerebro, grasa, pulmón, intestino, músculo e hígado, así como en ganglios simpáticos, corazón y vejiga. El CB2 está expresado en el sistema inmune, y aparentemente no tiene relación con el metabolismo energético. El sistema endocanabinoide tiene usualmente una sobreexpresión en pacientes obesos y responde a estímulos externos como la actividad física y la ingesta de alimentos. Rimonabant, al bloquear el receptor CB1, disminuye el tono endocanabinoide, reduciendo la ingesta de alimentos a través de acciones a nivel hipotalámico, sistema mesolímbico y nervio vago, así mismo estimula directamente la expresión de adiponectina en el tejido adiposo blanco.2,33
Dosis: de 5 a 20 mg/día.2,33
Efectos adversos: generalmente es bien tolerado. Los efectos adversos más frecuentes son: malestar abdominal, náusea y diarrea, depresión del estado de ánimo, ansiedad, agitación, alteraciones del sueño, entre otros.2,33,34
Efectividad: en el estudio RIO (Rimonabant in obesity) se ha observado que rimonabant ocasiona una pérdida significativa de peso. Así mismo, se ha observado mejoría en los componentes del síndrome metabólico, como la disminución de los niveles de glucosa e insulina, reducción de triglicéridos e incremento del colesterol de alta densidad (c-HDL), en comparación con placebo. También se han reportado disminución en los niveles de proteína C reactiva y de hemoglobina glucosilada, así como reducción de los niveles de adiponectina y de la progresión de aterosclerosis coronaria. La pérdida de peso reportada varía de 3.1 kg con dosis de 5 mg, y de 6.9 kg con 20 mg a un año de tratamiento. Comparado con placebo, el uso de 20 mg de rimonabant produce reducción en el peso de 6.3 vs 1.6 kg y de circunferencia de cintura de -6.1 vs -2.5 cm, respectivamente, a favor de rimonabant. Se ha reportado que la continuación del tratamiento posterior a dos años ocasiona una pérdida promedio de 7.4 kg, observándose con la suspensión del tratamiento un efecto de recuperación del peso. Este medicamento ha sido aprobado en adultos, sin embargo aún no existen estudios que aprueben su uso en pacientes pediátricos.33,34
Topiramato
Mecanismo de acción: monosacárido sulfamato sustituido, utilizado como agente antiepiléptico. Bloquea los canales de sodio e incrementa la actividad GABAérgica, adicionalmente inhibe algunas isoenzimas de la anhidrasa carbónica.
Dosis: las dosis utilizadas son de 25 a 600 mg/ día.35 Se ha encontrado que entre mayor sea la dosis, se obtiene una mayor pérdida de peso.14
Farmacocinética: absorción gastrointestinal rápida, con eliminación renal. Se fija en 13 a 17% a proteínas plasmáticas, y sufre cambios mediante hidroxilación, hidrólisis y glucuronización. Los pacientes pediátricos tienen una depuración más alta y una vida media de eliminación más corta.
Efectividad: se estima una pérdida de peso en comparación con placebo de 6.5%.14
Efectos secundarios: se ha reportado un abandono del tratamiento hasta en 32%, asociado a efectos adversos como: parestesias, boca seca, cefalea, alteración en la percepción de los sabores, mareo, somnolencia, fatiga, constipación, diarrea, dispepsia, problemas respiratorios y fatiga, como los más frecuentes.14,35
Indicaciones: se ha utilizado en pacientes con conductas compulsivas de alimentación sin conductas inapropiadas para pérdida de peso, observándose mejoría en estas conductas y en la obesidad.35 Debido a la falta de estudios, no se pueden hacer recomendaciones para el tratamiento de la obesidad.14
II. Fármacos que incrementan el gasto energético
a) Hormonas tiroideas
Fueron los primeros medicamentos utilizados para la pérdida de peso, reportándose su uso desde 1893. Estimulan el metabolismo y el gasto energético; sin embargo, para alcanzar un efecto sobre la pérdida de peso se requiere de la producción de hipertiroidismo, con consecuencias catabólicas en músculo, hueso y corazón, por lo que a la fecha no se recomiendan con este objetivo.13
b) Fármacos noradrenérgicos
Incrementan el metabolismo mediante la estimulación de los receptores β2 adrenérgicos (sibutramina), estimulando la secreción de norepinefrina con estimulación secundaria de receptores α y β adrenérgicos (efedrina), o retardando la degradación de norepinefrina (cafeína). Pueden presentar efectos adversos graves relacionados con la actividad adrenérgica (temblor, incremento de la presión arterial, hiperglucemia, etc.).12
III. Fármacos que afectan la absorción de nutrimentos
a. Fase preabsortiva
Inhibidores del vaciamiento gástrico, que incremenetan la saciedad de forma directa o mediante la acción de hormonas intestinales (amilina, péptido similar a glucagón)
b. Fase absortiva
1. Inhibodores de la α-glucosidasa como la acarbosa, pero a pesar de su mecanismo de acción, a dosis habituales no ha demostrado una pérdida de peso significativa.12
2. Inhibidores de la absorción de grasa como el orlistat.36
Orlistat10
Fórmula química: tetrahidrolipstatina, derivado parcialmente hidratado de la lipstatina endógena producida por Streptomyces toxytricini31 (Fig. 5).

Mecanismo de acción: inhibidor reversible de la lipasa gástrica y pancreática fijándose a ésta en la luz del tubo digestivo. Ocasiona una reducción en la cantidad de grasa disponible para la absorción intestinal y, por lo tanto, incrementa la excreción de grasa en las evacuaciones. Orlistat no inhibe otras enzimas y no afecta lipasas sistémicas4 (Fig. 6).
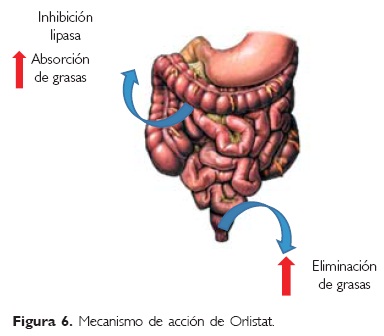
Dosis: en pacientes pediátricos se han utilizado dosis de 120 mg tres veces al día,38,40 se administra una hora antes o durante los alimentos.
Farmacocinética: Orlistat tiene una pobre absorción intestinal22 y disminuye la absorción de grasas en 30% (16 g/día) en personas que consumen 30% de grasa en la dieta.4 Tiene un inicio de acción de 24 a 48 horas, con una duración de 48 a 72 horas. Se metaboliza en la pared gastrointestinal y forma metabolitos inactivos en 83%. Se excreta 97% en heces y el resto en orina.
Efectos secundarios: se han reportado diarrea, flatulencias, dolor abdominal, evacuaciones grasas, incontinencia fecal, manchado de ropa interior, entre otros.20 Existen estudios que han observado la presencia de estos síntomas entre un 50 y 100% de los pacientes.4,39 Estos efectos pueden desaparecer con el tiempo, probablemente debido a la disminución en la ingesta de grasas para evitarlos y teniendo un efecto benéfico en la pérdida de peso y en la mejoría de los factores de riesgo metabólico.22,41 En un estudio en adolescentes, se encontró 31.8% de abandono del tratamiento en el primer mes, secundario a los efectos adversos.39 También se ha reportado que de los pacientes que continúan el tratamiento, el apego en el número de tomas es de aproximadamente 80%.42,43 Se han reportado casos que requieren suplementación adicional de vitamina D debido al incremento en la resorción ósea, a pesar de la prescripción diaria de multivitamínicos.22 Aunque es difícil establecer una relación causa-efecto, se han reportado casos de enfermedad litiásica vesicular en niños en tratamiento con orlistat que incluso han requerido tratamiento quirúrgico.2 Se ha documentado también la presencia de efectos secundarios no gastrointestinales como cefalea, dolor de espalda, infecciones de vías respiratorias superiores, fatiga, ansiedad, alteraciones del sueño, piel seca, alteraciones menstruales, artritis, mialgias y otitis. Un meta-análisis reportó una presencia de efectos adversos serios en 0.03%.14
Efectividad: los pacientes en tratamiento con orlistat logran una pérdida de peso significativamente mayor en comparación con placebo, y con mayor frecuencia logran mantener su peso. Los estudios demuestran que los pacientes presentan 2.7 kg ó 2.9% más de reducción de peso en comparación con placebo en un año de seguimiento.14,20 Un meta-análisis reporta una media de pérdida de peso de 2.59 kg en comparación con placebo, con un total de 5.39 kg.14,22 En un estudio multicéntrico aleatorizado en adolescentes de 12 a 16 años, se obtuvo una reducción del IMC de 0.55 kg/m2 en el grupo de orlistat, en comparación con un incremento del IMC de 0.31 kg/ m2 en el grupo placebo. En este mismo estudio, no se observaron diferencias en los niveles de lípidos y glucosa, sugiriendo que la pérdida de peso fue muy pequeña para modificar los factores de riesgo metabólico.43 A diferencia del estudio anterior, otros investigadores han encontrado resultados más alentadores. Cruz y col.,38 reportaron una reducción del IMC de 4.20 kg/m2, en comparación a placebo. En otro estudio, en pacientes adolescentes, se encontró una diferencia promedio de -6.27 kg con el uso de orlistat vs +4.16 kg con placebo y un IMC -4.09 kg/m2 vs +0.11 kg/m2, respectivamente, con un seguimiento de 5 a 15 meses.39 Se ha demostrado que orlistat puede limitar el riesgo cardiovascular, independientemente de las reducciones del peso corporal, al disminuir los niveles de colesterol total, colesterol de baja densidad (c-LDL), insulina de ayuno y glucosa de ayuno.22-40 Por otra parte, orlistat puede disminuir el riesgo de desarrollar diabetes, y en los pacientes diabéticos mejorar el control glucémico, el perfil lipídico y favorecer la pérdida de peso y el mantenimiento del mismo.44 De la misma forma, se ha asociado con una reducción significativa de la presión arterial sistólica y diastólica. Los estudios en donde se combina orlistat con sibutramina no han demostrado un beneficio adicional.20
Indicaciones: se recomienda su uso en pacientes con un IMC igual o mayor de 30 kg/m2 o igual o mayor de 27 kg/m2, en presencia de otros factores de riesgo. La FDA aprueba su uso en pacientes mayores de 12 años con obesidad, aunque existen estudios en los cuales han administrado el medicamento en niños hasta de ocho años de edad;41 sin embargo, debido a la falta de estudios a largo plazo, desconocemos si puedan existir efectos adversos, sobre todo en cuanto al crecimiento y el desarrollo en pacientes prepúberes.
Contraindicaciones: pacientes con malabsorción crónica o colestasis, y en casos de hipersensibilidad a la fórmula.9
Interacciones medicamentosas: puede disminuir la absorción de fármacos como la amiodarona y ciclosporina, alterar la farmacocinética de anticoagulantes debido a una deficiencia en la absorción de vitamina K.
Observaciones: se requiere suplementación con vitaminas liposolubles, las cuales deben ingerirse dos horas antes o dos horas después de la toma del medicamento.20,37,40
c. Fase postabsortiva
En este grupo se consideran moduladores del metabolismo como la hormona de crecimiento, que ha sido utilizada con el objetivo de incrementar la masa magra y disminuir el tejido graso, la testosterona para intentar disminuir la grasa visceral y mejorar las alteraciones metabólicas asociadas con resistencia a la insulina en hombres obesos con hipoandrogenismo y la metformina, que mejora la sensibilidad a la insulina.12 Todavía no existen resultados concluyentes de los dos primeros fármacos para el tratamiento de la obesidad, sin embargo, metformina pudiera tener un papel importante.
Metformina10
Mecanismo de acción: pertenece al grupo de las biguanidas, y actúa como un agente sensibilizador de insulina con propiedades antihiperglucemiantes potentes, actuando a través de los siguientes mecanismos (Fig. 7):
a. Supresión de la producción hepática de glucosa mediante la activación de la AMPK (AMP-activated protein kinase) ocasionando disminución de los niveles de insulina e inhibiendo la lipogénesis.
b. Incremento de la sensibilidad periférica a la insulina al interrumpir el proceso oxidativo mitocondrial en el hígado y corregir las alteraciones en el metabolismo intracelular del calcio en los tejidos sensibles a insulina (hígado, musculoesquelético y adipocitos) y en el tejido cardiovascular.2,45 Ocasiona pérdida de peso mediante la supresión del apetito, incrementando los niveles del péptido 1 similar a glucagón,2 aunado a la disminución de la hiperinsulinemia potenciando el efecto de pérdida de peso en pacientes con obesidad e insulino-resistencia.2,9,45
c. Dosis: en adolescentes con obesidad, hiperinsulinemia y antecedentes familiares de DM2, se han utilizado dosis de 500 mg cada 12 horas.38 Se recomienda iniciar con dosis bajas, generalmente de 500 mg/día, debiéndose de administrar junto con los alimentos para evitar síntomas gastrointestinales. Se podrán realizar incrementos de 500 mg cada una a dos semanas, de acuerdo a las variables metabólicas del control glucémico. Dosis máxima de 2 550 mg/día.45
Farmacocinética: metformina tiene una biodisponibilidad de 50 a 60%. No se fija a proteínas, tiene un amplio volumen de distribución, con una acumulación máxima en la pared del intestino delgado. Tiene una vida media de 1 a 4.9 horas. Se excreta sin cambios en 40 a 60% por vía renal a través de filtración glomerular y, posiblemente, por secreción tubular, y el restante 30% se excreta por las heces. Debido a lo anterior, la disminución en la función renal puede ocasionar acumulación del fármaco, sin embargo, no se han establecido dosis específicas de ajuste en pacientes con daño renal. Se puede eliminar mediante hemodiálisis.45,46
Efectos secundarios: habitualmente es bien tolerada, pero se ha reportado que 5% de los pacientes presentan intolerancia debida a los efectos gastrointestinales, y 6 a 7% abandonan el tratamiento debido a los efectos adversos.9,45 Los efectos secundarios más frecuentemente reportados son: diarrea, náusea, vómito, flatulencia y malestar abdominal, los cuales suelen ser dosis dependientes y pueden evitarse con incrementos paulatinos de la dosificación, con reducción de la misma, o con la administración conjunta con los alimentos. Los mecanismos de estos efectos gastrointestinales son poco claros, pero probablemente se encuentren relacionados con una acumulación de altas cantidades de metformina en el tejido intestinal, con una elevación local de la producción de lactato; 10 a 30% de los pacientes que reciben tratamiento por tiempo prolongado, pueden desarrollar malabsorción de vitamina B12.9,45 Se ha asociado la administración de sibutramina con la producción de acidosis láctica, sin embargo, en una revisión sistemática no se encontró evidencia formal de que metformina causara acidosis láctica, aún en pacientes con insuficiencia renal u otras comorbilidades, aunque se sugiere tener precaución en pacientes con comorbilidades múltiples y severas.47 No se han reportado casos de acidosis láctica en pacientes pediátricos.9
Efectividad: la evidencia de que metformina pueda tener un lugar en el tratamiento de la obesidad no es del todo clara y hay información limitada en población pediátrica. Se sabe que metformina tiene efectos benéficos en la reducción de factores de riesgo cardiometabólicos como disminución de la hiperglucemia, mejoría de la función vascular y endotelial, y mejoría en el perfil lipídico.45 Parece ser que el peso previo al tratamiento es un predictor importante de la pérdida y del mantenimiento del mismo, es decir, entre mayor sea el peso inicial, se observará mayor pérdida de peso.48 En pacientes jóvenes con obesidad, hiperinsulinemia e historia familiar de DM2, se ha observado disminución en el IMC y de la insulina en ayuno de forma significativa.38 Se realizó un estudio en adolescentes no diabéticos con seguimiento a seis meses, encontrado una reducción significativa del IMC, de los niveles de glucosa y de la insulina en ayuno, sin otras intervenciones asociadas.49 Otro estudio en pacientes pediátricos de 9 a 18 años de edad, reportó una pérdida de peso de 4.35 kg, reducción del IMC de 1.26 kg/m2 y disminución de la circunferencia de cintura en 2.8 cm más en comparación con placebo, con mejoría en el porcentaje de grasa corporal, de la insulina de ayuno y de la sensibilidad a la insulina.50 Un trabajo similar en pacientes adolescentes obesos hiperinsulinémicos, demostró resultados similares, aunado a una reducción de los niveles de leptina y mejoría en el perfil lipídico.51 Se ha valorado la utilidad de metformina en pacientes que toman drogas psicotrópicas, teniendo resultados poco concluyentes.52
Indicaciones: metformina está indicada en pacientes con DM2 y síndrome de ovarios poliquísticos.38 Su papel como tratamiento para la pérdida de peso es todavía controversial.
Contraindicaciones: enfermedad cardiaca, hepática, renal o gastrointestinal, así como en aquellos pacientes que serán intervenidos quirúrgicamente.9 Así mismo, se encuentra contraindicado en casos de alcoholismo y en infección activa moderada a severa. La administración de material de contraste puede alterar la función renal, ocasionando acumulación del fármaco, por lo que se deberá tener precaución en esta situación. También se ha descrito la posibilidad de acumulación de lactato en pacientes sometidos a anestesia general por desarrollar hipotensión e hipoxia. Se deberá administrar con cautela en ancianos.45
Interacciones medicamentosas: la cimetidina y los medios de contraste pueden disminuir la excreción renal.45,46
Otros fármacos
Más de 120 drogas potenciales para el tratamiento de la obesidad se encuentran en varios estadios de investigación, pero al momento todavía no existe un tratamiento único que resulte efectivo,4 probablemente debido a que la mayoría de los casos de obesidad tienen un origen multifactorial. Entre algunos de los tratamientos en fases de investigación, y en otros que se han utilizado para tipos específicos de obesidad, encontramos:
Leptina10
Mecanismo de acción: la palabra leptina derivada del griego leptos que significa "delgado", la cual es producida por las células grasas y circula a niveles proporcionales al contenido de grasa corporal. Cruza la barrera hematoencefálica y se une a su receptor en el hipotálamo, activando señales que inhiben la ingesta de alimentos e incrementa el gasto energético.53 Se sabe que la leptina afecta la expresión génica y la vía sintética de sustancias anorexigénicas y orexigénicas.
Indicaciones: solamente en pacientes con déficit selectivo de esta hormona.
Efectividad: la deficiencia de leptina es poco frecuente, ocasionando una obesidad mórbida de inicio temprano. El tratamiento con leptina en estos pacientes produce efectos benéficos en la masa grasa, hiperinsulinemia, hiperlipidemia y en la función tiroidea con resultados espectaculares.54 La hipótesis de que la obesidad humana resulta de una deficiencia de leptina no ha sido comprobada, y se ha sugerido que generalmente los pacientes obesos son resistentes a leptina y probablemente los defectos se localicen a nivel post receptor, por lo que no responden al tratamiento con leptina.53
Zonisamida
Se desconoce el mecanismo de acción, se han observado resultados significativos en la pérdida de peso; sin embargo, aún faltan más estudios para ser recomendada.14 Las dosis utilizadas en general son de 100 mg/día, la cuales se pueden incrementar de acuerdo a la respuesta hasta 600 mg/día. Se ha reportado que en un lapso de 16 semanas se puede obtener una pérdida de peso de 6% en coMparación de 1% con placebo.14
Octreótide
Se ha utilizado en casos de obesidad hipotalámica.9 En este tipo de pacientes se ha observado supresión de la insulina y estabilización del peso y del IMC, reportándose generalmente como seguro y bien tolerado.55
Ácidos grasos omegd-3
Los ácidos grasos omega-3 son ácidos poliinsaturados, cuyo primer doble enlace (contando a partir del grupo metilo terminal) se encuentra en el carbono 3. Los principales incluyen el ácido lino-lénico, el eicosapentanoico y el docosahexanoico. Los ácidos grasos omega-3 disminuyen la síntesis y secreción de partículas de colesterol de muy baja densidad (c-VLDL) e incrementan la salida de triglicéridos de las partículas c-VLDL y de los quilomicrones, a través del incremento en la regulación de lipoproteinlipasa.56
Se ha propuesto que los ácidos grasos poliinsaturados Ω-3 pueden modular los componentes de adiposidad, inflamación y metabolismo de los ácidos grasos, con lo que se disminuye la conversión hacia síndrome metabólico y el riesgo cardiovascular.57 Se ha asociado su consumo con disminución en la agregación plaquetaria, con efecto benéfico en el control glucémico, inflamación, oxidación,58 sensibilidad a la insulina,59 en el incremento de los niveles de adiponectina60,61 y en la disminución de los marcadores inflamatorios,62 aunque los estudios no han mostrado consistencia.
Los ácidos grasos omega-3 han sido aprobados por la FDA como una medida efectiva para disminuir los niveles de triglicéridos. La Academia Americana del Corazón recomienda el consumo de estos ácidos para disminuir el riesgo cardiovascular, ya que se ha documentado que pueden disminuir la incidencia de arritmias, muerte súbita, aterosclerosis y, de forma discreta, la presión arterial.56 En pacientes pediátricos se ha encontrado que la suplementación con 1 000 mg de ácido alinolénico puede mejorar el perfil lipídico.63
En cuanto a la pérdida de peso en pacientes adultos, se ha encontrado que la suplementación de ácidos grasos omega-3 incrementa la pérdida de peso en conjunto con dietas con muy bajo aporte energético64 y pueden prevenir la formación de cálculos de colesterol durante una pérdida de peso rápida.65 No hay estudios en población pediátrica que demuestren el papel benéfico de los ácidos grasos omega-3 en la pérdida de peso, pero se puede considerar su uso cuando existen alteraciones en el perfil lipídico, específicamente en hipertrigliceridemia.
Otros fármacos
Investigaciones recientes han encontrado que existen células madre en el tejido adiposo que pueden ser responsables de la hiperplasia del tejido adiposo. Se han utilizado fármacos que puedan controlar la proliferación de estas células como la GSK3 (Glycogen Synthase Kinase 3), pudiendo tener un papel en el control de la obesidad, aunque todavía los estudios se encuentran en fase experimental.66
En estudios de investigación se encuentran péptidos gastrointestinales y pancreáticos que regulan la ingesta de alimentos. Entre algunos de ellos encontramos:9,53,67,69
• Antagonistas del receptor 1 canabinoide como el MK-0364, CP-945-598, SLV-319, AVE-1625.
• Inhibidores de lipasa como el cetilistat.
• Fragmento de hormona de crecimiento como el AOD 9604.
• Agonistas selectivos de serotonina como el lorcaserina, vabicaserina, BVT 933-5, ATHX-1055.
• Antagonistas de la colecistocinina entre otros.
• Zonisaida, exenatide y miméticos de incretinas.
• Agonistas del receptor 4 de melanocortina. Antagonistas de ghrelina.
• También se están investigando antagonistas del neuropéptido Y, el cual tiene actividades orexigénicas y de disminución del gasto energético.
• Análogos de adiponectina.
Conclusiones
Los medicamentos actualmente utilizados para el tratamiento de la obesidad en adultos incluyen: sibutramina, orlistat, fentermina, dietilpropión, fluoxetina y bupropión. La pérdida de peso con estos diferentes fármacos, de acuerdo a un metaanálisis, se muestran en el cuadro 3.14,70 No existen estudios que comparen la efectividad de estos tratamientos entre sí.
En general, la mayoría de los autores concuerdan que el tratamiento farmacológico se debe reservar a:
• Pacientes que tienen factores de riesgo relacionados con la obesidad.
• Pacientes con falta de respuesta a un programa de dieta estructurado y modificaciones en el estilo de vida. Estos cambios deberán realizarse antes de iniciar la farmacoterapia y mantenerse durante la misma. Si bien, entre más temprano se inicie el tratamiento farmacológico se observan mejores resultados, y se desconocen los efectos adversos que se pueden presentar a largo plazo.
• Pacientes que conocen que después de la suspensión del medicamento se puede presentar una recuperación del peso y que se desconoce cual debe ser la duración ideal del mismo.
• Pacientes que comprenden las limitaciones del tratamiento farmacológico, incluyendo la necesidad de cambios concomitantes en el estilo de vida, el hecho de que la efectividad de los medicamentos disminuye a los seis meses del tratamiento, así como la falta de datos sobre seguridad a largo plazo. Los únicos fármacos aprobados en la actualidad para su utilización en edades pediátricas son orlistat y sibutramina.
• Pacientes que conocen que la pérdida de peso atribuible a los medicamentos es modesta y que al tratarse de una enfermedad crónica se requiere de medidas de alimentación, actividad física o terapia conductual que lleven a cambios en el estilo de vida de forma permanente.
• Pacientes que saben que la elección del medicamento debe basarse en los factores de riesgo relacionados, los mecanismos de acción, los efectos adversos asociados, y si se conoce la causa de la obesidad.
Referencias
1. Liou TH, Wu CH, Chien HC, Un WY, Lee WJ, Chou P. Anti-obesity drug use before professional treatment in Taiwan. Asia Pac J Clin Nutr. 2007; 16: 580-6. [ Links ]
2. Freemark M. Pharmacotherapy of childhood obesity: An evidence-based, conceptual approach. Diabetes Care. 2007; 30: 395-402. [ Links ]
3.Dietz WH, Robinson TH. Assessment and treatment of childhood obesity. Pediatr Rev. 1993; 14:337-43. [ Links ]
4. Spear BA, Barlow SE, Ervin C, Ludwig DS, Saelens BE, Schetzina KE, et al. Recommendations fortreatment of child and adolescent overweight and obesity. Pediatrics. 2007; 120: S254-88. [ Links ]
5. Bray GA, Greenway FL. Current and potential drugs for treatment of obesity. Endocr Rev. 1999; 20: 805-75. [ Links ]
6. Ioannides-Demos LL, Proietto J, Tonkin AM, McNeil JJ. Safety of drug therapies used for weight loss and treatment of obesity. Drug Saf. 2006; 29: 277-302. [ Links ]
7. Moyers SB. Medications as adjunct therapy for weight loss: approved and off-label agents in use. J Am Diet Assoc. 2005; 105: 948-59. [ Links ]
8. Douketis JD, Feightner JW, Attia J, Feldman WF, with the Canadian Task Force on Preventive Health Care. Periodic health examination, 1999 update: I. Detection, prevention and treatment of obesity. CMAJ. 1999; 160: 513-25. [ Links ]
9. Uli N, Sundararajan S, Cuttler L. Treatment of childhood obesity. Curr Opin Endocrinol Diabetes Obes. 2008; 15: 37-47. [ Links ]
10. Dalmau J, Alonso M, Gómez L, Martinez C, Salinas S. Obesidad infantil. Recomendaciones del Comité de Nutrición de la Asociación Española de Pediatría. Parte II. Diagnóstico. Comorbilidades. Tratamiento. An Pediatr Bare. 2007; 66: 294-304. [ Links ]
11. Reitman MC, Schadt E. Pharmacogenetics of metformin response: a step in the path toward personalized medicine. J Clin Invest. 2003; 117: 1226-9. [ Links ]
12. Scheen AJ, Lefébvre AJ. Pharmacological treatment of obesity: present status international. J Obes. 1999; 23: 47-53. [ Links ]
13. Finer N. Sibutramine: its mode of action and efficacy. Int J Obes. 2002; 26: S29-S33. [ Links ]
14. Li Zhaoping, Maglione M, Tu W, Mojica W, Arterbur D, Shugarman L, et al. Meta-Analysis: Pharmacologic treatment of obesity. Ann Intern Med. 2005; 142: 532-46. [ Links ]
15. Glenny AM, O'Meara S, Melville A, Sheldon TA, Wilson C. The treatment and prevention of obesity: A systematic review of the literature. Int J Obes. 1997; 21:715-37. [ Links ]
16. Persson I, Andersen U, DeckertT. Treatment of obesity with fenfluramine. EurJ Clin Pharmacol. 1973; 6: 93-7. [ Links ]
17. Epstein LH, Myers MD, Raynor HA, Saelens BE. Treatment of pediatric obesity. Pediatrics. 1998; 101:554-70. [ Links ]
18. Zwiauer KF. Prevention and treatment of overweight and obesity in children and adolescents. Eur J Pediatr. 2000; 159: S56-S68. [ Links ]
19. Racetle SB, Deusinger SS, Deusinger RH. Obesity; over-view of prevalence, etiology, and treatment. Phys Ther. 2003; 83: 276-88. [ Links ]
20. Chaput JP, St-Pierre S, Tremblay A. Currently available drugs forthe treatment of obesity: Sibutramine and or-listat. Mini Rev Med Chem. 2007; 7: 3-10. [ Links ]
21. Nisoli E, Crruba MO. An assessment of the safety and efficacy of sibutramine, an anti-obesity drug with a novel mechanism of action. Obes Rev. 2000; 1: 127-39. [ Links ]
22. Steinbeck K. Treatment options. Best Pract Res Clin Endocnnol Metab. 2005; 19: 455-69. [ Links ]
23. Hansen DL, Toubro S, Stock MG, Macdonald IA, As-trup A. The effect of sibutramine on energy expenditure and appetite during chronic treatment without dietary restriction. Int J Obes. 1999; 23: 1016-24. [ Links ]
24. Berkowitz RI, Fujioka K, Daniels SR, Hoppin AG, Owen S, Perry AC, et al. Effects of sibutramine treatment in obese adolescents. A randomized trial. Ann Intern Med. 2006; 145: 81-90. [ Links ]
25. Fanghánel G, Cortinas L, Sánchez-Reyes L, Berber A. A clinical trial of the use of sibutramine forthe treatment of patients suffering essential obesity. Int J Obes. 2000; 24: 144-50. [ Links ]
26. Cole J, Levin A, Beake B, Kaiser P, Scheinbaum M. Sibutramine: A new weight loss agent without evidence of the abuse potential associated with amphetamines. J Clin Psychopharmacol. 1998; 18:231-6. [ Links ]
27. Fanghánel G, Cortinas L, Sánchez-Reyes L, Berber A. Second phase of a double-blind study clinical trial on sibutramine forthe treatment of patients suffering essential obesity: 6 months aftertreatment cross-over. Int J Obes. 2001; 25: 741-7. [ Links ]
28. Berkowitz RI, Wadden TA, Tershakovec AM, Cronquist JL. Behaviortherapy and sibutramine forthe treatment of adolescent obesity. A randomized controlled trial. JAMA. 2003; 289: 1805-12. [ Links ]
29. Arterburn DE, Crane PK, Veenstra DL. The efficacy and safety of sibutramine for weight loss. A systematic review. Arch Intern Med. 2004; 164: 994-1003. [ Links ]
30. Krejs GJ. Metabolic benefits associated with sibutramine therapy. Int J Obes. 2002; 26: S34-7. [ Links ]
31. Godoy-Matos A, Carrara L, Vieira A. Treatment of obese adolescents with sibutramine: a randomized, double-blind, controlled study. J Clin Endocnnol Metab. 2005; 90: 1460-5. [ Links ]
32. García-Morales LM, Berber A, Macías-Lara CC, Lucio-Ortiz C, del-Río-Navarro BE, Dorantes-Álvarez LM. Use of sibutramine in obese Mexican adolescents: A 6-month, randomized, double-blind, placebo-controlled, parallel-group trial. Clin Ther. 2006; 28: 770-82. [ Links ]
33. Rubio MA, Gargallo M, Millán Al, Moreno B. Drugs in the treatment of obesity: sibutramine, orlistat and rimonabant. Public Health Nutr. 2007; 10: 1200-5. [ Links ]
34. Pi-Sunyer FX, Aronne LJ, Heshmati HM, Devin J, Rosenstock J, for the RIO-North America Study Group. Effect of rimonabant, a cannabinoid-1 receptor blocker, on weight and cardiometabolic risk factors in overweight or obese patients. RIO-North America: A randomized controlled trial. JAMA. 2006; 295: 761-75. [ Links ]
35. McElroy SL, Shapira NA, Arnold LM, Keck PE, Rosenthal NR, Wu S, et al. Topiramate in the long-term treatment of bine-eating disorder associated with obesity. J Clin Psychiatr. 2004; 65: 1463-9. [ Links ]
36. Henness S, Perry CM. Orlistat a review of its use in the management of obesity. Drugs. 2006; 66: 1625-56. [ Links ]
37. McNellyW, Benfield P. Orlistat. Drugs. 1998; 56: 241-9. [ Links ]
38. Cruz ML, Shaibi GQ, Weigensberg MJ, Spruijt-Metz D, Ball GDC, Goran Ml. Pediatric obesity and insulin resistance: Chronic disease risk and implications for treatment and prevention beyond body weight modification. Annu Rev Nutr. 2005; 25: 435-68. [ Links ]
39. Ozkan B, Bereket A, Turan S, Keskin S. Addition of orlistat to conventional treatment in adolescents with severe obesity. Eur J Pediatr. 2004; 163: 738-41. [ Links ]
40. Krempf M, Louvet JP, Allanic H, Miloradovich T, Joubert JM, Attali JR. Weight reduction and long-term maintenance after 18 months treatment with orlistat for obesity. Int J Obes. 2003; 27: 591-7. [ Links ]
41. Norgren S, Danielsson P, Jurold R, Lotborn M, Marcus C. Orlistat treatment in obese prepubertal children: A pilot study. Acta Paediatr. 2005; 93: 666-70. [ Links ]
42. McDuffie JR, Calis KA, Uwaifo GI. Three-month tolerability of orlistat in adolescents with obesity-related comorbid conditions. Obes Res. 2002; 10: 642-50. [ Links ]
43. Chanoine JP, Hampl S, Jensen C, Boldrin M, Hauptman J. Effect of orlistat on weight and body composition in obese adolescents: A randomized controlled trial. JAMA. 2005; 293: 2873-83. [ Links ]
44. Hollander PA, Elben SC, Hirsch IB, Kelley D, McGill J, TaylorT, et al. Role of orlistat in the treatment of obese patients with type 2 diabetes. Diabetes Care. 1998; 21: 1288-94. [ Links ]
45. Kirpichnikov D, McFarlane SI, Sowers JR. Metformin: An Update. Ann Intern Med. 2002; 137: 25-33. [ Links ]
46. Campbell RK, White JR, Saulie BA. Metformin: A new oral biguanide. Clin Ther. 1996; 18:360-71. [ Links ]
47. Salpeter S. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus. Cochrane Database Syst Rev. 2004; 3: CD002967. [ Links ]
48. Hansen DL, Astrup A, Toubro S, Finer N, Kopelman P, Hilsted J, et al. Predictors of weight loss and maintenance during 2 years of treatment by sibutramine in obesity. Results from the European multi-centre STORM trial. IntJ Obes. 2001; 25: 496-501. [ Links ]
49. Freemark M, Bursey D. The effects of metformin on body mass index and glucose tolerance in obese adolescents with fasting hyperinsulinemia and a family history of type 2 diabetes. Pediatrics. 2001; 107: e55. [ Links ]
50. Srinivasan S, Ambler GR, Baur LA, Garnett SP, Tepsa M, Yap F, et al. Randomized, controlled trial of metformin for obesity and insulin resistance in children and adolescents: Improvement in body composition and fasting insulin. J Clin Endocnnol Metab. 2006; 91: 2074-80. [ Links ]
51. Kay JP, Alemzadeh R, Langley G, D'Angelo L, Smith P, Holshouser S. Beneficial effects of metformin in normoglycemic morbidly obese adolescents. Combined metformin treatment and low-calorie diet had a significant antiobesity effect in hyperinsulinemic obese adolescents compared to a low-calorie diet alone. Metabolism. 2001; 50: 1457-61. [ Links ]
52. Morrison JA, Cottingham EM, Barton BA. Metformin for weight loss in pediatric patients taking psychotropic drugs. Am J Psychiatry. 2002; 159: 655-7. [ Links ]
53. Korner J, Aronee LJ. The emerging science of body weight regulation and its impact on obesity treatment. J Clin Invest. 2003; 111: 565-70. [ Links ]
54. Gibson WT, Farooqi S, Moreau M, Depaoli AM, Lawrence E, Trussell RA. Congenital leptin deficiency due to ho-mozygosity for the Δ133g mutation: Report of another case and evaluation of response to four years of leptin therapy. J Clin Endocnnol Metab. 2004; 89: 4821 -6. [ Links ]
55. Lustig RH, Hinds PS, Ringwald-Smith K, Christensen RK, Kaste S, Shreiber RE, et al. Octreotide therapy of pediatric hypothalamic obesity: A double-blind, placebo-controlled trial. J Clin Endocnnol Metab. 2003; 88: 2586-92. [ Links ]
56. Bays HE, Tighe AP, Sadovsky R, Davidson MH. Prescription omega-3 fatty acids and their lipid effects: physiologic mechanisms of action and clinical implications. Expert Rev Cardiovasc Then 2008; 6: 391-409. [ Links ]
57. Robinson LE, Buchholz AC, Mazurak VC. Inflammation, obesity, and fatty acid metabolism: influence of n-3 po-lyunsaturated fatty acids on factors contributing to metabolic syndrome. Appl Physiol Nutr Metab. 2007; 32: 1008-24. [ Links ]
58. Barre DE. The role of consumption of alpha-linolenic, eicosapentaenoic and docosahexaenoic acids in human metabolic syndrome and type 2 diabetes -a mini-review. J Oleo Sci. 2007; 56: 319-25. [ Links ]
59. Risérus LJ. Fatty acids and insulin sensitivity. Curr Opin Clin Nutr Metab Care. 2008; 11: 100-5. [ Links ]
60. Kratz M, Swarbrick MM, Callahan HS, Matthys CC, Havel PJ, Weigle DS. Effect of dietary n-3 polyunsaturated fatty acids on plasma total and high-molecular-weight adiponectin concentrations in overweight to moderately obese men and women. AmJ Clin Nutr. 2008; 87: 347-53. [ Links ]
61. Nelson TL, Stevens JR, Hickey MS. Adiponectin levels are reduced, independent of polymorphisms in the adiponectin gene, after supplementation with alpha-linolenic acid among healthy adults. Metabolism. 2007; 56: 1209-15. [ Links ]
62. FaintuchJ, Horie LM, Barbeiro HV, Barbeiro DF, Soriano FG, Ishida RK, et al. Systemic inflammation in morbidly obese subjects: response to oral supplementation with alpha-linolenic acid. Obes Surg. 2007; 17: 341-7. [ Links ]
63. Lohner S, Marosvolgyi T, Bums I, Schmidt J, Molnár D, Decsi T. Dietary supplementation of obese children with 1000 mg alpha-linolenic acid per day: a placebo-controlled double blind study. Orv Hetil. 2007; 148: 1499-503. [ Links ]
64. Kunesová M, Braunerová R, Hlavaty P, Tvrzická E, Stanková B, Skrha J, et al. The influence of n-3 polyunsaturated fatty acids and very low calorie diet during a short-term weight reducing regimen on weight loss and serum fatty acid composition in severely obese women. Physiol Res. 2006; 55: 63-72. [ Links ]
65. Méndez-Sánchez N, González V, Aguayo P, Sánchez JM, Tanimoto MA, Elizondo J, et al. Fish oil (n-3) polyunsaturated fatty acids beneficially affect biliary cholesterol nucleation time in obese women losing weight. J Nutr. 2001; 131: 2300-3. [ Links ]
66. Zaragosi LE, Wdziekonski B, Fontaine C, Villageois P, Peraldi P, Dani C. Effects of GSK3 inhibitors on in vitro expansion and differentiation of human adipose-derived stem cells into adipocytes. Curr Top Med Chem. 2008; 8: 205-30. [ Links ]
67. Mendieta-Zerón H, López M, Diéguez C. Gastrointestinal peptides controlling body weight homeostasis. Gen Comp Endocnnol. 2008; 155:481-95. [ Links ]
68. Heal DJ, Smith SL, Fisas A, Codony X, Buschmann H. Selective 5-HT6 receptor ligands: progress in the development of a novel pharmacological approach to the treatment of obesity and related metabolic disorders. Pharmacol Then 2008; 117: 207-31. [ Links ]
69. Bastarrachea R, Tejero E, Cai Guowen, Comuzzie AG. Farmacogenómica de la diabesidad: Corrigiendo las alteraciones glucolipometabólicas secundarias a un exceso de tejido adiposo. Rev Endocrinol Nutr. 2004; 12: 80-9. [ Links ]
70. Padwal R, Li SK, Lau DCW. Long-term pharmacotherapy for overweight and obesity: a systematic review and meta-analysis of randomized controlled trials. Int J Obes. 2003; 27: 1437-46. [ Links ]














