Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.62 no.1 México ene./feb. 2005
Caso clínico
Linfoma cutáneo angiocéntrico de células T que semeja hidroa vacciniforme
Angiocentric cutaneous lymphoma in a 14 year old female adolescent
Dr. Armando Quero–Hernández1, Dr. Luis M. Sánchez–Navarro2, Dra. Zoila Socorro–López3, Dr. Daniel Carrasco–Daza4
1 Área de Oncología Pediátrica,
2 Dermatología,
3 Anatomía Patológica, Hospital General Dr. Aurelio Valdivieso, Oaxaca;
4Anatomía Patológica, Instituto Nacional de Pediatría, México, D.F., México.
Solicitud de sobretiros:
Dr. Armando Quero Hernández,
Área de Oncología Pediátrica, Hospital General Dr. Aurelio Valdivieso, Secretaría de Salud del Estado de Oaxaca,
Av. Porfirio Díaz # 400, Col. Reforma,
C. P. 68000, Ciudad de Oaxaca, Oaxaca, México.
Fecha de recepción: 25–02–2004.
Fecha de aprobación: 08–12–2004.
Resumen
Introducción. Los linfomas cutáneos son procesos linfoproliferativos malignos de células B o T, con una variedad de manifestaciones clínicas, sin que exista enfermedad extracutánea al momento del diagnóstico. Existen reportes de casos de lesiones cutáneas previas, determinadas por fotosensibilidad, que se asocian a linfomas cutáneos. Se presenta el caso de un paciente femenino con diagnóstico de linfoma cutáneo angiocéntrico que semeja hidroa vacciniforme.
Caso clínico. Adolescente femenino de 14 años de edad, que ingresó al Hospital General Dr. Aurelio Valdivieso del Estado de Oaxaca en el mes de octubre de 2003. Cuadro actual: 8 meses previos a su ingreso con dermatosis en áreas expuestas al sol, caracterizadas por vesículas y pápulas, que evolucionaron a úlceras y necrosis en miembros torácicos y piernas, con hepatoesplenomegalia y edema centrofacial. La histopatología de la lesión reveló vasculitis angiocéntrica, angiodestructiva, con linfocitos atípicos y paniculitis. Se definió el diagnóstico de linfoma cutáneo angiocéntrico. Se instaló quimioterapia combinada con involución de su dermatosis y compromiso sistémico.
Conclusión. El presente caso cumple con criterios clínico e histopatológicos de linfoma cutáneo angiocéntrico, con adecuada respuesta a quimioterapia de combinación, sobre todo basada en antraciclinas.
Palabras clave. Hidroa vacciniforme; vasculitis angiocéntrica; linfoma cutáneo angiocéntrico.
Abstract
Introduction. The cutaneous lymphoma is a malignant lymphoproliferative process of B or T, cells with a variety of clinical manifestation without extracutaneous disease at the time of diagnosis. There are case reports in the literature which have associated prior cutaneous injuries, with cutaneous lymphoma as determined by photosensitization. The present case report is of a female patient with diagnosis of cutaneous angiocentric lymphoma which resembled hydroa vacciniform.
Case report. Female adolescent 14 year of age who was admitted to Hospital General Dr. Aurelio Valdivieso in the State of Oaxaca, Mexico. Eight months prior to hospital admission she presented dermatosis in areas exposed to the sun, characterized by vesicles, papules which evolved to ulcers and necrosis in arms and legs, she also presented with hepatosplenomegaly and facial edema. The histopatology of the lesions revealed angiodestructive, angiocentric vasculitis with atypical lymphocytes and paniculitis. The diagnosis of angiocentric cutaneous lymphoma was made. The patient was treated with combined chemotherapy with involution of her dermatosis and systemic findings.
Conclusion. The present case fulfills the histopathology and clinical criteria of an angiocentric cutaneous lymphoma, with suitable response to combined chemotherapy based on anthracyclines.
Key words. Hydroa vacciniforme; angiocentric vasculitis; angiocentric cutaneous lymphoma.
Introducción
Los linfomas cutáneos son procesos linfoproliferativos malignos –de linfocitos T o B– cuya manifestación clínica se caracteriza por una amplia variedad de lesiones cutáneas, sin existir enfermedad extracutánea en el momento del diagnóstico, con una historia natural de afección de ganglios linfáticos, infiltración visceral y sistémica.1
Los linfomas cutáneos en niños son raros. Los datos disponibles por lo general son de adultos, cuya incidencia es de 0.3/1 000 000.2 En ellos, la piel es la segunda localización de linfomas primarios extranodales. Siendo en 50% de los casos micosis fungoide, síndrome de Sezary, 25% linfomas T periféricos y 25% linfomas de células B.3,4
La distribución compartamental de linfocitos T en la piel se da preferentemente en epidermis, dermis papilar, plexo vascular superficial, y en la profundidad del tejido graso subcutáneo. Los linfocitos B se localizan en dermis media y profunda, plexo vascular profundo y tejido graso. Esta localización diferenciada de los subtipos linfocitarios dará carácter propio a las formas clínicas de los linfomas cutáneos. Las lesiones cutáneas se caracterizan por la evolución en diferentes etapas, iniciando con erupción macular, localizadas en zonas no expuestas al sol, y que pueden durar meses, después se agregan parches eccematosos, de superficie lisa, prácticamente son lesiones no palpables, y por último, la fase de tumor, detectándose lesiones nodulares debajo de la dermis superficial y úlceras.5
Existen varios mecanismos patogénicos para el desarrollo de linfomas cutáneos que incluyen translocaciones, reordenamientos o deleciones, alteraciones de los genes de supresión tumoral bcl2.6 Por la naturaleza inmunitaria de las células linfocitarias se cree que las exposiciones crónicas a sustancias químicas, pesticidas, etc., puedan predisponer al desarrollo de los linfomas cutáneos. La participación viral de los retrovirus es aún motivo de investigación.7
En los pacientes con sospecha de linfoma cutáneo debe confirmarse su diagnóstico mediante toma de biopsias de los sitios sospechosos, realizar estudios de inmunofenotipo, citogenética, establecer su etapa mediante el sistema de estadificación propuesto por el Cutaneous T–Cell Lymphoma Workshop que permitirá establecer las variables pronósticas.
Existen reportes de casos donde las lesiones cutáneas previas, sobre todo determinadas por fotosensibilidad, se asocian con linfomas cutáneos, o éstos aparecen después de un período de latencia que va de meses a años.8,9 Estas lesiones se caracterizan por enfermedad vesicular recurrente, con necrosis y escaras vacciniformes sobre áreas expuestas al sol, a nivel microscópico se describe necrosis epidérmica con formaciones vesiculares intraepidérmicas, definiendo a esta entidad como hidroa vacciniforme. Ruiz–Maldonado y col.10 definen una nueva entidad que se caracteriza por compartir algunas similitudes clínicas de la hidroa vacciniforme, pero que a diferencia de ésta, compromete el estado general del paciente, con afección extracutánea (hepatoesplenomegalia) y úlceras grandes, tanto en áreas expuestas al sol como en aquellas sin exposición, y en su casuística tres pacientes desarrollaron linfoma cutáneo.
El objetivo del presente trabajo es informar el caso de un paciente del sexo femenino con diagnóstico de linfoma de tipo angiocéntrico cutáneo, y su respuesta al manejo de quimioterapia combinada, que comparte características de la forma severa de la hidroa vacciniforme o de la paniculitis vasculítica cicatrizal edematosa.
Presentación del caso clínico
Se trata de paciente del sexo femenino de 14 años de edad, que procede de Tuxtepec, Oaxaca, México, quien ingresó al Hospital General Dr. Aurelio Valdivieso en el mes de octubre del año 2003. Con el antecedente heredofamiliar de un abuelo paterno que cursó con tuberculosis pulmonar. Proviene de medio socioeconómico bajo, convive en hacinamiento. No tiene antecedentes personales patológicos de importancia para su padecimiento actual.
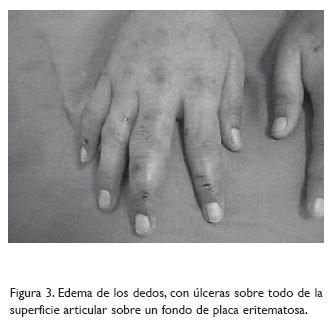
El cuadro actual lo inició ocho meses previos a su ingreso, con una lesión de tipo nodular localizada en antebrazo derecho, que de manera espontánea se resolvió, quedando una mancha de tipo hipocrómica. Cinco meses después aparecen en sitios expuestos al sol pápulas y vesículas sobre un fondo eritemato–violáceo, que evolucionaron a ulceración y necrosis de las partes afectadas, asociándose con edema de cara y ataque a su estado general, así como fiebre sin cuantificar y sin predominio de horario. A la exploración física: peso 38.5 kg, temperatura 37.8° C, frecuencia cardiaca 85 por minuto y frecuencia respiratoria de 22 por minuto. Pálida de piel y de las mucosas, edema de cara y manos, sobre todo palpebral bilateral dando el aspecto de "facies leonina" (Figs. 1, 2), cuello con ganglios menores de 1 cm, aislados, móviles, blandos, indoloros. Tórax de forma y tamaño normal. Glándulas mamarias: Tanner 3. En abdomen se palpó el hígado a 2 x 3 x 3 cm debajo de las líneas convencionales. Genitales: Tanner 3. En piel: dermatosis polimorfa diseminada a cara, miembros torácicos, nalgas, espalda, muslos y piernas, de predominio en superficies expuestas al sol, caracterizados por pápulas eritematosas, manchas purpúricas infiltradas, algunas con tendencia a la necrosis (Figs. 3, 4), otras sembradas por vesículas, que al romperse dejan úlceras regulares y cicatrices de tipo varioliforme y en sacabocado. Llama la atención úlcera de 4 cm de diámetro con mancha eritemato–purpúrica perilesional, localizada en región maleolar externa del tobillo izquierdo.



Resultados de laboratorio: biometría hemática completa con hemoglobina de 12.8 g/dL, hematócrito 39.2%, leucocitos 2 900/mm3, neutrófilos 75%, linfocitos 21%, monocitos 2%, plaquetas de 62 000/mm3. Las pruebas funcionales hepáticas: TGO 135 UI/L, TGP 109 UI/L, fosfatasa alcalina 1 602 U/L, proteínas totales 4.6 g/dL, albúmina 0.7 g/dL, globulina 3.9 g/dL. Hemocultivo negativo; urocultivo con 250 000 UFC/mm3 de Escherichia coli; cultivo de secreción de úlcera maleolar con Pseudomonas aeruginosa.
El perfil de anticuerpos antinucleares negativos (anti–DNA nativo, anti–músculo liso, anti–mitocondriales). Tomografía axial computada abdominal con aumento difuso de la glándula hepática, sin reforzamientos ni anormalidades estructurales, bazo aumentado de tamaño, de forma homogénea y sin reforzamientos con el contrastado.
Se realizó mapeo–biopsia y en los cortes histológicos se observaron fragmentos de piel con necrosis epidérmica multifocal y regeneración; espongiosis acentuada y exocitosis focal e irregular, con formación de microvesículas subepidérmicas, intraepidérmicas y epidermotropismo. La dermis papilar y reticular mostraba un infiltrado mononuclear compuesto por linfocitos atípicos con angiotropismo y angiodestrucción y necrosis isquémica de células tumorales (Figs. 5, 6 y 7).



Biopsias óseas sin datos de infiltración tumoral. En el estudio de inmunohistoquímica las células neoplásicas fueron positivas a CD3 (80%), CD 10 (60%), CD30 (80%), negativas a CD20, tdt, CD 15, ALK y CD56.
Integrándose el diagnóstico de linfoma cutáneo angiocéntrico de inmunofenotipo "T".
La paciente fue tratada con quimioterapia basada en: vincristina 1.5 mg/m2/día, doxorrubicina 50 mg/m2/día, ciclofosfamida 1 200 mg/m2/día, prednisona 100 mg/m2/días 1 a 5 en cursos de cada 21 días y esteroide tópico, así como diversos esquemas de antimicrobianos, ajustándose de acuerdo a los reportes de cultivos y su sensibilidad. Las lesiones cutáneas, al igual que el edema facial y de las extremidades, remitieron en el tercer curso de quimioterapia. A los nueve meses del diagnóstico y después de seis cursos del esquema de manejo, reingresó con pancitopenia periférica severa, fiebre y mal estado general, falleciendo a las 24 horas con datos de choque séptico. Cultivos de piel ulcerada, orina y sangre positivas a Pseudomonas sp. No se realizó autopsia.
Discusión
La piel es uno de los tejidos más amplios del organismo y una de sus principales funciones es la de ser una barrera protectora contra microorganismos invasores, además de tener en su compartimiento a células con funciones específicas en la respuesta inmunológica. Expuesta también a múltiples factores externos, tales como sustancias químicas, físicas, virales, etc., todos ellos con el potencial de desencadenar procesos mutacionales que pudieran sobreexpresar oncogenes, alteración de la apoptosis o bien cambios en los factores de regulación de la proliferación celular y dar lugar al desarrollo de una amplia variedad de neoplasias linfoides cutáneas.
El caso que aquí se informa, inicia con lesiones exclusivamente cutáneas, con un período de evolución relativamente corto, llegando a afectar 20% de la superficie corporal, caracterizado por dermatosis polimorfa, de predominio fotosensible y cuya evolución morfológica fue: pápulas, vesículas, manchas eritemato–purpúricas, necrosis, úlceras, cicatriz varioliforme, asociado a edema centro facial y de manos. Se integró el diagnóstico clínico e histopatológico de linfoma cutáneo primario de tipo angiocéntrico de células T y alteraciones microscópicas de hidroa vacciniforme de la que clínicamente es idéntica a la forma severa descrita e individualizada por Ruiz–Maldonado y col.10 como paniculitis vasculítica edematosa cicatrizal. Los casos aislados de la asociación de hidroa vacciniforme y linfoma cutáneo primario han señalado un período de latencia que va de meses a años para el desarrollo de neoplasia. En la paciente de este informe, las lesiones iniciaron ocho meses previos a su ingreso y se documentó la coexistencia de ambas alteraciones histopatológicas. No existe aún una respuesta para explicar esta asociación, se ha postulado el papel del virus Epstein–Barr en la patogenia de ambas entidades, Iwatsuki y col.11 documentaron la infección latente del virus Epstein–Barr con cambios infiltrativos angiocéntricos e histopatológicos de hidroa vacciniforme, relación que no se ha observado con las micosis fungoides o síndrome de Sézar y/o con otro tipo de linfoma cutáneo primario.
Igualmente existen otros reportes de casos en donde el aspecto clínico inicial fue de hidroa vacciniforme y años después presentaron alteraciones histopatológicas de linfoma cutáneo.12–14
Heo y col.15 reproducen artificialmente lesiones similares a hidroa vacciniforme al exponer a una niña coreana a radiaciones UVA y UVB en áreas expuestas, llamando la atención la detección serológica del virus Epstein–Barr, así como por hibridación un infiltrado en dermis de tipo mononuclear positivo para el mismo virus. Concluyen que es necesaria la fotoprotección para prevenir la progresión a procesos linfoproliferativos malignos, en donde un papel primordial aún no aclarado es la infección del virus Epstein–Barr.
Los linfomas cutáneos primarios representan un grupo heterogéneo de neoplasias de células B y T, con una amplia variabilidad de presentación clínica, cambios histopatológicos e inmunofenotípicos, así como respuesta diferenciada al tratamiento y pronóstico. El linfoma angiocéntrico grado III, conocido también como linfoma nasal/tipo nasal de células T/NK de acuerdo con la clasificación de la Organización Mundial de la Salud y que se corresponde con el linfoma cutáneo primario de células T grandes CD 30, categorizado como una variedad agresiva por la clasificación de linfomas primarios cutáneos de la EORTC.16,17 Morfológicamente se observa un infiltrado de linfocitos pequeños, número variable de linfocitos atípicos e inmunoblastos, células plasmáticas, eosinófilos e histiocitos. Un aspecto característico es la infiltración perivascular por linfocitos y la oclusión de la luz vascular, acompañándose con necrosis isquémica de las células tumorales.18 Su curso clínico parece depender de la proporción de células grandes y puede ser indolente o agresivo. El pronóstico de los pacientes con linfoma cutáneo va a depender del tipo de lesión así como de la extensión de la piel afectada. Se reconocen como factores pronósticos adversos: una afección cutánea mayor de 10%, los que presentan la etapa de tumor y se asocie con eritrodermia, placas o parches. En el esquema de manejo en las etapas localizadas se han empleado desde radioterapia localizada, o bien extensa, combinadas con quimioterapia o bien estas últimas solas, con supervivencia libre de enfermedad a cinco años de 65 a 85% y aquellos casos en que la piel se ha comprometido en más de 10% la frecuencia de supervivencia a dos años es de 40%.
En el esquema de quimioterapia su efectividad se ha observado cuando en ésta se incluyen antraciclinas.19–21
El presente caso se piensa cumple con los criterios clínicos e histopatológicos para considerarlo como un linfoma cutáneo angiocéntrico de células T (paniculitis vasculítica edematosa cicatrizal). Se considera, al igual que Magaña y col.,22 corresponde en su clasificación al espectro de linfomas angiocéntricos, conocidos previamente con diferentes nombres; hidroalike, hidro vacciniforme maligno, paniculitis edematosa cicatrizal, hidroa asociado a malignidad.
Llama la atención el tiempo relativamente corto (ocho meses) desde el inicio de su padecimiento para definirse como un linfoma cutáneo, la respuesta al tercer curso de quimioterapia y que fallece a los nueve meses de seguimiento por proceso infeccioso sistémico por P. aeruginosa. Por lo que se contribuye a la literatura con uno de los pocos casos que presentan tal situación.
Referencias
1. Wilson L, Barry M, Edelson R, Heald P. Lymphoma of the skin. En: Devita V, Hellman S, Rosenberg S, editores. Cancer. Principles and practice of oncology. 5a ed. USA: Lippincott Williams and Wilkins; 1997. p. 2220–33. [ Links ]
2. Harris NL, Jaffe ES, Stein H.A revised European–American classification of lymphoid neoplasm's: a proposal from the International Lymphoma Study Group. Blood. 1994; 84: 1361–92. [ Links ]
3. Carbia S, Hochman A, Deicas I. Linfomas cutáneos ulcerados, diez años de experiencia. Medicina. 2000; 60: 565–9. [ Links ]
4. Connors JM, His ED, Foss FM. Lymphoma of the skin. Hematology. 2002; 263–82. [ Links ]
5. Lever WF, Schaumburg LG. Histopathology of the skin. Philadelphia: JB Lippincott; 1990. p. 819. [ Links ]
6. Yunis J, Mayer M,Amesen M. bcl–2 and other genomic alterations in the prognosis of large–cell lymphoma. N Engl J Med. 1989; 320: 1047. [ Links ]
7. Wnag CY, Snow JL. Lymphoma associated with human immunodeficiency virus infection. Mayo Clin Proceed. 1995; 70:665. [ Links ]
8. Oono T, Arata J, Masuda T, Ohtsuki Y. Coexistence of Hidroa vacciniforme and malignant lymphoma. Arch Dermatol. 1986; 122: 1306–9. [ Links ]
9. Ibarra–Durán G, Rodríguez–Jurado R, Rodríguez–Moguel L. Linfoma T cutáneo angiocéntrico en una niña con hidroa vacciniforme. Rev Mex Dermatol. 1991; 5: 344–8. [ Links ]
10. Ruiz–Maldonado R, Millán–Parrilla F, Orozco–Covarrubias M. Edematous, scarring vasculitic panniculitis: a new multisystemic disease with malignant potential. J Am Acad Dermatol. 1995; 32: 37–44. [ Links ]
11. Iwatsuki K, Ohtsuka M, Harada H. Clinicopathologic manifestations of Epstein–Barr virus–associated cutaneous lymphoproliferative disorders. Arch Dermatol. 1997; 133: 1081–6. [ Links ]
12. Cho KH, Kim CW, Heo DS. Epstein–Barr virus–associated peripheral T cell lymphoma in adults with hydroa vacciniforme–like lesions. Clin Exp Dermatol. 2001; 26: 242–7. [ Links ]
13. Tabata N,Aiba S, Ichinohazama R. Hydroa vacciniforme–like lymphomatoid papulosis in a Japanes child: a new subset. J Am Dermatol. 1995; 32: 378–81. [ Links ]
14. Barrionuevo C, Anderson B, Zevallos–Giampetri E. Hydroalike cutaneous T–cell lymphoma: a clinicopathologic and molecular genetic study of 16 pediatric cases from Peru. App Immunohistochem Mol Morphol. 2002; 10:7–14. [ Links ]
15. Heo EP, Park SH, Kim TH. Artificial reproduction of atypical hydroa vacciniforme caused by latent Epstein–Barr virus infection. International J Dermatol. 2003; 42:476–9. [ Links ]
16. Willemze R, Kerl W, Sterry E. EORTC Classification for primary cutaneous lymphoma: a proposal from the cutaneous study group of the European Organization for Research and Treatment of Cancer. Blood. 1997; 1: 354–71. [ Links ]
17. Fink–PR, Zenahlik P, Back B, Smolle J, Kerl H, Cerroni L. Primary cutaneous lymphomas: applicability of current classification schemes (European Organization for Research and Treatment of Cancer, World Heath Organization) based on clinicopathology features observed in a large group of patients. Blood. 2002; 99: 800–5. [ Links ]
18. Lipford E, Margolich J, Fauci A. Angiocentric immunoproliferative lesions: a clinicopathology spectrum of post–thymic T cell proliferations. Blood. 1985; 5: 1674. [ Links ]
19. Skarin A, Dorfman D. Non Hodkgin's lymphoma: current classification and management. Cancer JC. 1997; 47: 351–72. [ Links ]
20. Hoppe–R.The role of radiation therapy in the management of the non–Hodgkin's lymphomas. Cancer (Abstracts). 1985; [ Links ]
21. Glick J, Kim K, Earle J. An ECOG randomized phase III trial of CHOP vs CHOP+ radiotherapy for intermediate grade early stage non–Hodgkin's lymphoma. Proc Am Soc Clin Oncol (Abstracts). 1995. [ Links ]
22. Magaña M, Sanguenza P, Gil–Beristain J, Sánchez–Sosa S. Angiocentric cutaneous T–cell lymphoma of childhood (hydroalike lymphoma): a distinctive type of cutaneous T–cell lymphoma. J Am Acad Dermatol. 1998; 38: 574–9. [ Links ]














