Introducción
La estimulación permanente mediante dispositivos puede inducir disincronía eléctrica y mecánica al hacer que el ventrículo derecho (VD) se contraiga antes que el izquierdo (VI) (disincronía interventricular) y que el tabique interventricular lo haga antes que las paredes laterales (disincronía intraventricular)1. En términos históricos, se han descrito ya episodios clínicos adversos atribuidos a la estimulación del VD en pacientes con disfunción del nódulo sinusal, como tasas altas de insuficiencia cardíaca (IC) congestiva, fibrilación auricular, dilatación del VI y un incremento de la mortalidad2.
La estimulación apical del VD ocasiona una alteración del patrón de activación del VI, similar al bloqueo de rama izquierda, y sobreviene una conducción eléctrica que inicia en el VD, activa al tabique interventricular de forma anómala (de derecha a izquierda) y da lugar al final a un notorio retraso de la activación de la pared lateral del VI, con la consiguiente prolongación de la duración del QRS3, lo que provoca una contracción ventricular ineficiente con asincronía y pérdida del trabajo miocárdico4.
Tayal, et al. describieron un serie de 27,704 pacientes con un incremento significativo del riesgo de 10% para el desarrollo de IC en el transcurso de dos años luego del implante, una cifra similar a la de estudios previos2. Además, existió un notorio mayor riesgo entre el primer y el sexto meses de seguimiento; los pacientes de sexo masculino, el infarto de miocardio previo y la insuficiencia renal crónica se relacionaron con mayor riesgo de desarrollar IC.
Otros estudios han mostrado un deterioro de la función sistólica determinado por la caída de la FEVI en promedio de 10% en los primeros días tras la implantación del dispositivo5. Por esta razón se considera que es necesario un seguimiento clínico y con ecocardiografía de estos pacientes, en especial en los primeros seis meses, lapso en el cual es probable identificar a la gran mayoría de sujetos con IC después del implante de un catéter6. Aquéllos con antecedente de infarto de miocardio tuvieron mayor disminución de la FEVI7, algo tal vez atribuido a la fibrosis miocárdica subyacente, mayor asincronía ventricular y una mayor anchura del QRS, de tal modo que el VI es más vulnerable al efecto perjudicial de la estimulación artificial8. Algo semejante se ha demostrado en portadores de enfermedad renal crónica, en la cual el mecanismo puede ser efecto de una cantidad considerable de fibrosis miocárdica9.
El tratamiento de resincronización cardíaca (TRC) ha demostrado beneficio en los pacientes que tienen indicación de estimulación permanente con IC y deterioro grave de la función sistólica (FEVI < 35%)10. Las guías recientes de la European Society of Cardiology han incorporado esta premisa11; sin embargo, esto no es igual para pacientes con FEVI normal, en quienes existe evidencia limitada12, aunque podría plantearse esta conducta en enfermos con mayor riesgo de desarrollar IC, por ejemplo los individuos con antecedente de infarto agudo de miocardio y enfermedad renal crónica6.
Se ha observado un deterioro de la FEVI de 12.3% en una cohorte de pacientes que recibieron un marcapasos definitivo con previa función sistólica conservada del VI durante el seguimiento a 4.3 ± 3.9 años13, definido como una reducción menor del 40% o una disminución mayor del 10% de la FEVI previa. En un análisis multivariado de esta cohorte, un PEVD ≥ 20% se relacionó en sumo grado con deterioro de la FEVI. Se estableció además que aquéllos con hipertrofia ventricular izquierda y una tasa de estimulación mayor de 40% durante los últimos seis meses fueron parámetros relacionados con la presencia de mayor asincronía mecánica del VI14.
Como se ha mencionado, la FEVI es determinante para la indicación de TRC. Aunque el método biplano es el más robusto para determinar los volúmenes y la fracción de expulsión mediante la ETT2D, su variabilidad interobservador e intraobservador puede ser alta, con diferencias notificadas hasta de 18%15. Los volúmenes ventriculares por esta técnica se han subestimado en comparación con la norma de referencia, esto es, la resonancia magnética cardíaca16. Cuando se realizó la cuantificación de la FEVI respecto de la ETT2D y la resonancia magnética cardíaca se reconocieron discrepancias en cuanto a la indicación de TRC en 28% de los pacientes usando el punto de corte de la guía actual. La ecocardiografía con contraste puede reducir la variabilidad intraobservador e interobservador para el cálculo de los volúmenes y la fracción de expulsión17. Con base en estos hallazgos, el punto de corte para la selección de pacientes que se benefician de TRC depende de la herramienta de imagen utilizada, sin poder extrapolar un solo punto de corte para todas las herramientas de cálculo. Pese a ello, algún subgrupo de pacientes con fracción de expulsión de 30 a 40% podría incorporarse en las guías futuras18. Los individuos con FEVI mayor del punto de corte habitual, pero con un verdadero bloqueo completo de la rama izquierda, podrían beneficiarse de una TRC19.
Synchromax para el estudio de la asincronía eléctrica
La derivación DII del ECG de superficie sintetiza la actividad septal, dirección y velocidad a través de él, mientras que la derivación V6 registra la activación de la pared libre del VI. Por esa razón, en ausencia de trastornos de la conducción, la DII es positiva y con una duración normal, una activación desde la base del SIV hasta la punta con velocidad normal y, por otro lado, V6 es casi idéntica, positiva y con igual duración y volumen espacial porque sigue el mismo patrón de activación. Mediante un cálculo matemático, el equipo toma las diferentes variables: dirección del impulso (de la base al vértice o viceversa), duración del QRS, volumen de ambas curvas, tiempo de máxima activación de cada cavidad y demoras en la propagación parietal, y luego realiza un índice de sincronía de 00 a 1.0 (00 es la sincronía perfecta y 1.00 la disincronía completa20).
A simple vista es posible observar algunos detalles imposibles de analizar en el ECG de superficie, entre ellos el sentido de la activación, de la base a la punta o viceversa (QRS positivo o negativo, respectivamente), la simultaneidad en la activación, y el retraso de la propagación (QRS ancho). Por ejemplo, en ritmo sinusal con QRS normal ambas curvas son simétricas, simultáneas angostas y con el mismo volumen (Fig. 1).

Figura 1 Secuencia de ritmo sinusal procesada por Synchromax. Procesamiento de la señal comparada de la derivación DII con la V6, con índice de disincronía normal (0.06).
La anchura del QRS por sí sola no parece ser un marcador adecuado para diagnosticar disincronía21 y, si se considera la evidencia de que la dispersión morfológica de la despolarización ventricular es un marcador mucho más eficiente (como lo demuestran Bonomini, et al. con el concepto de varianza espacial del QRS22,23), Synchromax es una herramienta óptima para estos fines, dado que de modo no invasivo e instantáneo, y sin procedimientos dependientes del operador, puede diagnosticar con criterios morfológicos (y no sólo espaciales) la disincronía eléctrica, además de que cuantifica la importancia de la disincronía eléctrica, tanto en el momento del implante como durante el seguimiento.
La estimulación desde el vértice del ventrículo derecho semeja un bloqueo de rama izquierda del haz de His: se pierden los vectores iniciales septales y el QRS se torna ancho y mellado; el eje eléctrico se desvía hacia la izquierda; la pared lateral se activa tardíamente y se produce disincronía electromecánica (Fig. 2)24 con la consecuente caída de la FEVI y la posible aparición de insuficiencia mitral, que reduce aún más la fracción de expulsión anterógrada19.

Figura 2 A: Comparación de las derivaciones DII y V6 tomadas con Synchromax en un paciente con ritmo estimulado por marcapaso en el ventrículo derecho, tipo implantado apical. La activación del ventrículo derecho (VD) antecede a la del ventrículo izquierdo (VI) y el retardo del VI para máximo voltaje es de 29 milisegundos (ms); toda la actividad eléctrica ventricular toma 154 ms. B: Valores de corte para disincronía (trazos de Synchromax). En números verdes, de arriba abajo, dos casos de ECG normal y, al final, un caso de bloqueo de rama derecha (0.38). Al centro, en números naranjas, pacientes con bloqueo de rama izquierda (0.41) y hemibloqueo anterior izquierdo (0.52, 0.66). A la derecha, con números rojos, de arriba abajo, pacientes con hemibloqueo anterior izquierdo (0.84), marcapaso en la punta del ventrículo derecho (0.97) y bloqueo avanzado de rama izquierda (1.0)22.
Cuando se trata de pacientes con dispositivos permanentes, que se encuentran crónicamente estimulados, y que estudió el sistema Synchromax, se ha encontrado que cerca del 72% de los enfermos alteró su asincronía eléctrica y un 54% mostró notable asincronía del VI (ID > 0.7)24.
Estudio de la asincronía mecánica del VI mediante ecocardiografía
La ecocardiografía y en particular las técnicas de Doppler tisular codificado en color son los métodos utilizados de forma más amplia para este fin, ya que poseen una alta resolución temporal y permiten el análisis de la motilidad segmentaria de una manera sencilla. No obstante, la asincronía mecánica ventricular analizada mediante Doppler tisular se basa en la motilidad ventricular longitudinal en una dimensión única y tiene como limitación principal la dependencia del ángulo de incidencia del haz de ultrasonido (Fig. 3A)25.
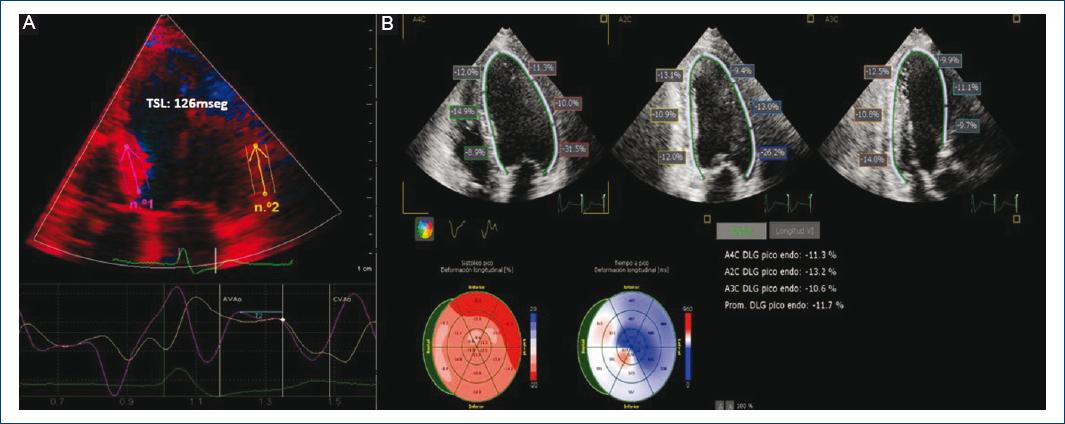
Figura 3 Análisis por ecocardiografía de la asincronía mecánica del VI en paciente con marcapasos permanente. A: Diferencia en tiempo septal-lateral (TSL) obtenida por Doppler tisular de 126 ms; se muestran n1 (línea púrpura) con activación septal y n2 (línea amarilla) con activación lateral del VI. B: Imágenes de deformación miocárdica longitudinal del VI obtenidas desde las vistas de cuatro, dos y tres cámaras, respectivamente. C: Esquema ojo de buey sobre deformación miocárdica longitudinal y tiempo al punto máximo sistólico de activación de todos los segmentos; se observan en azul las zonas con mayor retraso.
Las imágenes de deformación (strain) o el análisis de deformación con ecocardiografía emplean imágenes Doppler de tejido o ecocardiografía de seguimiento de pecas (Fig. 3B). Este último método es menos dependiente del ángulo y cubre toda la pared ventricular, en contraste con la imagen Doppler tisular, y por tanto es más confiable para la detección de la activación de segmentos retrasados (Fig. 3C). El retraso de la pared septal y lateral se obtiene con imágenes de velocidad Doppler tisular, calculada por la diferencia de tiempo entre el punto máximo de velocidad (Doppler) o la contracción (Doppler o seguimiento de pecas) de la pared basal septal y lateral19.
Valor agregado de la ecocardiografía tridimensional
En fecha reciente, la ecocardiografía tridimensional transtorácica (E3DTR) en tiempo real ha demostrado que puede proveer el análisis del VI mediante una única adquisición de forma completa y simultánea. La evaluación simultánea del cambio sistólico de múltiples regiones de un volumen obtenido del VI y el cálculo del índice de asincronía sistólica (IAS) permitirían integrar información de una forma más fidedigna en comparación con otros métodos convencionales de la ecocardiografía bidimensional26.
Macron, et al.27 confirmaron que la E3DTR es una técnica simple, reproducible y de rápida evaluación, y hace posible además determinar los volúmenes ventriculares en telediástole y telesístole, el volumen sistólico y la fracción de expulsión del VI, además de cuantificar la asincronía mecánica ventricular respecto de la resonancia cardíaca28,29. En una serie de 35 pacientes con estimulación apical permanente se observó una disminución de 4.1% de la fracción de expulsión volumétrica, además de un significativo retraso de la activación de las paredes septal y posterior a nivel medioventricular, y reveló un IAS de 7 ± 4% vs. 5.3 ± 2.1% en individuos sin estimulación apical30.
La serie de un estudio de 93 pacientes que recibieron estimulación permanente del VD evaluados por ecocardiografía tridimensional mostró que el 49% de éstos tuvo parámetros de asincronía por E3DTR, toda vez que se compararon con 93 controles normales, en los que el valor de referencia a partir del cual existió asincronía mecánica ventricular se determinó como una desviación estándar del tiempo al mínimo volumen regional de los 16 segmentos ventriculares (Tmvr-16S) mayor que 16 ms, correspondiente al tiempo que difiere de los controles normales en más de 2 desviaciones estándar. Estos pacientes con asincronía mecánica ventricular izquierda determinada a través de esta técnica registraron una menor fracción de expulsión y un mayor volumen al final de la diástole en comparación con los controles normales. Se estableció además que los enfermos con hipertrofia ventricular izquierda y una tasa de estimulación mayor de 40% durante los últimos seis meses fueron parámetros relacionados con la presencia de mayor asincronía mecánica del VI31.
Por lo regular, la duración del ancho del QRS ha sido el parámetro de elección para diferenciar a los pacientes que se benefician de una TRC, sin perder de vista que el aumento de la duración del QRS es una expresión de mayor asincronía eléctrica ventricular. Sin embargo, hasta la fecha no se dispone de un método cuantitativo de responder esta pregunta. En la actualidad, el nuevo sistema no invasivo Synchromax ha permitido la cuantificación del grado de asincronía ventricular en una escala de 0 a 1 en distintos escenarios clínicos, incluidos los pacientes con estimulación apical. De manera adicional, hasta la fecha no se han correlacionado estos hallazgos con los datos de la asincronía mecánica resultante de estos pacientes. La ecocardiografía ha demostrado ser útil en sus distintas modalidades para la cuantificación de este fenómeno. Si se considera que la resincronización es una alternativa terapéutica para mejorar la función ventricular en individuos con insuficiencia cardíaca, y que a su vez la indicación debe ser precisa para obtener el mejor resultado, es importante detectar la alteración de la sincronía mecánica. El mero hallazgo de asincronía eléctrica parece no confirmar la existencia de asincronía mecánica y es necesario obtener información de ambas alteraciones para definir conductas que hagan posible modificar las decisiones clínicas. El avance de la tecnología ofrece en la actualidad herramientas más exactas para estos estudios, como el Syncromax, para estudiar la actividad eléctrica y la ecocardiografía en sus distintas modalidades y analizar la actividad mecánica. No existen hoy día estudios que analicen la correlación existente entre el estudio de la actividad eléctrica con esa técnica y el de la mecánica con la referida al utilizar ultrasonido; se requieren otros estudios de investigación que determinen si existe o no un vínculo definido entre las alteraciones eléctricas y las mecánicas (Fig. 4).

Figura 4 Estudio de la asincronía ventricular izquierda en paciente con marcapasos permanente con deterioro de la función sistólica unos meses después del implante admitido por cuadro de insuficiencia cardíaca. A: Adquisición volumétrica tridimensional del VI y cálculo de volúmenes ventriculares (volumen telediastólico: VTd de 149 ml; volumen telesistólico: VTs de 88 ml) y fracción de expulsión tridimensional (FEVI 3D de 40%). B: Cálculo de la asincronía mecánica del VI mediante el índice de asincronía sistólica (IAS de 4.4%) y la dispersión del tiempo al punto máximo de los 16 segmentos del VI (Tmvr-16S de 42 ms). C: Cálculo de la asincronía eléctrica mediante sistema no invasivo Synchromax con cálculo de un índice de asincronía de 1 (gravemente asincrónico).
Conclusiones
El estudio de la asincronía eléctrica y mecánica como resultado de la estimulación apical permanente del VD puede ocasionar deterioro de la función sistólica del VI y la aparición de insuficiencia cardíaca. La detección y estudio oportunos de esta alteración son cruciales para identificar a los pacientes que se benefician de una transición a un tratamiento de resincronización cardíaca. El cálculo de la asincronía eléctrica resultante de la cuantificación mediante el sistema Synchromax y la asincronía mecánica como consecuencia de ésta estudiada con la ecocardiografía en sus distintas modalidades son técnicas que facilitarían tomar decisiones clínicas. A pesar de ello, se requieren estudios de cohorte de pacientes que posibiliten establecer con precisión la presencia de ambos fenómenos y a la vez determinar los puntos de corte a partir de lo cual un grado de asincronía eléctrica produzca asincronía mecánica del VI.











 nueva página del texto (beta)
nueva página del texto (beta)


