Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Archivos de cardiología de México
versão On-line ISSN 1665-1731versão impressa ISSN 1405-9940
Arch. Cardiol. Méx. vol.79 no.2 Ciudad de México Abr./Jun. 2009
Imágenes en cardiología
Aneurisma de aorta torácica por úlcera aterosclerótica penetrante: tratamiento endovascular, híbrido o cirugía. Revisión
Penetrating atherosclerotic ulcer of the thoracic aorta: endovascular treatment, hybrid or surgery. A review
Magali Herrera–Gomar,1* Marco Antonio Alcántara–Meléndez,1 Catalina Lomelí–Estrada,2 Celso Mendoza–González,2 Carlos Alberto Aguirre–Molina,1 José Antonio Lorenzo–Negrete,5 Eric Kimura–Hayama,3 Martín Rosas–Peralta,4 y Fause Attie–Cury6
1 Residente de tercer año de Cardiología. Instituto Nacional de Cardiología Ignacio Chávez (INCICh). México, D.F. México.
2 Médico adscrito, Cardiología adultos, INCICh.
3 Jefe del Departamento de Tomografía, INCICh.
4 Jefe del Servicio, Cardiología adultos, INCICh.
5 Jefe del departamento, Cardiología adultos, INCICh.
6 Director del Instituto Nacional de Cardiología.
* Autor para correspondencia:
Magali Herrera Gomar.
Instituto Nacional de Cardiología Ignacio Chávez.
Juan Badiano Núm. 1, Col. Sección XVI, Delegación Tlalpan,
14080 México, D.F. México.
Correo electrónico: magalihg@yahoo.com.
Recibido el 13 de mayo de 2008.
Aceptado el 28 de enero de 2009.
Resumen
Los aneurismas de aorta pueden acompañarse de síndromes aórticos agudos (SAA) que cursan con debilitamiento de la capa media, lo cual condiciona un riesgo de ruptura aórtica, con alta morbilidad y mortalidad. La úlcera penetrante constituye 5% de los SAA y resulta de una progresiva erosión de una placa ateromatosa que penetra la lámina elástica interna y permite la formación de un hematoma en la media de la pared aórtica. El tratamiento endovascular es una alternativa al tratamiento quirúrgico en los SAA que ha demostrado una adecuada tasa de éxito; sin embargo, existe en la actualidad otra modalidad que se conoce como tratamiento híbrido (quirúrgico y endovascular) que parece estar dando adecuados resultados. El caso que analizamos a continuación es el de un paciente que tuvo una úlcera penetrante. El hematoma resultante generó un aneurisma contenido con riesgo de ruptura. Además, en este estudio comentaremos las opciones en el tratamiento de estos pacientes.
Palabras clave: Aneurisma de aorta torácica; Síndromes aórticos agudos; Úlcera aórtica penetrada; Tratamiento endovascular; Tratamiento híbrido; Cirugía; México.
Abstract
The aortic aneurysm is part of the acute aortic syndromes (AAS). Aortic aneurysms have a weakened tunica media. Acute aneurysm expansion may herald rupture with high morbility and mortality. Five percent of AAS are diagnosed as pentetrating atherosclerotic ulcer which is an ulceration of an atherosclerotic lesion of the aorta that penetrates the internal elastic lamina and allows hematoma formation within the tunica media of the aortic wall. Endovascular treatment is an alternative to surgery and has provided an adequate rate of successful repair.
There is another type of treatment which combines surgery and endovascular repair (the hybrid open–endovascular repair) which provides adequate results. The afford mention case is about a patient with a penetrating atherosclerotic ulcer. The hematoma that results from this ulcer extends and self–contains the aneurysm, with a high risk of rupture. We will also describe the aneurysm treatment options.
Key words: Thoracic aortic aneurysm; Acute aortic syndromes; Penetrating atherosclerotic ulcer; Endovascular treatment; Hybrid open endovascular repair, surgery; Mexico.
Caso clínico
Hombre de 59 años de edad, con antecedente de tabaquismo e hipertensión arterial sistémica de reciente diagnóstico. Dos meses antes refirió dolor en tórax posterior, irradiado a tórax anterior, intensidad 8/10, e irradiado a brazo izquierdo, de una hora y media de duración que mejoró discretamente con la administración de analgésicos. Se inició tratamiento con antinflamatorios y antibióticos, sin mejoría de la sintomatología. Acudió con médico otorrinolaringólogo, quien realizó laringoscopia, evidenciando parálisis de la cuerda vocal izquierda, por lo que le ordenó tomografía de tórax (TAC) que mostró placas de ateroma en paredes de la aorta, con aneurisma que se origina adyacente al inicio de la arteria innominada, y que se extiende a arco aórtico, involucrando el origen de la carótida común y la subclavia izquierda, con trombo mural a nivel del arco aórtico.
El diámetro máximo del aneurisma es de 90.7 × 84.8 mm. Se observa, además, compresión del nervio recurrente laríngeo, placas de ateroma calcificadas en el trayecto de las arterias coronarias, sobre todo en la descendente anterior (DA), bulas en ápices de ambos pulmones y mínimos cambios fibrocicatriciales.
El paciente fue referido al Instituto Nacional de Cardiología Ignacio Chávez (INCICh) en donde se le ingresó con descontrol hipertensivo, y se manejó durante cuatro días con antihipertensivo intravenoso; se continuó su estudio en el tercer piso de hospitalización.
A la exploración física llamó la atención la presencia de un levantamiento del segundo espacio intercostal izquierdo a nivel de la línea media clavicular, y que se correspondía con el latido cardiaco. En el área precordial se observaron levantamiento paraesternal izquierdo sistólico sostenido y choque del ápex apenas palpable en el sexto espacio intercostal izquierdo a nivel de la línea axilar media. Ruidos cardiacos rítmicos; el primero, de características normales y el segundo, intenso. En mesogastrio había masa pulsátil, palpable, que invadía flanco izquierdo. No se palpó hepatomegalia; las extremidades eran eutróficas, normorreflécticas, con fuerza muscular adecuada y simétrica.
Sus estudios de laboratorio mostraron Hb de13.5 mg/dL; plaquetas, 238 000; leucocitos, 6 800; glucosa, 100; BUN, 11; Cr, 0.9; Na, 137; K, 3.6; y Cl, 103.
Los Rx de tórax, tomados con equipo portátil, evidenciaron tejidos blandos, óseo y pulmonar aparentemente sin alteraciones; la silueta cardiaca estaba respetada, con ensanchamiento mediastinal secundario a gran dilatación aneurismática del cayado aórtico (Figura 1).

El ECG mostró ritmo sinusal, FC 73 latidos por min; aQRS 60°; transición de la onda R en V3; hipertrofia del ventrículo izquierdo; ondas T acuminadas de V3–V6, sugestivas de sobrecarga sistólica (Figura 2).

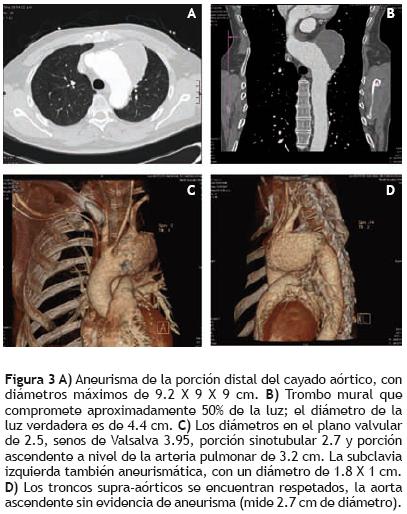
Se realizó angiotomografía de aorta, la que demostró la presencia de un aneurisma de la porción distal del cayado aórtico, con diámetros máximos de 9.2 X 9 X 9 cm (Figura 3A), con trombo mural que compromete aproximadamente 50% de la luz. El diámetro de la luz verdadera es de 4.4 cm2 (Figura 3B). Los diámetros en el plano valvular de 2.5, senos de Valsalva 3.95, porción sinotubular 2.7 y porción ascendente a nivel de la arteria pulmonar de 3.2 cm. La subclavia izquierda también es aneurismática, con un diámetro de 1.8 X 1 cm (Figura 3C). Los troncos supraaórticos se encuentran respetados; la aorta ascendente, sin evidencia de aneurisma, tiene 2.7 cm de diámetro (Figura 3D). Presenta enfermedad ateroesclerótica de la totalidad de la aorta y se observan placas de ateroma en DA proximal y medial, así como en arteria circunfleja proximal (sin embargo, no se realizó protocolo para visualizar estas arterias).
En parénquima pulmonar se aprecian espacios enfisematosos centrolobulillares aislados, apicales, bilaterales. Se solicitó, además, una angiorresonancia aórtica. En la angiotomografía de aorta abdominal se encontró un aneurisma infrarrenal de 4.5 × 4 cm con trombo en su interior (Figura 4).

El caso se discutió en la sesión médico–quirúrgica del piso y se decidió hacer corrección quirúrgica del aneurisma en un solo tiempo. Se comentó a los familiares el gran riesgo que el procedimiento tenía. La cirugía duró ocho horas y al salir a la terapia posquirúrgica tuvo como complicación daño neurológico extenso, confirmado por electroencefalograma. El paciente falleció luego de permanecer cuatro días en posoperatorio temprano.
Discusión
Aneurisma aórtico se refiere a la dilatación patológica de la luz aórtica normal que afecta a uno o varios segmentos. Para ser aneurisma debe estar localizado y encontrarse de forma permanente en la aorta, con un diámetro de al menos 1.5 veces el normal esperado para ese segmento aórtico. Los aneurismas suelen describirse por su localización, tamaño, aspecto morfológico y origen. La forma de un aneurisma puede ser fusiforme, la más frecuente, o sacular. Un aneurisma fusiforme tiene una dilatación simétrica que afecta a toda la circunferencia de la pared aórtica. Los aneurismas saculares tienen una dilatación más localizada, que parece una evaginación de una sola porción de la pared aórtica, como sucedió en este paciente.
Los aneurismas verdaderos de la aorta, según su localización, pueden ser: a) del seno de Valsalva; b) de la aorta ascendente; c) del cayado aórtico; d) de la aorta descendente; e) abdominal, y f) toracoabdominal.1
Este caso es un aneurisma toracoabdominal de origen aterosclerótico. Cabe mencionar que la presencia de un aneurisma aórtico puede ser un marcador de enfermedad aórtica más difusa. Hasta 13% de los pacientes a quienes se les diagnostica un aneurisma de aorta tienen múltiples aneurismas, de manera que 25% a 28% de quienes tienen aneurismas torácicos también presentan aneurismas abdominales. Por esta razón al paciente al que se le descubre un aneurisma aórtico se le debe estudiar toda la aorta en busca de otros aneurismas.2
Entre los factores de riesgo asociados a la formación de aneurismas se encuentran tabaquismo, edad, hipertensión arterial, hiperlipidemia y aterosclerosis.3 El sexo y la herencia genética también influyen en la formación de aneurismas; los hombres tienen 10 veces más riesgo de tener aneurismas aórticos, comparados con las mujeres, y éstas tienen un mayor riesgo de presentar ruptura del aneurisma.4
La pared de la aorta está compuesta por elastina y colágeno, la degradación de estas proteínas estructurales favorece el ensanchamiento de la aorta, con incremento en la tensión de la pared y la formación del aneurisma.5 La aterosclerosis se ha considerado clásicamente la causa subyacente del aneurisma de la aorta abdominal; la aorta abdominal infrarrenal está más afectada por el proceso aterosclerótico y por ello es la zona más común de formación de aneurismas.
Uno de los mecanismos que explica el origen aterosclerótico de las enfermedades de la aorta es la úlcera aórtica penetrante, que en este caso se observa en algunas proyecciones de la tomografía. La úlcera se ubica en la lámina elástica interna formando un hematoma en la capa media. Su evolución patogénica comprende la posibilidad de aneurismas aórticos saculares o fusiformes, o la producción de seudoaneurismas que llegan en el 10% a la ruptura aórtica. No es frecuente que puedan producir disecciones.6
A largo plazo, una úlcera aterosclerótica penetrante causa dilatación aórtica debido al adelgazamiento local de la media. Harris y colaboradores reportaron que más de 50% de los 18 pacientes que siguieron durante 1 a 7 años desarrollaron aneurismas aórticos. El diámetro del segmento aórtico involucrado puede ser un factor de riesgo para la ruptura de la aorta. Se reconoce que un diámetro de 20 mm en la úlcera es un predictor de progresión de la enfermedad con valor predictivo positivo (VPP) de 100% y valor predictivo negativo (VPN) de 71%.7 Otro factor independiente de progresión de enfermedad es la presencia de dolor recurrente, incontrolable o que se incrementa progresivamente.
Debido a la presencia de nuevos y muy exactos métodos diagnósticos para valorar la aorta en su totalidad, la úlcera aterosclerótica penetrada explica de 2.3% a 7.6% de los pacientes sintomáticos con sospecha de síndrome aórtico agudo. El caso de nuestro paciente es excepcional debido a que se considera un síndrome aórtico agudo que sobrevivió a la penetración de una úlcera aterosclerótica. Recientemente la Sociedad Europea de Cardiología adoptó una nueva clasificación de las enfermedades aórticas hecha por Svensson y colaboradores, que considera a la úlcera aterosclerótica penetrada como una disección aortica clase 4.8 La conocida clasificación de Stanford se utiliza para categorizar a la úlcera aterosclerótica penetrada de acuerdo con la localización de la enfermedad. En este caso es tipo B.
Los síntomas de las úlceras penetradas pueden ser similares a las disecciones aórticas como en este caso, en el cual se presentó dolor un mes y medio antes del diagnóstico del aneurisma. Las complicaciones incluyen el desarrollo de un hematoma intramural debido a erosión de los vasa vasorum por la úlcera, la formación de pseudoaneurismas, la progresión a la disección aórtica y, en más de 40% de los casos, ruptura.9
El tamaño basal del aneurisma es quizás el mejor factor predictivo de la velocidad de su expansión, de manera que los aneurismas mayores se expanden más rápidamente que los pequeños, probablemente como consecuencia de la ley de Laplace. Una velocidad rápida de expansión produce aparentemente la ruptura del aneurisma, especialmente en los abdominales de 5 cm o más de diámetro.10
Tratamiento
El momento óptimo de la reparación quirúrgica de los aneurismas de la aorta torácica sigue siendo incierto, por varias razones. En primer lugar, los datos disponibles sobre la evolución natural de los aneurismas torácicos son limitados, especialmente respecto a los resultados de la intervención quirúrgica. En segundo lugar, con la incidencia elevada de enfermedades cardiovasculares coexistentes en esta población, muchos pacientes fallecen de otras enfermedades cardiovasculares antes de que sus aneurismas se rompan. Finalmente, la cirugía de aorta torácica tiene riesgos significativos, sobre todo en el cayado y en la aorta descendente, que en muchos casos pueden superar a los posibles beneficios de la reparación aórtica. 11
Tratamiento quirúrgico
Durante las pasadas cuatro décadas ha habido una importante disminución de la morbilidad y mortalidad en la reparación abierta de los aneurismas toraco–abdominales, debido a la mejoría en las técnicas anestésicas y quirúrgicas.12 A pesar de lo anterior, esta intervención quirúrgica se asocia a una morbilidad y mortalidad significativa aun en los casos de bajo riesgo.13
La presencia de una úlcera penetrante aterosclerótica debe ser considerada para la realización de un procedimiento agresivo, preferentemente quirúrgico, independientemente de la localización de la lesión, pero considerando el tamaño y profundidad de la úlcera. La técnica quirúrgica es la misma para los síndromes aórticos agudos y los aneurismas aórticos, y consiste en prevenir o aliviar las complicaciones potencialmente mortales, como el dolor resistente al tratamiento, un diámetro aórtico que aumenta con rapidez o signos de ruptura aórtica inminente, aunque también pueden tratarse de forma intervencionista mediante la inserción de una endoprótesis vascular autoexpandible.
La cirugía consiste en la resección y el reemplazo del segmento comprometido; según su localización cobra importancia el reimplante de las colaterales involucradas en su trayecto.
Los aneurismas de la aorta torácica descendente tienen gran riesgo de perforación en estructuras vecinas y ruptura, lo cual implica que éstos sean quirúrgicos. Si el paciente se presenta a la consulta con dolor, hemoptisis o hematemesis, la intervención es de urgencia. Los aneurismas de la aorta abdominal por debajo de los 50 mm de diámetro necesitan seguimiento cada 3–6 meses, con el fin de evaluar su progresión. Si su tamaño es superior está indicada la cirugía. Con presentación de síntomas, la elección es la quirúrgica sin que se tenga en cuenta el diámetro. También deben tenerse en consideración los factores de riesgo (hipertensión arterial, cirugías previas abdominales, entre otros), los cuales se asocian a la presencia de complicaciones tempranas, ya que en pacientes con más número de factores de riesgo la indicación quirúrgica debe ser precoz.
Después de la reparación de un aneurisma se debe poner especial atención en el estado neurológico, así como en pacientes con reparación tipo trompa de elefante, ya que la prótesis puede obstruir la circulación espinal.14 La paraplejia es la complicación más temida de las reparaciones en aorta descendente y toracoabdominal.15 Otras complicaciones de la reparación de aneurismas son el sangrado, enfermedad vascular cerebral (EVC) por embolización de los restos de la placa aterosclerótica o el coágulo, el infarto del miocardio, y la insuficiencia renal o pulmonar.16
De acuerdo con Culliford y colaboradores (1982),17 Carbol (1988)18 Donaldson y Ross (1982),19 la mortalidad hospitalaria después de la reparación de aneurismas de aorta ascendente es de 4% a 10%. En series contemporáneas el rango va desde 2% hasta 17%; Coselli20 y Ueda21 reportaron una mortalidad operatoria de 6% a 12% y EVC de 3% a 22%. Según Crawford22 y Kitamura,23 los índices de sobrevida después de la cirugía de un síndrome aórtico crónico son de aproximadamente 60% a cinco años, y de 30% a 40% a 10 años.
Tratamiento endovascular
El tratamiento endovascular con la colocación de stent en la aorta es un tratamiento prometedor, una alternativa menos invasiva y, reconociendo los altos índices de morbilidad y mortalidad que da la cirugía, se considera una opción terapéutica para los pacientes con úlcera aterosclerótica penetrada.24 Reduce el riesgo de complicaciones neurológicas como la paraplejia, que se presenta en 0% a 1.6%. El éxito del procedimiento se ha visto en 100% de un total de 54 pacientes reportados en 13 diferentes instituciones. Se observó cicatrización total de la úlcera en 94% de los pacientes, complicaciones neurológicas hospitalarias en 6%, y la mortalidad hospitalaria fue de 5%. El seguimiento de los pacientes se ha logrado de 7.3 meses a 24.4 (media 13.5) meses en 48 pacientes, y 46 (96%) de éstos todavía vivían al final del procedimiento.
Las indicaciones para la reparación endovascular en pacientes asintomáticos son la presencia de complicaciones como la úlcera penetrada, o en pacientes que son considerados de alto riesgo para la cirugía por la presencia de dolor intratable o recurrente, pseudoaneurisma, ruptura contenida e incremento del derrame pleural.25
El concepto de insertar una endoprótesis vascular para reparar con urgencia un síndrome aórtico agudo es atractivo.26 Un número cada vez mayor de disecciones aórticas agudas de tipo B se repara de esta manera, con pocos indicios de morbilidad periprocedimiento, lo que permite el tratamiento de la mala perfusión, la interrupción de las pérdidas sanguíneas y, finalmente, la reconstrucción de la aorta disecada. La inserción de una endoprótesis vascular en la disección aórtica complicada distal empieza a ganar adeptos y, en manos expertas, se asocia con pocas complicaciones periféricas o neurológicas;27 con ella se obtienen mejores resultados a corto y largo plazo que con el tratamiento médico o quirúrgico en grupos de alto riesgo con una disección de tipo B.28
De manera adicional, en los pacientes de alto riesgo no candidatos a cirugía debido a la edad, a la comorbilidad o a una preferencia personal, la reparación endovascular ofrece un tratamiento paliativo para la enfermedad que, de otra manera, hubiese debido abandonarse a su curso natural.
En informes recientes se apoya la noción de que la inserción de una endoprótesis vascular es más segura y proporciona mejores resultados que la cirugía en la disección de tipo B.29
Los resultados del seguimiento a corto plazo son excelentes, con una supervivencia > 90% al cabo de un año; las rupturas pueden sellarse y los diámetros aórticos disminuyen generalmente con la trombosis completa de la falsa luz. Esto señala que la inserción de la endoprótesis puede facilitar la curación de la disección, a veces de la aorta completa, incluidos los segmentos abdominales.
El informe del registro EUROSTAR/Reino Unido incluye los resultados de la primera gran serie de pacientes tratados con endoprótesis vasculares autoexpandibles en la aorta torácica.30 En este registro combinado, en 131 pacientes con disección aórtica (5% proximal, 81 % distal y 14% sin clasificar) se insertaron endoprótesis vasculares; 57% presentaba síntomas de ruptura, dilatación aórtica u oclusión de una rama lateral. Aunque todavía faltan datos relevantes a largo plazo, en 89% se alcanzó el éxito técnico primario a expensas de una mortalidad de 8.4% a los 30 días.31 Al igual que en el metaanálisis,11 en 0.8% de los pacientes tratados se produjo una paraplejia y la supervivencia al cabo de un año después del tratamiento fue de 90%.32
La reparación endovascular por cateterismo no ha logrado eliminar el riesgo de paraplejia y la incidencia varía hasta 2.7%.
Los resultados de la fase II del estudio multicéntrico GORE–Tag thoracic endovascular stent demostraron una mortalidad a 30 días de 1.5%,33 paraplejia temporal o permanente en 3%, EVC en 4% y la sobrevida a dos años fue de 97% con sobrevida de 75%.34 Los resultados preliminares con seguimiento a mediano plazo de los aneurismas torácicos reparados quirúrgicamente, comparados con la colocación de stent en aorta, demostraron mejor mortalidad con la reparación endovascular 10% vs 15% con la reparación abierta, pero sobrevida similar a los 48 meses de seguimiento, 54% para injerto del stent y 64% para la reparación abierta.
Rodríguez JA y colboradores,35 en una publicación reciente, evaluaron el tratamiento con la endoprótesis aprobada por la Food and Drug Administration (FDA) para el manejo de las patologías de la aorta torácica. La población que estudiaron incluyó a pacientes que eran candidatos a cirugía y aquellos con riesgo prohibitivo para la misma. Fueron 324 pacientes sometidos a dicho procedimiento entre marzo de 1998 y marzo de 2006. Ciento cincuenta y siete pacientes (48.5%) tuvieron aneurismas de etiología aterosclerótica. De los casos que fueron operados de manera electiva, 14.2% tuvieron complicaciones. Del total, 1.5% tuvo paresia. La incidencia de paraplejia se asoció con el abordaje retroperitoneal, el sangrado perioperatorio mayor de 1 000 mL y un aneurisma mayor de 40 cm. En conclusión, se consideró a la colocación de prótesis endovascular como un procedimiento alternativo a la cirugía abierta para las patologías de la aorta torácica. La mortalidad a 30 días se comparó favorablemente con la de la reparación abierta.
Tratamiento híbrido
La técnica híbrida consiste en la combinación de revascularización anterógrada de los vasos supraórticos o las arterias viscerales y la completa exclusión de los aneurismas toracoabdominales aórticos con la colocación de endoprótesis.
En el estudio HOER de Donas y colaboradores,36 publicado en 2007, se realizó una revisión de la literatura de lo publicado respecto al procedimiento híbrido en pacientes con aneurismas toracoabdominales. Se incluyeron 13 estudios con 58 pacientes, 37 fueron hombres (64.4%) con edad media de 68.1 años. Debido a sus comorbilidades, todos los pacientes fueron elegidos para la reparación abierta y la colocación de la endoprótesis. El seguimiento fue de 14.5 ± 8.7 meses y el diámetro medio del aneurisma fue de 71.5 cm; 229 de los 234 injertos viscerales permanecieron permeables durante el seguimiento. Uno de los pacientes requirió reintervención por un injerto ocluido. El estudio HOER mostró que los resultados a mediano plazo de los pacientes de alto riesgo que tienen aneurismas aortoabdominales son prometedores, sin embargo, se requieren conclusiones y evidencias más concretas, con seguimiento a largo plazo para conocer la utilidad real de este procedimiento.
En el estudio más reciente publicado por Lee WA,37 se revisaron 70 pacientes con aneurismas toracoabdominales que fueron sometidos a procedimiento híbrido. La mortalidad perioperatoria y las complicaciones asociadas a la primera fase del procedimiento fueron de 24% y 25%, respectivamente; el seguimiento fue de 7 ± 12 días, con un promedio de 27 ± 27 días entre cada procedimiento. La reparación endovascular o la segunda etapa del procedimiento se realizó en 92% de los pacientes. El seguimiento se logró efectuar en 11 pacientes que completaron las dos fases del procedimiento, cuya duración fue de 8 a 12 meses. Los pacientes no requirieron terapia intensiva y la estancia hospitalaria después de la segunda fase del procedimiento fue de 2 ± 2 días. El procedimiento híbrido, por lo tanto, reduce el porcentaje de complicaciones, y se puede considerar en pacientes de alto riesgo para cirugía en relación con la edad, comorbilidades o consideraciones anatómicas.
Conclusiones
El síndrome aórtico agudo sigue teniendo una alta mortalidad a pesar de los avances diagnósticos y terapéuticos de la última década. El mejor conocimiento de la historia natural y de las variables pronósticas de esta enfermedad debe ser de gran ayuda para indicar la estrategia terapéutica más adecuada. Sin embargo, la sospecha clínica precoz y la experiencia del cirujano continúan siendo los aspectos fundamentales que se relacionan con la mortalidad en la fase aguda. La introducción del tratamiento intravascular ha abierto nuevas perspectivas en el tratamiento del síndrome aórtico agudo que afecta a la aorta descendente. Es una excelente opción para el tratamiento precoz de las complicaciones y consigue, en la mayoría de casos, un remodelado aórtico que puede modificar la historia natural y mejorar el pronóstico de esta enfermedad.38 Por lo tanto, la colocación de un stent intraluminal es una alternativa accesible a la cirugía abierta para la reparación de aneurismas de aorta torácica.39 La morbilidad y mortalidad se pueden comparar con la cirugía de forma favorable.40 La paraplejia continúa siendo baja en incidencia y el incremento de ésta se observa con el abordaje retroperitoneal, incrementando las pérdidas sanguíneas perioperatorias.
Bibliografía
1. Erbel R, Zamorano J. The aorta. Aortic aneurysm, trauma and dissection. Crit Care Clin 1996; 12:733–66. [ Links ]
2. Isselbacher, EM (2006). Enfermedades de la aorta. En: Zipes Douglas P., Libby P., Bonow R. O., Braunwald E. (Eds.), Braunwald. Tratado de Cardiología. (7a ed., 1403–1433). Madrid, España: Elsevier. [ Links ]
3. Lederle FA, Johnson GR, Wilson SE, Chute EP, et al. Prevalence and associations of abdominal aortic aneurysm detected through screening. Aneurysm Detection and Management (ADAM) Veterans Affairs Cooperative Study Group. Ann Intern Med 1997; 126:441 –80. [ Links ]
4. Lederle FA, Johnson GR, Wilson SE. Abdominal aortic aneurysm in women. J Vasc Surg 2001 ;34:122–6. [ Links ]
5. Randall B, Griepp M, Ergin A, Galla JD, et al. Natural history of descending thoracic and thoracoabdominal aneurysms. Ann Thorac Surg Jun 1999;67(6):1927–30; discussion 1953–8. [ Links ]
6. Olsson C, Thelin S, Stahle E, Ekborn A, et al. Thoracic aortic aneurysm and dissection: Increasing prevalence and improved outcomes reported in a nationwide population–based study of more than 14,000 cases from 1987 to 2002. Circulation 2006;114:2611–8. [ Links ]
7. Harris JA, Bis KG, Glover JL, Bendick PJ, et al. Penetrating atherosclerotic ulcers of the aorta. J Vasc Surg 1994;19:90–8. [ Links ]
8. Erbel R, Alfonso F, Boileau C, Dirsch O, et al. Diagnosis and management of aortic dissection. Eur Heart J 2001 Sep;22(18):1642–81. [ Links ]
9. Holger Eggebrecht, Dietrich Baumgart, Axel Schmermund, Ulf Herold, Peter Hunold, Heinz Jakob, et. al. Penetrating atheronetrating atherosclerotic ulcer of the aorta: Treatmen by endovascular stent–graft placement. Curr Opin Cardiol 2003; 18:431–435. [ Links ]
10. Davies RR, Gallo A, Coady MA, Tellides G, Botta DM, Burke B, et al. Novel measurement of relative aortic size predicts rupture of thoracic aortic aneurysms. Ann Thorac Surg. Jan 2006;81:169–177. [ Links ]
11. Elefteriades JA. Natural history of thoracic aortic aneurysms: indications for surgery, and surgical versus nonsurgical risks. Ann Thorac Surg. Nov 2002;74(5):S1 877–80; discussion S1892–8. [ Links ]
12. Kouchoukos NT, Dougenis D. Surgery of the thoracic aorta. N Engl J Med 1997 Jun 26;336(26):1876–88. [ Links ]
13. Svensson LG, Crawfford ES, Hess KR, Coselli JS, et al. Experience with 1509 patients undergoing thoracoabdominals aortic operations. J Vasc Surg 1993;17:357–68. [ Links ]
14. Minatoya K, Karck M, Hagl C, Meyer A, et al. The impact of spinal angiography on the neurological outcome after surgery on the descending thoracic and thoracoabdominal aorta. Ann Thorac Surg 2002 Nov;74(5):S1870–2; discussion S1892–8. [ Links ]
15. LeMaire SA, Miller CC, Conklin LD, Schmittling ZC, et al. Estimating group mortality and paraplegia rates after thoracoabdominal aortic aneurysm repair. Ann Thorac Surg 2003 Feb;75(2):508–13. [ Links ]
16. Suzuki T, Mehta RH, Ince H, Nagai R, et al. Clinical profiles and outcomes of acute type B aortic dissection in the current era: Lessons from the International Registry of Aortic Dissection (IRAD). Circulation 2003;108 Suppl II:S312–7. [ Links ]
17. Crawford ES, Coselli JS, Svensson LG, Safi HG, et al. Diffuse aneurismal disease (chronic aortic dissection, Marfan, and mega aorta syndromes) and multiple aneurysm. Treatment by subtotal and total aortic replacement emphasizing the elephant trunk operation. Ann Surg 1990;211:521 –37. [ Links ]
18. Cabrol C, Gandjbakhc I, Pavie A. Surgical treatment of ascending aortic pathology. J Card Surg. 1988 Sep;3(3):167–80. [ Links ]
19. Donaldson RM, Ross DN. Composite graft replacement for the treatment of aneurysms of the ascending aorta associated with aortic valvular disease. Circulation. 1982 Aug;66(2 Pt 2):I116–21. [ Links ]
20. Coselli JS, Conklin LD, LeMaire SA. Thoracoabdominal aortic aneurysm repair: review and update of current strategies. Ann Thorac Surg. 2002 Nov;74(5):S1881–4; discussion S1892–8. [ Links ]
21. Ueda T, Fleischmann D, Rubin GD, Dake MD, Sze DY. Imaging of the thoracic aorta before and after stent–graft repair of aneurysms and dissections.Semin Thorac Cardiovasc Surg. 2008 Winter;20(4):348–357. Review. [ Links ]
22. Crawford ES, Coselli JS, Svensson LG, Safi HG, Hess KR. Diffuse aneurismal disease (chronic aortic dissection, Marfan, and mega aorta syndromes) and multiple aneurysm. Treatment by subtotal and total aortic replacement emphasizing the elephant trunk operation. Ann Surg. 1990; 211: 521–537. [ Links ]
23. Kitamura M, Hashimoto A, Akimoto T, Tagusari O, et al. Operation for type A aortic dissection: Introduction of retrograde cerebral perfusion. Ann Thorac Surg 1995; 59:1195–9. [ Links ]
24. Attia Ch, Villard J, Boussel L, Farhat F, et al. Endovascular repair of localized pathological lesions of the descending thoracic aorta: Midterm results. Cardiovasc Intervent Radiol 2007;30(4):628–37. [ Links ]
25. Moffatt SD, Mitchell RS. Endovascular stent management of thoracic aneurysms and dissections. Card Surg Adult 2003; 1191 –204. [ Links ]
26. Morasch MD. Percutaneous techniques for aneurysm repair. J Vasc Surg 2006 Feb;43 Suppl A:69A–72A. [ Links ]
27. Nienaber CA, Ince H, Weber F. Emergency stent–graft placement in thoracic aortic dissection and evolving rupture. J Card Surg 2003;18:464–70. [ Links ]
28. Beregi JP, Haulon S, Otal P. Endovascular treatment of acute complications associated with aortic dissection: midterm results from a multicenter study. J Endovasc Ther 2003;10:486–93. [ Links ]
29. Eggebrecht H, Nienaber CA, Neuhauser M, Baumgart D, Kische S, Schmermund A, et al. Endovascular stent–graft placement in aortic dissection: a meta–analysis. Eur Heart J 2006;27:489–98. [ Links ]
30. Leurs L, Bell R, Degrieck Y, Thomas S, Hobo R, Lundbom J, EUROSTAR, UK Thoracic Endograft Registry collaborators. Endovascular treatment of thoracic aortic diseases: combined experience from the EUROSTAR and United Kingdom Thoracic Endograft registries. J Vasc Surg 2004;40:670–9. [ Links ]
31. Pretre R, Von Segesser LK. Aortic dissection. Lancet 1997;349:1461–4. [ Links ]
32. Gowda RM, Misra D, Tranbaugh RF. Endovascular stent grafting of descending thoracic aortic aneurysms. Chest 2003 Aug;124(2):714–9. [ Links ]
33. Makaroun MS, Dillavou ED, Kee ST. Endovascular treatment of thoracic aortic aneurysms: Results of the phase II multicenter trial of the GORE TAG thoracic endoprosthesis. J Vasc Surg 2005 Jan;41(1):1–9. [ Links ]
34. Sullivan TM, Sundt TM 3rd. Complications of thoracic aortic endografts: spinal cord ischemia and stroke. J Vasc Surg 2006 Feb;43 Suppl A:85A 8A. [ Links ]
35. Rodríguez JA, Olsen DM, Shtutman A, Aguiar–Lucas L, et al. Application of endograft to treat thoracic aortica pathologies. A single center experience. J Vasc Surg 2007 Sep;46(3):413–20. [ Links ]
36. Donas KP, Czerny M, Guber I, Teufelsbauer H et al. Hybrid Open–endovascular Repair for Thoracoabdominal Aortic Aneurysms: Current Status and Level of Evidence. Eur J Vasc Endovasc Surg 2007;34:528–33. [ Links ]
37. Lee WA, Brown MP, Martin TD, Seeger JM, et al. Early results after staged hybrid repair of thoracoabdominal aortic aneurysms. J Am Coll Surg 2007 Sep;205(3):420–31. [ Links ]
38. Masip AE. Avances en el síndrome aórtico agudo. Rev Esp Cardiol 2007;60:428–39. [ Links ]
39. Stone DH, Brewster DC, Kwolek CJ, Lamuraglia GM, et al . Stent–graft versus open–surgical repair of the thoracic aorta: Mid–term results. J Vasc Surg 2006 Dec;44(6):1188–97. [ Links ]
40. Scott Mitchell R., Michel S. Makaroun, Gregario Sicard. A comparative trial of open versus stent graft repair of descending thoracic aneurysms. AATS 2005 Meeting Abstract; 2005. [ Links ]














