Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.77 no.4 Ciudad de México oct./dic. 2007
Comunicación breve
Daño miocárdico grave en un caso de síndrome de Barlow
Severe myocardial disease in a case of Barlow's syndrome
Nydia Ávila Vanzzini,* Jorge Kuri Alfaro,* Sergio Trevethan Cravioto,** Nilda Espínola Zavaleta,* Laura Rodríguez Chávez,* José A Carballo Quiñones,* y Héctor Herrera Bello***
* Médico Adjunto de la Consulta Externa. Consulta Externa del Instituto Nacional de Cardiología Ignacio Chávez, México.
** Jefe de la Consulta Externa. Consulta Externa del Instituto Nacional de Cardiología Ignacio Chávez, México.
*** Cardiólogo egresado del Instituto Nacional de Cardiología y Jefe de Terapia Intermedia Médica Sur.
Correspondencia:
Nydia Ávila Vanzzini.
Consulta Externa del Instituto Nacional de Cardiología Ignacio Chávez.
(INCICH, Juan Badiano No. 1 Sección XVI. Delegación Tlalpan.
04480, México, D.F.).
Tel: (55) 55 73 29 11 Ext. 11 96.
E–mail: vazzny74@yahoo.com
Recibido: 15 de noviembre de 2006.
Aceptado: 17 de julio de 2007.
Resumen
El síndrome de Barlow, es una entidad caracterizada por prolapso valvular mitral, que además cursa con una amplia gama de signos y síntomas. Sabemos que su expresión clínica es muy variada, existiendo casos con poca expresión, como los que con frecuencia se ven en la práctica diaria o bien el lado totalmente opuesto, en el cual, es tan complejo el síndrome que lleva al paciente a tener alteraciones hemodinámicas que menoscaban por mucho su calidad de vida e incluso modifican su pronóstico, llevándolo a la muerte temprana. El caso que presentamos es justamente el de una paciente de 25 años, quien tuvo un síndrome de Barlow, que comprometió de manera significativa su clase funcional como consecuencia de las alteraciones en la función contráctil del corazón y que finalmente la llevaron a la muerte.
Palabras clave: Prolapso de la válvula mitral. Miocardiopatía. Insuficiencia cardíaca.
Abstract
The Barlow's syndrome is a disease characterized by the presence of mitral valve prolapse and a wide range of signs and symptoms. We know that its manifestations has a great variety existing cases with little clinical expression as those seen frequently in daily practice or the other side opposite completely in which, the syndrome is so complex getting to the patient to present many symptoms secondary to hemodynamics alterations that reduce by much its quality of life and even modify its prognosis. The case that we present is a female patient of 25 years old with Barlow's syndrome and functional class II–III of New York Heart Association as a result of the alterations in the contractility function of the heart that finally caused her death.
Key words: Mitral valve prolapse. Cardiomyopathy. Heart failure.
Introducción
El prolapso de la válvula mitral es una entidad clínica bien reconocida desde 1963, cuando finalmente se tuvo la confirmación clínica, fonomecanocardiográfica y angiográfica de que el suceso que condiciona el típico chasquido mesosistólico y el soplo regurgitante (en algunas ocasiones), es una consecuencia de la protrusión de una o ambas valvas de la mitral hacia la aurícula. Se han descrito una serie de desórdenes adicionales comunes en estos pacientes, lo cual implica que el daño no está limitado sólo a la válvula mitral. En su gama de alteraciones se incluyen eventos clínicos, radiológicos, auscultatorios, fonomecanocardiográficos, anatómicos, hemodinámicos, angiográficos, familiares y genéticos, lo que ha llevado a considerar a esta patología como un síndrome, reconocido como síndrome de Barlow (SB),1 en honor a la persona que lo describió originalmente.
Uno de los componentes más interesantes del SB, en lo que al corazón se refiere, es el hallazgo de miocardiopatía, que se expresa por una morfología muy peculiar de la pared dada por "indentaciones," patrones anormales de contracción e incluso hipertrofia, sin que para esto último exista una justificación hemodinámica. Tales alteraciones morfológicas han sido descritas por diferentes autores a lo largo de los años.2–7
El SB puede tener expresiones clínicas distintas, existiendo casos poco floridos en donde apenas son perceptibles los hallazgos y otros muy demostrativos en donde se conjuntan una gran variedad de alteraciones. Presentamos el estudio completo de una paciente con SB, que resultó muy interesante debido a la gravedad, complejidad y pronóstico que exhibió su caso.
Reporte de caso
Paciente femenino de 25 años de edad, sin antecedentes familiares de importancia. Desde los 8 años de edad inició con disnea de grandes esfuerzos que fue lentamente progresiva hasta ser de moderados a pequeños esfuerzos a la edad de 23 años. Refirió además lipotimias, llegando en dos ocasiones a síncope en relación a esfuerzo físico moderado; presentó ocasionalmente palpitaciones de inicio y fin súbito y dolor precordial opresivo, que cedía al reposo. En el seguimiento la paciente refirió además fotosensibilidad, eritema malar ocasional, fotofobia, relacionados a leve exposición solar. La exploración física mostró una talla de 1.52 m y peso 48 kg. Presión arterial de 110/70 y frecuencia cardíaca de 70 latidos por minuto (LPM). Normocéfala, pabellones auriculares con discreta hipoplasia del hélix derecho, hipoplasia de cintura escapular bilateral, con asimetría en la altura de los hombros, disminución de fuerza en ambos brazos 3/5 y fuerza conservada en antebrazos 5/5, hiperlordosis lumbar. En la exploración cardiovascular, destacó el choque del ápex desplazado al 6to. EII, 2 cm fuera de la línea medio clavicular, tenía un chasquido mesosistólico audible en foco mitral, a partir de donde se auscultaba un soplo mesotelesistólico III/IV, el cual se irradiaba hacia el borde paraesternal izquierdo.
Laboratorio y gabinete
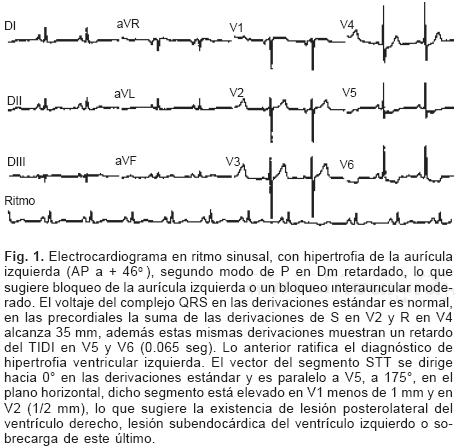
La biometría hemática, química sanguínea, perfil de lípidos, pruebas funcionales hepáticas, electrolitos séricos, examen general de orina y pruebas de función tiroidea fueron normales. Perfil inmunológico: Anticuerpos antinucleares y anticardiolipina negativos. Complemento y factor reumatoide dentro de lo normal. El electrocardiograma: (Fig. 1). Hipertrofia tanto auricular como ventricular izquierda, el vector del segmento STT se dirige hacia 0º en las derivaciones estándar y es paralelo a V5, a – 175° en el plano horizontal. Dicho segmento está elevado en VI, menos de 1 mm, y en V2 (1/ 2 mm), lo que sugiere la existencia de lesión posterolateral del ventrículo derecho o subendocárdica del ventrículo izquierdo o sobrecarga sistólica de este ventrículo. Sin embargo, en la prueba de esfuerzo, el STT se desvió hacia arriba, a–100° en el plano frontal y hacia –175° en el horizontal. Esto sugiere la existencia de una zona de lesión posterolateral de ambos ventrículos, con mayor extensión en el ventrículo derecho. La radiografía de tórax (Fig. 2) mostró cardiomegalia grado III a expensas del ventrículo izquierdo, el perfil izquierdo tiene imagen de 4 arcos y se observa crecimiento de la aurícula derecha, tiene datos de hipertensión venocapilar pulmonar. Son muy evidentes las alteraciones óseas que presentaba la paciente tanto en columna dorsal como a nivel de la cintura escapular.

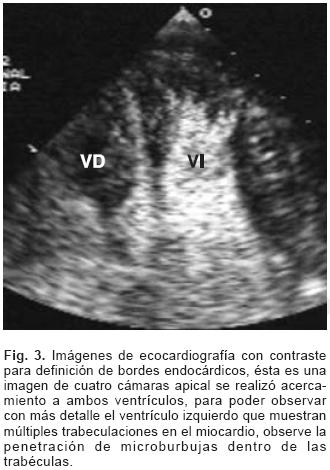
El ecocardiograma transtorácico convencional mostró diámetros del ventrículo izquierdo ligeramente aumentados, septum interventricular de 12 mm y pared posterior de 12 mm. La fracción de expulsión fue de 65%. En la válvula mitral se observó prolapso de la valva posterior con insuficiencia importante; se midió hipertensión arterial pulmonar moderada. Existió además disfunción diastólica tipo 1; la imagen de la pared posterior recordó al miocardio no compactado, por lo que se aplicó además contraste documentándose múltiples trabeculaciones en esta cara, sin que se completaran los criterios diagnósticos para clasificarla como miocardiopatía no compactada (Fig. 3). Finalmente a través de estudio Doppler tisular se buscó asincronía en la contracción no documentándose en reposo. El estudio Holter evidenció algunas extrasístoles ventriculares de una sola morfología y aisladamente dupletas; también se observaron algunas extrasístoles supraventriculares aisladas. Presentó descenso recto del segmento ST de 2 mV durante la frecuencia cardíaca máxima (146 LPM).
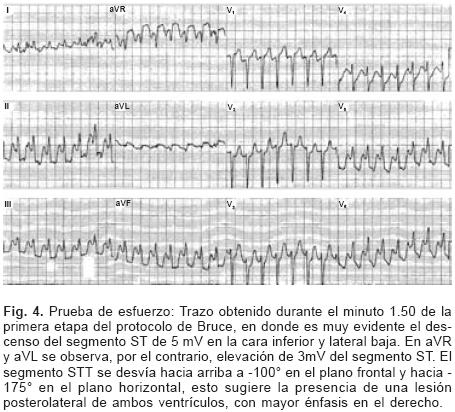
La prueba de esfuerzo (Fig. 4) realizada en banda, con protocolo de Bruce mostró una mala capacidad funcional y se suspendió por disnea y angor al minuto 1.50 de la primera etapa, con un costo energético de 4.6 METS, alcanzando una frecuencia cardíaca de 159 LPM, con respuesta hipotensiva. La prueba eléctrica evidenció desnivel negativo del segmento ST de 5 mV en derivaciones DII, DIII aVF y de V4 a V6. Se realizó un estudio de perfusión miocárdica en el cual se encontró infarto no transmural del ápex, con isquemia ligera del tejido residual, isquemia moderada de la pared anterior, disminución del engrasamiento sistólico y de la movilidad del ápex, función sistólica del ventrículo izquierdo de 59%. Por lo anterior se sometió la paciente a cateterismo cardíaco.
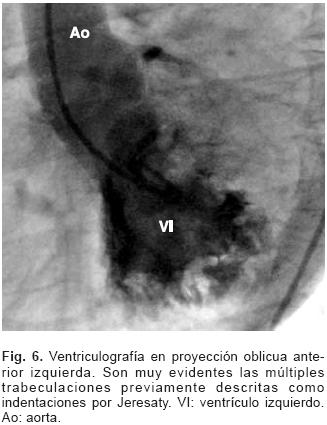
Cateterismo cardíaco izquierdo presión diastólica del ventrículo izquierdo (VI) = 29 mm Hg, presión sistólica del VI = 100 mm Hg. La ventriculografía (Fig. 5) mostró hipocinesia de la pared posteroinferior y del ápex, insuficiencia mitral severa, con hipertrofia de los músculos papilares. Llama la atención la presencia de múltiples trabeculaciones que se hacen evidentes en la proyección oblicua izquierda de la ventriculografía (Fig. 6). En el registro de presiones intraventriculares y raíz de aorta no se encontraron gradientes. Cateterismo derecho: Presión diastólica del ventrículo derecho (VD) 12 mmHg, presión sistólica del VD: 55 mmHg, presión sistólica de la arteria pulmonar: 55 mm Hg. La carrera oximétrica no mostró alteraciones. Durante el procedimiento la paciente desarrolló taquicardia supraventricular, lo que impidió que se realizara coronariografía, pero el análisis indirecto de las coronarias no mostró alteraciones. Posteriormente se realizó una angiotomografía, la cual confirmó que las arterias coronarias eran normales. Bajo este hallazgo y el antecedente de isquemia e incluso infarto en la medicina nuclear, realizamos un estudio de resonancia magnética nuclear con perfusión (Fig. 7). Ésta mostró un patrón fibrótico de la pared del VI, observado tras la administración de contraste endovenoso y en el reforzamiento tardío existió un patrón en parches con involucro predominantemente de la pared septal con extensión anterior y compromiso apical, en el eje corto del ventrículo izquierdo también se observaron múltiples trabeculaciones ("indentaciones"), hallazgo que recordó a las imágenes observadas en el ecocardiograma de contraste descrito previamente.
Como parte del estudio del síncope, se hizo una prueba de inclinación que resultó fuertemente positiva para disautonomía, pero fue negativa para síncope.
Los estudios inmunológicos se reportaron negativos, lo cual descartó que la paciente tuviera algún padecimiento de tipo reumatológico, que pudiera explicar parte de la sintomatología que presentaba.
En busca de alguna otra etiología que pudiera estar afectando el miocardio también se realizó biopsia periumbilical para descartar infiltración amiloide, la cual resultó negativa.
La paciente fue propuesta para plastía de la válvula mitral, pero dado la mala función ventricular que presentaba ante mínimo estrés, se opto por dejarla a libre evolución. Se propuso para estudio electrofisiológico, en busca de focos arritmogénicos y ablación de los mismos, sin embargo, la paciente falleció en los días previos al estudio en su domicilio. Por la descripción de los familiares, inferimos que la causa de la muerte fue cardíaca, posiblemente desarrolló una arritmia que la llevó a edema agudo de pulmón y a la muerte.
Discusión
El presente caso reviste gran importancia, por la expresión clínica tan compleja del síndrome, en el que se conjuntan tantos signos y síntomas, como hasta la fecha se han descrito, que lamentablemente llevaron a la muerte a la paciente. Una de las anomalías que más ha llamado la atención en este caso es la "miocardiopatía" que acompaña al SB y, aunque no está clara su etiología, se ha documentado su presencia en varias series de pacientes como es el caso de Scampardonis et al.6 en su estudio de 87 casos, en los que documentó cinco tipos distintos de patrón de contracción anormal en el 82% de sus casos. Dentro de sus conclusiones, destaca que el componente miocárdico del SB está expresado como patrones asinérgicos de contracción, que usualmente no deterioran la función ventricular. Otros autores que tuvieron hallazgos similares fueron Gooch et al,5 reportaron una incidencia del 70.8% de asinergia tanto sistólica como diastólica. Liedtke et al,8 documentaron que existe una contracción reducida en el anillo de la válvula mitral y la porción ventricular proximal a éste. Con tales hallazgos se sospechó que la alteración en la válvula mitral es debida a una pérdida del soporte posteroinferior del anillo, a consecuencia de los trastornos miocardiopáticos asociados al síndrome, que facilitan el prolapso de la válvula durante la sístole. En el caso de nuestra paciente también hemos documentado la presencia de una miocardiopatía, que se hace evidente en la ventriculografía, en donde se muestran patrones alterados de contracción, siendo importante la afección en la cara posteroinferior y el ápex. De acuerdo a los patrones descritos por Scampardonis et al,6 el caso corresponde a patrón de pie de bailarina. Otro dato importante de mencionar en este sentido es que durante el ecocardiograma de contraste se evidenció la presencia de múltiples trabeculaciones. Este mismo hallazgo fue confirmado en la ventriculografía y en la resonancia magnética; esto ya había sido descrito anteriormente por Jeresaty,7 como "indentaciones", en 5 casos. El hallazgo en el gammagrama cardíaco, en el cual se encuentra aperfusión en los sitios de acinesia, se correlaciona con el estudio de resonancia magnética que sugiere fibrosis en esas mismas zonas.
En cuanto a los hallazgos electrocardiográficos, ocurren anormalidades en dos terceras partes de los pacientes con SB. El más típico consiste en la franca inversión de la onda T en las derivaciones DII, DIII y aVF,9,11también puede presentarse la prolongación del intervalo QT, y aunque es poco común su asociación con el SB, su presencia aumenta el riesgo de muerte súbita.12 Por otro lado, las taquiarritmias principalmente supraventriculares o bien ventriculares son hallazgos frecuentes de los monitoreos Holter de estos pacientes; también se ha observado la presencia de disfunción del nodo sinusal llegando incluso al paro sinusal. Los bloqueos de la conducción auriculoventricular y la preexcitación también han sido documentados.9,11 Pero uno de los datos más importantes es la presencia de depresión del segmento ST durante la prueba de esfuerzo, un hallazgo poco frecuente en el síndrome, y para el cual no se tiene una explicación clara, se cree que en algunos pacientes pueden estar implicadas alteraciones de las arterias coronarias y en otros se ha explicado como una diferente respuesta metabólica del miocardio ante el estrés.13 En el caso que reportamos observamos que en la prueba de esfuerzo los cambios del segmento ST aparecen desde la primera etapa del protocolo de Bruce y son acompañados de alteraciones hemodinámicas que obligaron a suspender la prueba. El estudio de monitoreo ambulatorio de la paciente mostró estos mismos hallazgos en el segmento ST, en cuanto la paciente desarrollaba algún esfuerzo.
Las alteraciones óseas torácicas encontradas en la paciente, como las observadas en la cintura escapular y en la columna, son las mismas que se han descrito en el síndrome por otros autores.5
Con el análisis de estos resultados y de los estudios de función ventricular previa, pensamos que el origen de la mala función ventricular y los cambios del segmento ST ante mínimos esfuerzos, aunados a la sintomatología de la paciente, obedecen a la presencia de la miocardiopatía que acompaña el síndrome y que, sin duda, en el caso de la paciente tenían expresión muy importante, al grado que pensamos que tuvo gran peso en su desenlace fatal. Anteriormente ya se había documentado que la disfunción ventricular es demostrable durante la prueba de esfuerzo.13
Un dato que no podemos dejar de comentar es que el prolapso de la válvula mitral puede estar asociado a otras anomalías, como el síndrome de Marfan, hasta en un 4%.14 Por otro lado, existen formas aisladas de prolapso de la válvula mitral que están asociadas con alteraciones osteomusculares muy similares a las que se observan en el síndrome de Marfan, lo que ha llevado a especular que quizá el SB sea un Marfan frustrado, el cual afecta en estos casos a la válvula mitral, primordialmente en su anillo y en el tejido miocárdico que lo circunda. Otra anomalía asociada con relativa frecuencia es la presencia de defectos septales atriales hasta en un 5% en prolapsos bien documentados, pero su incidencia es un hallazgo de hasta el 37% en prolapsos clínicamente no manifiestos. También puede coexistir con coronariopatías y otras alteraciones cardíacas.
Conclusión
Nos queda claro que el espectro clínico del síndrome de Barlow puede ir de ser prácticamente nulo, con escasos signos y síntomas o bien puede llevar a una grave disfunción ventricular, que comprometa la clase funcional y el pronóstico de los pacientes al grado de causar la muerte de manera temprana, como sucedió con nuestra paciente. Por lo tanto una de las principales aportaciones de este trabajo es tener en mente que el SB, puede comprometer la vida de los pacientes y por otro lado es importante recordar que la disfunción ventricular puede ser explicada por el síndrome per se. Este dato puede obviar una serie de estudios en busca de posibles etiologías en cuanto a la miocardiopatía que pudieran presentar estos pacientes.
Referencias
1. Baklow JB, Pocock WA, Marchand D, Denny M: The significance aflate systolic murmurs. Am Heart J 1963; 66: 443–452. [ Links ]
2. Grossman H, Fleming R, Engle MA, Levin AH, Ehlers KH: Angiocardiography in the apical systolic click syndrome: left ventricular abnormality, mitral insufficiency, late systolic murmur and inversion of Twaves. Radiologyl968; 91: 898–892. [ Links ]
3. Engle MA: The syndrome of apical systolic click, late systolic murmur and abnormal T waves. Circulation 1969; 39: 1–6. [ Links ]
4. Ehlers KH, Engle MA, Levin AR, Grossman H, Fleming RJ: Left ventricular abnormality with late mitral insufficiency and abnormal electrocardiogram. Am J Cardiol 1970; 26: 333–338. [ Links ]
5. Gooch AS, Vicencio F, Maranhao V, Golberg H: Arrhythmias and left ventricular asynergy in the prolapsing mitral leaflet syndrome. Am J Cardiol 1972; 29: 611–619. [ Links ]
6. Scampardonis G, San Yang S, Maranhao V, Goldemberg H, Gooch A: Left ventricular abnormalities in prolapsed mitral leaflet syndrome. Circulation 1993; 158: 287–297. [ Links ]
7. Jeresaty RM: The syndrome associated with mild systolic click and/or late systolic murmur: analysis of 32 cases. Chest 1971; 59: 643–647. [ Links ]
8. Liedtke AJ, Gault JH, Leaman DM, Blumenthal MS: Geometry of left ventricular contraction in the systolic click syndrome. Characterization of a segmental myocardial abnormality. Circulation 1973; 47: 27–36. [ Links ]
9. Barlow JB, Pocock WA: The problem of non–ejection systolic clicks and associated mitral systolic murmurs: emphasis on the billowing mitral leaflet syndrome. Am Heart J 1975; 90: 636–655. [ Links ]
10. Fontana ME, Pence HL, Leighton RF, Wooley CF: The varying clinical spectrum of the systolic click– Late systolic murmur syndrome. Circulation 1970; 41: 807–815. [ Links ]
11. Winkle RA, Lopex MG, Fitzgerald JW: Arrhythmias in patients with mitral valve prolapse. Circulation 1975; 52: 73–79. [ Links ]
12. Shappell SD, Marshall CE, Brown RE, Bruce TA: Sudden death and the familial occurrence of mid–systolic click, late systolic murmur syndrome. Circulation 1973; 48: 1128–1134. [ Links ]
13. Sloman G, Wong M, Walker J: Arrhythmias on exercise in patients with abnormalities of the posterior leaflet of the mitral valve. Am Hear J 1972; 83:312–316. [ Links ]
14. Allen H, Harris A, Leatham A: Significance and prognosis of an isolated late systolic murmur: a9 — to 22 years follow up. Br Heart J 1974; 36: 525–527. [ Links ]














