Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.77 no.3 Ciudad de México jul./sep. 2007
Revisión de temas cardiológicos
Paradigmas y paradojas de la hipertrofia ventricular izquierda: desde el laboratorio de investigación a la consulta clínica
Paradigms and paradoxes of left ventricular hypertrophy: from the research laboratory to the clinical consultation
Eduardo Manuel Escudero, Oscar Andrés Pinilla
Centro de Investigaciones Cardiovasculares. Facultad de Ciencias Médicas. Universidad Nacional de La Plata, Argentina.
Correspondencia:
Eduardo M Escudero.
60 y 120 (1900)
La Plata, Argentina,
Fax:+54-221-425-5861.
E-mail address: escu@arnet.com.ar
Recibido: 21 de septiembre de 2006
Aceptado: 15 de mayo de 2007
Resumen
La hipertrofia ventricular es considerada un mecanismo de adaptación del corazón ante diferentes sobrecargas; estas sobrecargas pueden generar a través de los mecanismos intracelulares utilizados distintas respuestas que se asocien o no con compromiso funcional del miocardio. Cuando la hipertrofia se acompaña de disfunción ventricular pudiendo ser el inicio de un proceso que conduce a la insuficiencia cardíaca, se pone en duda si ese mecanismo es realmente una adecuada adaptación a la sobrecarga. Analizando las modificaciones estructurales y funcionales del ventrículo izquierdo encontradas en ratas secundarias a hipertensión arterial, reducción del diámetro de la aorta ascendente, administración de isoproterenol y/o a infarto de miocardio y en pacientes hipertensos, con estenosis aórtica y con miocardio-patía hipertrófica se puede inferir la presencia de un mecanismo no adecuado de adaptación. Por el contrario las diferentes características de la respuesta ventricular ante la sobrecarga provocada por ejercicio o por el embarazo en humanos señalan una verdadera adaptación a la sobrecarga. En un verdadero desafío a lo conocido sería correcto especular con la necesidad de estimular el desarrollo de hipertrofia fisiológica en determinadas situaciones patológicas o llegar a modificar la respuesta patológica en fisiológica.
Palabras clave: Hipertrofia ventricular izquierda. Función ventricular izquierda. Hipertrofia fisiológica.
Summary
Cardiac hypertrophy can occur as an adaptative response to increased cardiac workload. Different types of cardiac hypertrophy arise from a combination of genetic, physiologic, and environmental factors. When hypertophic growth of the heart leads to left ventricular dysfunction and heart failure, the response is considered as maladaptive or pathological hypertrophy. After analyzed left ventricular functional and structural changes in rats induced by arterial hypertension, banding of aortic root, isoproterenol administration, or myocardial infarction, as well as in patients with arterial hypertension, aortic stenosis, or hypertrophic miocardiopathy, we found a maladaptive response considered as pathological hypertrophy. However, the adaptation of the left ventricle, found in response to physical activity or to pregnancy in humans, seems to help the heart adapt to the increase in workload acting as physiological hypertrophy. These considerations allow us to speculate for the use of future interventions to stimulate the development of physiological hypertrophy in several pathological situations or to change a pathological into a physiological response.
Key words: Left ventricular hypertrophy. Left ventricular function. Physiological hypertrophy.
Introducción
Distintas condiciones fisiológicas y/o patológicas pueden colocar al corazón en situaciones de sobrecarga que lo llevan a desarrollar diferentes respuestas de adaptación.1 Una de esas respuestas está caracterizada por el aumento del tamaño de los cardiomiocitos (hipertrofia) para mejorar la producción de fuerza y no por aumento en el número de los mismos (hiperplasia), debido a su rápida diferenciación después del nacimiento.2,3 Recientemente se ha propuesto que también algunos cardiomiocitos provenientes de células cardíacas indiferenciadas podrían participar en menor grado en esta adaptación a la sobrecarga.4
Definición
El concepto de hipertrofia se basa en la identificación del aumento de peso del corazón determinado principalmente por el aumento del tamaño de los miocitos. Se debe tener en cuenta que si bien las células musculares cardíacas constituyen el menor porcentaje de todas las células del miocardio, como lo muestra la figura 1, al ser las más grandes la variación de su tamaño determinará un impacto significativo en el peso final del corazón.
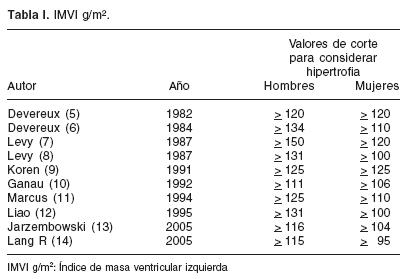
Si bien es claro el concepto de hipertrofia, existen dificultades para definir un límite de masa ventricular izquierda que determine la presencia o no de la misma. Como veremos en el desarrollo de esta revisión, se utilizarán diferentes referencias para considerar la existencia de hipertrofia: algunas basadas en comparaciones con corazones normales y otras tomando valores de corte con fundamento epidemiológico.5-14 En la tabla I se encuentran valores de cortes utilizados por diferentes autores para determinar la presencia de hipertrofia ventricular izquierda.
Causas determinantes
La repuesta hipertrófica puede ser desencadenada por mecanismos naturales de sobrecarga como el determinado por el crecimiento, el desarrollado durante el embarazo o el inducido por la actividad física; o por mecanismos de sobrecarga patológicos de presión y/o volumen secundarios a hipertensión arterial, estenosis o insuficiencia valvular, miocardiopatía primaria y/o infarto agudo de miocardio.
La realización de diferentes intervenciones en animales de laboratorio, en este caso ratas, permite estudiar las características de las respuestas hipertróficas como lo muestra la figura 2. Los datos corresponden al índice de masa ventricular izquierda encontrada en ratas espontáneamente hipertensas, en ratas expuestas a la administración de isoproterenol, en animales a los que se les redujo el diámetro de la raíz aórtica por la colocación de un clip o a los que se les provocó un infarto de miocardio por ligadura de la arteria descendente anterior. En todos los ejemplos señalados se observa el desarrollo de hipertrofia, teniendo en cuenta los valores de la masa ventricular encontrada en ratas controles con presión arterial normal tipo Wistar.

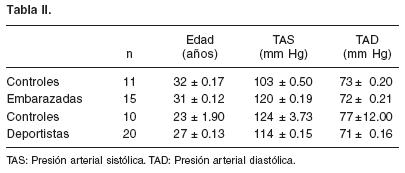
Cuando nos trasladamos al escenario clínico, podemos ver los efectos de distintos estímulos fisiológicos como el embarazo o la actividad deportiva sobre la masa ventricular izquierda como los muestra la figura 3. En estos casos la definición de hipertrofia surge del análisis comparativo de la masa ventricular con individuos sedentarios o mujeres de similar edad no embarazadas. Al estudiar la hipertrofia, se debe tener en cuenta si la misma es determinada por un incremento proporcionalmente mayor del espesor parietal que de los diámetros ventriculares o viceversa para establecer la presencia de hipertrofia concéntrica o excéntrica.14 En los modelos de hipertrofia analizados se puede ver que la respuesta generó una hipertrofia concéntrica como lo reflejan los valores del espesor relativo de la pared (Fig. 3). La edad y los valores de presión arterial fueron similares en los grupos controles de referencia y en los grupos con sobrecarga tanto en el estudio de deportistas como en embarazadas, datos que están representados en la tabla II.
En el hombre la respuesta hipertrófica puede ser desencadenada por diferentes situaciones patológicas. En la figura 4 se puede ver el índice de masa ventricular izquierda obtenida por ecocardiograma en pacientes con hipertensión arterial y estenosis aórtica severa representando al grupo con sobrecarga de presión y pacientes con miocardiopatía hipertrófica primaria como manifestación de la adaptación secundaria a mutación de proteínas contráctiles. Los valores de la masa obtenida son comparados con un grupo control.

En los estadios iniciales de la hipertensión arterial podemos encontrar aumento de la masa ventricular izquierda, en relación a grupos controles, aún sin criterios para definir presencia de hipertrofia; estas evidencias indican de alguna forma la existencia de una respuesta del miocardio ante elevaciones leves de la presión arterial. En la figura 5 se pueden ver los resultados obtenidos al analizar la masa ventricular izquierda en varones jóvenes con valores de presión arterial óptima, normal alta15 y ligeramente elevada, que certifican lo analizado anteriormente.15,16

En ambos casos, humanos y ratas, la masa ventricular fue calculada a partir de un estudio ecocardiográfico de acuerdo a Devereux y col.17 Los valores de masa fueron normalizados por la superficie corporal en el hombre y por el peso del animal en las ratas a los efectos de poder realizar comparaciones más adecuadas.
La hipertrofia a nivel celular
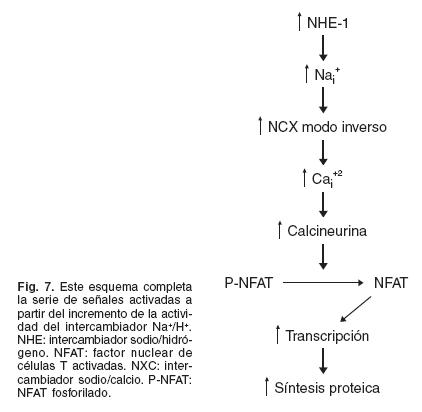
Como fue mencionado anteriormente, el aumento del tamaño de los miocitos es un elemento característico de la hipertrofia. Este aumento del tamaño se desencadena a través de la activación por estímulos externos de diferentes señales intracelulares que actuando sobre el núcleo favorecen una mayor síntesis de proteínas produciendo una reduplicación de sarcó-meros que determinan un incremento del tamaño de la célula. En ese camino de señales se produce una mayor actividad del intercambiador Na+/H+ (Fig. 6)18 que genera finalmente un aumento del calcio intracelular y la activación de diferentes enzimas calcio-dependientes entre las cuales debemos destacar a la calcineurina cuya expresión está elevada en ratas espontáneamente hipertensas19 (Fig. 7).
En experiencias realizadas en nuestro laboratorio se ha observado que el tamaño de los miocitos medidos a través de técnicas histo-métricas o calculado por la resistencia eléctrica de la membrana20,21 (Fig. 8), en poblaciones de ratas con hipertrofia secundaria a hipertensión arterial o a la inducida por isoproterenol era mayor a la de los animales normotensos o sin estímulo adrenérgico. En otro modelo experimental se pudo comprobar que las células musculares cardíacas de las áreas no infartadas de corazones de ratas normotensas tipo Wistar también mostraban un incremento de su tamaño en relación a animales controles, como expresión de remodelamiento. En la figura 9 se observan imágenes representativas de células musculares cardíacas en las situaciones mencionadas.
La hipertrofia en el miocardio
Si bien el concepto de hipertrofia se asocia al aumento del tamaño de los miocitos, el miocardio está configurado por otros elementos que también participan de la respuesta a los estímulos determinantes del crecimiento de la célula miocárdica, como quedó ejemplificado en la figura 1. Los efectos directos del estiramiento o las sustancias liberadas por el miocito pueden actuar sobre las otras células del miocardio, como los fibroblastos, estimulando su hiperplasia y la activación para la producción de diferentes componentes de la matriz extracelular, como el colágeno. Estas modificaciones estructurales si bien son necesarias para el mantenimiento de la morfología del miocardio pueden resultar perjudiciales si la respuesta está incrementada, por las consecuencias funcionales como se analizará más adelante. Diferentes observaciones en nuestro laboratorio han demostrado el aumento del colágeno intersticial por encima de los valores normales en ratas espontáneamente hiper-tensas o en hipertrofias secundarias a isoproterenol o al desarrollo de un infarto agudo de miocardio (IAM).20,22,23 El aumento del colágeno en el intersticio del miocardio se acompañó en esas observaciones con un incremento de los niveles séricos del péptido precursor de colágeno (PIP).22,24
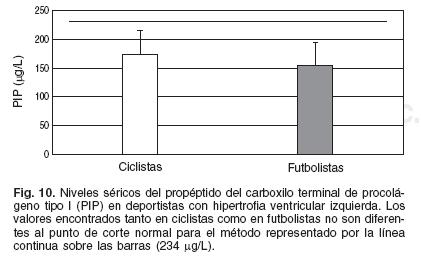
En la hipertrofia inducida por el ejercicio los niveles del péptido referido no se modifican, sustentando el rol adaptativo de la hipertrofia en esa situación, como se puede ver en observaciones previas de nuestro grupo25 (Fig. 10).
La hipertrofia fisiológica y la hipertrofia patológica
Si bien el desarrollo de hipertrofia en respuesta a un estímulo de sobrecarga ha sido interpretado como un mecanismo de adaptación, diferentes estudios epidemiológicos han demostrado el valor pronóstico independiente desfavorable de la misma tanto en la población general26-28 como en poblaciones de hipertensos29-31 o en pacientes con episodios isquémicos agudos.32,33 Sin embargo, existen situaciones donde ese aumento en el peso del miocardio, secundario a un aumento del tamaño de los miocitos y a un incremento proporcional de los elementos estructurales cumple realmente una función de adaptación. Hemos citado nuestra experiencia en el estudio de atletas con hipertrofia y podemos agregar las observaciones realizadas en mujeres embarazadas donde se encuentra un aumento de la masa ventricular en respuesta a los estímulos de sobrecarga.
La diferenciación entre estos dos tipos de respuesta debe buscarse en las características morfológicas del miocardio vinculado con el porcentaje de colágeno encontrado que no debe pasar de un 3% y en las consecuencias funcionales que analizaremos posteriormente.
La función ventricular en la hipertrofia miocárdica
Función sistólica
La valoración del comportamiento de la función sistólica en el corazón hipertrófico ha generado resultados disímiles.34-38 Esta discordancia puede ser explicada en parte por la utilización de distintos protocolos de estudio y por la influencia que las modificaciones de carga y el remodelamiento, impuestos por los determinantes de la hipertrofia, tienen sobre los parámetros elegidos para la evaluación de la función sistólica.
Los resultados obtenidos en nuestro laboratorio muestran una disminución de la capacidad contráctil del ventrículo izquierdo en las ratas hipertensas, expresada por la falta de aumento del porcentaje de acortamiento a pesar de la disminución de la postcarga como resultado de la hipertrofia concéntrica (Fig. 11).39
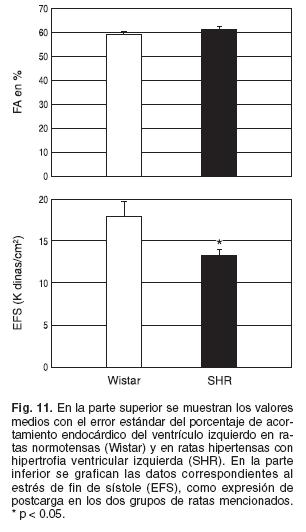
Cuando analizamos en humanos el acortamiento de las fibras longitudinales del ventrículo izquierdo por ecocardiograma, utilizando la velocidad de deformación de un segmento de la pared ventricular (strain-rate),40 se observó una disminución de la contracción en corazones hipertróficos por hipertensión en relación a la observada en controles sin hipertrofia ventricular y en atletas con hipertrofia fisiológica41 (Fig.12).

Estas observaciones son coincidentes con las referidas en la literatura en relación al comportamiento contráctil en miocitos aislados o en músculos papilares, donde la hipertrofia patológica se acompaña de un deterioro de la contractilidad.39 Esa alteración en el desarrollo de la hipertrofia puede deberse a una modificación de las proteínas volviendo a patrones fetales, o a la presencia de elementos que modifiquen la sensibilidad al calcio de las proteínas contráctiles, como fue propuesto para el miocito insuficiente.42 En este último mecanismo han sido consideradas entre otras causas el aumento de radicales libres y la mayor concentración de calcineurina.43 En nuestro laboratorio se ha comprobado que la calcineurina está sobre-expresada y probablemente hiperactiva en las ratas SHR que muestran un deterioro de la función contráctil dando base de sustentación a las especulaciones anteriores.19
Función diastólica
La diastole o el proceso que permite el correcto llenado del corazón para la eyección del flujo necesario para la perfusión de los tejidos, comprende un proceso activo de relajación, el llenado ventricular y un proceso pasivo determinado por la distensibilidad de la cámara ventricular. La disfunción diastólica se puede producir por el compromiso funcional de cualquiera de esas partes aisladamente o en forma conjunta.
En la hipertensión arterial una de las causas más frecuentes de hipertrofia, se detectan alteraciones de la función diastólica por disminución de la relajación en forma temprana, incluso previo al desarrollo de hipertrofia.15 En general el aumento de la masa ventricular se acompaña de alteración en la relajación debido a modificaciones en la retoma de calcio del retículo sarcoplásmico.44 Por otra parte, el aumento en el porcentaje de fibras de colágeno en la hipertrofia no adaptativa aumenta la rigidez del miocardio como lo representa la figura 13,24 contribuyendo a la alteración de la función diastólica.
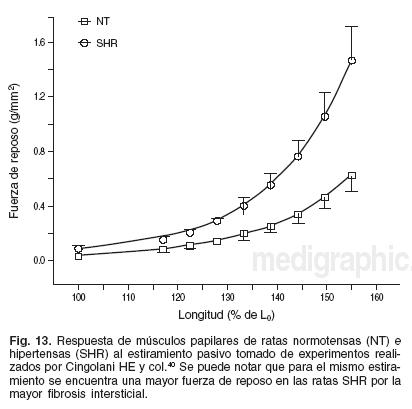
La hipertrofia fisiológica de los atletas no presenta alteraciones de la relajación, probablemente por la falta de fibrosis y por el mantenimiento de la retoma de calcio dentro de lo normal (Fig. 14).

El camino a la insuficiencia cardíaca
El desarrollo de insuficiencia cardíaca como consecuencia de la hipertrofia implica la aparición de síntomas y signos resultantes de la acumulación de líquido en los tejidos y/o la disminución en la perfusión de los mismos.45,46
En ese contexto podemos encontrar en la población de hipertróficos, aunque hayamos señalado un deterioro temprano de la función contráctil probablemente compensada por la reduplicación de sarcómeros, la presencia de síntomas y signos de insuficiencia cardíaca con fracción de eyección normal. Este cuadro clínico es identificado como insuficiencia cardíaca diastólica o con función sistólica normal.34,35
En el extremo final de la evolución, como lo vemos en ratas SHR de más de 20 meses de edad (se debe tener en cuenta que el promedio de vida de estas ratas es de 24 meses) se aprecia una disminución de la función sistólica como lo muestra la figura 1547 asociado a evidencias clínicas de insuficiencia cardíaca como el aumento de la frecuencia respiratoria, expresión de disnea y a un incremento del peso de los pulmones por congestión secundaria a la claudicación ventricular izquierda.
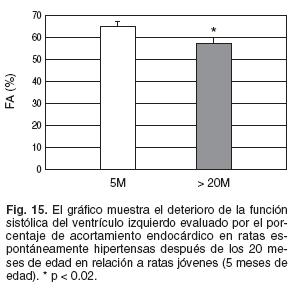
El deterioro de la función ventricular se produce como consecuencia por un lado de la alteración en disponibilidad de calcio en el miocito provocada entre otras causas por la disminución de la actividad y/o expresión de SERCA;48 por la modificación de la sensibilidad de las proteínas contráctiles a la concentración de calcio42 y por la muerte programada de las células contráctiles (apoptosis).49 La matriz extra-celular participa de alguna forma de esa alteración como resultado de una mayor actividad de las metaloproteinasas que degradan el colágeno 1 favoreciendo el deslizamiento de las células y la alteración en la integración de la fuerza realizada por cada miocito.50
Conclusión
Existe todavía una gran cantidad de caminos que no han sido recorridos y algunos ni imaginados en el escenario de la hipertrofia ventricular. Si bien las diferentes formas de hipertrofia cardíaca pueden resultar de una combinación de factores genéticos, fisiológicos y ambientales, los mecanismos moleculares subyacentes que inducen respuestas fisiológicas o patológicas no están aún totalmente dilucidados.
En un verdadero desafío a lo conocido sería correcto especular con la necesidad de estimular el desarrollo de hipertrofia fisiológica en determinadas situaciones patológicas o llegar a modificar la respuesta patológica y transformarla en fisiológica.
Referencias
1. Frey N, Olson EN: Cardiac hypertrophy: the good, the bad and the ugly. Annu Rev Physiol 2003; 65: 45-79. [ Links ]
2. Russel B, Motlagh D, Ashley WW: Form follows function: How muscle shape is regulated by work. J Appl Physiol 2000; 88: 1127-1132. [ Links ]
3. Sadoshima J, Izumo S: The cellular and molecular response of cardiac myocytes to mechanical stress. Annu Rev Physiol 1997; 59: 551-571 [ Links ]
4. Urbanek K, Quaini F, Tasca G, Torella D, Castaldo C, Nadal-Ginard B, et al: Intense myocyte formation from cardiac stem cells in human cardiac hypertrophy. Proc Nati Acad Sci USA 2003; 100(18): 10440-10445. [ Links ]
5. Devereux RB, Savage DD, DRayer JIN, Laragh JH: Left ventricular hypertrophy and function in high-, normal-, and low-renin forms of essential hypertension. Hypertension 1982; 4: 524-531. [ Links ]
6. Devereux RB, Lutas EM, Cásale PN, Kligfield P, Eisenberg RR, Hammond IW, et al: Standarization of M-Mode echocardiographic left ventricular anatomic measurements. J Am Coll Cardiol 1984; 4: 1222-1230. [ Links ]
7. Levy D, Anderson KM, Plehn J, Savage DD, Christiansen JC, Castelli WP: Echocardio graphically determined left ventricular structural and functional correlates of complex or frequent ventricular arrhythmias on one-hour ambulatory electro cardio graphic monitoring. Am J Cardiol. 1987; 59(8): 836-840. [ Links ]
8. Levy D, Savage DD, Garrison RJ, Anderson KM, Kannel WB, Castelli WP: Echocardio graphic criteria for left ventricular hypertrophy: The Framingham heart study. Am J Cardiol 1987; 59: 956-960. [ Links ]
9. Koren MJ, Devereux RB, Cásale PN, Savage DD, Laragh JH: Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991; 114(5): 345-352. [ Links ]
10. Ganau A, Devereux RB, Roman MJ, De Simone G, Pickering TG, Saba PS, et al: Patterns of left ventricular hypertrophy and geometric remodeling in essential hypertension. J Am Coll Cardiol 1992; 19: 1550-1558. [ Links ]
11. Marcus R, Krause L, Weder AB, Domínguez -Meja A, Schork NJ, Julius S: Sex-specific determinants of increased left ventricular mass in the Tecumseh Blood Pressure Study. Circulation 1994; 90(2): 928-936. [ Links ]
12. Liao Y, Cooper RS, McGee DL, Mensah GA, Ghali JK: The relative effects of left ventricular hypertrophy, coronary artery disease, and ventricular dysfunction on survival among black adults. JAMA 1995; 273: 1592-1597. [ Links ]
13. Jarzembowski TM, JanickiPK, SukernikMR: Presence of concentric left ventricular remodeling and concentric left ventricular hypertrophy are associated with increased intraoperative fluid administration during large bowel surgery. Anesthesiology 2005; 103: A446. [ Links ]
14. Lang RM, Bierig M, Devereux RB, Flachs kampf FA, Foster E, Pellikka PA, et al: Chamber Quantification Writing Group; American Society of Echo cardio graphy's Guidelines and Standards Committee; European Association of Echocardio graphy. Recommendations for chamber quantification: a report from the American Society of Echo cardiography's Guidelines and Standards Committee and the Chamber Quantification Writing Group, developed in conjunction with the European Association of Echocardio graphy, a branch of the European Society of Cardiology. J Am Soc Echocardiogr 2005; 18(12): 1440-1463. [ Links ]
15. Escudero EM, de Lena S, Cingolani HE: Estructura y función del ventrículo izquierdo en jóvenes estudiantes varones de la Universidad Nacional de La Plata con hipertensión arterial en estadio I. Medicina 1997; 57: 181-190. [ Links ]
16. Escudero EM, De Lena S, Graff-Iversen S, Almiron M, Cingolani HE: Left ventricular diastolic function in young men with high normal blood pressure. Can J Cardiol 1996; 10: 959-964. [ Links ]
17. Devereux RB, Reichek N: Echo cardiographic determinations of left ventricular mass in man: anatomic validation of the method. Circulation 1977; 55: 613-618. [ Links ]
18. Yamazaki T, Komuro I, Yazaki Y: Role of the rennin - angiotensin system in cardiac hypertrophy. Am J Cardiol 1999; 83: 53H-57H. [ Links ]
19. Garciarena CD, Ennis IL, Escudero EM, Pérez NG, Cingolani HE: La regresión de la hipertrofia cardíaca inducida por inhibición del NHE-1 se acompaña de disminución de la expresión de calcineurina A/3. Medicina 2005; 65(Supl. II): 181-182. [ Links ]
20. Ennis IL, Escudero EM, Pérez NG, Camilión de Hurtado MC, Cingolani HE: Regression of isoproterenol induced myocardial hypertrophy by Na+/H+ exchanger inhibition. Hypertension 2003; 41(6): 1324-1329. [ Links ]
21. Aiello EA, Villa-Abrille MC, Escudero EM, Portiansky EL, Pérez NG, Camilión de Hurtado MC, et al: Myocardial hypertrophy of normotensive Wistar-Kyoto rats. Am J Physiol Heart Circ Physiol 2004; 286: H1229-H1235. [ Links ]
22. Pérez NG, Escudero EM, Portianski EL, Camilión de Hurtado MC, Cingolani HE. Regression andprevention of hypertrophy and fibrosis by Na+/H+ exchange inhibition. J Mol Cell Cardiol 2002; 34: A 17. [ Links ]
23. Pérez NG, Piaggio MR, Ennis IL, Garciarena CD, Morales C, Escudero M, et al: Phosphodiesterase 5A Inhibition induces Na+/H+ exchanger blockade and protection against myocardial Infarction. Hypertension. 2007; 49: 1095-1103. [ Links ]
24. Cingolani HE, Rebolledo OR, Portiansky EL, Pérez NG, Camilión de Hurtado MC. Regression of hypertensive myocardial fibrosis by Na+/ H+ exchange inhibition. Hypertension 2003; 41(2): 373-377. [ Links ]
25. Escudero EM, Tufare AL, Rebolledo O, Pellegrini L, Lobrutto C: Serum carboxyl-terminal propeptide of procollagen type I in exercise-induced left ventricular hypertrophy. Clin Cardiol 2004; 27(8): 471-474. [ Links ]
26. Kannel WB, Dauenberg AL, Levy D: Population implications of electrocardiographic left ventricular hypertrophy. Am. J Cardiol 1987; 60: 851-931. [ Links ]
27. Levy D, Garrison RJ, Savage DD: Prognostic implications of echocardiographically determined left ventricular mass in the Framingham Heart Study. N Engl J Med 1990; 322: 1561-1566. [ Links ]
28. Levy D, Salomon M, D'Agostino RB, Belanger AJ, Kannel WB: Prognostic implications of baseline electrocardiographic features and their serial changes in subjects with left ventricular hypertrophy. Circulation, 1994; 90: 1786-1793. [ Links ]
29. Casale PN, Devereux RB, Milner M, Zulio G, Harshfield GA, Pickering TG, et al: Value of echocardio graphic measurement of left ventricular mass in predicting cardiovascular morbid events in hypertensive men. Arch Intern Med 1986; 105: 173-178. [ Links ]
30. Schillaci G, Verdecchia P, Porcellati C, Cuccurullo O, Cosco C, Perticone F: Continuous relation between left ventricular mass and cardiovascular risk in essential hypertension. Hypertension 2000; 35: 580-586. [ Links ]
31. Brown DW, Giles WH, Croft JB. Left ventricular hypertrophy as a predictor of Coronary Heart Disease Mortality and the effect of hypertension. Am Heart J 2000; 14: 848-856. [ Links ]
32. East MA, Jollis JG, Nelson CL, Marks D, Peterson ED: The influence of left ventricular hypertrophy on survival in patients with coronary artery disease: Do race and gender matter? J Am Coll Cardiol 2003; 41: 949-954. [ Links ]
33. Ghali JK, Liao Y, Cooper RS: Influence of left ventricular geometric patterns on prognosis in patients with or without coronary artery disease. J Am Coll Cardiol 1998; 31: 1635-1640. [ Links ]
34. Palmon LC, Reichek N, Yeon SB, Clark NR, Brownson D, Hoffman E, et al: Intramural myocardial shortening in hypertensive left ventricular hypertrophy with normal pump function. Circulation 1994; 89(1): 122-31. [ Links ]
35. Lutas EM, Devereux RB, Reís G, Alderman MH, Pickering TG, Borer JS, et al: Increased cardiac performance in mild essential hypertension: left ventricular mechanics. Hypertension 1985; 7: 979-988. [ Links ]
36. Shimuzu G, Hirota Y, Kita Y, Kawamura K, Saito T, Gaasch WH: Left ventricular midwall mechanics in systemic arterial hypertension: myocardial function is depressed in pressure-overload hypertrophy. Circulation 1991; 83: 1676-1684. [ Links ]
37. Devereux RB, Roman MJ, Palmieri V, Okin PM, Boman K, Gerdts E, et al: Left ventricular wall stresses and wall stress-mass-heart rate products in hypertensive patients with electrocardiographic left ventricular hypertrophy: The LIFE study. J Hypertension 2000; 18: 1129-1138. [ Links ]
38. Aurigemma GP, Silver KH, Fox MA, Gaasch WH: Depressed midwall and long axis shortening in hypertensive left ventricular hypertrophy with normal ejection fraction. J Am Coll Cardiol 1995; 26: 195-202. [ Links ]
39. Escudero EM, Tufare AL, Ennis IL, Garciarena CD, Pinilla O A, Carranza VB: Análisis ecocardiografico del efecto de diferentes inhibidores del intercambiador Na+/H+ sobre la estructura y función sistólica del ventrículo izquierdo en ratas espontáneamente hipertensas. Medicina 2006; 66: 392-398. [ Links ]
40. D'hooge J, Heimdal A, Jamal F, Kukulski T, Bijnens B, Rademakers F, et al: Regional strain and strain rate measurements by cardiac ultrasound: principles, implementation and limitations. Eur J Echocardiogr 2000; 1(3): 154-170. [ Links ]
41. Tufare AL, Escuero EM, Ankudowicz V: Deterioro temprano de la contractilidad en la hipertrofia secundaria a hipertensión. Revista FAC 2005; 34 (Supl. II): 53. [ Links ]
42. Pérez NG, Hashimoto K, McCune S, Altschuld RA, Marbán E: Origin of contractile dysfunction in heart failure: calcium cycling versus myofilaments. Circulation 1999; 99: 1077-1083. [ Links ]
43. Molkentin JD, Lu JR, Antos CL, Markham B, Richardson J, Robbins J, et al: A calcineurin-dependent transcriptional pathway for cardiac hypertrophy. Cell 1998; 93: 215-228. [ Links ]
44. Cingolani OH, Yang X-P, Cavasin MA, Carretero O A: Increased systolic performance with diastolic dysfunction in adult spontaneously hypertensive rats. Hypertension 2003; 41(2): 249-254. [ Links ]
45. Vasan RS, Benjamin EJ, Levy D: Congestive heart failure with normal left ventricular systolic function. Clinical approaches to the diagnosis and treatment of diastolic heart failure. Arch Intern Med 1996; 156(2): 146-157. [ Links ]
46. Mandinov L, Eberli FR, Seiler C, Hess OM: Diastolic Heart Failure. Cardiovasc Res 2000; 45(4): 813-825. [ Links ]
47. Tufare AL, Escudero EM, Camilión de Hurtado MC: Hipertrofia ventricular izquierda y progresión a la insuficiencia cardíaca en ratas espontáneamente hipertensas. XI Congreso Argentino de Hipertensión Arterial. 6-9 de Mayo 2004, Buenos Aires, Argentina. [ Links ]
48. Matsui H, MacLennan DH, Alpert NR, Periasamy M: Sarcoplasmic reticulum gene expression in pressure overload-induced cardiac hypertrophy in rabbit. Am J Physiol 1995; 268 (1 Pt 1): C252-258. [ Links ]
49. Williams RS: Apoptosis and Heart Failure. N Engl J Med 1999; 341(10): 759-760. [ Links ]
50. Ahmed SH, Clark LL, Pennington WR, Webb CS, Bonnema DD, Leonardi AH, et al: Matrix metalloproteinases/tissue inhibitors of metalloproteinases: relationship between changes in proteolytic determinants of matrix composition and structural, functional, and clinical manifestations of hypertensive heart disease. Circulation 2006; 113(17): 2089-2096. [ Links ]














