Services on Demand
Journal
Article
Indicators
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos de cardiología de México
On-line version ISSN 1665-1731Print version ISSN 1405-9940
Arch. Cardiol. Méx. vol.77 n.3 Ciudad de México Jul./Sep. 2007
Investigación clínica
Biopsia endomiocárdica. Revisión y experiencia de 176 procedimientos
Endomiocardial biopsy. Revision and experience of 176 procedures
Raúl San Luis-Miranda,* José Luis Lázaro-Castillo,* Jaime Munayer-Calderón,** Hornero A. Ramírez-Reyes,* Laura Arias-Monroy,*** Tomás Aldana-Pérez,* Antonio Amaya-Hernández,* José Luis León-Ávila,* Guillermo Gómez-Campos****
* Médico adscrito al Servicio de Hemodinamia.
** Jefe de Servicio de Hemodinamia.
*** Médico adscrito a Cardiopediatría. Unidad Médica de Alta Especialidad Dr. Antonio Fraga Mouret Centro Médico La Raza.
**** Médico patólogo. Unidad Médica de Alta Especialidad Dr. Gaudencio González Garza Centro Médico La Raza. Instituto Mexicano del Seguro Social
Correspondencia:
Dr. Raúl San Luis Miranda.
Unidad Médica de Alta Especialidad. Dr. Gaudencio González Garza.
Centro Médico La Raza. 4° piso
Departamento de Hemodinámica.
Vallejo Esq. Jacarandas s/n Col. La Raza,
México D.F.
Tel: 57 24 59 00 ext. 23442 y 23443 (Hospital).
E-mail: dr_sanluiscardio@yahoo.com.mx
Recibido: 10 de abril de 2006
Aceptado: 09 de mayo de 2006
Resumen
La biopsia endomiocárdica, es de ayuda diagnóstica para diversas cardiopatías. Se realizaron 176 procedimientos en 65 pacientes, 43 masculinos y 22 femeninos, edad 29.8 ±11.5 años (4 días a 66 años). En el grupo A (n = 26) pacientes postrasplante cardíaco, se realizaron 137 procedimientos, 39 en trasplante heterotópico y 98 ortotópico. En el grupo B integrado por 39 pacientes con cardiopatías diversas, se realizaron 39 procedimientos. El acceso fue por vía yugular en 3 pacientes (1.7%), la vía femoral se utilizó en 173 (98.3%) pacientes; 168 (95%) por vía venosa; vía arterial en 5 (2.5%). Se presentaron complicaciones mayores en 3 pacientes (1.7%). La biopsia endomiocárdica tiene una morbilidad y mortalidad muy baja. La ayuda diagnóstica histológica para la decisión terapéutica en el grupo A fue del 100%. En pacientes postrasplante cardíaco hay una mortalidad de 0% y complicaciones graves en el 1.7% tales como enfermedad vascular cerebral (EVC) y fístula coronaria derecha al ventrículo derecho. La vía de acceso más frecuentemente utilizada en nuestra serie fue la vía venosa femoral.
Palabras clave: Biopsia endomiocárdica. Trasplante heterotópico. Trasplante ortotópico.
Summary
Endomyocardial biopsy (EB) is often used in the clinical evaluation of several cardiac disease. Hundred-seventy-six consecutive procedures were performed in 65 patients, 43 men and 22 women mean age was 29.86 ± 11.53 (range 4 days to 66 years). Group A, 26 post-cardiac transplantation patients in whom 137 EB were performed (39 heterotopic and 98 orthotopic), average sample 5.2 biopsy for each patient. Group B (n = 39) was studied for several cardiac diseases during cardiac diagnostic catheterism. The jugular venous approach was performed in 3 patients (1.7%), femoral in 173 patients. Major complications were found in 3 (1.7%) cases consisting in cerebrovascular accident (stroke) and coronary fistula into the right ventricle. Endomyocardial biopsy provides a low incidence of adverse reactions, mortality was 0%.
Key words: Endomyocardial biopsy. Heart transplatation. Heterotopic and orthotopic heart transplatation.
Introducción
La biopsia endomiocárdica (BE) obtenida por vía percutánea fue descrita por Sakakibara S. en 1962.1 El procedimiento se ha perfeccionado y debido a un mayor conocimiento histopatológico, ha logrado colocarse como estudio de ayuda diagnóstica para la evaluación de pacientes con diversas cardiopatías.2 En 1984 la OMS establece a la BE como de utilidad, considerando que permite confirmar el diagnóstico clínico sospechado, al mostrar hallazgos anatomopatológicos los cuales llegan a ser de gran utilidad, sin embargo la BE puede no aportar ningún dato específico sobre la sospecha clínica y en algunos casos pueden ser mayores los riesgos que el beneficio.3 La indicación actual de la BE llega a ser concluyente en los pacientes trasplantados en quienes el adecuado y preciso diagnóstico histopatológico de rechazo junto al efecto de la medicación inmunosupresora ha llevado a una sobrevida de estos pacientes al año del 85 y un 75% a los cinco años. Después de múltiples estudios y reportes histopatológicos la Sociedad Internacional de Trasplante Cardíaco ha establecido y difundido los criterios histopatológicos que definen el <<rechazo>> de forma precisa y uniforme, por lo cual llega ser incuestionable la utilidad de este estudio en estos casos.4-8 Al igual que en otras unidades donde se realiza trasplante cardíaco en nuestro hospital la BE es el estudio de rutina ante la sospecha precoz del rechazo cardíaco así como también del control seriado y posterior a las dosis extras de drogas inmunosupresoras.
La BE se llega también a realizar en pacientes con diagnóstico de miocardiopatías diversas, entre ellas la miocardiopatía dilatada con el fin de descartar probable etiología viral y severidad de proceso inflamatorio, sin embargo, los reportes de confirmación de miocarditis por BE aun con los mayores avances tecnológicos llega a ser en promedio de un 54%; esta baja incidencia diagnóstica asociada al aún controvertido manejo con inmunosupresores ha llevado a cuestionar la indicación de este procedimiento en este tipo de alteraciones.9-16 Otras indicaciones establecidas son el monitoreo de cardiotoxicidad por antracíclicos, cardiomiopatías primaria (hipertrófica-restrictiva), secundarias (amiloidosis - hemocromatosis - sarcoidosis - fibrosis endomiocárdica) así como en el estudio de diversos tumores intracardíacos, en donde la certeza diagnóstica varía dependiendo del caso sin embargo se han descrito varios estudios17-22 en donde se confirma la efectividad de la BE para diversas miocardiopatías.
Masón y O'Connell establecen que las indicaciones para la BE pueden ser:23-28
a) Definitivas: monitoreo trasplante cardíaco y cardiotoxicidad por quimioterapia (antracíclicos).
b) Posibles: diagnóstico de miocardiopatías secundarias, detección y monitoreo de miocarditis, miocardiopatía hipertrófica y de fibrosis endomiocárdica).
c) Dudosas: (para pronóstico en miocardiopatías dilatadas idiopáticas).
En un futuro, con los avances en el estudio histopatológico la BE podrá aportar mayor información, con lo que se ampliarían las indicaciones de este estudio.29,30
El procedimiento puede llevarse a cabo vía yugular interna (técnica Satnford-Mason) y vena femoral para muestra de ventrículo derecho (Vd), y por la arteria femoral para el ventrículo izquierdo (Vi) con la técnica de Seldinger modificada31-34 en ambos casos se realiza con control fluoroscópico en los laboratorios de hemodinámica como procedimiento aislado o como complemento de valoración hemodinámica y angiográfica de la cardiopatía de base. Se describe por algunos autores la realización de BE de Vd vía yugular interna en las unidades de cuidado intensivo o intermedio mediante control de ecocardiograma transtorácico (ETT) con buenos resultados.35-40 A partir de los años 80 con el perfeccionamiento de los introductores y biotomos41-44 ha sido más fácil el abordaje y la realización de la BE, sin embargo, el procedimiento tiene riesgos, describiéndose la posibilidad de complicaciones en el 0.13 al 4% de los estudios, siendo los más frecuentes, arritmias (fibrilación auricular y ventricular 1%), reacción vasovagal (0.6%), perforación-hemopericardio - taponamiento cardíaco de (0.7%), perforación del septum interventricular (0.3%), fístulas coronarias (0.3%), neumotorax, lesión del nervio laringorrecurrente, disección, trombosis periférica, enfermedad vascular cerebral tipo embólica, muerte (0.05 al 0.7%).45-48
Hay que informar siempre a los familiares sobre estas posibles complicaciones, sin embargo también hay que considerar que en un alto porcentaje estos riesgos están en relación directa con el número de biopsias tomadas, la técnica utilizada y la experiencia del operador. Una complicación descrita y en ocasiones poco valorada es el incremento paulatino de la insuficiencia la tricúspide (IT) posterior a varias BE seriadas.49-51 Sabemos que la IT se presenta <<per se>> en pacientes trasplantados, sin embargo el traumatismo directo, continuo, realizado por las camisas y biotomos, llegan a lesionar el aparato valvular y subvalvular. Se menciona en diversos estudios que los factores que afecta la incidencia y severidad de la IT son: a) grado-severidad de rechazo, b) número de BE y de muestras, c) tamaño del corazón donante. La IT post BE es una complicación en la cual el ETT llega a ser de gran utilidad para evitar que se presente o se incremente, ya que durante el procedimiento permite una visualization directa de las estructuras anatómicas (valvular y subvalvular de la tricúspide) involucradas, guiando al operador, para evitar una lesión directa al mismo tiempo que apoyaría a seleccionar el sitio para la toma de muestras.52-54
Es muy importante el considerar al ETT como apoyo durante la BE principalmente en pacientes con factores positivos descritos previamente y la presencia de IT que ha incrementado posterior a procedimientos previos.
La BE tiene limitaciones potenciales como es la obtención de muestras insuficientes y/o no adecuadas (menor de 1.5 mm o cuando el tejido obtenido se compone principalmente de endocardio o tejido fibroso de sitios de biopsias previas). Así mismo no hay que olvidar que por ser un procedimiento <<a ciegas>> donde las muestras obtenidas pueden ser áreas de miocardio aun sin cambios histopatológicos característicos o poco específicos. Si la BE tomada posee características adecuadas para su estudio histológico es probable que ayude a diagnosticar y clasificar en forma definitiva la enfermedad, brindando con esto el beneficio al paciente. Se describe que la BE permite un porcentaje de ayuda diagnóstica que va del 15 al 67% en el estudio de cardiomiopatías y de un 100% para el control del trasplante cardíaco y cardiotoxicidad por antracíclicos.56-58 Es muy importante el realizar un análisis del diagnóstico previo a la indicación de una BE, para valorar riesgo beneficio. Como se mencionó anteriormente en un gran número de casos, la necesidad de cateterismo cardíaco como estudio de la cardiopatía de base, lo cual permite realizar la BE en el mismo estudio.
Objetivo
Análisis de las BE realizadas en diversas cardiopatías, establecer la frecuencia, número de procedimientos, técnica(s) utilizada(s), calidad de muestras obtenidas, resultado por patología y complicaciones.
Material y métodos
En el Servicio de Hemodinámica del Hospital General Centro Médico Nacional <<La Raza>> en México, de enero de 1995 a diciembre de 2004 se sometieron 65 pacientes a 176 BE, se analiza edad, sexo, diagnóstico, número de biopsias/ paciente, vía de acceso femoral-yugular, venosa-arterial, calidad de las muestras, complicaciones y reporte de patología.
La indicación clínica del procedimiento fue apoyada por lo descrito por Masón y en lo establecido en el protocolo de manejo del paciente trasplantado en nuestra unidad (Tabla I). El estudio se realiza en forma programada, con ayuno previo de 6 h para los pacientes pediátricos y 8 h para los adultos. No se indicó ningún manejo preanestésico. La BE se realizó bajo vigilancia y monitoreo continuo, administrando en niños sedación con base narcótica de midazolam 100 µg/kg/dosis y fentanyl 1 mg/kg más la administración local de xilocaína al 1%; en adultos el procedimiento se realizó sólo con anestesia local y en algunos casos con la administración de midazolam.

La selección de la vía de acceso fue elegida por el médico a cargo del procedimiento, en base al diagnóstico y lo solicitado para su estudio. La utilización de la vena yugular interna se realizó por los lincamientos de Satnford descrita por Masón y el abordaje de la vía femoral se realizó mediante la técnica de Seldinger modificada. Se obtuvieron de 3 a 5 muestras por estudio, tratando que éstas fueran igual o mayores a 1.5 mm, (calidad macroscópica adecuada). Cuando la vía de acceso fue arterial se administró heparina 100 UI/kg/dosis o 5,000 UI IV dosis única posteriores a la toma de las muestras. Se dividió a los pacientes en dos grupos: Grupo A, pacientes con trasplante de corazón (TC) y grupo B, pacientes con cardiomiopatías diversas (CD) (Fig. 1).

Resultados
De enero de 1985 a diciembre de 2004 se realizó en el Servicio de Hemodinámica 6,634 estudios de cateterismo diagnóstico-terapéutico, de éstos, 176 correspondieron a BE (2.6%), las cuales se realizaron en 65 pacientes siendo del sexo masculino 43 (66%) y femenino 22 (34%), con rango de edad de 4 días a 66 años (media 29.86 ± 11.53 y mediana de 34.25 años). En el grupo A compuesto por 26 pacientes se realizaron 137 BE, siendo 39 en trasplante heterotópico (PTH) y 98 en ortotópico (PTO), con un promedio de 5.2 BE por paciente (Tabla II).

Las 39 BE restantes correspondieron a pacientes con cardiopatías diversas (grupo B) las cuales se realizaron durante el estudio de cateterismo para valoración hemodinámica (presión arterial pulmonar, cuñas, coronariografía, relación de gastos y resistencias vasculares).
Se optó como vía de acceso inicial la vía yugular en 5 pacientes (2.5%); se realizó en forma adecuada y exitosa en 3 pacientes (60%); en 2 (40%) no fue posible completar el procedimiento, debido a que presentaban cuello corto, obesidad, intranquilidad por dolor en el sitio de acceso, optando por la vía femoral, logrando completar el estudio sin complicaciones.
El total de procedimientos vía femoral (arterial y venosa) fue de 173 (98%). Vía arteria femoral en 5 casos (2.5%). La vena femoral como acceso inicial se utilizó en 166, sin embargo incluyendo los dos fracasos por vía yugular el número total de BE vía vena femoral fue de 168 (95%). De todas las BE por vía femoral en 5 (2.5%) se presentó dificultad para la colocación del equipo o toma de muestra; esto en 4 pacientes trasplantados con múltiples cateterismos venosos en donde existía una gran fibrosis en la región, abordando la vena contralateral, y en otro no se logró introducir el equipo por vía venosa, optando la arterial. Sólo en un paciente (0.56%) portadora de cardiomiopatía hipertrófica restrictiva de probable origen infiltrativo de 14 años, no fue posible tomar la biopsia ya que durante el paso de la camisa presentó bloqueo AV completo ameritando colocar marcapaso temporal, restableciendo ritmo de sinusal de base 30 minutos después, optando por suspender el procedimiento.
Se realizó en total 5 BE izquierdas en pacientes PTH en quienes se encontró imposibilidad por la vía venosa al paso en la anastomosis auricular o por quedar con estenosis y en un caso por la presencia de un gran trombo en la aurícula derecha del corazón donante, logrando realizar y completar la BE en forma satisfactoria.
Complicaciones menores. Se presentaron en 5 pacientes (2.8%). Un paciente con arritmias tipo extrasístoles ventriculares frecuentes, transitorias, y bloqueo AV completo transitorio. Dos casos con hematoma y dos con trombosis de la vena femoral, ameritando sólo uno de ellos manejo quirúrgico.
Complicaciones mayores. Se presentaron en 3 casos (1.7%), dos con enfermedad vascular cerebral (EVC) tipo embólico, ambos pacientes con trasplante heterotópico en quienes se realizó la BE por vía arterial, en uno el evento se presentó con sintomatología ya concluido el procedimiento, remitiendo los signos a las 30 h sin secuela alguna; en el segundo paciente el fenómeno embólico se presentó al caer la cuerda guía al Vi nativo, el cual se encontraba muy dilatado en el intento de canular la neo-aorta, con signos y síntomas típicos inmediatos, dejando como secuela hemiplejía. El ecocardiograma postbiopsia mostró la presencia de un trombo en Vi del corazón nativo que no se había observado previamente. En un paciente se observó fístula coronaria izquierda (descendente anterior) al ventrículo derecho, encontrando una PSAP 35 mm Hg y relación de gastos de 1.4:1 (Fig. 2). Hay que mencionar que las complicaciones mayores sólo se presentaron en BE de pacientes postrasplante de corazón, en tanto que las BE realizadas en el grupo de cardiomiopatías diversas fue del 0%, aun en el paciente de 4 días de vida. Con relación a la vía de acceso y complicaciones; por vía yugular fueron del 0%, vía arterial femoral del (27%) y vena femoral (3.5%). No se presentó ningún caso de incremento de insuficiencia tricuspídea postbiopsia endomiocárdica.

Durante cada BE se tomaron de 3 a 5 muestras (total 796), las cuales fueron colocadas inmediatamente en un frasco con solución formol al 10% enviadas a patología, donde se realiza tinción de hematoxilina-eosina, tricrómico de Masson. A pesar de que fueron reportadas 56 muestras (9%) como insuficientes, con presencia de endocardio y/o muestra pequeña, se pudo realizar el estudio histológico gracias al número de biopsias tomadas en cada caso.
En pacientes PTC (Grupo A) la ayuda diagnóstica fue del 100% permitiendo al equipo de trasplante normar conducta de manejo inmunosu-presor, como se muestra en la Tabla III el grado más frecuentemente encontrado fue 1 B [n = 77 (56%)].

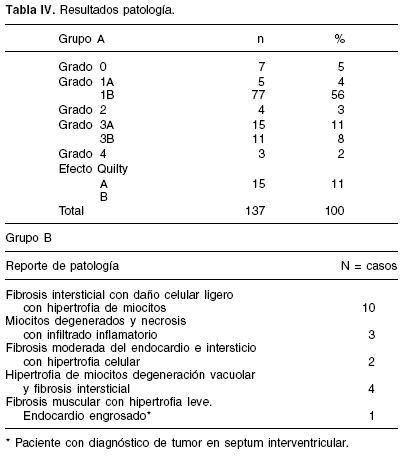
En el grupo de cardiomiopatías diversas (Grupo B) el reporte de patología se describe en la Tabla IV y éste fue integrado al análisis clínico de cada paciente para completar su estudio y posibilidad diagnóstica. Sólo se describe el reporte de patología de 20 pacientes, ya que éstos provienen de otros hospitales. Es importante señalar que en los 6 pacientes con diagnóstico de tumor la BE no aportó ayuda para confirmación diagnóstica histopatológica.
Discusión
Desde la descripción por Kono en 1962 de la BE se ha utilizado cada día con mayor frecuencia como estudio en la evaluación histopatológica del miocardio, permitiendo una visión de la patogénesis y etiología de diversas enfermedades cardiovasculares. En 1974 Caves describió a la BE como método diagnóstico en la evaluación del rechazo en pacientes trasplantados de corazón, el mayor número de nuestros procedimientos se realizó como protocolo de estudio-control de estos pacientes. La vía de acceso por vía yugular se realizó sólo en 5 casos y fue exitosa sólo en 3 (60%) de los casos. Nosotros consideramos que la vía yugular es de primera elección para la BE en trasplante ortotópico, sin embargo por la necesidad de frecuentes estudios es necesario alternarla con la vía femoral. La BE en pacientes PTH puede realizarse tanto por vía yugular como femoral, sin embargo debido a la necesidad de una mayor manipulación en la búsqueda de la anastomosis intra-auricular y colocación de la camisa al Vd donado, lo sitúa al procedimiento como de mayor dificultad técnica, por estas razones nosotros en pacientes PTH utilizamos preferentemente la vía femoral, sin embargo en algunos casos la imposibilidad del paso por la anastomosis intra-auricular ya sea por posición (situación espacial) y/o obstrucción de la misma no se logra pasar al ventrículo derecho donado, obligando en estos casos la realización de la BE del Vi por vía arterial femoral, así la toma de BE de Vi en PTH es una alternativa viable y efectiva en todos los casos.
La BE como estudio de cardiomiopatías diversas puede realizarse indistintamente tanto por vía venosa yugular o femoral, cada caso deberá individualizarse; sin embargo, debido a la necesidad de cateterismo (vía femoral) como estudio complementario, la BE se realiza durante el mismo estudio hemodinámico.
La posibilidad de realizar en forma efectiva y exitosa una BE por vía femoral venosa es de 99.3%, similar a lo reportado en la literatura. Por vía yugular el porcentaje de éxito fue del 60%, sin embargo esto último como ya se mencionó resulta muy bajo, y se debe considerar que la muestra es pequeña. Se reporta en la literatura una mayor posibilidad tanto de fracaso como de complicaciones (> 12%) por vía yugular en comparación con la femoral. Las muestras obtenidas en los 176 procedimientos permitieron el estudio histopatológico en todos los casos, a pesar de que el 9% de las muestras fueron reportadas como no adecuadas, por esto consideramos la necesidad de tomar más de 3 muestras, realizando un análisis macroscópico durante su extracción para tratar de asegurar su calidad y su utilidad por patología. Las complicaciones descritas durante la BE son bajas, desde 0.1 al 2% siendo las más frecuentes la perforación cardíaca, hemopericardio, tamponade, arritmias, embolización sistémica y muerte. Nosotros encontramos que la BE realizada en pacientes con cardiomiopatías diversas presentó una morbilidad y mortalidad del 0%, similar a lo reportado en la literatura, aun en la etapa neonatal. Sin embargo, las complicaciones se presentaron en pacientes trasplantados, siendo las más frecuentes la presencia de un hematoma residual, trombosis de vena femoral, arritmias, cifras proporcionales a lo descrito por Bhargavara y Sekiguchi. Se presentaron 2 embolismos cerebrales en pacientes PTH, un caso relacionado directamente al procedimiento y el segundo debido a que el corazón nativo se encontraba muy dilatado con severa disfunción ventricular izquierda con trombos intracavitarios los cuales fueron movilizados durante el procedimiento, siendo por esta razón que el ecocardiograma transtorácico debe realizarse previo a la biopsia con búsqueda intencionada de trombos, en todos los pacientes postrasplante de corazón y principalmente en aquéllos tipo heterotópico y en los que existan posibilidades de abordaje vía arterial antes de llevarlos a la toma de la BE izquierda. Un paciente (0.56%) desarrolló una fístula coronaria izquierda al ventrículo derecho, vista a los 2 años postrasplante en control de coronariografía de rutina, esto debido a BE frecuentes y a la toma múltiple en un mismo sitio de endomiocardio, a pesar del intento de cambiar el sitio y colocación del biotomo para la toma de muestras, es un riesgo potencial en pacientes múltiples biopsiados. No se presentó ningún caso de incremento de insuficiencia tricuspídea postbiopsia endomiocárdica inmediata.
Conclusiones
La BE en pacientes en adultos y niños (incluyendo recién nacidos) portadores de cardiomiopatías diversas puede realizarse simultáneamente durante el estudio de cateterismo-diagnóstico con una muy baja morbilidad y mortalidad.
La BE como estudio control en pacientes postrasplante de corazón se puede llegar a realizar efectivamente en todos los casos, presentando una mortalidad de 0%.59 Pacientes con PTH llegan a presentar mayor dificultad técnica y posibilidad de fenómenos embólicos, si el abordaje es arterial, por lo que es necesario el estudio ecocardiográfico reciente y ante la menor duda de trombos intracavitarios un ecocardiograma transesofágico.61-64
Para la BE por vía arterial en pacientes PTH, se debe realizar una valoración con ecocardiograma previa que descarte trombo intracavitario, administrar heparina inmediatamente después de canular la arteria manteniendo un sistema de infusión a presión continua para el lavado constante de la camisa con solución con heparina y aspiraciones continuas entre cada toma de muestras, todo ello para disminuir así la incidencia de embolismo.
La toma de más de 3 muestras durante el procedimiento, así como su análisis macroscópico, aumenta la posibilidad de que éstas sean adecuadas y útiles para su estudio histopatológico. La BE como estudio control en pacientes PTC permitió normar conducta terapéutica en el 100% de los casos.
Referencias
1. Sakakibara S, Konno S: Endomyocardicil biopsy. Jpn Heart J 1962; 3: 537-543. [ Links ]
2. Mason JW, Connell JB: Clinical merit ofendomyocardial biopsy. Circulation 1989; 79: 971-979. [ Links ]
3. Organización Mundial de la Salud. Comité de Expertos. Cardiomiopatías. Serie de informes Técnicos. 697. Ginebra, Suiza, 1984. [ Links ]
4. Billingham ME: The pathology of transplanted hearts. Sem Thorac Cardiovasc Surg 1990; 2(3): 223-240. [ Links ]
5. Fowles RE, Mason JW: Endomyocardial biopsy. Ann Intern Med 1982; 97: 885-894. [ Links ]
6. Munayer CJ: Biopsia endomiocárdica en la detección de complicaciones de trasplante cardíaco. En: Calderón M, Martínez E, Galvan J, Bonilla L: Trasplante de corazón. México. McGraw-Hill, Ed. 1998: 171-174. [ Links ]
7. Caves PK, Marshall HW: Serial transvenous biopsy of the transplanted human heart. Lancet 1974; 11: 821-824. [ Links ]
8. Fowles RE: Cardiac biopsy. New York. Futura Publishing. Ed. 1992. [ Links ]
9. Mason JW, John B, O' Connell JB: Clinical merit of endomyocardial biopsy. Circulation 1989; 79(5): 971-979. [ Links ]
10. Ferrans VJ, Roberts WC: Myocardial biopsy: A useful diagnostic procedure or only a research tool. Am J Cardiol 1978; 41: 965-967. [ Links ]
11. Popma JJ, Cigarroa RG, Buja LM, Hills LD: Diagnostic and prognostic utility of right-sided catheterization and endomyocardial biopsy in idiopathic dilated cardiomyopathy. Am J Cardiol 1989; 63: 955-958. [ Links ]
12. Mason JW: Endomyocardial biopsy: the balance of success and failure. Circulation 1985; 2: 185-188. [ Links ]
13. Mason JW, Billingham ME, Rica DR: Treatment of acute inflammatory miocarditis assisted by endomyocardial biopsy. Am J Cardiol 1980; 45: 1037-1044. [ Links ]
14. Yonesaka S, Becker AE: Dilated cardiomyopathy: diagnostic accuracy of endomyocardial biopsy. Br Heart J 1987; 58: 165-71. [ Links ]
15. Mason JW, Billingham ME, Rica DR: Treatment of acute inflammatory miocarditis assisted by endomyocardial biopsy. Am J Cardiol 1980; 45: 1037-1044. [ Links ]
16. Bristow MR, Mason JW, Billingham ME: Doxorubicin cardiomyopathy: Evaluation by phonocardiography, endomyocardial biopsy and cardiac catheterization. Ann Intern Med 1978; 88: 168-175. [ Links ]
17. Leatherbury L, Chandra RS, Shapiro SR, Perry LW: Value of endomyocardial biopsy in infants, children and adolescents with dilated orhypertrophic cardiomyopathy and myocarditis. J Am Coll Cardiol 1988; 12: 1547-54. [ Links ]
18. Camerini F, Salvi A, Sinagra G: Endomyocardial biopsy in dilated cardiomyopathy and myocarditis: which role? Int J Cardiol 1991; 31: 1-8. [ Links ]
19. Baandrup U, Olsen ECJ: Critical analysis of endomyocardial biopsies from patients suspected of having cardiomyopathy. Morphological and morphometric aspects. Br Heart J 1981; 45: 475-86. [ Links ]
20. Hoshino T, Fujiwara H, Kawai C, Hamashima Y: Myocardial fiber diameter and regional distribution in the ventricular wall of normal adult hearts, hypertensive hearts and hearts with hypertrophic cardiomyopathy. Circulation 1983; 67: 1109-16. [ Links ]
21. Nakayama Y, Shimizu G, Hirota Y: Functional and histopathologic correlation in patients with dilated cardiomyopathy: an integrated evaluation by multivariate analysis. J Am Coll Cardiol 1987; 10: 186-92. [ Links ]
22. Sánchez J, Perrone S, Torino A, Guevara E, Bustamante LM, Perez HR, et al: Seguridad de la biopsia endomiocárdica transyugular del ventrículo derecho guiada por ecocardio grafía bidimensional en pacientes postrasplante cardíaco. Rev Fed Arg Cardiol 1999; 28: 77-85. [ Links ]
23. Baandrup U, Oslen E: Critical analysis of endomyocardial biopsies from patients suspected of having cardiomyopathy. I: morphological aspects. Br Heart J 1981; 45: 475. [ Links ]
24. Shanez JG, Ghali J, Billingham ME: Interobserver variability in the pathologic interpretation of endomiocardial biopsy results. Circulation 1987; 75: 401-405. [ Links ]
25. Report ofWHO/ISFC task force on the definition and classification of cardiomyopathies. Br Heart J 1980; 44: 672-683. [ Links ]
26. Aretz HT: Myocarditis: The Dallas criteria. Hum Pathol 1987; 18: 619-24. [ Links ]
27. Seferovic PM, Maksimovic R, Vasiljevic JD: Endomyocardial biopsy: a meta-analysis of diagnostic value. Posgrad Med J 1994; 70: 21-7. [ Links ]
28. Mason JW: Techniques for right and left ventricular endomyocardial biopsy. Am J Cardiol 1978; 41: 887-892. [ Links ]
29. Tanganelli P, Di Lenarda A, Bianciardi G: Correlation between histomorphometric findings on endomyocardial biopsy and clinical findings in idiopathic dilated cardiomyopathy. Am J Cardiol 1989; 64: 504-6. [ Links ]
30. Tashiro A, Masuda T, Segawa I: Morphometric comparison of mitochondria and myofibrils of cardiomyocytes between hypertrophic and dilated cardiomyopathy. Arch A Pathol Anat Histopathol 1990; 416: 473-478. [ Links ]
31. Lurie PR, Fujita M, Neustein HB: Transvoscular endomyocardial biopsy in infants and small children: Description of a new technique. Am J Cardiol 1978; 42: 453-457. [ Links ]
32. Kawai CH, Kltaura Y: New endomyocardial biopsy catheter for the left ventricle. Am J Cardiol 1977; 40: 453-457. [ Links ]
33. Martínez -Ríos MA: Cateterismo cardíaco. 2a. ed. México. Trillas, 1997: 469-473. [ Links ]
34. Blomstrom-Lundqvist C, Noor AM, Eskilsson J, Persson S: Safety of transvenous right ventricular endomyocardial biopsy guided by two-dimensional echocardiography. Clin Cardiol 1993; 16:487-492. [ Links ]
35. French JW, Popp RL, Pltlick PT: Cardiac localization of transvascular bioptome using 2 dimensional echocardiography. Am J Cardiol 1983; 51: 219-224. [ Links ]
36. Pierand L, El Allaf D, D'Orio V, Demoulin JC, Carlier J: Two dimensional echocardiographic guiding of endomyocardial biopsy. Chest 1985; 6: 759-762. [ Links ]
37. Mortensen SA, Egleblad H: Endomyocardial biopsy guided by cross-sectional echocardiography. Br Heart J 1983; 50: 246-248. [ Links ]
38. Williams GA, Keintz RP, Habermehl KK, Nelson JG, Kennedy HL: Clinical experience with two dimensional echocardiography to guide endomyocardial biopsy. Clin Cardiol. 1985; 8(3): 137-140. [ Links ]
39. Ragni T, Martinelli L, Goggi C, Speziale G, Rinaldi M, Roda G, Pedrezolli C: Echocontrolled endomyocardial biopsy. J Heart Transplant 1990; 9: 538-542. [ Links ]
40. Caves PK, Shulz W, Dong E: New instrument for transvenous cardiac biopsy. Am J Cardiol 1974; 33(2): 264-267. [ Links ]
41. Holmgrem D, Solymar Bo, Sunnergardh J: Endomyocardial biopsy in heart- transplanted children: comparison of sheaths to guide biopsy forceps. Pediatr Cardiol 2004; 19: 410-413. [ Links ]
42. Lurie PR: Revision of pediatric endomyocardial biopsy technique. Am J Cardiol 1987; 60: 368-370. [ Links ]
43. Anderson JL, Marshall HW: The femoral venous approach to endocardial biopsy: Comparison with internal jugular and trans arterial approaches. Am J Cardiol 1984; 53: 833-837. [ Links ]
44. Parrillo JE: Transvenous endomyocardial biopsy. Chest 1986; 90: 155-157. [ Links ]
45. Rapport d' un Comité d' Experts de OMS: Les Myocardiopathies. Suisse: Organisation Mondiale de la Santé, 1984: 74. [ Links ]
46. Vasiljevic JD, Kanjuh V, Seferovic P, Olsen ECJ: Diagnostic endomyocardial biopsy findings in 160 consecutive patients: the Yugoslavian experience. Am J Cardiovasc Pathol 1990; 3: 199-207. [ Links ]
47. Decker JW, Hare JM, Baughamam LK: Complications of transvenous right ventricular endomyocardial biopsy in adults patients with cardiomyopathy: a seven-year survey of 546 consecutive diagnostic procedures in a tertiary referral center. J Am Coll Cardiol 1992; 19: 43-47. [ Links ]
48. Cooper DK, Frazer RC, Rose AG, Ayzenberg O, OldfieldGS, Hassoulas J, etal: Technique, complications, and clinical value of endomyocardial biopsy in patients with heterotopic heart transplant. Thorax 1982; 37: 727-731. [ Links ]
49. Hausen B, Albes JM, Rohde R, Demertzis S, Mugge A, Schafers H: Tricuspid valve regurgitation attributable to endomyocardial biopsies and rejection in heart transplantation. Ann Thorac Surg 1995; 59: 1134-1140. [ Links ]
50. Alberti E, Pinamonti B, Salvi A, Camerini F: Two dimensional echocardiographic monitoring during percutaneous endomyocardial biopsy. G Ital Cardiol 1987; 17: 201-205. [ Links ]
51. Weston MW: Comparison of costs and charges for fluoroscopic and echocardiographic-guided endomyocardial biopsy. Am J Cardiol 1994; 74: 840-843. [ Links ]
52. Hausen B, Albes JM, Rohde R, Demertzis S, Mugge A, Schafers H: Tricuspid valve regurgitation attributable to endomyocardial biopsies and rejection in heart transplantation. Ann Thorac Surg 1995; 59: 1134-1140. [ Links ]
53. Hsu D, Sptoniz H: Echocardiographic diagnosis of cardiac allograft rejection. Prog Cardiovasc Dis 1990; 33: 149-154. [ Links ]
54. Lewen M, Bryg R, Miller L, Williams G, Labovitz A: Tricuspid regurgitation by Doppler echocardiography after orthotopic cardiac transplant. A J Cardiol 1987; 59(15): 137-141. [ Links ]
55. Caves PK, Stinson EB, Billingham ME, Rider AK, Shumway EN: Diagnosis of human cardiac allograft rejection by serial cardiac biopsy. J Thorac Cardiovasc Surg 1973; 66: 461-469. [ Links ]
56. Fenoglio JJ, Ursell P, Kellog CF, Drusin RE, Weiss MB: Diagnosis and classification of myocarditis by endomyocardial biopsy. N Engl J Med 1983; 308(1): 12-18. [ Links ]
57. Parillo JE, Aretz HT, Palacios I, Fallón J, Block P: Use of transvenous myocardial biopsy to diagnose and accurately evaluate disease of the myocardium. Circulation 1984; 69(1): 93-101. [ Links ]
58. Baughman KL, Baumgartner WA, Reitz BA, Achuff SA: Monitoring of allograft rejection. Heart and heart-lung transplantation. Philadelphia, Saunders Co, 1990, p 162. [ Links ]
59. Reynolds T, Halfman M: The role of cardiac sonographer in the evaluation of the heart transplant recipient. J Am Soc Echocard 1989; 2(16): 431-438. [ Links ]
60. Hauptman PJ, Gass A, Goldman M: The role of echocardiography in heart transplantation. J Am Soc Echocard 1993; 6(5): 496-509. [ Links ]
61. Hsu D, Sptoniz H: Echocardiographic diagnosis of cardiac allograft rejection. Prog Cardiovasc Dis 1990; 33(3): 149-160. [ Links ]
62. Strachovsky G, Seldis SM, Katz S, McNulty MM: Two dimensional echocardiographic monitoring during percutaneous endomyocardial biopsy.J Am Coll Cardiol 1985; 6(3): 609-611. [ Links ]
63. Brockway B: Echocardiographic and cardiac transplantation: a literature review and practical approach. J Am Soc Echocard 1989; 2(6): 425-430. [ Links ]














