Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.76 supl.2 Ciudad de México abr./jun. 2006
Presentación
Fisiopatología de la insuficiencia cardíaca
Pathophysiology of heart failure
Arturo Méndez Ortiz*
* Médico adjunto, Cardiología Adultos 3° piso, INCICH. Coordinador Programa de Trasplante Cardíaco, INCICH.
Correspondencia:
Dr. Arturo Méndez Ortiz.
(INCICH Juan Badiano Núm. 1, 14080, Tlalpan, México D.F.)
E–mail: Mendez_Arturo@yahoo.com
Resumen
El abordaje en el estudio y tratamiento de la insuficiencia cardíaca ha sido dirigido predominantemente a la activación neuroendocrina, con el uso de agentes terapéuticos que contrarrestan dichas alteraciones, como lECAs, betabloqueadores, aldosterona, antagonistas AT, con resultados satisfactorios a mediano plazo, en poblaciones controladas en estudios multicéntricos. No obstante, el beneficio a largo plazo parece reducirse, y la enfermedad avanza a estadios terminales. El presente escrito, revisa otros mecanismos de daño miocárdico y las medidas preventivas potenciales para incorporarse al manejo estandarizado de la insuficiencia cardíaca.
Palabras clave: Activación neuroendocrina. Apoptosis. Inflamación. Estrés oxidativo.
Summary
Treatment of heart failure has been successfully target biologically, to counteract deleterious effects resulting from neuroendocrine activation, with the use of several agents (e.g., angiotensine–converting enzyme inhibitors, beta–adrenergic receptor blockers, spironolactone), that provide benefical effects, demonstrated in multicentric trials in controlled populations. However, this mid–term benefit, becomes less effective with time, resulting in progression of the disease to terminal stages and death. The purpose of this paper is to review other pathophysiologic pathways and the potential application of preventive measures to be incorporated in the standardized treatment of heart failure.
Key words: Neuroendocrine activation. Apoptosis. Inflammation. Oxidative stress.
La insuficiencia cardíaca es un síndrome heterogéneo resultante de daño estructural de la fibra miocárdica a través de diversos mecanismos como cardiomiopatía idiopática, infarto agudo del miocardio, hipertensión arterial sistémica o valvulopatía cardíaca, entre otras causas. La prevalencia de la insuficiencia cardíaca (IC) se ha ido incrementando en forma significativa a medida que la terapéutica actual ha reducido la mortalidad de la cardiopatía isquémica en particular del infarto agudo del miocardio (IAM). Las medidas terapéuticas para modificar el pronóstico de IC no han tenido el mismo nivel de éxito. A principios de los años 90, se contaban en los Estados Unidos cerca de 4.5 millones de pacientes (pts) con insuficiencia cardíaca, cerca de 500,000 casos nuevos anuales y 550,000 admisiones hospitalarias cada año.
Durante esa década la farmacoterapia estaba orientada a contrarrestar alteraciones en diversas vías metabólicas, fundamentalmente la respuesta neuroendocrina, con bloqueadores de receptores betaadrenérgicos, inhibidores de la enzima convertidora de angiotensina, espironolactona, etc. (Fig. 1). Aunque el beneficio reportado en estudios multicéntricos en cuanto a clase funcional y sobrevida, indicaban la efectividad de estos fármacos, sus beneficios parecen perderse con el tiempo. Estudios de prevalencia al inicio del siglo XXI indicaban que la IC siguió avanzando, con más de 5,500,000 pts registrados, más de 500,000 casos nuevos por año, más de 900,000 admisiones hospitalarias y más de 300,000 defunciones por año.1
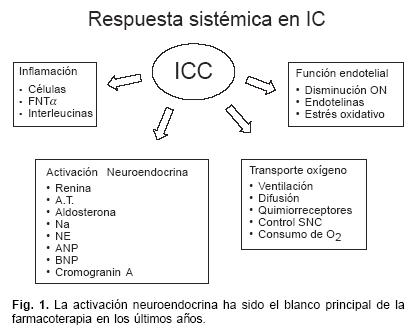
La explicación probable a estos números es que el tratamiento se inicia tardíamente, cuando ya se han establecido síntomas de IC o los parámetros de función ventricular son muy bajos. Estas limitaciones nos muestran la necesidad de abordar otros aspectos de la fisiopatología a la fecha menos desarrollados y que en el futuro pudieran ser la clave para frenar el avance de esta enfermedad.
Apoptosis e insuficiencia cardíaca
Cualquiera que sea la etiología de la IC, los mecanismos de progresión del daño se resumen en dos opciones; 1) la pérdida progresiva de la función contráctil de la fibra miocárdica y 2) la pérdida progresiva de células miocárdicas a través de apoptosis.
La apoptosis (APT) es un mecanismo por medio del cual los organismos multicelulares disponen de las células, en forma eficiente cuando expira su vida útil para la recuperación de sustratos, sin las consecuencias bioquímicas de la necrosis miocítica. Recientemente se ha demostrado que en la IC hay un aumento discreto pero sostenido de actividad apoptósica y pérdida miocítica progresiva que con el tiempo participa en forma significativa en el establecimiento de este síndrome y de su pronóstico.
La apoptosis (APT) es mediada por dos vías centrales de muerte: La vía extrínseca, que utiliza receptores de muerte en la superficie celular; y la vía intrínseca, que involucra mitocondrias y retículo endoplásmico. En la vía extrínseca, los ligandos de muerte (IL) inician la apoptosis al unirse a su receptor, esto estimula el reclutamiento del dominio de muerte asociado a Fas (FADD), el cual incorpora procaspasa–8 al complejo de señalización inductor de muerte (DISC) y activa a la procaspasa–3 y al resto de la cascada de procaspasas.2
En contraste, la vía intrínseca traduce una amplia variedad de estímulos extra e intracelulares que incluyen la pérdida de factores tróficos, toxinas, radiación, hipoxia, estrés oxidativo, daño isquemia–reperfusión y daño en el ADN. Cada uno de los estímulos provoca la activación de diferentes disparadores, pero al final coinciden en una vía común que produce proteínas proapoptósicas Bcl–2, éstas a su vez disparan la liberación de apoptósicos mitocondriales, como el citocromo c. Una vez en el citoplasma, el citocromo c se une a Apaf–1 y se activa el reclutamiento de procaspasa–9 hacia un complejo multiproteico llamado apoptosoma. Dentro del apoptosoma la procaspasa–9 se activa y provoca la activación de la cascada de procaspasas y finalmente APT (Fig. 2).
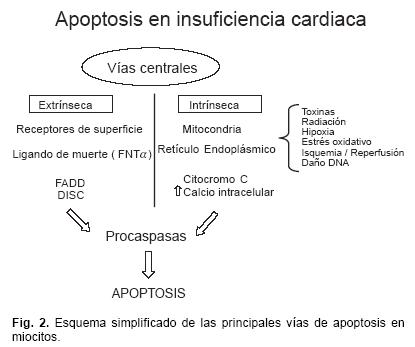
Tanto la vía extrínseca como la intrínseca están reguladas por una variedad de inhibidores endógenos de APT. La proteína inhibidora FLIP (Fas–Associated Protein–Like Interleukine–1), se une e inhibe a la procaspasa–8 en el complejo de señalización inductor de muerte (DISC). Las proteínas antiapoptósicas Bcl–2, inhibe la liberación de apoptógenos mitocondriales. En la vía extrínseca el represor de apoptosis ARC interacciona directamente con el Fas, FADD y procaspasa–8, lo cual previene el acoplamiento del DISC, impidiendo la activación de la cascada de procaspasas.
La eficiencia en el proceso de muerte celular usualmente requiere la neutralización de las vías inhibitorias, así como la activación de los mecanismos efectores.
En el IAM, la pérdida miocítica está fundamentalmente provocada por necrosis, resultado de la hipoxia. No obstante en las zonas marginales al infarto, se produce pérdida celular a través de mecanismos de APT, por medio de la vía intrínseca. Tardíamente, en las regiones distantes al infarto, los miocitos muestran aumento en la expresión de receptores de muerte y en la circulación sanguínea hay un aumento de las interleucinas específicas para este receptor, lo que puede activar la vía extrínseca y provocar la pérdida miocítica tardía que caracteriza a la remodelación patológica en los pts que desarrollan IC postinfarto3 (Fig. 3).

En los pts con insuficiencia cardíaca debida a miocardiopatía dilatada idiopática, se ha demostrado un ligero incremento en el índice de APT entre los miocitos, que va de 0.08% a 0.25%, en comparación de sujetos control, que mostraron índice de 0.001% a 0.002%, no es posible determinar si el incremento de APT se estableció antes o después del inicio de la enfermedad.4 Modelos experimentales en ratones demostraron que un índice de APT de 0.23%, provocó dilatación ventricular e insuficiencia cardíaca en los especímenes estudiados, en comparación con un índice de apoptosis de 0.002% en sujetos control, lo que demuestra que aun índices tan bajos pueden ser responsables de IC a mediano plazo.5
De lo anterior se desprende la potencial aplicación terapéutica con fármacos bloqueadores de APT, en pts expuestos a factores tóxicos (antra–ciclinas), infecciosos (miocarditis), o sobrevivientes de un IAM.
Estrés oxidativo e insuficiencia cardíaca
El término estrés oxidativo describe una situación en donde la producción de sustancias oxígeno reactivas (ROS), es mayor que la habilidad inherente de los tejidos para barrer y neutralizar los efectos de estas moléculas. Un incremento en el estrés oxidativo ha sido demostrado en diversos modelos experimentales de IC. Por ejemplo, se conoce que los radicales libres participan en la fisiopatología de la miocardiopatía inducida por adriamicina, y que el uso de antioxidantes como probucol y vitamina E, atenúan su cardiotoxicidad. Otros mecanismos inductores de IC, como las sobrecargas crónicas y la provocación de infartos por ligadura de coronarias, también han mostrado aumento del estrés oxidativo.6
En pts con IC, se puede encontrar evidencia indirecta de aumento del estrés oxidativo, a través de la elevación de radical pentano en el aire espirado (un marcador no específico de peroxidación lipídica) o la medición de niveles séricos de isoprostano. Recientemente se ha demostrado que la capacidad de los neutrófilos para generar superóxido, está aumentada en pts con insuficiencia cardíaca; y que estos niveles disminuyen tras la administración prolongada de vitamina C.7
Las reservas antioxidantes pueden estar disminuidas en la insuficiencia cardíaca, ya sea como una anormalidad primaria o como consecuencia del aumento en la producción de sustancias oxígeno– reactivas. Las principales enzimas antioxidantes son la superóxido dismutasa (SOD), catalasa y glutatión peroxidasa. Las cuales disminuyen en modelos experimentales de IC y su reducción se previene con la administración de vitamina E.
Las sustancias oxígeno–reactivas (ROS) pueden afectar en forma adversa la estructura y función cardíacas a través de varias vías; estudios in vitro han mostrado que las ROS impiden la función contráctil al interrumpir el proceso de acoplamiento excitación–contracción. Las ROS deprimen la respiración mitocondrial y reducen la habilidad del miocito para generar ATP, con reducción de función contráctil en preparaciones de fibra aislada.8
Las ROS actúan también como moléculas de señalización intracelular, induciendo APT miocítica, y se ha sugerido que juegan un papel importante en la transición de hipertrofia ventricular a IC, cuyo desarrollo se retarda en sujetos tratados con antioxidantes.9
No obstante que en modelos experimentales se ha demostrado efecto preventivo de las sustancias antioxidantes, los estudios clínicos que han utilizado suplemento oral con vitamina E, coenzima Q10 y alopurinol, no han demostrado ningún beneficio en los síntomas o en los índices funcionales.10 El carvedilol, con efectos antioxidantes, no ha demostrado aportar beneficios adicionales con respecto a otros beta–bloqueadores (Fig. 4).
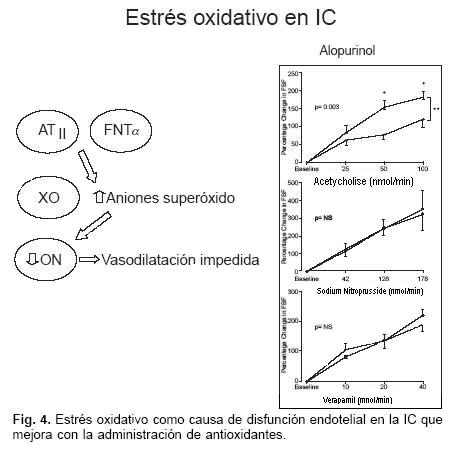
Inflamación e insuficiencia cardíaca
La actividad inflamatoria sistémica provoca un aumento en la IC por liberación de citocinas por el endotelio, músculo liso vascular, leucocitos y por el propio miocardio. La elevación de las diferentes interleucinas participa en la fisiopatología del síndrome y correlaciona con el pronóstico en forma independiente de otros marcadores.
La interleucina inflamatoria mayormente estudiada es el factor de necrosis tumoral alfa (FNT–α). En 1985, en pts en choque séptico, se encontró una sustancia circulante con efecto depresor miocárdico.11 Más tarde se determinó que esa sustancia era el FNT–α, desde entonces ha sido fuertemente implicado en la fisiopatología de la IC. La concentración sérica de FNT–α está aumentada en pts con insuficiencia cardíaca, y existe una correlación entre los niveles séricos y el grado de disfunción ventricular, síntomas, caquexia cardíaca y sobrevida. Estudios en animales han demostrado que la sobreexpresión o la infusión crónica de FNT–α conduce a miocarditis, hipertrofia y dilatación ventricular, disfunción sistólica, fibrosis miocárdica, apoptosis miocítica y aumento en mortalidad; todo lo cual puede ser revertido por un inhibidor unido al FNT–α12 (Fig. 5). Estudios clínicos tempranos con el uso de antagonistas del FNT–α (Etanercept), sugieren una mejoría en los síntomas y la tolerancia al ejercicio, así como un incremento en la fracción de expulsión.13 Si este grupo de medicamentos puede modificar a largo plazo la historia natural de la IC, está por determinarse en estudios futuros.

Otras citocinas inflamatorias se han estudiado como marcadores pronósticos en pts con insuficiencia cardíaca. Los niveles plasmáticos de interleucina–6(IL–6) por arriba de 5.6 pg/mL predice que la probabilidad de sobrevida a 2 años es equivalente a tener FEVI de 17% y a tener consumo máximo de O2 <11.5 mL/kg/min.
Disfunción endotelial en insuficiencia cardíaca
La función endotelial, evaluada por vasodilatación y vasoconstricción dependientes de endotelio es anormal en la IC. La insuficiencia cardíaca está asociada con aumento en la actividad de la enzima convertidora de angiotensina (ECA), activación de citoquinas, aumento del estrés oxidativo y disminución del flujo sanguíneo periférico. Estos cambios pueden impedir la función endotelial a través de disminución de la síntesis y liberación de óxido nítrico (ON), aumento en la degradación de ON y aumento en la producción de endotelina–1.14
Las citocinas inflamatorias, particularmente el factor de necrosis tumoral (TNF)–alfa, están aumentadas en la insuficiencia cardíaca crónica y pueden contribuir a reducir la síntesis y liberación de ON, interfiriendo la estabilidad del RNA mensajero de la sintetasa de óxido nítrico (SON) y regula a la baja la expresión de SON.15 Estudios recientes sugieren que los niveles plasmáticos de TNF–α están relacionados con el grado de disfunción endotelial evaluada con acetilcolina y que la progresión en los niveles de TNF–α está relacionada directamente con el deterioro en la clase funcional.
La hemodinámica juega un papel importante en la alteración de la respuesta vasodilatadora en pts inactivos con insuficiencia cardíaca crónica. La disminución crónica del flujo sanguíneo se refleja en una disminución del estrés de fricción sobre el endotelio vascular, con la consecuente disminución de la liberación de ON y de la respuesta vasodilatadora dependiente del flujo, misma que puede revertirse con el entrenamiento físico y abre otro recurso en el tratamiento del síndrome de insuficiencia cardíaca.
El conjunto de alteraciones neurohumorales, como la activación adrenérgica, caracterizada por niveles plasmáticos elevados de norepinefrina, arginina vasopresina, el aumento de actividad del sistema renina–angiotensina–aldosterona y el aumento en los niveles de citocinas inflamatorias, provocan, además de las alteraciones ya descritas, un aumento en el estrés oxidativo con incremento en la producción de compuestos oxígeno–reactivos, siendo los más importantes el anión superóxido (O2 –), peróxido de hidrógeno (H2O2) y radicales hidroxilo(OH–). El mecanismo propuesto para la disfunción endotelial causada por los compuestos oxígeno–reactivos es a través del aumento de la biodegradación del ON causado por la disminución en la SOD. Los compuestos oxigeno–reactivos, al reaccionar químicamente con el ON forman peroxinitritos, que imparte daño oxidativo adicional hacia el endotelio16 (Fig. 6).

El aumento en el estrés oxidativo contribuye de una manera importante a la fisiopatología de la IC, al iniciar apoptosis en los miocitos a través del factor nuclear (NF) kB y ejerciendo efectos inotrópicos negativos. Este aumento en el estrés oxidativo ha dado lugar a intentar la administración de compuestos antioxidantes como parte del tratamiento de la IC, cuyo lugar en la clínica está aún por establecerse.17
Si bien el daño miocárdico central es el fenómeno primario que da lugar la activación neuroendocrina y la disfunción endotelial, una vez establecidos, éstos a su vez modifican el curso de la enfermedad y provocan interacciones con el músculo cardíaco de manera que existen mecanismos de retroalimentación constantes que determinan el curso clínico de la IC y en forma parcial explican en algunos casos que el deterioro físico sea mayor que el esperado para el grado de disfunción miocárdica o bien que dicho deterioro sea menor que lo esperado aun en casos de daño miocárdico muy grave.18
Mediciones no invasivas del diámetro de la arteria radial, flujo y velocidad de la onda de pulso, han mostrado que el diámetro vascular disminuye progresivamente a medida que la severidad de la insuficiencia cardíaca crónica aumenta. Cambios similares han sido demostrados con respecto a la distensibilidad arterial. La respuesta vasodilatadora evaluada a través de la administración intra–arterial de acetilcolina también disminuye en relación a la severidad de la insuficiencia cardíaca.
Se ha demostrado asociación con valor pronóstico entre los marcadores de activación neuroendocrina y la severidad de la insuficiencia cardíaca, como los niveles séricos de norepinefrina, sodio y aldosterona. Pero también se han establecido marcadores de disfunción endotelial, como los niveles séricos de endotelina–1, cuya elevación se asocia con el grado de impedimento de la función ventricular y también se ha encontrado que correlaciona estrechamente con el grado de hipertensión arterial pulmonar.17–19
Siendo el incremento en los niveles de endotelina–1 el principal factor de vasoconstricción, se han desarrollado estudios experimentales y clínicos, con el uso de bosentán y sitaxsentán, ambos antagonistas de receptores de endotelina, sobre todo en el contexto de hipertensión arterial pulmonar, logrando en resultados preliminares disminución de las resistencias arteriales pulmonares y mejoría a corto plazo en la clase funcional. Sin embargo, su papel a largo plazo está aún por determinarse, debido principalmente a la baja tolerancia con el uso prolongado de dichos fármacos.
Finalmente, se trabaja en el uso de antagonistas del FNT–α, de los cuales el prototipo es el etanercept, que en estudios experimentales ha demostrado disminución en el grado de apoptosis a nivel del endotelio vascular, y en estudios clínicos un aumento en la respuesta vasodilatadora dependiente del endotelio. Aún está por determinarse su utilidad a largo plazo en poblaciones grandes.13
Referencias
1. Hunt SA, et al: ACC/AHA Guideline Update for the Diagnosis and Management of Chronic Heart Failure in the Adult–Summary Article. Circulation 2005,112: 1825–1852. [ Links ]
2. Foo RS, Mani K, Kitsis RN: Death begets failure in the heart. J Clin Invest 2005: 115; 565–571. [ Links ]
3. Bennett MR: Apoptosis in the cardiovascular system. Heart 2002; 87: 480–487. [ Links ]
4. Olivetti G, et al: Apoptosis in the failing human Aeart. N Engl J Med 1997; 336: 1131–1141. [ Links ]
5. Wencker D, et al : A mechanistic role for cardiomyocyte apoptosis in heart failure. Cell; 2003: 1497–1504. [ Links ]
6. MacCarthy PA, Shah AM: Oxidative stress and heart failure. Coronary Artery Disease. 2003; 14: 109–113. [ Links ]
7. McMurray J, Chopra M, Abdullah I, Smith WE, Dargie HJ: Evidence of oxidative stress in chronic heart failure in humans. Eur Heart J 1993; 14: 1493–1498. [ Links ]
8. Xie YW, Kaminski PM, Wolin MS: Inhibition of cardiac muscle contraction and mitochondria! respiration by endogenous peroxynitrite formation during posthypoxic reoxygenation. Circ Res 1998; 82:891–897. [ Links ]
9. Hare JM: Oxidative stress and apoptosis in heart failure progression. Circ Res 2001; 89: 198–200. [ Links ]
10. Yusuf F, Dagenias G, Pogue J, Bosh J, Slight P: Vitamin E supplementation and cardiovascular events in high–risk patients. The Heart Outcome Prevention Evaluation Study Investigators. N Engl JMed 2000; 342: 154–160. [ Links ]
11. Parrillo JE, Burch C, Shellhamer JH, et al. A circulating myocardial depressant substance in humans with septic shock. J Clin Invest 1985; 76: 1539–53. [ Links ]
12. Kapadia S, Torre–Amione G, Yokohama T, et al: TNF binding proteins modulate the negative inotropic properties of TNF–α in vitro. Am J Physiol 1995; 268: H517–25.1 [ Links ]
13. Bozkurt B, Torre–Amione G, Warren MS, et al: Results of targeted anti–tumor necrosis factor therapy with etanercept (ENBREI) in patients with advanced heart failure. Circulation 2001; 103:1044–7. [ Links ]
14. Bauersachs J, Fraccarollo D, Schafer A, Ertl G: Angiotensin–Converting Enzyme Inhibition and Endothelin Antagonism for Endotelial Dysfunction in Heart Failure: Mono– or Combination Therapy. J Cardiovasc Pharmacol 2002; 40: 594–600. [ Links ]
15. Kaye D, Ahlers B, AutelianoD, Chin–Dustin J. In Vivo and In Vitro Evidence for Impaired Arginine Transport in Human Heart Failure. Circulation 2000; 102: 2707–2712. [ Links ]
16. López A, Casado S: Heart Failure, Redox Alterations, and Endotelial Dysfunction. Hypertension 2001; 38: 1400–1405. [ Links ]
17. Rossig L, Hoffmann J, Hugel B, Mallat Z, Haase A, Freyssinet JM, et al: Vitamin C Inhibits Endothelial Cell Apoptosis in Congestive Heart Failure. Circulation 2001; 104: 2182–2187. [ Links ]
18. Fang Z, Marwick T: Vascular dysfunction ang heart failure: Epiphenomenon or etiologic agent? Am Heart J 2002; 143:383–390. [ Links ]
19. Macdonald J,Kennedy N, Struthers A: Effects of spironolactone on endothelial function, vascular angiotensin converting enzyme activity, and other prognostic markers in patients with mild heart failure already taking optimal treatment. Heart 2004; 90: 765–770. [ Links ]














