Services on Demand
Journal
Article
Indicators
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos de cardiología de México
On-line version ISSN 1665-1731Print version ISSN 1405-9940
Arch. Cardiol. Méx. vol.76 suppl.2 Ciudad de México Apr./Jun. 2006
Presentación
Hemotransfusión como factor de riesgo en cirugía cardíaca
Risk of blood transfusion in cardiac surgery
Xenia Serrano Valdés*
* Médico adscrito al Servicio de Anestesia Cardiovascular. Instituto Nacional de Cardiología Ignacio Chávez.
Correspondencia:
Xenia Serrano Valdés.
Servicio de Anestesia Cardiovascular. Instituto Nacional de Cardiología, Ignacio Chávez
(INCICH, Juan Badiano Núm. 1. Col. Sección XVI, Tlalpan 14080. México, D.F).
Resumen
El sangrado ocurre frecuentemente en pacientes que se someten a cirugía cardíaca. Aunque el sangrado inesperado después de la cirugía es común, reducir este sangrado es un objetivo importante, debido a que éste se asocia a importantes complicaciones. El sangrado durante y después de las operaciones cardíacas y los efectos de la hemodilución durante la circulación extracorpórea, frecuentemente conllevan a la transfusión de sangre. A pesar de los esfuerzos institucionales para disminuir la frecuencia de transfusión sanguínea en la cirugía cardíaca, la incidencia es aún alta. Si la transfusión fuera completamente segura, no habría tanto problema. Sin embargo, las reacciones adversas asociadas con la transfusión son las siguientes: reacciones febriles, hemolíticas y las complicaciones infecciosas. Recientemente, la transfusión sanguínea ha sido asociada a otras como: infecciones de la herida quirúrgica, neumonía, disfunción renal, sepsis severa, mortalidad intrahospitalaria y aumento en la mortalidad a 5 años.
Palabras clave: Transfusión sanguínea. Complicaciones. Cirugía cardíaca.
Summary
Bleeding occur frequently in patients undergoing cardiac surgery. Although unexpected bleeding after this surgery is common, reducing this bleeding is a desirable clinical goal, because such bleeding is associated with adverse outcomes. Bleeding during and after cardiac operations and the hemodilution effects of cardiopulmonary bypass commonly result in blood transfusions. Despite institutional efforts to curtail the frequency of blood transfusions in cardiac operation, the frequency remains high. If transfusions were completely safe, differing thresholds would not matter. However, the adverse reactions associated with transfusions are: febrile reactions, hemolytic and infectious complications may occur. Most recently, blood transfusions have been linked to postoperative wound infections, pneumonia, renal dysfunction, severe sepsis, hospital mortality and increased 5–year mortality.
Key words: Blood transfusion. Complications. Cardiac surgery.
Antecedentes
Una de las principales complicaciones de los pacientes (pts) que se someten a cirugía cardiaca (QxC) es el sangrado perioperatorio. Este sangrado y los efectos de la hemodilución por la circulación extracorpórea (CEC) llevan al uso necesario de la transfusión sanguínea (TS).
EUA reporta más de 600,000 cirugías, con una incidencia de transfusión aproximadamente del 10%,' de las cuales el 20% es usada sólo en QxC. La decisión de transfundir al pte es invariablemente para promover la hemostasia o mejorar la capacidad de transporte de oxígeno (TO2) en la sangre. Sin embargo, existe poco o ningún consenso sobre quién debe ser transfundido y la decisión de cuándo transfundirse, varía entre los mismos médicos de un hospital.
La mayoría de estos pts transfundidos se comporta bien después de la QxC sin ninguna aparente evidencia de complicaciones relacionadas a la TS. Sin embargo el seguimiento clínico de éstos ha permitido identificar una alta incidencia de complicaciones–relacionadas a la transfusión que se presentan en estos pts, siendo las más importantes: secundarias a una transfusión equivocada, las infecciosas, hematológicas e inmunológicas, entre otras2 (Tabla I). Así también no se puede ignorar la gran preocupación hospitalaria que existe ante un constante incremento de costos por la alta demanda de productos sanguíneos y el consecuente aumento en la estancia intrahospitalaria.
El impacto que ha causado este "Riesgo–Beneficio" de la TS, es de particular preocupación en el momento de la evaluación global de la QxC y su relación con el pronóstico de los mismos, debido a los riesgos médicos de esta población de pts, a la naturaleza del procedimiento y al gran número de componentes sanguíneos transfundidos.
Complicaciones de la transfusión sanguínea
Reacciones hemolíticas
A pesar de los avances en el entendimiento de los antígenos de las células rojas y su importancia clínica, las reacciones hemolíticas agudas fatales continúan ocurriendo en un rango de 1 en 250,000 en 1 millón de transfusiones. Aproximadamente la mitad de todas las muertes por reacciones hemolíticas agudas, son causadas por incompatibilidad ABO como consecuencia de errores que ocurren generalmente fuera del laboratorio. Una vigilancia estrecha en la identificación correcta de pte y unidades sanguíneas ha disminuido el número de reportes de muertes por reacciones hemolíticas.
Aproximadamente 1 en 1,000 pts tiene manifestaciones clínicas de reacciones tardías postransfusional y 1 en 260,000 pts tienen una franca reacción hemolítica, debido a que los pts tienen anticuerpos a antígenos menores de células rojas que no fueron detectados por un ensayo de anticuerpo de rutina antes de la transfusión. En EUA la incidencia de muerte por reacción hemolítica tardía es de 6 al año, que refleja el 10% de todas las muertes debido a transfusión de paquete globular en un período de 10 años.3
Contaminación bacteriana del paquete globular
El organismo más comúnmente implicado en la contaminación bacteriana de células rojas (paquete globular–(PG), es la Yersinia enterocolítica. Se han descrito también otros organismos gram–negativos.
La contaminación bacteriana de unidades de sangre está directamente relacionada al tiempo de almacenamiento, sin embargo se ha comprobado la contaminación en PGs hasta en un lapso de 7 a 14 días.
Los síntomas clínicos típicos, inician durante la transfusión y el tiempo promedio de muerte fue solamente de 25 hrs en todos los pts que fueron transfundidos con PGs infectados por Yersinia en un estudio realizado en EUA de 1987–1996. En Nueva Zelanda refieren un rango de contaminación por yersinia de 1/65,000 de unidades de PG transfundidos, con un rango de muerte de 1 en 104,000.
Contaminación bacteriana de las plaquetas
El riesgo de sepsis relacionado al uso de plaquetas se reporta de 1 en 12,000. Siendo mayor el riesgo con la transfusión del pool plaquetario (es de múltiples donadores) que cuando se transfunde una aféresis plaquetaria (es de un solo donador).
Debido al riesgo elevado de crecimiento bacteriano con el tiempo de almacenamiento, la vida media de las plaquetas almacenadas a 20–24°C es de 5 días. La presentación clínica de los pts con sepsis relacionada con plaquetas es más variable que la de los infectados por transfusión de PG contaminado bacterialmente. Clínicamente puede ir de fiebre leve (que no puede ser diferenciada de la fiebre por reacción no hemolítica transfusional), a sepsis aguda, hipotensión y muerte.
La sepsis debido a la transfusión de plaquetas contaminadas puede no diagnosticarse clínicamente en parte debido a que los organismos encontrados generalmente son los mismos implicados en las infecciones relacionadas con los catéteres. El rango de mortalidad total reportado en la literatura en sepsis asociada a plaquetas es del 26%.4
Daño pulmonar agudo postransfusional
El daño pulmonar agudo relacionado a la transfusión (TRALI), se caracteriza por un síndrome de distress respiratorio (síndrome de insuficiencia respiratoria–SIRPA), que ocurre dentro de las primeras 4 horas posteriores a la transfusión y es caracterizado por disnea, hipoxia secundarios a la presencia de edema pulmonar no cardiogénico. La frecuencia estimada de este daño pulmonar es aproximadamente de 1 en 5,000 transfusiones, aunque se cree que esta cifra está subestimada.5 Se han enumerado diferentes posibles causas del TRALI:
• Una respuesta secundaria a anticuerpos en el plasma del donador de sangre, que reaccionan con los antígenos de los leucocitos del receptor. Éstos pueden ser anticuerpos a epítopes del sistema de antígeno leucocitario humano (HLA) o bien a otros antígenos leucoci–tarios. Los anticuerpos HLA pueden dirigirse contra antígenos HLA clase I (A,B,C), que se encuentran en todos los leucocitos y en muchos otros tejidos, o antígenos HLA clase II, que se encuentran principalmente en linfocitos B y monocitos y en otros tipos celularescomo células endoteliales. Estos anticuerpos se unen y activan a los leucocitos en la sangre periférica, los cuales son secuestrados en el pulmón donde causan el daño celular endotelial que lleva a la profunda pérdida de líquidos dentro de los alvéolos.6
• Otro mecanismo sugerido para el desarrollo de TRALI, es que la porción reactiva de lípidos existentes en las células de los componentes sanguíneos almacenados por largo tiempo, pueden activar a los neutrófilos y causar daño pulmonar.
El TRALI ocurre con una frecuencia de 1 en 5–10,000 unidades de productos que contengan plasma. La severidad y la frecuencia del TRALI, se relaciona con el uso de productos que contengan grandes cantidades de plasma, tales como sangre total, plasma fresco congelado. Sin embargo se han reportado casos después de la transfusión de paquetes globulares reducidos en plasma (conteniendo aproximadamente 70 mL plasma), crioprecipitados o con un mínimo de 50 mL de sangre total. La mortalidad es de hasta 5%, reportada en la Mayo Clinic en 1985.7
Inmunomodulación
Los efectos inmunosupresores de la sangre alogénica (de banco de sangre) están relacionados a la exposición a leucocitos y la subsiguiente sensibilización que se produce.
La inmunosupresión es una condición de suma importancia clínica en los pts que se someten a cualquier tipo de trasplante, pero así también en aquellos pts con cáncer, e intervenidos de QxC con CEC. Un gran número de estudios observacionales, retrospectivos han reportado la relación entre la exposición de sangre alogénica y el aumento en la ocurrencia de cáncer y un aumento en la incidencia de infecciones postoperatorias.8
De un estudio de 120 pts que se sometieron a tratamiento quirúrgico de resección de carcinoma colorrectal, se observó un rango de infecciones 3 veces mayor en pts que se administró sangre de banco en relación a los que se transfundió sangre autóloga. Pero no observando afectación en la sobrevida final de los mismos.9 Von de Watering, encontró que la leucorreducción no tuvo efectos en los rangos de infección postoperatoria en pts que se sometieron a QxC, aunque sí se demostró que la mortalidad a los 60 días en este grupo fue aproximadamente la mitad que en el grupo control (sin leucorreducción) (3.4% vs 7.8%)
Muchos estudios prospectivos, se han visto afectados por dificultades estadísticas o metodológicas, pero todos sugieren que la exposición a sangre alogénica aumenta el riesgo de recurrencia de cáncer y de infecciones postoperatorias.
Infecciones postoperatorias en QxC
Los resultados en el pronóstico a corto y largo plazo de los pts después de QxC están estrechamente relacionados con el desarrollo de infecciones postoperatorias. La neumonía intrahospitalaria, medias–tinitis, bacteriemia y sepsis de cualquier origen son frecuentes procesos infecciosos que influyen de manera importante en el pronóstico de estos pts. Esto ha llevado a identificar actualmente los diferentes factores de riesgo que se asocian a cada tipo de infecciones; en el caso de la neumonía, mediastinitis, bacteriemia, sepsis como son: terapia antibiótica de amplio espectro, edad mayor de 65 años, sexo femenino, tiempo prolongado de ventilación mecánica, una evaluación alta de APACHE (evaluación de fisiología aguda y de salud crónica) II, y el desarrollo de falla orgánica múltiple, obesidad, el uso de doble mamaria interna en la cirugía de revascularización coronaria, dehiscencia esternal, reintervención.
La bacteriemia dentro de las 96 hrs de la QxC con CEC, se relaciona con hipertensión arterial pulmonar, diabetes y la infusión de inotrópicos. Papel de la transfusión: Sin embargo la TS perioperatoria juega un papel importante en la morbilidad de estos pts; diecisiete de 19 estudios han demostrado que la TRANSFUSIÓN SANGUÍNEA es el mejor predictor y el más significativo para el desarrollo de infecciones postoperatorias.11 Leal–Noval SR, identifica las variables que se relacionan con infecciones en el postoperatorio de QxC y concluye en un estudio realizado en 738 pts, bajo un análisis multivariado que 592 (82%) fueron transfundidos. Ciento cincuenta y ocho pts (21.4%) se transfundieron con al menos 1 plasma y 89 (12%) se transfundieron con al mínimo 1 U de plaquetas. Como en otros estudios, la asociación de transfusión con infección fue dosis–dependiente, mostrando la siguiente relación, la transfusión de > 4 U de componentes sanguíneos (cualquier combinación de PG, plasma (PL), plaquetas (Plaq)) se asocia con infección y neumonía. La transfusión de > 4U PG se asocia a infección, neumonía intrahospitalaria, y mediastinitis12 (Fig. 1). La mortalidad y estancia intrahospitalaria, en aquellos que no fueron transfundidos vs transfusión fue (rango de mortalidad 13.3% vs8.9%, respectivamente [p < 0.01]; estancia en UCI 6.1 ± 7.2 días contra 3.7 ± 2.8 días, respectivamente [p < 0.01].
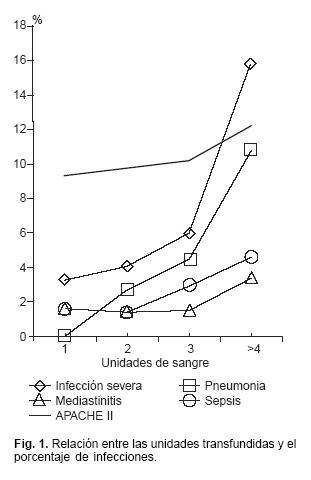
Daño miocárdico en QxC: El rol de la transfusión
El uso de la CEC durante la QxC, produce un síndrome caracterizado por activación de diversas vías de coagulación, fibrinólisis e inflamación, que conducen a alteraciones en la hemostasia y activación del sistema fibrinolítico.
Debido al efecto de fármacos usados perioperatoriamente en QxC y al efecto de la CEC en la integridad de la membrana de las plaquetas, se produce una disfunción plaquetaria importante que deteriora aún más la hemostasia conduce al mayor uso de hemoderivados sanguíneos.
La activación por contacto, causa la activación de kalicreína, la formación de bradicininas e inducción de la vía del complemento; el cual crea una "Reacción inflamatoria, denominada SÍNDROME DE RESPUESTA INFLAMATORIA SISTÉMICA (RIS)", que se caracteriza por activación de leucocitos y plaquetas, que llevan a un daño orgánico múltiple.
Todas estas alteraciones hematológicas e inmunológicas llevan a la frecuente necesidad de transfusión de productos sanguíneos alogénicos, situación que se asocia a un daño por sí misma. La transfusión alogénica libera plaquetas viejas, leucocitos y citokinas a la circulación sistémica que contribuyen a un mayor daño miocárdico y de otros órganos.13 Existen evidencias de la correlación que existe ente los marcadores de daño miocárdico y el grado de elevación de citokinas.14
El daño miocárdico que se produce por el RIS secundario a CEC, puede ser disminuido por el uso de productos sanguíneos leucorreducidos, minimizando la activación leucocitaria, y/o evitando la transfusión de hemoderivados, para disminuir los niveles totales de citokinas circulantes.
Morbilidad en QxC y tiempo de almacenamiento de los paquetes globulares
Es conocido que los eritrocitos almacenados más de 2 semanas, pueden producir isquemia visceral y un aumento en la susceptibilidad al desarrollo de infecciones postoperatorias. Leal–Noval y cols,15 en un estudio para determinar la influencia entre el tiempo de almacenamiento del PG y la morbilidad en QxC. Se incluyeron 897 pts, en los cuales se estudiaron estancia en la UCI mayor de 4 días, tiempo de ventilación mecánica mayor de 1 día, rango de infarto al miocardio perioperatorio y rango de infecciones severas postoperatorias. La duración del tiempo de almacenamiento de los eritrocitos no fue asociada a estancia en UCI, ventilación mecánica prolongada o aumento en los rangos de infarto perioperatorio, mediastinitis o sepsis. Sin embargo, cada día de almacenaje de la unidad más vieja fue asociada con un aumento en el riesgo de neumonía en un 6% (95% IC, 1–11; P = 0.018).
Transfusión sanguínea alogénica y aumento en la mortalidad en cirugía
Engoren y cols,16 estudiaron 1,915 pts que se sometieron a una primera y única cirugía de revascularización coronaria y compararon 2 grupos, aquéllos con y sin transfusión. Seiscientos cuarenta y nueve de los 1,915 pts estudiados (34%) recibieron TS durante su hospitalización. Los pts transfundidos fueron los de mayor edad, menor talla, mujeres con mayor frecuencia y con más enfermedades comórbidas. Los pts transfundidos tuvieron el doble de la mortalidad en 5 años (15% vs 7%) de los pts no transfundidos. Después del ajuste de los factores que confundían el estudio, la transfusión fue asociada fuertemente con un 70% de aumento en la mortalidad (radio de riesgo = 1.7; 95% IC = 1.4–2.0; p = 0.001). Transfusión, enfermedad vascular periférica, enfermedad pulmonar obstructiva crónica, NYHA clase IV y la edad fueron los predictores significativos de mortalidad a largo plazo ante un análisis multivariado. Por lo tanto los autores concluyen que la TS durante o después de la cirugía de revascularización coronaria está relacionada con aumento en la mortalidad a largo plazo (Fig. 2).
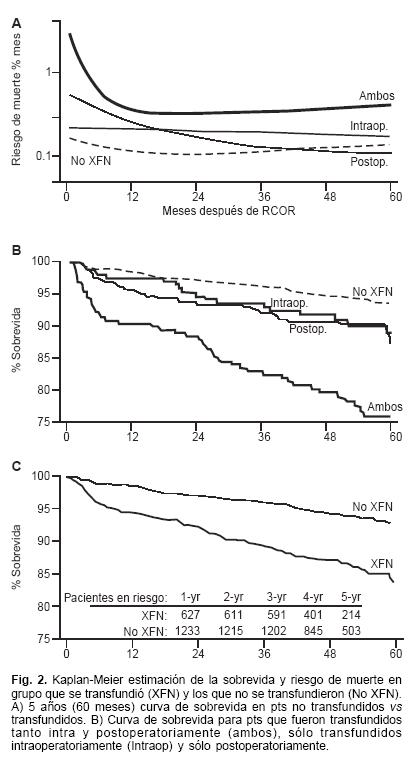
Referencias
1. Engoren MC, Aviv RH, et al: Effect of blood transfusion on long–term survival after cardiac operation. Ann Thorac Surg 2002; 74: 1180–6. [ Links ]
2. Goodnough Johnston MF, et al: The variability of transfusion practice in coronary artery bypass surgery. JAMA 1991; 265: 86–90. [ Links ]
3. Sazama K: Reports of 355 transfusion–associated deaths. 1976–1985. Transfusion 1990; 30: 583–90. [ Links ]
4. Goldman M, Blajchman MA: Blood product associated bacterial sepsis. Transfusion. Med Rev 1991; 5: 73 83. [ Links ]
5. Goodnough LT: Risk of blood transfusion. Anesthesiology. Clin N Am 2005; 23: 241–252. [ Links ]
6. Silliman CC, Boshkov LK: Transfusion–related acute lung injury: epidemiology and prospective analysis of etiologic factors. [ Links ]
7. Wallis JP: Transfusion–related acute lung injury (TRALI)–under–diagnosed and under–reported. British Jour of Anaest 2003; 90(5): 573–5. [ Links ]
8. Berdín JO, Heddle NM, Blojchman MA: Biologic effects of leucocytes present in transfused cellular blood products. Blood 1994; 84: 1703–21. [ Links ]
9. Mynster T, Christensen IJ, et al: Effects of the combination ob blood tranfusion and postoperative infectious complications on prognosis after surgery for colorectal cancer. Britsh Jour of Surg 2000; 87: 1553–62. [ Links ]
10. Van de Watering LMG, Hermans J, et al: Benefícial effects of leukocyte depletion of transfused blood on postoperative complications in patients undergoing cardiac surgery: a randomized clinical trial. Circulation 1998; 97: 562–8. [ Links ]
11. Mezrow CK, Bergstein I, Tartter PI: Postoperative infections after autologous and homologous blood transfusion. Transfusion 1992; 32: 27–30. [ Links ]
12. Leal–Noval, Santiago Ramón MD, Ferrari R, et al: Transfusion of blood components and postoperative infection in patients undergoing cardiac surgery. Chest 2001; 119(5): 1461–68. [ Links ]
13. Shore–Lesserson L: Myocardial injury in Cardiac Surgery: The role of transfusion. Journal of Card and Vase Anest 2000; 14 (3)suppl 1: 11–14. [ Links ]
14. Pearl JM, DrinkwaterDC, et al: Leukocyte–depleted reperfusion of transplanted human hearts prevents ultrastructural evidence of reperfusion injury. J Surg Res 1992; 52: 298–308. [ Links ]
15. Leal–Noval SR, Jara–Lopez I, et al: Influence of erythrocyte concentrate storage time on postsurgical morbidity in cardiac surgery patients. Anesthesiology 2003; 98(4): 815–22. [ Links ]
16. Shander A, et al: Clinical outcomes in Cardiac Surgery: Conventional surgery vs bloodless surgery. Anesthesiology Clin N Am 2005; (23): 327–345. [ Links ]














