Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.75 no.4 Ciudad de México oct./dic. 2005
Investigación clínica
Cirugía de Fontan. Factores de riesgo a corto y mediano plazo
Fontan operation: factors influencing early and late outcomes
Juan Calderón–Colmenero,* Samuel Ramírez,* Regina Viesca,* Liliana Ramírez,* Miguel Casanova,* José Antonio García Montes,* Emilia Patino,* Carlos Zabal,* Alfonso Buendía*
* Servicio de Cardiología Pediátrica.
Correspondencia:
Dr. Juan Calderón–Colmenero.
Instituto Nacional de Cardiología "Ignacio Chávez"
(INCICH Juan Badiano No. 1 Col. Sección XVI, Tlalpan,
14080 México, D.F.)
E–mail: juanecalderon@yahoo.com.mx
Recibido: 07 de Julio de 2005
Aceptado: 13 de octubre de 2005
Resumen
Se presenta un análisis retrospectivo de pacientes sometidos a cirugía de Fontan, de enero de 1989 a diciembre 2003, con el fin de evaluar los resultados, así como las variables clínicas y hemodinámicas que inciden en su morbilidad y mortalidad. Se estudiaron un total de 81 pacientes con los siguientes diagnósticos: 53 con atresia tricuspídea, 14 con atresia pulmonar con septum intacto, 11 con conexión atriouniventricular y 3 con anomalía de Ebstein. A 61 pacientes se les realizó Fontan con túnel intra–atrial y en 20 se utilizó un tubo extracardíaco, fenestrados en 53 pacientes. La mortalidad operatoria (< 30 días) fue 13% para atresia tricuspídea y 25% en el resto, siendo básicamente ésta por choque cardiogénico y arritmias graves. La sobrevida global fue de 71% en 55 meses de seguimiento. Hubo que desmantelar el Fontan en 5 casos. De las diversas variables analizadas se encontró 2.8 veces más riesgo de morir en pacientes sin fenestración y 3.6 veces cuando a las 72 hrs postquirúrgicas la presión de atrio izquierdo fue > 10 mmHg y la presión media de la arteria pulmonar > 20 mmHg. Las complicaciones más relevantes fueron: arritmias (38%), enteropatía perdedora de proteínas (8%) y eventos trombóticos cerebrales (1 %). El 52% de los pacientes han reingresado siendo las principales causas falla hemodinámica e infecciones.
Palabras clave: Cirugía de Fontan. Cardiopatías congénitas. Atresia tricuspídea.
Summary
The purpose of this retrospective study was to determine the outcome of patients who underwent a Fontan procedure at National Heart Institute "Ignacio Chavez", Mexico, from January 1989 to December 2003. We had 81 patients with a mean age of 7 years old: 53 with tricuspid atresia, 14 with pulmonary atresia and intact septum, 11 with univentricular atrioventricular connection and 3 with Ebstein's anomaly. An intra–atrial tunnel was performed on 61 patients and an extracardiac conduit on the rest. Of all, 53 underwent a fenestration. The surgical mortality was 13% fortricuspid atresia and 25% for the other diseases. We had an overall mortality of 28.4%, being the main causes cardiogenic shock and arrhythmia. The global survival was 71% in 55 months of following. Takedown was indicated on 5 patients. The patients without fenestration showed to have 2.8 times more risk of death. The mean pulmonary artery pressure > 20 mm Hg plus the left atrium pressure > 10 mmHg increased the death risk 3.6 times. Of the 52% who required readmission, the main causes were hemodynamical failure and infections. The more relevant complications were: arrhythmia (38%), protein–losing enteropathy (8%) and thrombotic cerebral events (1.4%).
Key words: Congenital heart disease. Fontan's surgery. Tricuspid atresia.
Introducción
La cirugía de Fontan, propuesta en su inicio para el manejo de atresia tricuspídea, es ahora también indicada en otras cardio–patías congénitas complejas que tienen como característica primordial un solo ventrículo funcional. El principio quirúrgico consiste en establecer conexión del retorno venoso sistémico con las ramas de la arteria pulmonar y del ventrículo único funcional con la circulación sistémica, con el fin de disminuir el trabajo de dicho ventrículo, separar la sangre venosa pulmonar de la sistémica y aliviar con esto la hipoxemia.1
La técnica propuesta en 1971 por Fontan y Baudet, ha sufrido cambios en los últimos 30 años disminuyendo su morbimortalidad, lo que ha dado como consecuencia lógica una mayor sobrevida de los pacientes y nuevos caminos en el manejo de estos pacientes. Esta cirugía es paliativa y su fisiología establece efectos deletéreos tanto en la circulación pulmonar como en la sistémica, lo cual implica un deterioro en la clase funcional a largo plazo.2–4
El objetivo del presente trabajo fue analizar la experiencia alcanzada en los pacientes con car–diopatía congénita con fisiología univentriculary que fueron sometidos a esta técnica quirúrgica en nuestra Institución.
Material y métodos
Se realizó un análisis retrospectivo de todos los pacientes sometidos a cirugía de Fontan en el período comprendido entre enero de 1989 a diciembre del 2003.
Se dividió a los pacientes en dos grupos, el primero incluyó pacientes con atresia tricuspídea y el segundo con otros diagnósticos como: anomalía de Ebstein, atresia pulmonar con septum intacto y conexión atriouniventricular. En ambos grupos se compararon variables como: edad, sexo, peso, talla, superficie corporal y antecedente de procedimientos quirúrgicos previos como fístulas sistémico–pulmonar, bandaje de la arteria pulmonar o derivación cavopulmonar bidireccional.
Se consideraron factores de riesgo para la realización de la cirugía de Fontan: presión media de la arteria pulmonar (PAMP) > 20 mmHg; resistencias arteriolares pulmonares (RAP) > 2U•W; disfunción del ventrículo sistémico, definida por una fracción de expulsión (FE) < 60% o por una presión diastólica final del ventrículo sistémico (D VI) > 10 mmHg; y los índices del tamaño de las ramas pulmonares: Nakata < 250 mm2/m2 y/o McGoon < 2. El índice de Nakata se calculó como el área de la rama derecha de la arteria pulmonar (RDAP) + área de la rama izquierda de la arteria pulmonar (RIAP)/superficie corporal. El índice de McGoon se calculó como el diámetro de RDAP + diámetro de RIAP/diámetro de la aorta descendente a nivel del diafragma. Además, se midió por medio de ecocardiografía, el grado de insuficiencia de la válvula atrioventricular y la fracción de eyección del ventrículo sistémico.
Los pacientes sometidos a esta cirugía en el período señalado fueron intervenidos por el mismo cirujano cardiovascular. Las técnicas realizadas fueron la derivación cavopulmonar total con túnel intracardíaco o mediante tubo extracardíaco, ambas con o sin fenestración. Las variables postoperatorias analizadas fueron: PAMP > 20 mmHg; presión media del atrio izquierdo (PAI) > 10 mmHg a las 72 horas; saturación arterial de oxígeno (SaO2); volumen y duración de los derrames pleurales en relación a la superficie corporal.
También se analizó la presentación de complicaciones como: obstrucción en el sitio de la anastomosis o cierre precoz de la fenestración, arritmias, hemorragias, alteraciones neurológicas, parálisis diafragmática y quilotórax. Se obtuvo las causas de reintervención, incluyendo desmantelamiento del Fontan y/o realización de fenestración postoperatoria, así como tiempo de ventilación mecánica, estancia en terapia intensiva y hospitalaria.
La mortalidad se definió como operatoria cuando ocurrió dentro de los 30 días posteriores a la cirugía de Fontan, así como tardía la posterior a dicho lapso.
Análisis estadístico
Para la comparación de las variables cuantitativas se calcularon la media y su desviación estándar. Para el análisis de las variables cualitativas se aplicaron las pruebas de: Chi cuadrada, comparación de tasas y proporciones y límites de confianza para la distribución binomial. También se calculó razón de momios y riesgo relativo. Todo valor de p < 0.05 se consideró significativo.
Resultados
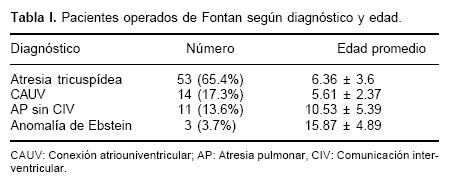
Los pacientes estudiados fueron 81, de los cuales 53 tenían diagnóstico de atresia tricuspídea y los 28 restantes incluían a 14 pacientes con atresia pulmonar con septum intacto, 11 con conexión atriouniventricular y 3 con anomalía de Ebstein (Tabla I).
La edad promedio de ambos grupos, al momento de la cirugía fue de 7.15 ± 4.41 años, con un rango entre 1.85 y 22.7 años, siendo mayor la media en el grupo de mujeres con rango de 8 ± 5.22 años en relación al de hombres de 6 ± 2.8 años (Tabla II).

En cuanto al género, 44 fueron del sexo femenino y 37 del masculino, sin diferencias entre ambos grupos. En cuanto al peso la media fue de 21.39 kg, siendo de 19 kg en el grupo I (atresia tricuspídea) y de 29.6 kg en el otro grupo.
De los pacientes estudiados, 31 fueron llevados directamente a cirugía de Fontan, y 50 ( 65%) tenían antecedente de algún procedimiento paliativo siendo 58% fístula de Blalock–Taussig modificada (FBT), 28% derivación cavopulmonar bidireccional (DCPB) y 13% bandaje de la arteria pulmonar. Sólo 8% de los pacientes tuvo más de un procedimiento; a tres se les realizó FBT y posteriormente DCPB; dos casos bandaje de la arteria pulmonar y dos años después DCPB. Por último, a dos pacientes se les realizó DCPB bilateral, ya que tenían vena cava superior izquierda persistente. El tiempo transcurrido entre el procedimiento paliativo y la cirugía de Fontan tuvo una media de 4.8 años con rango de 1 a 13.6 años.
Los parámetros hemodinámicos prequirúrgicos fueron: promedio de edad 7.15 años (2 a 23 años); PAMP de 7.22 mmHg (7–22 mmHg); presión diastólica final del ventrículo izquierdo (D2VI) 7.63 mmHg (2–8 mmHg); resistencias vasculares arteriolares pulmonares de 1.87 ± 1.25 U•W; índice de Nakata de 285 mmVm2 (102 a 508), y McGoon de 2 (1 a 3). La media de SaO2 fue de 78% (59 a 92%). El grado de insuficiencia de la válvula atrioventricular fue ligero en 12 pacientes y moderado en 4. La fracción de eyección varió entre 42% y 83%, con media de 64%. Del total de los pacientes, 12 (14%) presentaban algún grado de distorsión en las ramas de la arteria pulmonar, 6 presentaron estenosis posterior a algún procedimiento, 4 a FBT, uno a DCPB y el último a DCPB más bandaje de la arteria pulmonar. Del resto, 6 tenían distorsión de ramas pulmonares sin relación con algún procedimiento paliativo.
De acuerdo al tipo de cirugía realizada encontramos que a 61 pacientes (75%) se les realizó un túnel interatrial y al resto se le colocó un tubo extracardíaco. Se realizó fenestración a 53 pacientes (65%), de los cuales al 88% se les practicó túnel intracardíaco y en 22% se les colocó tubo extracardíaco.
Con la excepción de 2 (3%) todos los pacientes tuvieron apoyo con circulación extracorpórea (CEC) durante la cirugía. El promedio de tiempo de CEC fue de 120 min y el de pinzamiento aórtico de 56.7 min, sin diferencias estadísticamente significativas entre ambos grupos. No hubo relación estadísticamente significativa entre mortalidad y tiempo prolongado de circulación extracorpórea.
En cuanto a los parámetros hemodinámicos postoperatorios, la PAMP fue de 17 mmHg (7–30); PAI de 10.9 mmHg (5–20); SaO2 de 89% y fracción de eyección con media de 58% y rango de 40 a 78%.
Todos los pacientes presentaron derrame pleural y su duración varió de 2 a 54 días, con media de 16 días. El volumen promedio total de líquido pleural fue de 522.82 mL/m2/día (106.24 –2,042.6). El grupo de atresia tricuspídea fue de 519.08 mL/m2/día (106.24 – 2,042.6), y el segundo grupo de 578.7 mL/m2/día (134.5 –1,647.87). Trece pacientes presentaron quilotórax (16%), observándose en ellos un promedio mayor de días de derrame pleural, siendo de 28.3 días contra 16 días en pacientes sin quilotórax. Los pacientes que tuvieron derrame pleural por más de 15 días, no mostraron incremento en la mortalidad con respecto al resto del grupo.
Hubo 8 casos de parálisis diafragmática (10%), obstrucción de la anastomosis en 13 pacientes (16%), derrame pericárdico en 8 pacientes (7%). Dieciocho pacientes (22%) requirieron colocación de catéter de diálisis peritoneal por ascitis significativa. Se reportaron dos casos de síndrome de vena cava superior.
Se presentaron trastornos de la conducción o del ritmo en el 38%, con un total de 31 pacientes afectados, siendo los más frecuente: bloqueo atrioventricular completo en 7 pacientes, taquicardia ventricular en 7, ritmo nodal en 6, fibrilación ventricular en 4, ritmo auricular bajo en 3 y taquicardia auricular en 3 de ellos.
En la esfera neurologica, se presentaron 2 casos de evento vascular cerebral (2.4%), uno de ellos secundario a evento embólico por trombo en carótida izquierda y el otro secundario a endocarditis.
Hubo un total de 33 reintervenciones quirúrgicas: 7 para colocación de marcapaso definitivo; 6 por obstrucción de la anastomosis; 5 para pli–catura diafragmática; 5 casos para decorticación por derrame pleural persistente; dos pacientes para derivación; 4 reintervenciones para crear una fenestracion, de las cuales dos fueron fallidas; 2 ventanas pericárdicas por tamponade; un cierre de conducto torácico y finalmente un caso en el cual reconstruyó la anastomosis por dehiscencia de la misma. Se reportaron 12 pacientes con sangrado postquirúrgico (15%).
Se llevaron a cabo 13 cateterismos postquirúrgicos, 7 de los cuales fueron intervencionistas, incluyendo cierre de la arteria pulmonar con dispositivo Amplatzer, atrioseptostomía, colocación de stent para mantener abierta la fenestracion, ampliación de fenestracion con navaja y colocación de un stent para manejo de estenosis de la rama izquierda de la arteria pulmonar. Dos pacientes llevados a cirugía para realizar fenestracion fallecieron, ambos por choque car–diogénico. En otros dos casos la fenestracion fue fallida por lo que los pacientes se llevaron a cateterismo intervencionista donde se logró realizar la fenestracion.
Por último, en 5 pacientes hubo necesidad de desmantelar el Fontan, todos cumplían con criterios prequirúrgicos adecuados. En 4 se realizó túnel intra–atrial y el otro fue con tubo extracardíaco, 4 de ellos eran fenestrados. Las edades fluctuaban entre 3 y 9 años. En 4 casos se registraron presiones pulmonares postquirúrgicas elevadas (PAMP de 20 hasta 30 mmHg), con choque cardiogénico que requirió el uso de múltiples inotrópicos. El desmantelamiento se llevó a cabo a los 2, 3, 4 y 17 días de postoperatorio respectivamente. Después del desmantelamiento, a cuatro pacientes se les realizó fístula sistémico–pulmonar y en otro, derivación cavopulmonar bidireccional con FBT. Hubo una mortalidad del 60% (3 pacientes), la causa de fallecimiento fue choque cardiogénico.
El promedio de días de apoyo con ventilación mecánica fue de 4.93 días (6 h – 53 días). La estancia en terapia intensiva postquirúrgica fue de 6.7 días (1 – 54 días), y la estancia hospitalaria tuvo una media de 23 días (1.5 – 94 días). La mortalidad operatoria de atresia tricuspídea fue de 13%y en el otro grupo de 25%, y la tardía de 13% en el primer grupo, contra 7% en el segundo, sin haber diferencia estadística entre los grupos (Tabla III). El 71% de las muertes se registró en la primera semana de postoperatorio.

La mortalidad global, operatoria y tardía, fue del 28% (23 pacientes) y se distribuyó de la siguiente manera: en el grupo de atresia tricuspídea la mortalidad fue del 26% y en el otro, la mortalidad fue del 31%. Se realizó una comparación de proporciones por límite de confianza según distribución binomial, sin encontrar diferencia estadísticamente significativa.
Las principales causas de mortalidad operatoria fueron: choque (cardiogénico o séptico) y arritmias graves: taquicardia y fibrilación ventricular. En los pacientes que fallecieron después de los 30 días de postoperatorio hasta años después, el choque cardiogénico continuó siendo la principal causa de muerte, registrándose además fallecimientos por eventos vasculares cerebrales de tipo tromboembólicos, enteropatía perdedora de proteínas e insuficiencia renal crónica.
En cuanto a los factores asociados a mortalidad, se observó que existe 2.8 veces más riesgo de morir en los pacientes a quienes no se realizó fenestracion con riesgo relativo de 1.5 y razón de momios de 2.86. Por medio de comparación de proporciones, se analizaron variables preoperatorias como edad, género y peso, así como aquellas variables medidas en el estudio hemodinámico y en ecocardiografía, es decir PAMP, resistencias pulmonares, D2VI, índices de Nakata y McGoon, SaO2, fracción de eyección y grado de insuficiencia de la válvula atrioventricular, sin encontrar en ningún caso diferencia estadísticamente significativa (Tabla IV).

En referencia a las variables postoperatorias medidas se encontró que solamente la PAI mayor de 10 mmHg fue la única variable con significación estadística como predictor de mortalidad (incremento de riesgo 2.6 veces), y de manera asociada la PAMP mayor de 20 mmHg y PAI > 10 mmHg tuvieron un aumento de riesgo hasta de 3.6 veces de fallecer (Tabla V).
En el seguimiento, se observó que el número de pacientes libres de reingreso fue el 48%. Los pacientes que reingresaron tuvieron un promedio de 2.5 reingresos por paciente (límites 1 y 9). Las principales causas de reingreso fueron: derrame pleural en 13 pacientes (20%), insuficiencia cardíaca con deterioro en la clase funcional en 8 pacientes (12%). En segundo lugar, procesos infecciosos (12%) de diversas causas como: neumonía y absceso cerebral en dos pacientes respectivamente y artritis séptica e infección de herida quirúrgica. Otra causa de reingreso fue la realización de cateterismo (9%), para realizar o ampliar una fenestración. Hubo 8% reingresos por parálisis diafragmática y 8% por trastornos de la conducción para colocación de marcapaso. Los pacientes que más ingresos tuvieron presentaban enteropatía perdedora de proteínas.
La enteropatía perdedora de proteínas, se presentó en 6 pacientes (8%), cinco de ellos con atresia tricuspídea y el otro con conexión atriouniventricular. De éstos hubo dos defunciones por desequilibrio hidroelectrolítico y falla cardíaca, y el otro secundario a proceso infeccioso. El promedio de seguimiento posterior a la cirugía de Fontan fue de 55 meses en los sobrevivientes. La sobrevida global de los pacientes sometidos a cirugía de Fontan durante los 14 años de estudio en nuestra institución fue de 71% (Fig. 1).

Discusión
El advenimiento de la cirugía de Fontan ha mejorado la expectativa de pacientes con atresia tricuspídea o con fisiología cardíaca univentricular, mejorando su estado clínico al disminuir la carga volumétrica ventricular y lograr una mejor presión arterial de oxígeno. Sin embargo, la fisiología de Fontan implica un tipo de circulación no pulsátil hacia los pulmones, el incremento en la presión venosa sistémica y una respuesta hemodinámica alterada al estrés, así como un deterioro en la clase funcional a largo plazo en algunos pacientes.5
Hay estudios que reportan una tasa de supervivencia bajo condiciones óptimas de: 92% al mes, 88% al año, 86% a los 5 años y 73% a los 15 años posteriores a la cirugía de Fontan. El riesgo de muerte a partir de la cirugía, tiene una caída rápida inicial, que a los 6 meses se estabiliza para disminuir nuevamente a partir del sexto año de postoperatorio. No se han establecido hasta ahora factores que expliquen este deterioro a largo plazo, por lo que se ha considerado sea secundario al estado fisiológico de la circulación de Fontan per se.1
Al pasar el tiempo, se han ido creando estrategias para disminuir la morbi–mortalidad en estos pacientes, entre ellas destaca la realización de derivación cavopulmonar bidireccional como un primer tiempo quirúrgico, la realización de fenestración y la conversión de variantes de cirugía de Fontan a tubo lateral atrial o a tubo extracardíaco. Las técnicas anteriores han sido reportadas como útiles para reducir el riesgo de mortalidad y de complicaciones como: arritmias y enteropatía perdedora de proteínas.
Se ha mencionado la superioridad de la derivación cavopulmonar bidireccional en relación a la fístula sistémico–pulmonar, basado en que disminuye la posibilidad de distorsión de las ramas pulmonares y de producir hipertensión arterial pulmonar. Asimismo, permite que a edades tempranas se aminore la sobrecarga de trabajo del ventrículo sistémico al disminuir tanto la precarga como la postcarga, permitiendo una mejor tolerancia futura a la circulación tipo Fontan. En nuestro grupo sólo un 28% tenía como procedimiento previo una derivación cavopulmonar bidireccional en gran medida por la edad tardía en que se pudo abordar a estos pacientes. Es de resaltar que ninguno de los pacientes con DCPB previa tuvo mortalidad operatoria. Nuestro Instituto ha reportado la realización de DCPB inicial en niños menores de 1 año con buenos resultados.6
Uno de los criterios para la realización de la cirugía de Fontan es la edad, habiéndose reportado inicialmente como factor de riesgo ser menor de 3 años, por la posibilidad de obstrucción de la anastomosis. Sin embargo, en una serie de pacientes menores de dos años (promedio 1.5 años) que fueron intervenidos exitosamente, a pesar de lo cual se considera como edad óptima para la realización de la cirugía entre los 2 y 4 años de edad. De la misma manera, se ha reportado que pacientes mayores de 4 años son más propensos a tener hipertrofia ventricular y alteraciones en la contractilidad del ventrículo sistémico, pero en contraposición hay estudios que reportan buenos resultados en pacientes adultos.7–11 En nuestro estudio, la edad promedio fue de 7.15 años con un rango entre 2 y 23 años, no encontramos en nuestro grupo alguna edad de mayor riesgo de mortalidad.
Hay series que reportan que hasta 90% de los pacientes tenían al menos un procedimiento previo, siendo los más frecuentes las fístulas sistémico–pulmonares, así como derivación cavopulmonar bidireccional y bandaje de la arteria pulmonar. En nuestra serie un 65% de los pacientes tenían procedimientos previos, siendo los más frecuentes las fístulas sistémico–pulmonares (59%), seguidas de la derivación cavopulmonar bidireccional, con un tiempo entre la cirugía paliativa y el Fontan de 1 a 13.6 años, con promedio de 4.8 años. La mitad de los pacientes que tuvo distorsión de ramas pulmonares, la presentó posterior a cirugías paliativas, de las cuales 4 fueron fístulas sistémico–pulmonares, una derivación cavopulmonar bidireccional y otra bandaje de la arteria pulmonar más DCPB. Esto hace meditar que ningún procedimiento está exento de provocar distorsión de ramas y puede, por lo tanto, complicar el procedimiento quirúrgico del Fontan. A pesar de lo anterior, los pacientes que tuvieron procedimientos previos no presentaron incremento en la mortalidad comparados con el resto en nuestro análisis.
Los criterios que han sido descritos como predictores de una adecuada adaptación a la fisiología de la cirugía de Fontan son: PAMP menor de 15 mmHg, D2VI menor de 10 mmHg, tamaño y anatomía de las ramas pulmonares y resistencias vasculares pulmonares (<4U•W). Los parámetros preoperatorios encontrados en los pacientes de nuestro estudio, son comparables a los reportados en otras series y ninguno de ellos fue factor de riesgo para mortalidad.11–15
En este estudio se realizaron 61 procedimientos de Fontan intra–atriales y 20 extracardíacos. Se realizó fenestración a 65%, siendo a 88% de los primeros y a 22% de los segundos. La fenestración tiene por objetivo la disminución de la presión venosa así como la capacidad de mantener un adecuado gasto cardiaco, aún a expensas de la disminución de la saturación arterial de oxígeno.5 La indicación de fenestración para Stamm y colaboradores, era la presión media de la arteria pulmonar elevada o más de 2 U* W de resistencias vasculares pulmonares.7 En un artículo publicado por Castañeda y colaboradores, las indicaciones establecidas fueron: distorsión de ramas pulmonares, resistencias pulmonares mayores de 2 U«W, PAMP mayor a 18 mmHg, D2VI mayor de 12 mmHg e insuficiencia de la válvula atrioventricular.16–18
En series publicadas en nuestro Instituto, la indicación de fenestración ha sido la presencia de insuficiencia ligera a moderada de la válvula atrioventricular, alteración en la función ventricular o presión pulmonar elevada, niños menores de dos años o pacientes con fístula sistémico–pulmonar por tiempo prolongado. El cierre de la fenestración se realiza, de ser conveniente, al mejorar el estado clínico del paciente o si la saturación es menor de 85%, pudiendo ser por medio de cirugía o intervencionismo.19–21
En el presente estudio pudimos comparar los resultados en los 53 pacientes a quienes se llevó a cabo una fenestración, contra los 28 pacientes restantes. Se encontró dentro de los pacientes fenestrados una mortalidad de 20% contra una mortalidad de 42% del resto de los pacientes. En el análisis estadístico se encontró un riesgo de morir 2 veces mayor en los pacientes sin fenestración, por lo que consideramos a la fenestración un procedimiento útil para mejorar las condiciones hemodinámicas postoperatorias y disminuir el riesgo quirúrgico a expensas de compromiso en la saturación arterial, situación que se puede solucionar mediante cateterismo intervencionista una vez que las condiciones clínicas de los pacientes lo permitan. La mortalidad en este estudio fue de 28%, incluyendo mortalidad operatoria (17%) y tardía. En cuanto a la operatoria, la mayoría de las muertes suceden en la primera semana (71%), principalmente a falla ventricular y arritmias, como está reportado en la literatura. Otras causas referidas son: sepsis, eventos hemorrágicos o embólicos cerebrales, entre otros. Se ha mencionado que a partir de los 6 meses posteriores a la cirugía, la principal causa de muerte es la falla cardíaca y en segundo lugar la muerte súbita secundaria a arritmias.1,6,7
El promedio de tiempo de circulación extracorpórea en nuestro estudio fue de 120 min y el de pinzamiento aórtico de 56 min, comparable a otras series con CEC de 120 ± 27 min y PA 59 ± 20 min.7 Se estudió la posibilidad de que tiempos elevados de circulación extracorpórea fueran determinantes para la evolución, no encontrando ninguna diferencia significativa desde el punto de vista estadístico.
El tiempo promedio de ventilación mecánica en nuestra serie es mayor que el reportado por otros autores, siendo de 4.9 días (6 hrs a 53 días) versus 11.2h(4.7h a 32 días) situación que habrá que analizar y definir si es un perfil diferente de paciente el de nuestra población en el que inciden problemas como, por ejemplo, un pobre estado nutricional. La estancia en terapia postquirúrgica fue de 6 días (1 a 54 días) versus 2.7 días (1 a 93) en otras series. El promedio de saturación de oxígeno fue 89% tomando en cuenta a los pacientes fenestrados, comparable a otros estudios donde los no fenestrados tienen media de 93% ± 3, y los fenestrados de 87% ± 4.7
En este estudio observamos a la PAI > 10 mmHg como la variable postoperatoria estadísticamente significativa de riesgo de mortalidad, ya sea en forma aislada (con RR de 2.6 y RM 4.25) o asociada con una PAMP > 20 mmHg (RR de 3.6 y RM 6.2), sin embargo la PAMP por sí sola no fue un factor de riesgo (RR 0.55 y RM 0.47).
El derrame pleural después del Fontan contribuye a la morbilidad y a la hospitalización prolongada. Se cree que la respuesta inflamatoria inducida por la CEC resulta en un síndrome de fuga capilar, que se manifiesta como: edema intersticial, derrames y depresión de la función miocárdica. La presencia de daño endotelial posterior al Fontan ha sido reportada en estudios previos. Hay factores inflamatorios, hormonales (sistema renina–angiotensina, péptido auricular natriurético y vasopresina) e hidrostáticos involucrados en la etiología de los derrames pleurales persistentes. En base a lo anterior se ha reportado la utilidad de la ultrafiltración en estos pacientes para disminuir los mediadores proinflamatorios. Estudios previos reportan de un 13 hasta 39% de pacientes con este problema. Gupta y colaboradores reportan una duración promedio de tubos de drenaje pleural de 10 días con una media de drenaje de 14.7 mL/kg/día, encontrando como factores de riesgo significativos para una duración mayor a 15 días o drenaje mayor de 20 mL/ kg/día, la presencia de saturación de oxígeno baja preoperatoria, posiblemente relacionada con resistencias pulmonares altas, tiempos de CEC prolongados y la presencia de infecciones postoperatorias.23,24
Todos nuestros pacientes presentaron derrame pleural con un promedio de 522 mL/m2/día. No encontramos asociación entre el número de días de estancia de los drenajes o el volumen y la mortalidad, sin embargo, especialmente en los pacientes que desarrollaron quilotórax, la estancia de los drenajes tuvo una media de 28 días contra 16 días en promedio para el total de los pacientes. Está descrito que tiempos de estancia prolongados, además de incrementar el tiempo en el hospital, pueden predisponer a depleción proteica y aparición de infecciones.25–27
A pesar de contar con parámetros adecuados preoperatorios hubo 5 pacientes que requirieron desmantelamiento del Fontan por falla cardíaca importante e hipertensión arterial pulmonar. En otros centros, se ha reportado que pacientes con estas características son apoyados con asistencia ventricular permitiendo así la adaptación a la cirugía o ser llevados a desmantelamiento y a la colocación de una fístula, y en caso necesario, entrar a lista de trasplante cardíaco. La mortalidad reportada en pacientes con mala respuesta a la circulación tipo Fontan a quienes se inicia asistencia ventricular es de 70%. Nuestra opción fue llevar a los pacientes a desmantelamiento, dejando una DCPB o una FBT, sin embargo de los 5 pacientes, 3 fallecieron de forma temprana (60%).28
Se describe en este trabajo que hubo intervenciones postquirurgicas secundarias a obstrucción de tubo, dehiscencia de anastomosis y sangrado, sin considerarse éstas como secundarias a la nueva fisiología de Fontan. Posterior al manejo de las complicaciones descritas, se dio una adecuada adaptación al nuevo estado quirúrgico, igual que ha sido considerado en otros trabajos. Por otro lado, por medio de cateterismo se ha logrado llevar a cabo algunos de estos procedimientos, como embolización de colaterales, dilatación de alguna estenosis en ramas de la arteria pulmonar, así como realización de fenestración o cierre de la misma.5,7 En nuestra experiencia fue de gran utilidad, por ejemplo en el caso de realización de fenestraciones, ya que de las quirúrgicas hubo dos fallecimientos en quirófano y otras dos fenestraciones fallidas, que lograron efectuarse por medio de cateterismo, situación similar a lo reportado por otros trabajos donde se habla de cateterismo intervencionista exitoso para creación de fenestraciones en pacientes con enteropatía perdedora de proteínas, oclusión de fenestración o de colaterales, etc.29
Se sabe que el tipo de cirugía puede influir en la presentación posterior de arritmias, debido a la presencia de material de sutura, dilatación atrial y elevación de la presión intra–atrial. Algunas técnicas de Fontan, se consideran menos arritmogénicas como el túnel lateral o el tubo extra–cardíaco, sin embargo se debe tomar en cuenta que las arritmias pueden deberse también a anomalías electrofisiológicas primarias o incluso ser secundarias a falla cardíaca. Hay series donde se reportan la no relación entre la variante de cirugía de Fontan y el desarrollo de arritmias. Un estudio de Stamm reporta que a largo plazo es más frecuente encontrar bradiarritmias que taquiarritmias, y que las primeras son más frecuentes en pacientes conbradiarritmia preoperatoria. Se ha reportado que muchos pacientes presentan disfunción del nodo sinusal o bloqueo AV, requiriendo en 7 a 12% la inserción de marcapaso definitivo.22
El manejo con anticoagulación para prevenir eventos trombóticos no está aceptado para su uso en todos los pacientes, habiéndose propuesto la utilización de heparina de bajo peso molecular, y en muchos casos manejo solamente con antiagregantes plaquetarios. En nuestro estudio, hubo reingresos en varias ocasiones secundarios a hemorragias, principalmente de tubo digestivo, en pacientes anticoagulados. Sin embargo también se reporta la presencia de obstrucciones de anastomosis así como eventos de tromboembolia, lo que apoya la necesidad de manejo continuo anticoagulante y de llevar una estrecha vigilancia de los tiempos de coagulación. Hay estudios que recomiendan anticoagulación en caso de función ventricular reducida, flutter o fibrilación atrial. Está reportado en otras series que los eventos tromboembólicos ocurren más frecuentemente en pacientes con fenestración, y que la mayoría de ellos se encontraban sin anticoagulación.5–12 Por todo lo antes mencionado, uno de los retos es lograr establecer factores de riesgo de trombosis o embolia en cada paciente, que sustenten el uso de antiagregantes, anticoagulación o de una terapia combinada.
Una complicación importante descrita ha sido la enteropatía perdedora de proteínas (EPP), se ha reportado una incidencia de 4% y una mortalidad de 13%. Se ha atribuido a presión sistémica elevada que produce linfangiectasias y pérdida de proteínas.30–32 En el presente estudio se presentó en 4 de nuestros pacientes (5%). Se ha reportado también buena respuesta con el uso de bloqueadores de la enzima convertidora de angiotensina y diuréticos, sin embargo en nuestro estudio pudimos apreciar que los pacientes que desarrollaron EPP tuvieron un mayor número de reingresos con aspectos de morbilidad, como la hipocalcemia, que los hace más propensos a arritmias, y en pacientes con falla ventricular, los puede hacer más susceptibles a muerte súbita.
Conclusiones
La cirugía de Fontan es en nuestro instituto la opción para pacientes con fisiología de ventrículo único. La selección de los pacientes de acuerdo a los parámetros clínicos, ecocardiográficos y hemodinámicos utilizados, en especial las resistencias vasculares pulmonares, PAMP y la función ventricular izquierda, es determinante para la evolución de los pacientes, sin embargo se debe tomar en cuenta que procedimientos quirúrgicos como la fenestración, han demostrado ser de gran valor para disminuir la mortalidad. Por otro lado, factores postquirúrgicos como la presión media de la arteria pulmonar y la presión de atrio izquierdo a las 72 h, demostraron serpredictores de riesgo de mortalidad. De esta manera, el encontrar valores elevados debe alertar al clínico para una vigilancia estrecha y para valorar en cada caso la posibilidad de desmantelamiento como procedimiento de rescate, tomando en cuenta que la mortalidad es muy elevada. Se deben tomar en cuenta las alteraciones que produce la fisiología del Fontan de forma integral, y detectar así complicaciones como falla renal, eventos vasculares cerebrales embólicos, en–teropatía perdedora de proteínas, ya que al presentarse producen un claro deterioro en la clase funcional y estado clínico de los pacientes.
Referencias
1. Fontan F, Kirklin J, Fernández G, Costa F, Naftel D, Tritto F, et al: Outcome after a perfect Fontan operation. Circulation 1990; 81: 1520–36. [ Links ]
2. Mair D, Puga F, Danielson G: Late functional status of survivors of the Fontan procedure performed during the 1970 's. Circulation 1992: 86 (Suppl II) 11106–109. [ Links ]
3. Schwartz S, Dent C, Musa N, Nelson D: Single–ventricle physiology. Critical Care Clinics 2003; 19:3–11. [ Links ]
4. Mott A, Spray T, Gaynor W, Godinez R, Nicolson S, Steven J, et al: Improved early results with cavopulmonary connections. Cardiol Young 2001; 11:3–11. [ Links ]
5. Geegle R: Update on the modified Fontan procedure. Current Opinion in Cardiology 1997; 12: 51–62. [ Links ]
6. Calderón–Colmenero J, Ramírez Marroquín S, Lince R, Zabal C, Rijlaarsdam M, Buendía A, et al: Cirugía de Fontan enAtresia Tricuspídea. Experiencia del Instituto Nacional de Cardiología "Ignacio Chavez". Arch Inst Cardiol Mex 1997; 67:210–16. [ Links ]
7. Stamm C, Friehs I, Mayer J, Zurakowski D, Triedman J, Moran A, et al: Long–term results of the lateral tunnel Fontan operation. J Thorac Cardiovasc Surg 2001; 121:28–41. [ Links ]
8. Mainwaring R, Lamberti J, Uzark K, Spicer R, Cocalis M, Moore J: Effect of accessory pulmonary blood flow on survival after bidirectional Glenn procedure. Circulation 1999; 100 (19) Suppl: II 151–11 156. [ Links ]
9. Chun D, Schamberger M, Flashpohler J, Turrentine M, Brown J, Farrel A, et al : Incidence, outcome, and risk factors for stroke after the Fontan procedure. J Am Coll Cardiol 2004; 93: 270–81. [ Links ]
10. Weber H, Gleason M, Myers J, Waldhausen J, Cyran S, Baylen B: The Fontan operation in infants less than 2 years of age. J Am Coll Cardiol 1992; 19: 828–33. [ Links ]
11. Burkhart H, Dearani J, Mair D, Warnes C, Rowland C, Schaff H, et al: The modified Fontan procedure: Early and late results in 132 adult patients. J Thorac Cardiovasc Surg 2003; 125: 1252–9. [ Links ]
12. Sittiwangkul R, Akazie A, Van Arsdell G, Williams W, McCrindle B: Outcomes oftricuspid atresia in the Fontan Era. Ann Thorac Surg 2004; 77: 889–94. [ Links ]
13. Ro P, Rychik J, Cohen M, Mahle W, Rome J: Diagnostic assesment before Fontan operation in patients with bidirectional cavopulmonary anastomosis. Are noninvasive methods sufficient? J Am Coll Cardiol 2004; 44: 184–7. [ Links ]
14. Calderón–Colmenero J, Ramírez S, Rijlaarsdam M, Buendía A, Zabal C, Zarco E: Use of bidirectional cavopulmonary shunt in patients under one year of age. Cardiol Young 1995; 5: 28–30. [ Links ]
15. Choussat A, Fontan F, Besse P, Vallot F, Chauve A, Bricaud H: Selection criteria for Fontan's procedure. Pediatric Cardiology 1st ed, Anderson RN Shinebourne EA eds. Edinburgh Churchill Livingstone, 1977: 559. [ Links ]
16. Nakano T, Kado H, Ishikawa S, Shiokawa Y, Us–hinohama H, Sagawa K, et al: Midterm surgical results of total cavopulmonary connections: Clinical advantages of the extracardiac conduit method. J Thorac Cardiovasc Surg 2004; 127: 730–7. [ Links ]
17. Sheik A, Tang A, Roman K, Baig K, Mehta R, Morgan J, et al: The failing Fontan circulation: successful conversion of atriopulmonary connections. J Thorac Cardiovasc Surg 2004; 128: 60–6. [ Links ]
18. Castañeda A: From Glenn to Fontan. A continuing evolution. Circulation 1992: 86 (Suppl II): H 80–1184. [ Links ]
19. Goff D, Bloom E, Gauvreau K, Mayer J, Lock J, Jenkins C: Clinical outcome offenestratedFontan patients after closure: the first 10years. Circulation 2000; 102(17): 2094–9. [ Links ]
20. Ramírez–Marroquín S, Calderón–Colmenero J, Lince R, Zabal C, Rijlaarsdam M, Buendía A: Cirugía de Fontanfenestrado en pacientes de alto riesgo. Arch Inst Cardiol Mex 1998; 68: 377–82. [ Links ]
21. Senzaki H, Masutani S, Kobayashi J, Sasaki N, Asano H, Kyo S, et al: Ventricular afterloadand ventricular work in Fontan circulation: comparison with normal two–ventricle circulation and single ventricle circulation with Blalock–Taussig shunts. Circulation2002; 105: 2885–92. [ Links ]
22. Freedom R, Hamilton R, Yoo S, Mkailian H, Benson L, McCrindle B, et al: The Fontan procedure: analysis of cohorts and late complications. Cardiol Young 2000; 10(4): 307–31. [ Links ]
23. Mahle W, Todd K, Fyfe D: Endothelial function following the Fontan operation. Am J Cardiol 2003; 91: 1286–8. [ Links ]
24. Gupta A, Daggett C, Behera S, Ferraro M, Wells W, Starnes V: Risk factors for persistent pleural effusions after the extracardiac Fontan procedure. J Thorac Cardiovasc Surg 2004; 127: 1664–9. [ Links ]
25. Mastalir E, Kalil R, Horowitz S, Wender O, Sant'Anna J, Prates P, et al: Late clinical outcomes of Fontan operation in patients with tricuspid atresia. Arq Bras Cardiol 2002; 79: 12–25. [ Links ]
26. Gentles T, Mayer J, Gauvreau K, Newburger J, Lock J, Kupfer–Schmid J, et al: Fontan operation in five hundred consecutive patients: factors influencing early and late outcomes. J Thorac Cardiovasc Surg 1997; 114: 376–91. [ Links ]
27. Bridges N: Fenestration of the Fontan Baffle: benefits and complications. J Thorac Cardiovasc Surg 1998; 1:9–14. [ Links ]
28. Booth K, Roth S, Thiagarajan R, Almodovar M, del Nido P, Laussen P: Extra corporeal membrane oxygenation support of the Fontan and bidirectional Glenn circulations. Ann Thorac Surg 2004; 77: 1341–8. [ Links ]
29. Kaulitz R, Ziemer G, Paul T, Peuster M, Bertram H, Hausdorf G: Fontan–typeprocedures: residual lesions and late interventions. Ann Thorac Surg 2002; 74: 778–85. [ Links ]
30. Border W, Syed A, Michelfelder E, Khoury P, Uzark K, Manning P, et al: Impaired systemic ventricular relaxation affects postoperative short–term outcome in Fontan patients. J Thorac Cardiovasc Surg 2003; 126: 1760–64. [ Links ]
31. Leval MR: The Fontan circulation: what have we learned? what to expect?Pediatr Cardiol 1998; 19: 316–20. [ Links ]
32. Mertens L, Hagler D, Sauer U, Somerville J, Gewillig M: Protein–losing enteropathy after the Fontan operation: an international multicenter study. PLE study group. J Thorac Cardiovasc Surg 1998,115: 1063–73. [ Links ]














