Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Archivos de cardiología de México
versão On-line ISSN 1665-1731versão impressa ISSN 1405-9940
Arch. Cardiol. Méx. vol.71 no.2 Ciudad de México Abr./Jun. 2001
Investigación clínica
Hallazgos ecocardiográficos transesofágicos en pacientes menores de 40 años con evento vascular cerebral
Transesophageal echocardiographic changes in patients younger than 40 years with embolic stroke
Adriana A. Ortega Gutiérrez,* Jesús Vargas Barrón,* Francisco-Javier Roldán* Antonio Arauz Góngora,** Ángel Romero Cárdenas*
* Instituto Nacional de Cardiología "Ignacio Chávez". Departamento de Ecocardiografía. (INCICH. Juan Badiano No. 1, 14080 México, D.F.).
** Instituto Nacional de Neurología y Neurocirugía.
Correspondencia
Dra. Adriana A. Ortega Gutiérrez.
Juan Badiano No. 1, 14080 México, D.F.
Tel. 5573 29 11 ext. 1212. Fax 5573-09-94
Aceptado: 17 de abril de 2001.
Resumen
Las anomalías cardiovasculares con potencialidad embolígena causantes de eventos vasculares cerebrales (EVC) isquémicos en menores de 40 años son asintomáticas y asignológicas. La finalidad de este estudio es justificar la implementación del ecocardiograma transesofágico (ETE) en todo protocolo de estudio de paciente joven con EVC isquémico.
Material y métodos: Se estudiaron con ETE 34 pacientes menores de 40 años con EVC isquémico. Se complementó con estudio contrastado en búsqueda de cortocircuitos intracavitarios.
Resultados: 19 pacientes fueron del sexo masculino y 15 del femenino con edades de 18 a 40 años (media 31 años). Ninguno tuvo signos o síntomas cardiovasculares. Se detectaron 11 anomalías en 20 pacientes (58.8%). De éstas, 3 son consideradas como probablemente embolígenas: el foramen oval permeable (FOP), prolapso valvular mitral y dilatación ventricular y se encontraron en 12 pacientes (35.29%). En 8 pacientes con anomalías cardiovasculares se encontró como factor asociado un estado hipercoagulable; 4 con FOP, 2 con engrosamientos valvulares y 2 con nódulos valvulares.
Conclusión: En pacientes menores de 40 años con EVC isquémico, el ETE detecta fuentes embolígenas directas e indirectas, aún en pacientes sin sospecha de enfermedad cardiaca.
Palabras clave: Ecocardiografía transesofágica. Evento vascular cerebral isquémico. Fuente cardiaca embolígena.
Abstract
The potential cardioembolic sources for ischemic stroke in patients younger than 40 years could be asymptomatic. The purpose of this study is to justify routine implementation of transesophageal echocardiography (TEE) in the study of young patients with ischemic stroke.
Material and methods: 34 patients younger than 40 years with ischemic stroke were studied with TEE complemented with contrast study, looking for potential cardioembolic sources or intracardiac shunts.
Results: 19 patiens were male and 15 female with ages between 18-40 years (average 31 years). None had cardiac signs or symptoms. Eleven anomalies were detected in 20 patients (58.8%); of these, only 3 were considered as probably coursing with cardioembolic sources: patent foramen ovale (PFO), mitral valve prolapse, and ventricular enlargement, which were found in 12 patients (35.29%). In patients with cardiovascular anomalies, we found a hypercoagulable state, associated in eight patients with PFO (four patients), two with valvular thickening, and two with valvular nodules.
Conclusions: I n patients younger than 40 years with ischemic stroke, TEE is useful in detecting direct and indirect cardiac sources of embolism, even in those patients with unsuspected cardiac disease.
Key words: Transesophageal echocardiography. Ischemic stroke. Cardioembolic source.
Introducción
La patología cerebrovascular es la tercera causa de muerte después de la cardiaca y el cáncer; la primera productora de discapacidad permanente en adultos y una causa importante de internamientos hospitalarios.1 Los datos obtenidos a partir de series epidemiológicas indican que los eventos cardioembólicos representan el 30% de todos los eventos vasculares cerebrales (EVC) de tipo isquémico.2 La incidencia de EVC en pacientes jóvenes, menores de 45 años es de 4%3 y la cardioembolia en este grupo etáreo representa el 30% de la etiología. El estudio TOAST4 ha definido las anormalidades cardiacas como de alto o moderado riesgo embolígeno, entre las primeras destacan la fibrilación auricular, prótesis valvulares, cardiopatía reumática, endocarditis bacteriana, mixoma auricular y miocardiopatía dilatada. Existe una categoría llamada "de origen probable", basada en hallazgos ecocardiográficos que sugieren la posibilidad de origen cardioembólico, como la permeabilidad del foramen oval, la calcificación del anillo mitral, la disfunción ventricular, el trombo ventricular y la ateromatosis de la aorta ascendente. A excepción del índice de embolismo secundario a placas ateromatosas mayores de 4 mm, existen escasos datos en relación al riesgo de EVC asociado a estas entidades.5 La finalidad del ETE en pacientes con EVC es detectar anomalías cardiovasculares con potencialidad embolígena, para así instalar un tratamiento adecuado y evitar recurrencias.
En la actualidad, no existe consenso en cuanto a la utilidad del ecocardiograma transesofágico (ETE) en el protocolo de estudio del paciente joven con EVC y en general sólo se ha justificado su realización ante la sospecha clínica de cardiopatía o cuando después del protocolo habitual no se ha detectado causa evidente.6 Estas entidades cardiológicas consideradas como probablemente embolígenas son generalmente asintomáticas y en los pacientes la exploración física y de gabinete pueden ser normales.
El objetivo de este estudio es demostrar la utilidad del ecocardiograma transesofágico en el protocolo de estudio del paciente joven con EVC para detectar alteraciones cardiovasculares con potencialidad embolígena.
Material y métodos
Se incluyeron en el estudio 34 pacientes con edades comprendidas entre 18 y 40 años (media de 31 años), del sexo masculino 16 y 15 del sexo femenino; estudiados de junio del 2000 a enero del 2001 quienes fueron derivados al Instituto Nacional de Cardiología para la realización de ETE como protocolo de estudio de EVC de tipo isquémico diagnosticado por tomografía de cráneo y resonancia magnética en el Instituto Nacional de Neurología y Neurocirugía. El protocolo de estudio incluyó la realización de historia clínica con énfasis en el interrogatorio de antecedentes de hipertensión arterial (HAS), diabetes mellitus (DM), tabaquismo, alcoholismo, ingesta de drogas, obesidad, cardiopatía, dislipidemia, arritmia cardiaca, migraña, trombosis venosa periférica, tromboembolia pulmonar, abortos espontáneos, síndrome antifosfolípido primario (SAFP), EVC previo y hemorragia cerebral previa. El protocolo de estudio incluyó la realización de Doppler carotídeo, Doppler transcraneal, angiografía cerebral, y determinación sérica de proteína C, proteína S, antitrombina III, resistencia a proteína C activada y anticardiolipinas.
Se les realizó ecocardiograma transtorácico y transesofágico con equipo HP Sonos 5500 con transductor de 2.5 mHz y sonda transesofágica multiplanar de 5 mHz en las modalidades bidimensional, modo M y Doppler. Se evaluó el diámetro de las cavidades cardiacas, el funcionamiento valvular, la integridad de los tabiques interatrial e interventricular, la orejuela izquierda y las paredes de la aorta. El ETE se complementó con estudio contrastado con la inyección en vena periférica de solución glucosada agitada en búsqueda de permeabilidad del foramen oval.
Los hallazgos se analizaron como rangos y porcentajes. Todos los pacientes fueron informados del propósito del estudio, que se realizó con su consentimiento.
Resultados
En ningún paciente se detectaron signos o síntomas cardiovasculares. Se encontró el antecedente de HAS en 2 (2.9%), migraña en 10 (29.4%) y tabaquismo en 13 (38.2%). Un paciente tenía cardiopatía conocida (marcapaso definitivo por bloqueo aurículoventricular congénito) (2.9%).
Las mediciones de septum, pared posterior, raíz de aorta y fracción de expulsión fueron normales en todos los pacientes. En un paciente se encontró dilatación auricular izquierda, en otro dilatación ventricular izquierda y en uno más dilatación auricular y ventricular izquierda (lo que representa 2.9% para cada caso).
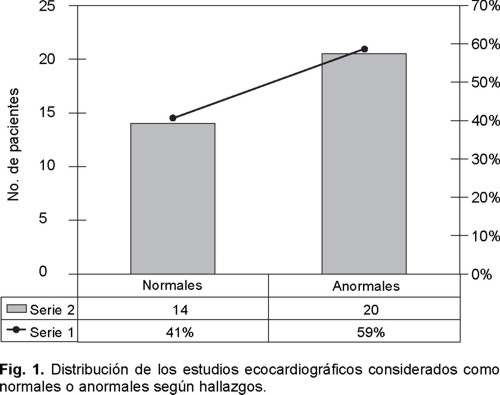
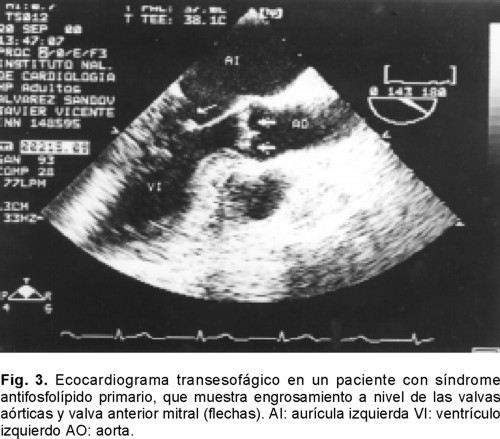
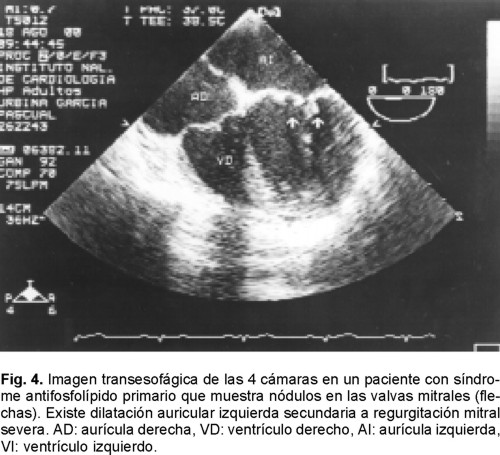
Por ETE se detectaron 11 anomalías cardiovasculares en 20 pacientes (58.8 %) (Fig. 1). De éstas, sólo 3 se han considerado como probablemente embolígenas: el foramen oval permeable (Fig. 2), el prolapso valvular mitral y la dilatación ventricular (encontrados en 12 pacientes, lo que representa el 35.29%). Se concluyó la posibilidad de etiología cardioembólica en 5 pacientes (14.7%), estado hipercoagulable en ocho (23.5%), vasculo-patía en tres (8.8%), aterosclerosis en dos (5.8%); la etiología no se precisó en tres (8.8%). En siete pacientes con anomalía cardiovascular se encontró como factor asociado síndrome antifosfolípido primario (cuatro con foramen oval permeable, dos con engrosamientos valvulares y uno con nódulos valvulares) (Figs. 3 y 4). En el paciente con trombos en el electrodo de marcapaso y foramen oval permeable se consideró la posibilidad de etiología cardioembólica asociada a estado hipercoagulable (causa-efecto).

Discusión
Existe debate acerca de cuales pacientes con EVC requieren estudio de imagen. Un estudio de costo beneficio7 concluyó que a pesar de un costo inicial mayor, el ETE fue de menor costo comparado con otras estrategias diagnósticas (como realizar sólo ETT seguido de ETE en pacientes con estudio anormal o sospecha clínica de cardiopatía). Un estudio canadiense publicado recientemente6 apoya que no existe evidencia suficiente a favor o en contra del ETE en pacientes con un ETT normal, ni en pacientes -incluso jóvenes- sin datos clínicos de cardiopatía. Husain y col8 consideran que, si el paciente no es candidato a anticoagulación o a corrección quirúgica, el ETE no estaría indicado porque sus hallazgos tendrían una implicación terapéutica escasa o nula. En sus lineamientos para la realización de ecocardiogramas, la Asociación Americana de Corazón (AHA) y el Colegio Americano de Cardiología (ACC) lo recomiendan en todo paciente menor de 45 años con EVC.9 De ahí que hasta el momento no existe consenso al respecto.
Las anomalías cardiovasculares han sido clasificadas de alto o moderado riesgo, basadas en su propensión para embolias.10 En nuestra serie de casos no encontramos ningún hallazgo ecocardiográfico considerado como de alto riesgo y sólo 3 de las 11 anomalías encontradas son consideradas de moderado riesgo: la permeabilidad del foramen oval, el prolapso valvular mitral y la dilatación ventricular. El significado de encontrar FoP en pacientes con EVC es aún incierto y es quizá de todas las causas de embolias el más complejo en términos de causalidad y profilaxis. Varios estudios han apoyado que existe una mayor incidencia de FoP en pacientes con EVC criptogénico.11 Se ha postulado la hipótesis de que el mecanismo es a través de embolia paradójica de trombo venoso o migración de trombo formado en un aneurisma del septum interauricular. En nuestra serie de casos, encontramos un paciente con trombos adheridos al cable del electrodo de marcapaso asociado a FOP, en el que se consideró la posibilidad de embolia paradójica. Se le encontró un estado hipercoagulable; además era portador de prolapso valvular mitral.
Un marcador anatómico puede identificar a pacientes de alto riesgo para EVC.12,13 Schuchlenz y cols.12 estudiaron un grupo de pacientes con EVC y FOP comparándolo con un grupo control con FOP sin otra patología y encontraron que el diámetro del foramen oval fue significativamente mayor (4 + 2 mm) en pacientes con EVC comparado con el control (2 + 1 mm) concluyendo que el diámetro del foramen oval es un factor de riesgo independiente para eventos isquémicos, en especial para recurrencias. Esto aporta bases para estudios posteriores diseñados para identificar pacientes de alto riesgo, enfocados en terapia preventiva (cierre percutáneo, cierre quirúrgico directo o tratamiento farmacológico).
El prolapso valvular mitral (PVM) se ha considerado como un factor de riesgo para EVC particularmente en pacientes jóvenes. El mecanismo aún no está claramente definido. Un subgrupo de pacientes con PVM y valvas redundantes identificados con ecocardiografía tienen un riesgo alto de embolia cerebral, endocarditis y muerte súbita.13 Se ha postulado que se puede formar un trombo de plaquetas y fibrina en la superficie de las valvas redundantes con posibilidad de embolización. Por esto se han empleado empíricamente agentes antiplaquetarios en pacientes con PVM e isquemia cerebral; sin embargo, no existen estudios que apoyen la utilidad de esta medida terapéutica.14 Hasta ahora, el prolapso valvular no es considerado como de alto riesgo.
Del resto de las anomalías encontradas en nuestra serie, merecen especial atención los engrasamientos y nódulos valvulares y su asociación con estado hipercoagulable. En este grupo, encontramos 8 pacientes con esta asociación. El 4% de los infartos cerebrales en jóvenes se atribuyen a alteraciones hematológicas que predisponen a trombosis. En la actualidad se ha reconocido que la trombosis arterial cerebral se asocia con deficiencia de elementos del sistema natural de anticoagulación.15 Recientemente se han estudiado y analizado las alteraciones cardiológicas que acompañan el síndrome antifosfolípido primario (SAFP). Espínola y col16 estudiaron una serie de 29 pacientes con SAFP en los que el 75.9% presentaron lesiones valvulares caracterizadas por nódulos irregulares adheridos al borde libre de las valvas aórticas y mitrales. Estos hallazgos concuerdan con los descritos por otros autores, quienes los consideran similares en localización y características ecocardiográficas a las lesiones de Libman-Sacks.17
Hasselaar y cols18 demostraron que el cultivo de células endoteliales de pacientes con lupus eritematoso sistémico y anticuerpos anticardiolipina tienen actividad procoagulante. Esto puede explicar en parte el mecanismo de trombosis y daño valvular en SAFP. Otros autores han propuesto que la patogénesis de estas lesiones consiste en proliferación vascular, infiltración por fibroblastos, necrosis y calcificación, más que trombosis local.19 Existen algunos trabajos que señalan un predominio entre las mujeres jóvenes afectadas de enfermedad vascular cerebral asociada a esta patología. Esta entidad, relativamente nueva, está aún en estudio en muchos aspectos de su patogénesis y la probabilidad de embolias a partir de la migración de pequeños elementos de estos nódulos valvulares aún no ha sido confirmada. Lo que resulta probable es la embolia paradójica de un trombo venoso, a través del foramen oval permeable. En el estudio, 4 pacientes con estado hipercoagulable tuvieron permeabilidad del foramen oval.
Conclusiones
Con base en nuestros hallazgos, podemos señalar las siguientes conclusiones:
1) Los pacientes menores de 40 años con EVC tienen elevada probabilidad de una fuente embolígena cardiovascular.
2) Algunas de las anomalías cardiovasculares relacionadas con EVC pueden no tener expresión clínica.
3) La ecocardiografía transesofágica es la técnica de elección para detectar, en forma no invasiva, anormalidades cardiovasculares potencialmente embolígenas.
Referencias
1. United States agency for Health Care Policy and Research. Post-stroke rehabilitation guideline panel. Clinical practice guidelines. Rockville, MD: U: S: Department of Health and Human services, 1995. AHCPR publication No. 92-0032. [ Links ]
2. Hinchey J, Furlan A, Barnett H: Cardiogenic brain embolism: incidence; varieties and treatment. In: Barnett HJM, Mohr JP, Stein B, Yatsu FM "Stroke, Pathophysiology, Diagnosis and Management". Ed 3., Philadelphia. Churchill-Livingstone, 1998; 1089. [ Links ]
3. Cianciulli T, Prezioso H, Lax J: Ecocardiografía clínica. Fuentes embolígenas cardiovasculares. En: Barrero C, Gimeno G, Liniado G, Mauro V. Cardiología 2000". Buenos Aires. Médica Panamericana, 1997; 643-689. [ Links ]
4. Adams H, Bendixen B, Kappelle L, Biller J, Lobe B, Gordon D, et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter trial. Stroke 1993; 24: 35-41. [ Links ]
5. Kistler J, Furie K: Patent foramen ovale diameter and embolic stroke: A part of the puzzle? Am J Med 2000; 109: 506-507. [ Links ]
6. Kapral M, Silver F: Canadian Task Force on preventive health care. Preventive health care, 1999 UPDATE: 2. Echocardiography for the detection of a cardiac source of embolus in patients with stroke: CMAJ 1999; 161: 989-96. [ Links ]
7. McNamara R, Lima J, Whelton P, Powe H: Echocardiography identification of cardiovascular sources of emboli to guide clinical management of stroke. A cost- effectiveness analysis. Ann intern Med 1997; 127: 775-787. [ Links ]
8. Husain AM, Alter M: Transesophageal echocardiography in diagnosing cardioembolic stroke. Clin Cardiol 1995; 18: 705-708. [ Links ]
9. Alpert J, Armstrong W, Aurigemma G, Beller G, Bierman F, Davidson T, et al: ACC/AHA Guidelines for the clinical application of echocardiography. A report of the American College of CardiologyAmerican Hearth Association Task Force on practice guidelines (Committee on Clinical Application of Echocardiography). JACC 1997; 29: 862-879. [ Links ]
10. Goldstein M, Barnett H, Orgogozo JM, Sartorius N, Symon L: Stroke-1989: Recommendations on stroke prevention, diagnosis and therapy. Report of the WHO Task Force on stroke and other cerebrovascular disorders. Stroke 1989; 20: 1407-1431. [ Links ]
11. Wein T, Bornstein N: Stroke Prevention. Cardiac and Carotid-related stroke. Neurologic Clinics. Houston, Sauders Co, 2000. [ Links ]
12. Schuchienz H, Weihs W, Horner S, Quehenberger F: The association between the diameter of a patent foramen ovale and the risk of embolic cerebrovascular events. Am J Med 2000; 109: 456-462. [ Links ]
13. De Castro S, Cartoni D, Fiorelli M, Rasura M, Beni S, Urani C, et al: Patent Foramen ovale and its embolic implicationes. Am J Cardiol 2000; 86: 51G-52G. [ Links ]
14. Brickner E: Cardioembolic stroke. Am J Med 1995; 100: 465-474. [ Links ]
15. Barinagarrementería F, Cantú C, De la Peña A, Izaguirre R: Prothrombotic states in young people with idiopathic stroke. A prospective study. Stroke 1994; 25: 287-290. [ Links ]
16. Espinola N, Vargas J, Colmenares T, Cruz F, Romero A, Keirns C, Amigo MC: Echocardiographic evaluation of patients with primary antiphospholipid syndrome. Am Heart J 1999; 137: 974-979. [ Links ]
17. Brenner B, Blumfeld Z, Markiewicz W: Cardiac involvement in patients with primary antiphospholipid syndrome. JACC 1991; 181: 931-936. [ Links ]
18. Hasselaar P, Derkson R, Oosting JD: Synergistic effect of low doses of tumor necrosis factor and sera from patients with systemic lupus erythematosus on the expression of procoagulant activity by cultured cells. Thromb Haemost 1989; 62: 654-660. [ Links ]
19. García R, Amigo MC, De la Rosa A: Valvular Heart disease in primary antiphospholipid syndrome: clinical and morphologial findings. Lupus 1996; 5: 56-61. [ Links ]














