Introducción
La maduración del ovocito de mamíferos es un proceso complejo y multifactorial que se inicia alrededor de la pubertad con el estímulo hormonal. Esta maduración del ovocito comprende una serie de cambios a nivel del núcleo, de la membrana plasmática y citoplásmicos que resultan en la formación de un óvulo capaz de ser fertilizado (Dalton et al., 2014).
El conocimiento de que altos niveles de AMPc participan como un factor inhibitorio en la maduración del ovocito (Conti et al., 2002; Duckworth et al., 2002; Kalinowski et al., 2004) y que el estímulo de la hormona luteinizante (LH) durante la pubertad es causante de la expansión y ruptura de las uniones comunicantes durante la maduración del ovocito (Kanatsu-Shinohara et al., 2000; Mehlmann, 2005), son algunos factores involucrados en este proceso, sin embargo, la participación de genes asociados con la maduración de ovocitos es muy limitada por ejemplo, la inhibición de la DNA metil transferasa 1 (Dnmt1) conduce a una disminución en el contenido del glutatión, en el número de mitocondrias, en la actividad de la glucosa-6-fosfato deshidrogenasa y en la distribución de los gránulos corticales (Huan et al., 2015); por su parte , la disminución de la expresión de RhoA en ovocitos causó fallas en la extrusión del cuerpo polar y el desarrollo embrionario (Zhang et al., 2014). En contraste a ellos, el silenciamiento de GPR3 elevó los porcentajes de maduración de los ovocitos, indicando que GPR3 es un regulador negativo de la maduración (Yang et al., 2012).
Por su parte el empleo de “modelos animales” como la generación de ratones nulos para genes específicos, también ha permitido la identificación de genes esenciales en la maduración, entre los que se encuentra TAF4b; ratones nulos para este gen producen ovocitos rodeados con un escaso número de células del cumulus, con bajas tasas de maduración y que, aún en el caso de ser fertilizados, se quedan detenidos como embriones de dos células (Falender et al., 2005).
Por otro lado, Cui et al., (2005) analizaron la expresión génica durante la maduración de los ovocitos del cerdo, identificando 13 incluido el gen ATPasa6 (ATP sintasa F0, subunidad 6), que forma parte de la ATP sintasa de la cadena respiratoria mitocondrial, responsable de fosforilar el ADP, para formar ATP con ayuda del gradiente de protones generado durante el transporte de electrones en la cadena respiratoria (Grover et al., 2008) (Figura 1). Sin embargo, en el terreno reproductivo, se desconoce el papel de la ATPasa6 y en particular en la maduración de ovocitos. A este respecto se ha identificado que el polimorfismo de este gen en espermatozoides humanos está asociado con problemas en la fertilización in vitro (Mao et al., 2015). Por otro lado, una mutación en la ATPasa6 y la sobreproducción de especies reactivas de oxígeno están relacionados con insuficiencia ovárica prematura humana (Venkatesh et al., 2010). Estos datos, aunados al hecho de que la ATPasa6 incrementa su expresión durante la maduración de los ovocitos del cerdo y a la importancia de la producción de ATP en la regulación de la maduración y desarrollo embrionario (Harris et al., 2009) sugieren que puede tener un papel fundamental en este proceso. Sin embargo, esto a la fecha no ha sido probado. Por lo tanto, el objetivo de este estudio se encaminó a determinar el papel de la ATPasa6 en la maduración de los ovocitos del cerdo in vitro, mediante su silenciamiento con RNA interferente.
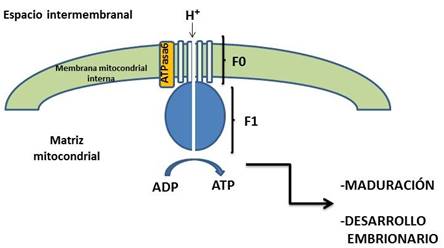
Figura 1 Esquema de la ATP sintasa o complejo V de la cadena respiratoria mitocondrial. Se muestran las subunidades F0 y F1 que la conforman, así como la ATPasa6, componente de F0. La formación de ATP por la ATP sintasa es un regulador de la maduración de ovocitos y el desarrollo embrionario (ver texto).
Material y Métodos
Todos los reactivos utilizados fueron de la marca Sigma (Sigma chemical Company, St Louis, MO EUA). Los reactivos y las soluciones se esterilizaron mediante filtración con membranas de 0.22 µm Millex-GV (Millipore). Todas las técnicas se realizaron bajo condiciones de esterilidad en campana de flujo laminar (Veco, México). Los procedimientos de Maduración in vitro (MIV) se realizaron cubriendo con aceite mineral.
Diseño experimental
Para determinar si la ATPasa6 tiene un papel en la maduración de los ovocitos del cerdo in vitro, se formaron dos grupos de estudio:
1) Grupo control, ovocitos microinyectados con RNAi para un gen de invertebrado, por tanto sin homología con algún gen de vertebrado (20 ovocitos por experimento).
2) Grupo experimental, ovocitos microinyectados con RNAi para ATPasa6 (20 ovocitos por experimento).
Los niveles de expresión de la ATPasa6 y de un gen constitutivo, β-actina, se analizaron al inicio de la maduración (t0) así como a las 24 y 48h de maduración. El efecto inhibitorio de la maduración se enfocó específicamente a las 24 h, cuando el RNAi tiene su máxima actividad inhibitoria, ya que posteriormente es degradado por la célula.
Tanto en el grupo control como en el experimental se analizó la progresión de la meiosis de los ovocitos al t0 y después de 44 h de incubación en “medio de maduración”, se identificaron ovocitos en estadio de vesícula germinal, metafase I o metafase II. Los experimentos se realizaron por triplicado en diferentes días.
Obtención y maduración de ovocitos porcinos
La maduración in vitro (MIV) de ovocitos porcinos se realizó de acuerdo con el método reportado por Casas et al., 2010. Se colectaron ovarios de cerdas prepúberes en el rastro, justo después de que los animales fueron sacrificados. Los ovarios se transportaron al laboratorio en solución salina 0.9% a 38ºC.
Los ovocitos rodeados por células del cumulus (COCs) se recuperaron del fluido folicular por punción con jeringa de 10 mL y aguja de 18G X 38 mm a partir de folículos de 3 a 6 mm de diámetro y se dejaron sedimentar, posteriormente fueron lavados con medio TL- HEPES-PVA. Bajo el microscopio se seleccionaron aquellos COCs en los que los ovocitos aparecían rodeados por una masa folicular compacta y presentaban un citoplasma granular uniforme. Estos COCs fueron lavados 3 veces en “medio de maduración” TCM-199 con bicarbonato y sales de Earle (In Vitro México) suplementado con PVA 0.1%, glucosa 3.05 mM y piruvato de sodio 0.91 mM, cisteina 0.57 mM y Factor de crecimiento epidérmico de glándula submaxiolar de ratón (10 ng/mL, Sigma) para posteriormente colocar de 30 a 35 COCs por pozo en una gota de 500 µL con el mismo medio y suplementado con las hormonas Folículo estimulante y Luteinizante de hipófisis porcina (0.5 μg/mL, Sigma). El medio se equilibró previamente con CO2 al 5% en una incubadora a 38.5 oC y humedad a saturación. Se dejaron madurar 48 horas en incubación en las mismas condiciones.
Microinyección de los ovocitos con RNAi
Las células de la granulosa fueron removidas de los COCs inmediatamente después de su recolección mediante su incubación con hialuronidasa al 1% durante 5 minutos a 37oC. Los ovocitos desnudos se colocaron en gotas de 3 mL de medio TL-HEPES en una caja de Petri y se cubrieron con aceite mineral. En cada experimento se formaron dos grupos (Experimental y Control): los ovocitos del grupo experimental fueron inyectados con 65 pL de Stealth RNAi 45-2001 (Invitrogen) para ATPasa6, en tanto que los del grupo control fueron microinyectados con un RNAi de invertebrado, sin presentar complementariedad con RNAm de vertebrados. Después de la microinyección, los ovocitos fueron incubados 48 h en medio TCM-199 bajo las condiciones mencionadas previamente.
Evaluación de la maduración de ovocitos mediante tinción con Hoechst
Posterior a la tinción con MTT y para remover el exceso de éste, los ovocitos se lavaron en gotas de 500 µL de PBS, se colocaron en otra caja, se cubrieron con 200 µL de Hoechst (3342) (45 μg/mL) en PBS, dejándolos durante 45 minutos en la oscuridad a 4°C. Posteriormente se lavaron en gotas de 500 μL de PBS, resuspendiendo de 2 a 3 veces para eliminar el exceso de Hoechst, y se colocaron en otra caja con 500 μL de fijador con PBS (glutaraldehído 50 μL/5mL), durante 20 minutos a temperatura ambiente y oscuridad. Después, aproximadamente 15 ovocitos se transfirieron a un portaobjetos con 20μL de medio de montaje (Glicerol-PBS 7:3), se colocó el cubreobjetos y se selló para su observación. La evaluación de la maduración de los ovocitos se llevó a cabo a 400 aumentos, utilizando un microscopio Zeiss, modelo Axioscop y filtro de fluorescencia con rango de excitación para luz ultravioleta (482 nm).
De acuerdo a las características observadas los ovocitos se clasificaron en: Inmaduros para aquellos que mostraron vesícula germinal (VG), en vías de maduración con cromosomas en Metafase I (MI) y Maduros para aquellos con cromosomas y primer cuerpo polar en extrusión Metafase II (MII) (Casas et al., 2010).
Ensayos de retrotranscripción y PCR
El RNA de ambos grupos de ovocitos se extrajo utilizando un estuche comercial de Promega. La retrotranscripción se llevó a cabo a 42° C durante 50 min. utilizando cebadores al azar y la enzima Superscript II (GibcoBRL). Los cebadores utilizados para amplificar por PCR a la ATPasa6 fueron los reportados por Cui et al., (2005), con las secuencias ATPasa6 F: 5’-CACCAAAAGGACGAACATGA-3’ y ATPasa6 R: 5’-TTCCTTGTGGAAGGAAGTGG-3’. Las secuencias de los cebadores de b-Actina usadas como control, son: b-Actina F: 5’- ATGGTGGGTATGGGTCAGAA-3’ y b-Actina R: 5’- CGGAGCTCGTTGTAGAAGGT-3’. La PCR se llevó a cabo durante 25 ciclos de 94°C por 30s, 60°C por 30s y 74°C por 1 min utilizando la enzima Taq DNA polimerasa de Promega. Los productos de PCR fueron separados en geles de agarosa al 2% y visualizados mediante tinción con bromuro de etidio.
Análisis estadístico
Los experimentos se llevaron a cabo por triplicado en diferentes días. La prueba t de Student se usó para evaluar las diferencias entre los grupos, que fueron consideradas significativas con p<0.05. El programa SPSS (SPSS Inc., Chicago, IL, USA) se utilizó para llevar a cabo los análisis estadísticos.
Resultados
La Figura 2 muestra el perfil de expresión de la ATPasa6 en ovocitos de cerdo madurados in vitro durante 48 h. La expresión de la ATPasa6 en ovocitos microinyectados con un RNAi de invertebrado (control) fue evidente desde el inicio de la maduración (tiempo 0, t0), su expresión continuó aumentando desde las 24 h, siendo un incremento significativo únicamente hasta las 48 h (p<0.05 con t de Student).

Figura 2 Patrón representativo de expresión de la ATPasa6 durante la maduración in vitro de los ovocitos del cerdo. A) La expresión de ATPasa6 y de β-actina (control de carga) en cada ovocito de cerdo se analizó mediante RT-PCR a las 0, 24 y 48h de maduración. En cada tiempo de maduración se analizaron 10 ovocitos por experimento. Los amplicones se corrieron en una electroforesis en gel de agarosa al 2 % y las bandas correspondientes fueron visualizadas mediante tinción con bromuro de etidio. B) Gráfica de la densitometría realizada a los amplicones de ATPasa6 y β-actina. Los valores de ATPasa6 fueron normalizados en relación a los de β-actina y se muestran como el promedio ± desviación estándar. Se observa un aumento de ATPasa6 en la maduración que es significativo a las 48h. Los experimentos se realizaron por triplicado en diferentes días. *Diferencia significativa con respecto al Control al tiempo 0, p<0.05 con t de Student.
La Figura 3 muestra el efecto del RNAi para la ATPasa6 en ovocitos. La expresión de la ATPasa6 disminuyó 71% (habiendo asignado al valor densitométrico de ATPasa6 en el grupo control un valor de 1) a las 24 h, cuando se comparó con aquellos ovocitos que recibieron únicamente el RNAi de invertebrados (p<0.05 con t de Student).

Figura 3 Silenciamiento de la ATPasa6 en ovocitos de cerdo madurados in vitro. A) Cada ovocito fue microinyectado con RNAi para la ATPasa6 (Experimento) o RNAi de invertebrado (Control) y después incubados en medio de maduración. La expresión de la ATPasa6 y de β-actina fue analizada a las 24h mediante RT-PCR (10 ovocitos por cada tiempo y experimento). Los amplicones se corrieron en una electroforesis en gel de agarosa al 2 % y las bandas correspondientes fueron visualizadas mediante tinción con bromuro de etidio. B) Gráfica de la densitometría realizada a los amplicones de la ATPasa6 y β-actina. Los valores de la ATPasa6 fueron normalizados en relación a los de β-actina y se muestran como el promedio ± desviación estándar. En los ovocitos microinyectados con RNAi para la ATPasa6 se observa una disminución significativa de la expresión de la ATPasa6. Los experimentos se realizaron por triplicado en diferentes días. *Diferencia significativa con respecto al control, p<0.05 con t de Student.
El análisis de la maduración de los ovocitos a las 48 h después del silenciamiento de la ATPasa6 indicó que el 62.5% de los que fueron microinyectados con RNAi lograron continuar con la meiosis hasta la metafase I y sólo el 33% alcanzó la metafase II, en contraste, el 67.5% de los del grupo control alcanzaron la metafase II de la meiosis, lo que corresponde a una disminución significativa del 51.1% (p<0.05 con t de Student; Figura 4).

Figura 4 Análisis del efecto del silenciamiento de la ATPasa6 sobre la maduración de ovocitos de cerdo in vitro. A) Los ovocitos fueron microinyectados con RNAi para la ATPasa6 (Experimento) o RNAi de invertebrado (Control) y fueron incubados en medio de maduración. A las 48 horas se analizó el porcentaje de ovocitos inmaduros (estadio de vesícula germinal, VG), en metafase I (MI) o metafase II (MII). Se usaron 20 ovocitos por grupo por experimento. Los experimentos se realizaron por triplicado en diferentes días. Los valores se muestran como el promedio ± desviación estándar. A las 48 h, la maduración de ovocitos (MII) microinyectados con RNAi para ATPasa6 (ATP-RNAi) es significativamente menor que el RNA de invertebrado usado como control (I-RNA). *Diferencia significativa con respecto al control, p<0.05 con t de Student.
Discusión
El presente estudio se encaminó a evaluar la participación de la ATPasa6 sobre la maduración in vitro de ovocitos utilizando como modelo el ovocito de cerdo. Los resultados mostraron que la expresión de la ATPasa6 fue silenciada en un 71% en aquellos que recibieron el RNAi para este gen. Este silenciamento de la ATPasa6 tuvo un impacto negativo sobre la maduración de los ovocitos, pues aunque el 62.5% de los ovocitos microinyectados con RNAi para ATPasa6 fueron capaces de progresar en la meiosis hasta la metafase I, únicamente el 33% de los ovocitos pudo alcanzar el estadio de metafase II.
La inhibición de la ATP sintasa, responsable de fosforilar el ADP para formar ATP (Grover et al., 2008) y vía canónica de regulación de la maduración del ovocito y el desarrollo embrionario temprano hasta el estadio de blastocisto (Harris et al., 2009; Koyama et al., 2014; Yuan et al., 2016; Lee et al., 2017), probablemente afectó la producción de ATP dentro del ovocito, lo que pudo causar que sólo el 33% de los tratados con el RNAi para la ATPasa6 alcanzaran la etapa de metafase II. Sin embargo no se descarta la posibilidad de que la ATP sintasa esté involucrada en otras vías metabólicas dentro del ovocito, por ejemplo, estudios recientes muestran que este complejo, puede regular la diferenciación celular participando en la maduración de las invaginaciones de la membrana interna mitocondrial, las llamadas crestas mitocondriales (Walker, 2013; Teixeira et al., 2015). Sin embargo, son necesarios más estudios para determinar si el bloqueo en la maduración de los ovocitos de los mamíferos por el silenciamiento de la ATPasa6 se basa en el efecto sobre las crestas mitocondriales del ovocito y de las células del cumulus que soportan su crecimiento y diferenciación.











 nova página do texto(beta)
nova página do texto(beta)


