INTRODUCCIÓN
En los diferentes ecosistemas acuáticos, metales como el calcio, cobalto, cobre, hierro, magnesio, manganeso, sodio y zinc (Ca, Co, Cu, Fe, Mg, Mn, Na, Zn) son esenciales a concentraciones traza. Mientras que, otros como el arsénico, cadmio, mercurio, plomo, etc., (As, Cd, Hg, Pb), provenientes de vertidos industriales y agrícolas se comportan como tóxicos a concentraciones muy bajas, por lo que no tienen un rol biológico benéfico para la biota (Bruins et al., 2000; Canli & Atli, 2003).
Dentro de esta clasificación, el cadmio como metal tóxico, persistente y bioacumulable genera estrés abiótico en los organismos acuáticos (Ivanina et al., 2008). Clasificado como carcinógeno humano en el grupo 1 por la Agencia Internacional para la Investigación sobre el Cáncer (IARC, 1993), cuando este metal entra al ecosistema acuático es potencialmente tóxico y es transferido a lo largo de la cadena trófica (Wright, 1994; Ruangsomboon & Wongrat, 2006). Entre las respuestas tóxicas el Cd presenta en primer lugar la alteración y competencia por los sitios de unión con metales esenciales especialmente el Zn, Fe, Cu y Ca, desplazándolos para unirse a los grupos tiol con la consecuente depleción de proteínas, enzimas (ej. glutatión peroxidasa, la superóxido dismutasa) y factores de transcripción (Mera et al., 2016). Aunque el Cd carece de actividad redox, indirectamente induce estrés oxidativo (Cailliatte et al., 2009), y se presenta tanto como un ión hidratado como en complejos iónicos orgánicos e inorgánicos. Las formas solubles del metal (en asociación con cloruros, sulfhidrilo, hidroxilo y grupos tiol) gobiernan en gran medida la actividad biológica del Cd; mientras que las formas insolubles en unión a sulfatos e hidróxido son inmóviles y absorbidas por el sedimento al depositarse en él (Vig, 2003; Faroon et al., 2012). Se ha demostrado que la concentración total disuelta del Cd tiende a incrementarse si se encuentra en forma iónica y varía con la concentración de Carbono Orgánico Disuelto (COD) (Fotovat & Naidu, 1998; Vig, 2003). En este contexto, las microalgas unicelulares son un componente fundamental de los distintos ecosistemas acuáticos, puesto que constituyen el primer eslabón que soporta a la cadena trófica acuática, representando la base de la producción fotosintética de gran parte del O2 y fijación de CO2 del planeta. De esta manera, cualquier alteración sobre el fitoplancton produciría un desequilibrio potencial en los niveles tróficos superiores con consecuencias negativas para la estabilidad del ecosistema (Franklin et al., 2000). En este contexto, los metales tóxicos al afectar a las comunidades planctónicas, provocan alteraciones en la fotosíntesis, crecimiento, inhibición de la actividad enzimática y la respiración (Yan & Pan, 2002). No obstante, la propiedad de persistencia y acumulación de los metales genera que algunas especies fotosintéticas sean sensibles, mientras que en otras se induzcan respuestas de bioacumulación, adaptación y resistencia (Gupta & Sandalio, 2012). En general, los niveles elevados de metales inducen la producción de especies reactivas de oxígeno (ROS); por tanto, como respuesta a ese estrés, la célula presenta mecanismos antioxidantes enzimáticos que incluyen a la superóxido dismutasa (SOD), catalasa (CAT), peroxidasa (POD) y sistemas no enzimáticos como el glutatión reducido (GSH), ascorbato y compuestos fenólicos (Xu et al., 2010).
De acuerdo con Macfie & Welbourn, (2014), entre los mecanismos principales que presentan las células fotosintéticas para mantener las concentraciones de iones metálicos libres en niveles que no superen las necesidades celulares se incluyen: (1) unión en la pared celular, (2) cambios en la permeabilidad de iones, (3) exclusión activa (ej. sistemas de eflujo), (4) biotransformación, (5) quelación extra e intracelular, y (6) compartimentación del metal. A partir de estos antecedentes, se ha propuesto que la capacidad de los metales de acumularse en las células microalgales por exposiciones continuas del contaminante metálico, daría lugar a mecanismos de resistencia a través de procesos adaptativos fisiológicos estimulados por cambios en la expresión genética y estructural (Belfiore & Anderson, 2001). No obstante, existe muy poca información sobre el comportamiento de la resistencia de los microorganismos fotosintéticos, especialmente en especies eucariotas de microalgas verdes a ambientes extremos, como la acidificación del hábitat, la presencia de altas concentraciones de otros metales y variaciones en la temperatura.
Por lo tanto, en esta revisión se examinan los principales mecanismos moleculares hasta el momento descritos que pueden estar involucrados en la resistencia de las microalgas a metales tóxicos, específicamente el cadmio; además de proporcionar una visión general sobre la influencia de distintos factores ambientales a esta respuesta, en episodios de corresistencia hacia otros metales de carácter tóxico y el conocimiento de los eventos moleculares por los que el Cd es absorbido por las microalgas con los mecanismos de resistencia que podrían proporcionar a posteriori los parámetros básicos, para el desarrollo de un sistema de monitoreo del grado de concentración del Cd, su biodisponibilidad y el comportamiento específico en interacción con otros metales en distintos ecosistemas acuáticos.
Respuestas Moleculares de Resistencia
Las microalgas expuestas al cadmio y bajo estrés provocado por éste, exhiben una diversidad de estrategias para mitigar los efectos adversos del metal (Zouari et al., 2016). Precisamente, existe información previa sobre la aparición de varios géneros de microalgas (Stigeoclonium, Chlorella, Chlamydomonas y Scenedesmus), resistentes a la exposición de distintos metales de carácter tóxico (ej. Cd, Pb, Cr) (Nishikawa & Tominaga, 2001; Pawlik-Skowrońska, 2001; Rehman & Shakoori, 2001; Baos et al., 2002; Lavoie et al., 2014). En otros estudios, se evaluó la sensibilidad de Dictyosphaerium chlrelloides por exposición al cromo como Cr(VI), evidenciando una destrucción masiva celular en la mayoría de la población, no obstante, se encontraron algunas cepas variantes resistentes con viabilidad a los ambientes contaminados con Cr(III) (Sánchez-Fortún et al., 2009; D’ors et al., 2010; Pereira et al., 2014). Dentro de los mecanismos básicos que se inducen por la exposición al Cd, se presenta la quelación intracelular a través de polipéptidos como las Metalotioneínas de clase III (Mt[III]), descrita a continuación.
Expresión de Mt(III)
Uno de los mecanismos que se han definido mejor en protistas, plantas, algas y algunos hongos sobre el proceso de detoxificación por metales tóxicos, es a través de la quelación de metales vía inducción del glutatión reducido (GSH) (Pantoja Munoz et al., 2016) y en la síntesis de Metalotioneínas de clase III (Mt[III]) a través de la fitoquelatina sintasa (PCS) enzima originalmente descubierta y caracterizada en la planta Silene cucubalus por Grill et al., (1989), siendo el Cd el mayor inductor de este sistema (activado también por Ag, Pb, Cu, Hg, Au, Zn) (Gekeler et al., 1988; Cobbett, 2000; Pawlik-Skowrońska, 2001; Mendoza-Cózatl et al., 2005). En 1992, Howe & Merchant revelaron que en Chlamydomonas reinhardtii la capacidad de quelación es a través de la expresión de Mt(III) al asimilar un 70% de Cd. Anteriormente, las metalotioneínas de clase III (MtIII), comúnmente denominadas fitoquelatinas (PCs) recibieron este nombre, al ser aisladas por primera vez de una planta superior (Rauvolfia serpentina) descubriéndose su capacidad de unirse a iones cadmio (Grill et al., 1985; Perales-Vela et al., 2006). La estructura general de las Mt(III) es (Ɣ-Glu-Cys) n -Gly, donde la longitud de la cadena “n” fluctúa entre 2 a 11 unidades con un peso molecular entre 2,000 a 10,000 Da (Grill et al., 1985; Steffens, 1990). Los primeros estudios sobre la identificación de isoformas de Mt(III) en microalgas lo llevaron a cabo en 1977 Stokes et al., en la clorofícea Scenedesmus acutiformis. Posteriormente, se han identificado estas Mt(III) en otras especies de microalgas del género Stichococcus y en diatomeas como en Thalassiosira (Knauer et al., 1998; Pawlik-Skowrońska et al., 2004). Estas proteínas se pueden unir a una gran variedad de metales en el citosol y, dependiendo del organismo, los complejos Mt(III)-metal y GSH-metal son transportados en forma activa dentro de la vacuola como se observó por primera vez en la microalga Dunaliella bioculata (Heuillet et al., 1986; Clemens, 2001). Al igual que otras metalotioneínas (ej. Mt(II)), las fitoquelatinas funcionan como apoenzimas con la consecuente activación con cofactores de iones metálicos esenciales e intervienen en la detoxificación de metales tóxicos (Thumann et al., 1991), como se observa en la Figura 1. Los complejos de Mt(III) de acuerdo a la inclusión de iones sulfuro se dividen en dos categorías: (I) la forma de bajo peso molecular (LMW) donde el metal tiene preferencia por su unión con grupos tiol (-SH) y (II) el complejo de alto peso molecular (HMW) donde iones de sulfuro inorgánico (S2-) están incorporados para formar nanopartículas (biomineralización) (Morelli & Scarano, 2001; Perales-Vela et al., 2006).
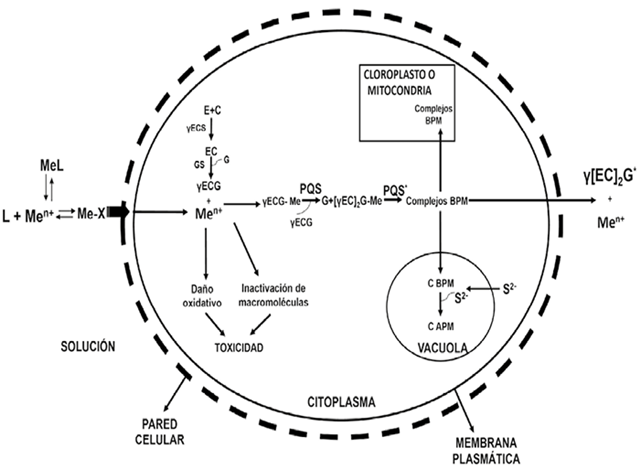
Figura 1 Mecanismo general de detoxificación de metales mediado por metalotioneínas de clase III (Mt(III)) en microalgas. Complejo metálico en solución (MeL), ion metálico libre (Men+), ligando biótico extracelular (X), ácido glutámico (E), cisteína (C), glicina (G), Glutatión sintetasa (GS), gamma glutamilcisteína (γEC), Glutatión (γECG), Metalotioneína n=2 (γ[EC]2G), Complejos de Bajo Peso Molecular (CBPM), Complejos de Alto Peso Molecular (CAPM), fitoquelatina sintasa (PQS), gamma glutamilcisteína sintetasa (γECS) (Perales-Vela et al., 2006).
Así, la formación de las Mt(III) puede realizarse principalmente por 3 procesos (Perales-Vela et al., 2006): (1) las Mt(III) se sintetizan en el citosol donde secuestran al Cd (II), los complejos Cd-Mt(III) son transportados posteriormente al cloroplasto y a las mitocondrias formando complejos de LMW; (2) las Mt(III) se sintetizan dentro de la vacuola donde se unen al Cd el cual es transportado como ion libre para formar complejos HMW y (3) ambos procesos co-existen y las Mt(III) se sintetizan en los tres compartimentos celulares (Mendoza-Cózatl et al., 2005). Anteriormente, se ha demostrado que la síntesis de Mt(III) está relacionada con el mecanismo de resistencia al cadmio y un aumento en su acumulación en protistas fotosintéticos como Euglena gracilis (Mendoza-Cózatl et al., 2002). En estudios genéticos previos, como el realizado por Ha et al., (1999), se demostró que mutantes PC-deficientes de crucíferas del género Arabidopsis, se comportan como hipersensibles al Cd. Sin embargo, se ha confirmado que no se induce la síntesis de Mt(III), bajo tratamientos con calor, frío, radiación ultravioleta (UV), anoxia y estrés oxidativo (Steffens, 1990).
Por otra parte, la entrada y la acumulación de iones metálicos por microorganismos, generalmente ocurre en dos etapas (Monteiro et al., 2012): (1) primero ocurre una adsorción inicial rápida, reversible y pasiva sobre la superficie celular donde los iones metálicos se adsorben a través de interacciones electrostáticas a grupos funcionales de la pared celular (OH-, SH-, COO-, PO4 3-, NO3 -RNH2-, RS- y RO-) (Figura 2); (2) Seguido por un proceso mucho más lento, irreversible, que implica el transporte activo de cationes metálicos a través de la membrana celular en el citoplasma, con la posterior unión a biomoléculas intracelulares (Perales-Vela et al., 2006; Zeraatkar et al., 2016).
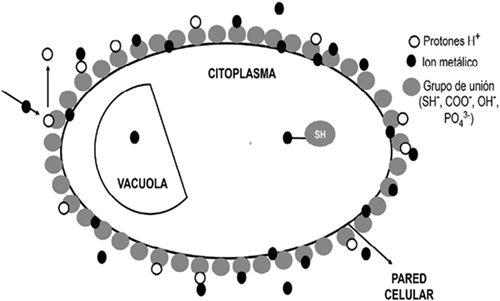
Figura 2 Mecanismo y diferentes grupos funcionales que participan en la biosorción de iones metálicos en microalgas (SH-, COO-, OH-, PO4 3-, etc.) (Zeraatkar et al., 2016).
Transportadores Ligados a la Resistencia al Cd
Es sabido que la captación (adsorción y absorción) de iones metálicos a través de la superficie de las microalgas se da por enlaces covalentes a través de grupos amino, carbonilo, carboxilo y sulfato (Perales-Vela et al., 2006). De igual forma, anteriormente ya se tenía conocimiento de que polisacáridos y proteínas presentes en las paredes celulares eran los principales responsables en el transporte de iones metálicos hacia el interior de la célula (Crist et al., 1981; Trevors et al., 1986). Como se menciona en el apartado anterior, en células de plantas, levaduras y microalgas, se conocen 5 familias de proteínas implicadas en el transporte activo de Cd a través de la membrana al interior de la célula: (1) antitransportador de M+/H+; (2) del tipo CPx ATPasas; (3) Facilitadores de difusión de cationes (CDF) que expulsan sustratos hacia el espacio periplásmico también denominado “familia de flujo de salida de cationes”; (4) los tipo Nramp su nombre proviene de proteínas asociadas a la resistencia de macrófagos (por sus siglas en inglés “Natural resistance associated macrophage proteins”); y (5) proteínas ZIP como ZRT-IRT (Guerinot, 2000; Williams et al., 2000). En levaduras, los transportadores Nramp, CDF y ZIP participan en el tráfico del ion Cd(II) entre el citosol y la vacuola (Mendoza-Cózatl et al., 2005). En las microalgas existe poca información de los transportadores involucrados en la movilización y en la capacidad de resistencia a cationes metálicos tanto esenciales como los utilizados por los no esenciales (Cd, Pb, As, Hg), creciendo en los últimos años el interés sobre su identificación y caracterización sobre estos organismos (ej. Chlamydomonas). Así, los transportadores Nramp de Chlamydomonas del tipo D2MT1 presentan amplia especificidad en el transporte de Mg> Mn > Cd > Cu > Fe, pero no a Zn (Rosakis & Köster, 2005). Page et al., (2009), identificaron a 2 transportadores con alta afinidad para Cu(II) y posiblemente para Cd(II) también sobre Chlamydomonas reinhardtii CTR1 y CTR2. Asimismo, se ha registrado un incremento en la transcripción de genes (EST2960 y EST2822) para la expresión de transportadores de sulfato en la membrana plasmática (por sus siglas en inglés PMST: EgPMST1, EgPMST2 y EgPMST3) en protistas fotosintéticos (Euglena gracilis) y microalgas que participan en la acumulación de metales tóxicos (García-García et al., 2012).
Con base en lo anterior, se ha propuesto que en las células fotosintéticas, el Cd induce el efecto conocido como “caballo de Troya”, ya que utiliza a los transportadores de los metales esenciales (ej. IRT1, transportador regulado de hierro tipo 1, o HMA4 transportador de Zn/Cd de tipo ATPasa) para internalizarse en la célula vegetal y provocar su respuesta tóxica (Cailliatte et al., 2009). Entre de los transportadores que utiliza el Cd destaca uno específico de calcio LCT1 de levaduras y CAX (H+/Ca2+) en Arabidopsis (Clemens et al., 1998). Una vez dentro en la célula fotosintética, el Cd se acumula en la vacuola a través de un antitransportador de M+/H+ ubicado en el tonoplasto (Salt & Wagner, 1993).
Conjuntamente, la biosorción, acumulación, toxicidad, y la adaptación a cationes de metales tóxicos por las microalgas pueden verse afectadas por varios factores que incluyen: (1) la concentración de iones metálicos, (2) la biomasa celular, (3) el pH, (4) la temperatura, y (5) la presencia de otros iones competidores (Zeraatkar et al., 2016).
Respuesta de Estrés a las Fluctuaciones del pH
Distintos factores ambientales afectan la toxicidad y la acumulación del cadmio en las microalgas. Uno de los parámetros esenciales que determina el comportamiento de los metales es el pH, modificando la especiación y biodisponibilidad de los mismos. Está claro que las propiedades fisicoquímicas del metal y del medio fijan la forma química en que éste puede presentarse (Vymazal, 1987; Canli & Atli, 2003). Asimismo, existe una gran cantidad de estudios que han demostrado que la toxicidad y la biodisponibilidad del Cd están determinadas por la concentración de la forma libre del metal (Allen et al., 1980; Campbel & Stokes, 1985; Franklin et al., 2000). La mayoría de los grupos de unión a metales en las microalgas son ácidos (por ejemplo, -COOH); estos grupos generan una superficie cargada negativamente a pH ácido, y en conjunto con las interacciones electrostáticas entre especies catiónicas y la superficie de la célula determinan en gran medida la biosorción del metal (Mehta & Gaur, 2005). Una disminución de la absorción de metales por las microalgas se ha observado con frecuencia a un pH extremadamente ácido (<2) debido a que probablemente la alta concentración de iones H+ generan la exclusión competitiva de la unión a los ligandos en la superficie celular (Campbel & Stokes, 1985; Gupta & Rastogi, 2008). En estudios previos realizados por Gipps & Coller, (1980) sobre la clorofícea Chlorella pyrenoidosa se encontró que, la absorción de Cd fue mayor a un pH de 8 que a 6.5. Posteriormente, en Scenedesmus obliquus, se reportó que la absorción y acumulación intracelular del Cd se dio a un rango de pH de 5-9 (Starý & Kratzer, 1982) Posteriormente, Pereira et al., (2013), revelaron que una cepa variante resistente de Dictyosphaerium chlorelloides a Cr(VI) (Dc1MCr(VI)R25) comparada con la variante tipo silvestre (Dc1Mwt), se comportó más resistente a la exposición de Cr(VI) a pH de 4.5 que de 7.5 tanto en la inhibición del crecimiento como en la actividad fotosintética.
Otro de los mecanismos que se inducen debido a la presencia de fluctuaciones de pH, es la expresión de las proteínas de choque térmico Hsp (por sus siglas en inglés “Heat-shock proteins”). Estas proteínas actúan en el plegamiento y ensamblaje de proteínas no nativas (desnaturalizadas), con actividad ATPasa, evitando la aglomeración de proteínas desnaturalizadas e incluso se ha demostrado que se expresan durante el estrés producido por metales tóxicos (Vierling, 1991; Jeffrey Morris, 2014). Asimismo, en estudios realizados por Bierkens et al., (1998), demostraron la inducción de algunas isoformas de Hsp70 en la microalga Raphidocelis subcapitata, debido a la acidificación del medio. Posteriormente, Gerloff-Elias et al., (2006) comprobaron la inducción y acumulación de estas mismas isoformas (Hsp70) en el mecanismo de adaptación de Chlamydomonas acidophila a fluctuaciones de pH y temperatura dependientes de ambientes acuáticos contaminados con elevadas concentraciones de metales (Fe, Al, Mn, Cr, Ni). En conjunto, se ha identificado una mayor inducción de ciertas proteínas periplásmicas comparadas con las proteínas citoplásmicas a diferentes valores de pH (9.0, 7.5, 6.0 y 5.5) sobre Synechocystis PCC6803. Así, entre las proteínas ácido-base inducidas en esta cianobacteria, se identificaron a la anhidrasa carbónica y a la oxalato descarboxilasa encargadas de la homeostasis del pH (Kurian et al., 2006). En el 2009, Zhang et al., identificaron mediante análisis proteómico sobre esta misma cianobacteria, la expresión de 39 proteínas inducidas a estrés por pH elevados y un tercio de las cuales corresponden a transportadores tipo ABC (glicoproteínas P dependientes de ATP) incluyendo 3 transportadores de fosfato. Entre otras de las proteínas identificadas destacan: MinD implicada en la división celular, Cya2 que participan en la señalización celular, PsaF con función sobre la actividad fotosintética y CoxB que tiene actividad sobre la respiración.
Resistencia al Estrés Inducido por Variaciones en la Temperatura e Irradiación
Las fluctuaciones de temperatura influyen directamente sobre la fluidez de la membrana celular, afectando el grado de saturación de los lípidos y la integración de proteínas transmembranales incrementando la salida de iones y otros solutos (Jeffrey Morris, 2014). De igual forma, las constantes de formación del complejo ligando-metal están regidas por la temperatura, y al aumentar en sus niveles por encima del rango óptimo en cultivos de microalgas no sólo se incrementa la capacidad de biosorción de los iones metálicos, sino también el número de sitios de unión implicados en la absorción metálica (Sari & Tuzen, 2009; Khan et al., 2012). Sin embargo, en otras investigaciones, se ha determinado que en las microalgas la absorción de iones metálicos es exotérmica, es decir, se incrementa la biosorción metálica cuando disminuye la temperatura (Gupta et al., 2010).
La primera respuesta al estrés producido por elevadas temperaturas es la desnaturalización proteíca que se traduce en pérdida de la actividad biológica, formación de agregados proteicos o en la inducción de la apoptosis celular. Para adaptarse a este estrés, las células fotosintéticas implican la inducción de chaperonas y proteasas como las Hsps para el replegamiento y degradación de proteínas (Vierling, 1991; Slabas et al., 2006). Como se mencionó anteriormente, se ha identificado el incremento de la síntesis de Hsp70 en Chlamydomonas acidophila en correlación a concentraciones elevadas de metales-temperatura (20-39°C) dependiente (Gerloff-Elias et al., 2006). La Hsp70 interviene en la degradación de proteínas defectuosas a través de la ruta del proteosoma (marcaje con ubiquitina por medio de la ubiquitina ligasa) (Lüders et al., 2000). En cultivos celulares de plantas superiores (Lycopersicon peruvianum), también se presentó la inducción de Hsp70 en respuesta al estrés producido por Cd (Neumann et al., 1994). Estos mismos investigadores demostraron que la Hsp70 se encontraba presente en el núcleo, el citoplasma y en la membrana plasmática, sugiriendo que esta proteína está implicada en la protección celular contra la exposición al Cd y al calor. Hihara et al., (2001) y posteriormente Summerfield & Sherman, (2008), identificaron a través de un análisis de microarreglos de DNA la expresión de una isoforma de HspA en la cianobacteria Synechocystis en respuesta a una alta intensidad lumínica, expuesta a elevadas temperaturas, en presencia de concentraciones salinas altas, estrés alcalino (pH 10), acidificación (pH 3) y exposición a la radiación UV.
A bajas temperaturas (por debajo de 20°C) las membranas se vuelven menos “fluidas” y la actividad de ciertas proteínas como las ATPasas se encuentra inhibida disminuyendo el transporte de solutos dentro y fuera de la célula (Jeffrey Morris, 2014). Los mecanismos que influyen en la adaptacion de las cianobacterias y otras microalgas a bajas temperaturas son la expresión de proteínas de choque frío (CAPs), proteínas anticongelantes (Antifreeze proteins: AFPs) y la acumulación de ácidos grasos poliinsaturados en membranas de diatomeas, dinoflagelados y microalgas verdes (Henderson et al., 1998; Mock & Kroon, 2002; Morgan-Kiss et al., 2002; Morgan-Kiss et al., 2006).
Napolitano & Shain (2004), encontraron que una de las estrategias de compensación adicional para el mantenimiento de las tasas de reacciones enzimáticas a temperaturas extremas en organismos fotosintéticos mesófilos y termófilos, consiste en elevar las tasas de producción de ATP (aumento de la fotofosforilación) y de adenilato total. Así, en la actividad fotosintética, cualquier estrés ambiental (ej. temperaturas bajas) que produzca una alteración entre la energía absorbida y la energía utilizada se detecta mediante el proceso redox a través del sistema de transporte de electrones y la acumulación de protones en las membranas de los tilacoides (Jeffrey Morris, 2014). De esta manera, el desequilibrio energético es corregido a través de la modulación a nivel de absorción de luz en el PSII (ej. disipación del exceso de energía en forma de calor NPQ) o a nivel de la energía utilizada a través de modulaciones de la actividad enzimática durante el ciclo de Calvin (Figura 3) y por medio de la regulación transcripcional traduciéndose a la adaptación a temperaturas extremas (Morgan-Kiss et al., 2006). Anteriormente, Lomas & Glibert, (1999), han propuesto que a bajas temperaturas y cuando la absorción de la luz excede los requerimientos energéticos del metabolismo, las poblaciones de diatomeas exhiben tasas relativamente elevadas en la absorción de NO3 - para modular el balance energético entre la producción y el requerimiento mismo.
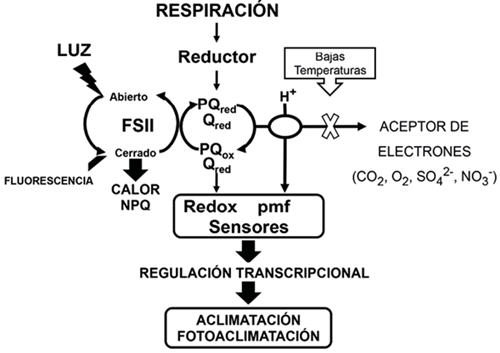
Figura 3 Sistema de transporte de electrones con actividad redox bajo variaciones en temperatura e intensidad lumínica. Fotosistema II (FSII), Procesos no fotoquímicos (NPQ-Calor), Plastoquinona reducida (PQred), Quinona reducida (Qred), Plastoquinona oxidada (PQox), Quinona reducida (Qox), fuerza protón-motriz (pmf) (Morgan-Kiss et al., 2006).
Con respecto a la respuesta generada por fluctuaciones en intensidad lumínica sobre las microalgas, la energía lumínica excesiva puede incrementar los niveles de moléculas a un estado excitado, como la clorofila triplete y el oxígeno singulete (1O2) (Okamoto et al., 2001). En adición, el anión superóxido (O2 • _ ) se genera durante la reducción del O2 en el PSI, la SOD (superóxido dismutasa) dismuta el O2 • _ a O2 y H2O2 y éste último tiene la capacidad de reaccionar con iones metálicos (ej., Cu (II), Fe(III)) produciendo el radical hidroxilo (HO•), un oxidante fuerte que puede reaccionar y generar estrés oxidativo sobre proteínas, enzimas clave (ej. RUBISCO en la fijación de CO2), peroxidación lipídica y alteraciones sobre el DNA; de la misma forma disminuye el rendimiento cuántico fotosintético, inhibición del crecimiento poblacional y la supervivencia de las microalgas (Takeda et al., 1995; Glatz et al., 1999). Ciertas cianobacterias y microalgas utilizan diferentes estrategias para contrarrestar la foto-oxidación de los rayos UV como son: (1) la evasión a través de la migración hacia zonas de bajo flujo de rayos UV (ej. Spirulina subsala); (2) la síntesis de pigmentos absorbentes de radiación UV (ej. escitonemina-370 nm), síntesis de metabolitos secundarios como aminoácidos tipo micosporina por vía del shikimato con una absorción máxima de 310 a 360 nm, antioxidantes (ej. síntesis de carotenoides, α-tocoferoles, ascorbato) y polisacáridos extracelulares (ej. producción de glicano extracelular en Nostoc commune) (Scherer et al., 1988; Ehling-Schulz et al., 1997; Quesada & Vincent, 1997); (3) mecanismos de reparación del DNA (ej. fotoreparación y reparación por escisión por el sistema SOS y el gen RecA identificado en cianobacterias) (Geoghegan & Houghton, 1987); (4) re-síntesis de proteínas sensibles a UV, por ejemplo, se ha detectado un aumento del recambio de las proteínas D1 y D2 del centro de reacción del PSII en Synechocystis sp. PCC6803 en respuesta a la irradiación UV-B (Sass et al., 1997); (5) Síntesis de Hsps y (6) la generación de NADPH (Ehling-Schulz & Scherer, 1999; Jeffrey Morris, 2014).
Comportamiento de Cepas de Microalgas Resistentes en la Interacción con Otros Metales
Otra de las variables a considerar sobre la resistencia al Cd en microalgas es, la interacción con otros metales. Esto es indispensable en el caso de resistencias cruzadas, cuando una especie o población es resistente a más de un metal al mismo tiempo (Gupta & Sandalio, 2012). Algunos autores sugieren que la existencia de diferencias en la sensibilidad de distintas especies de fitoplancton a la exposición de contaminantes metálicos, se deben a algún efecto estimulante sobre el crecimiento celular asociado con bajas concentraciones de Zn, Fe y Cu (Morelli & Scarano, 2001). Por otra parte, el comportamiento sinérgico que pudiera surgir debido a la interacción de distintos metales, podría aumentar el riesgo ambiental de bioacumulación (Baos et al., 2002). Por el contrario, la presencia de otros cationes metálicos en solución puede antagonizar la toxicidad del Cd (Torres et al., 1997). En el ambiente acuático, los metales Zn y Cd poseen la misma carga electrónica y una configuración electrónica similar, exhibiendo propiedades físicas y bioquímicas semejantes. Asimismo, comparten una afinidad equivalente a ligandos de S, N y O (Nieboer & Richardson, 1980; Newman & McCloskey, 1996) y en organismos acuáticos compiten con frecuencia por los mismos canales y transportadores, inhibiendo la unión y entrada de Ca y Mn (Wright, 1994; Barron & Albeke, 2000; Poteat et al., 2012). En contraste, el Ca ha demostrado ser altamente protector contra la absorción de Zn y Cd en organismos acuáticos (Barron & Albeke, 2000). De igual forma, las formas oxidadas del Mn (MnO x ) son muy reactivas con otros metales en su forma reducida (ej. Fe(II)) incluyendo al Cd modificando su biodisponibilidad y la posterior acumulación en sedimentos (Dong et al., 2000; Trivedi & Axe, 2000).
Poco se sabe de la interacción y el comportamiento molecular en la resistencia de las microalgas a diferentes metales tóxicos. En investigaciones realizadas por Navarro et al., (1997) y posteriormente por Avilés et al., (2003), demostraron que células de Euglena gracilis pretratadas con Hg(II) por 60 generaciones, mostraron mayor resistencia y acumulación al Cd después de 4 días de exposición, comparadas con las cepas tipo silvestre. Del mismo modo, Pawlik-Skowrońska (2003) reportó que una variante resistente de la microalga verde Stigeoclonium tenue aislada de aguas contaminadas por Zn presentó mayor tasa de acumulación de Pb y Zn comparado con la variante sensible. En bioensayos previos, Morsi Abd-El-Monem et al., (1998) demostraron que Scenedesmus acutus resistente al Cr(VI) también presentó una tasa de crecimiento máximo a concentraciones de Cu de 1.5 mg L-1, concluyendo que la variante es co-resistente a la exposición a otros metales. Asimismo, explicaron que la co-resistencia se debe a posibles mecanismos de exclusión celular y formación de complejos cúpricos con lo que se reduce la biodisponibilidad del metal en la célula. En investigaciones recientes, D’ors et al., (2016) estudiaron la interferencia de cationes metálicos tóxicos (Cd, Zn, Cr(III), Hg(II), Co, Fe(III) y Ag) sobre la respuesta fotosintética en una cepa resistente de Dictyosphaerium chlorelloides (DcCr(VI)R25) al Cr(VI), los resultados mostraron que el Zn fue el único metal con capacidad de interferencia en la actividad fotosintética de la cepa DcCr(VI)R25, mientras que los otros iones metálicos en mezclas binarias con el Zn mostraron una respuesta levemente antagónica.
Mecanismos Complementarios a la Resistencia de Metales
Uno de los mecanismos complementarios a la síntesis de Mt(III) es a través de la exclusión como una de las alternativas que han desarrollado las microalgas para mantener la homeostasis con metales presentes en el ecosistema (Perales-Vela et al., 2006). En varios estudios realizados en clorofíceas (Scenedesmus acutus), diatomeas y dinoflagelados, se demostró que este grupo de microalgas son más resistentes a la exposición a metales tóxicos, debido a la producción de exudados como polisacáridos extracelulares (aleloquímica) proporcionando una barrera para evitar la adsorción de varios cationes metálicos (Cr(VI), Cd y Cu(II)) (Corradi et al., 1998; Pistocchi et al., 2000). Por otro lado, Lavoie et al., (2009) encontraron en Chlamydomonas reinhardtii una acumulación de Cd de 2 a 4 veces mayor que en Pseudokirchneriella subcapitata. Asimismo, C. reinhardtii fue más resistente con una CE50 de 273nM comparada con el valor mostrado en P. subcapitata de 127nM. De igual forma, estos mismos investigadores demostraron que C. reinhardtii mostró mayor proporción de gránulos de Cd en cloroplastos y síntesis de altos niveles de PCs con oligómeros más largos y con mayor número de grupos tiol, con respecto a P. subcapitata, demostrando así las diferencias en estrategias de detoxificación del Cd y otros metales en varias especies de microalgas de agua dulce. En otros estudios utilizando rayos X, se ha documentado la presencia de gránulos compuestos por cadenas lineales de polifosfatos (poly-P) en el citoplasma y en vacuolas de varias especies de microalgas (ej. Dunaliella minuta) (Visviki & Rachlin, 1992; Nishikawa et al., 2006). Estas estructuras podrían participar en la desintoxicación de metales debido a la alta afinidad del fosfato a cationes metálicos y la baja solubilidad de los complejos de metal-fosfato (Lavoie et al., 2009).
Se ha confirmado que metales como el Cr(VI), induce la gametogénesis en Scenedesmus acutus produciendo cuatro células desprovistas de una pared celular propia, pero se observó que estas células compartían una envoltura común “madre” como un mecanismo de protección, ya que cada célula se encontraba delimitada por una membrana plasmática (Corradi et al., 1995). Igualmente, Rijstenbil, (2002) encontró un aumento en la reproducción sexual en la diatomea Ditylum brightwellii debido a la exposición al cobre (Cu2+). Por su parte, Scenedesmus incrassatulus exhibió una respuesta de plasticidad fenotípica como un evento de resistencia al Cd y Cu, creciendo en forma unicelular en presencia de estos cationes divalentes (con respecto al Cu(II)), mientras que cuando esta misma microalga fue expuesta al Cr(VI) se formaron coenobios irregulares correspondientes a las diversas etapas de la formación de autoesporas. No obstante, estos cambios fueron reversibles al retirar el Cu, pero no el Cd, debido a alteraciones irreversibles producidas por este metal. Estos resultados indicaron que los metales disminuyen la disponibilidad de energía en las microalgas a través de varios mecanismos, incluyendo el daño fotosintético mediante la producción de radicales libres, generando la reducción de la dominancia del coenobio de cuatro células en S. incrassatulus, y modificaciones sobre la cementación vacuolar en la formación del coenobio por estrés al Cd y Cu (Peña-Castro et al., 2004).
De forma simultánea a los mecanismos descritos que participan en la resistencia a metales, en investigaciones recientes se ha indicado una estrategia alternativa en la síntesis de aminoácidos como la prolina. En estos estudios, se ha demostrado en una cepa transgénica de Chlamydomonas reinhardtii, la expresión del gen de la enzima D1-pirrolina-5-carboxilato sintetasa con una producción de niveles elevados por encima del 80% de prolina, lo que resulta en una mayor capacidad de crecimiento a concentraciones altas de 100μM de Cd específicamente, lo que representa mayor resistencia en el orden de 4 veces mayor comparada con la del tipo silvestre (Mehta & Gaur, 1999; Siripornadulsil, 2002; Sharma & Dietz, 2006; Jamers et al., 2013).
CONCLUSIONES
La presencia de elevadas concentraciones de metales tóxicos como el Cd en los diferentes ecosistemas acuáticos debido a las actividades industriales y agrícolas, supone un riesgo potencial en condiciones que favorecen su bioacumulación y biomagnificación a lo largo de la cadena trófica. No obstante, al afectar a los primeros niveles tróficos acuáticos, también representa una presión selectiva sobre la generación de microalgas variantes resistentes con alta capacidad de supervivencia en ambientes contaminados por metales tóxicos. Esta selección de variantes resistentes condiciona y determina los diferentes mecanismos moleculares por los que se rige esa capacidad. A la vez establece los criterios por los cuales diferentes parámetros fisicoquímicos modifican la toxicidad, biodisponibilidad, solubilidad, adsorción y absorción, interacción con biomoléculas, y modificaciones genéticas que intervienen en las cepas resistentes. De igual forma, complejas interacciones se han puesto de manifiesto cuando varios metales y otras sustancias actúan de forma simultánea produciendo respuestas sinérgicas, antagónicas o aditivas.
Por consiguiente, el conocimiento de los mecanismos específicos del Cd sobre la actividad fotosintética, el balance de oxígeno, el comportamiento en la respiración e interacción con otros metales de carácter tóxico en microalgas eucariotas del phylum Chlorophyta, sigue siendo poco estudiado y marca el punto de partida para nuevas investigaciones enfocadas en el aislamiento de cepas de microalgas resistentes, para utilizarse como modelos biológicos en la identificación y posterior elucidación de los eventos genéticos y moleculares específicos, que determinan la resistencia en estas especies de microalgas. Esto mismo, establecerá en un futuro los principios básicos en el desarrollo biotecnológico de sistemas de monitoreo in situ para la rápida detección de concentraciones de Cd y otros metales tóxicos, a través de la tecnología de biosensores. Así como la implementación de métodos de biorremediación (ficorremediación) de cuerpos de agua contaminados por metales, utilizando a variantes resistentes de microalgas.











 nova página do texto(beta)
nova página do texto(beta)


