Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
TIP. Revista especializada en ciencias químico-biológicas
versión impresa ISSN 1405-888X
TIP vol.14 no.1 Ciudad de México jun. 2011
Artículo original
Producción de electricidad en celdas de combustible microbianas utilizando agua residual: efecto de la distancia entre electrodos
Electricity production in microbial fuel cells using wastewater: Effect of the distance between the electrodes
Germán Buitrón* y Jaime Pérez
Lab. Investigación en Procesos Avanzados de Tratamiento de Aguas, Unidad Académica Junquilla, Instituto de Ingeniería, Universidad Nacional Autónoma de México. Blvd. Juriquilla 3001, Querétaro, 76230 Querétaro, México. *E-mail: gbuitronm@ii.unam.mx.
Artículo recibido el 14 de febrero de 2011;
Aceptado el 25 de abril de 2011.
Resumen
Se evaluó la influencia de la separación de electrodos sobre la producción de electricidad y la eliminación de materia orgánica en celdas de combustible microbianas usando agua residual. Para ello se construyeron tres celdas de geometría semejante pero con diferente volumen. En promedio, se obtuvo una eficiencia de eliminación de materia orgánica del 71%. La duración del ciclo fue de 0.97 días para la celda de 40 mL, 1.03 días para la celda de 80 mL y 5.93 días para la celda de 120 mL. El aumento de distancia entre los electrodos (4, 8 y 12 cm) no causó un efecto negativo en la generación de electricidad, pues en la mayor separación (celda de 120 mL) se alcanzó un voltaje máximo de 660 mV, mientras que para las celdas de 40 y 80 mL fue de 540 mV y 532 mV, respectivamente. La densidad de potencia máxima se presentó en la celda con separación de 12 cm (408 mW/m2). Sin embargo, se observó que la potencia volumétrica disminuyó a medida que aumentó la separación entre los electrodos.
Palabras Clave: Agua residual, biodegradación, celdas de combustible microbianas, electricidad, tratamiento de aguas.
Abstract
The influence of the electrode separation on electricity production and organic matter removal was studied in microbial fuel cells using wastewater. Three cells were constructed with similar geometry, but different volume. On average, 71% of the initial organic matter was removed. cycle duration was 0.97, 1.03 and 5.93 days for the 40, 80 and 120 mL cells, respectively. The increment of the distance between the electrodes (4, 8 and 12 cm) did not affect electricity generation adversely. The higher voltage was obtained in the 120 mL cell (660 mV), whereas 540 and 532 mV were obtained for the 40 and 80 mL cells, respectively. Maximum power density was 408 mW/m2 and was obtained in the 12 cm cell. However, it was observed that volumetric power decreased as the separation between electrodes increased.
Key Words: Wastewater, biodegradation, microbial fuel cells, electricity, wastewater treatment.
Introducción
En México se generan alrededor de 250 m3/s de aguas residuales municipales. De esta cantidad se trata solamente cerca del 25%; el reto por resolver es enorme. Cuando se lleva a cabo el tratamiento, la mayoría de las instalaciones operan utilizando el proceso aerobio conocido como lodos activados. Este proceso es un alto consumidor de energía, la cual es necesaria para la aeración del sistema. En general, se necesita 1 kWh de energía para la oxidación de un para la oxidación de materia orgánica que contiene un kilogramo de carbono presente en el agua, alrededor de 0.5 kWh por m3 de agua residual a tratar. Existen procesos anaerobios que pueden reducir los costos de operación de los procesos, pero éstos son factibles cuando las aguas presentan altas concentraciones de materia orgánica, como las generadas en la agroindustria. Desde hace varios años se sabe que las bacterias pueden ser utilizadas para generar electricidad. Es interesante, entonces, llevar a cabo la degradación de la materia orgánica presente en las aguas residuales por una parte y, por otra, generar electricidad. El propósito de este sistema no sería competir con las tecnologías existentes para generar electricidad a gran escala, sino tratar el agua residual y obtener durante este proceso un producto de valor agregado. Es decir, ver el tratamiento del agua no sólo como algo necesario para la sustentabilidad, sino también como un proceso que valoriza la materia orgánica presente. Bajo condiciones adecuadas de desarrollo tecnológico, este tipo de proceso podría no solamente ser utilizado a gran escala para tratar aguas residuales de una ciudad o industria, sino también sería factible para ser instalado en pequeñas comunidades habitacionales o incluso en comunidades dispersas o aisladas del país.
Las celdas de combustible microbiano (CCM) son dispositivos que se encargan de convertir energía bioquímica a energía eléctrica mediante microorganismos[1,2]. Las bacterias obtienen la energía transfiriendo electrones desde un donador de electrones, como el acetato o el agua residual (materia orgánica), hacia un aceptor de electrones, como el oxígeno. Cuanto mayor sea la diferencia de potencial entre el donador y el aceptor, mayor será la ganancia energética para la bacteria y, generalmente, mayor será su tasa de reproducción y, por lo tanto, de eliminación de la materia orgánica. En una CCM, las bacterias no transfieren directamente los electrones a un aceptor final de electrones característico, sino que lo hacen a un electrodo, es decir hacia un ánodo. Posteriormente, los electrones pasan a través de una resistencia, u otra carga, hacia un cátodo, por lo que los electrones generados en la reacción son "cosechados" y convertidos directamente en energía eléctrica. El carbono orgánico es transformado a CO2. El ciclo se cierra cuando los protones migran hacia el cátodo en aerobiosis donde se combinan con el oxígeno y se forma agua. Para aumentar la eficiencia en la generación de electricidad y eliminación de los contaminantes, se investigan las especies que son capaces de transferir electrones, el diseño y los materiales que constituyen las celdas, la adición de mediadores químicos, membranas intercambiadoras de protones, las condiciones ambientales más favorables para la actividad microbiana, etc. Por ejemplo, se ha encontrado que algunos de los géneros con especies activas electrogénicamente son Geobacter, Shewanella y Clostridium, pero parece ser que la mejor respuesta la presentan los consorcios o lodos[2].
CCM en el tratamiento de aguas
En general las CCM han sido utilizadas para producir electricidad a partir de sustratos como la glucosa, el acetato y el lactato. Liu et al.[3] demostraron que es posible obtener electricidad en una CCM a partir de aguas residuales domésticas, acompañando el proceso de una remoción de la demanda química de oxígeno (DQO). Se observó una producción máxima de potencia de 26 mW/ m2 de electrodo y se removió el 80% de la DQO inicial del agua. Sin embargo, se obtuvo una eficiencia coulómbica del sistema, basada en la remoción de la DQO y en la generación de corriente, inferior al 12%, indicando que gran parte de la materia orgánica no contribuyó a la generación de electricidad. Rabaey et al.[4] evaluaron el desempeño de una CCM tubular obteniendo eficiencias coulómbicas para aguas residuales del orden de 96% y 48 W/m3 de compartimiento anódico. Las CCM han sido aplicadas también en el tratamiento de aguas de diversos orígenes[5,6], obteniendo densidades de potencia entre 240 y 500 mW/m2 y voltajes del orden de 200 a 400 mV.
En este trabajo se evaluó una estrategia de arranque para favorecer la colonización del ánodo y el efecto de la distancia entre electrodos sobre el desempeño de una celda de combustible microbiana que utiliza aguas residuales como sustrato.
Materiales y métodos
Se construyeron dos tipos de celdas. En un primer prototipo (tipo H) se evaluó la estrategia de colonización del ánodo. En los siguientes prototipos (celdas de una cámara) se evaluó el efecto de la distancia entre electrodos, variando el volumen de la celda, sobre la producción de electricidad. Ambos prototipos fueron operados por lotes.
Evaluación de la estrategia de puesta en marcha de la celda
Para esta etapa, la celda de combustible microbiana (Figura 1) consistió en dos matraces de vidrio de 200 mL. El ánodo se mantuvo en condiciones anaerobias cerrado con un tapón de hule y el cátodo en condiciones aerobias mediante el burbujeo de aire. Los electrodos consistieron en varillas de carbón de 0.5 mm de diámetro y 8 cm de longitud con un área de 10.55 cm2. Éstos se conectaron con alambre de cobre a un resistor variable y un voltímetro para el registro del voltaje. Las pruebas se llevaron a cabo con agitación continua de 90 rpm. Al ánodo se introdujo el agua residual a degradar. Se realizaron cinéticas tomando 5 mL de muestra a intervalos regulares de tiempo, cuidando de no introducir aire a la cámara del ánodo.

Se colocó un puente salino para el intercambio de protones y consistió en un tubo de vidrio de 5 mm de diámetro manteniendo una distancia entre ánodo y cátodo de 18 cm y doblado 6 cm en cada extremo a fin de facilitar su introducción en el ánodo y el cátodo. El puente se llenó con agar y sales de acuerdo con Du et al.[7]
Agua residual
Se trabajó con agua residual proveniente de la planta de tratamiento de aguas del Campus Juriquilla, UNAM. El agua residual contenía una DQO entre 192 y 430 mg DQOs/L. Se adicionó glucosa para mantener la concentración en 2250 mg/L. Cada prueba tuvo una duración de una semana.
Evaluación de la distancia entre electrodos sobre el desempeño de las CCM
Se construyeron tres celdas con diferentes volúmenes de una sola cámara y sin membrana protónica para estudiar su desempeño. A este respecto se ha visto que no es necesario mantener el cátodo sumergido en agua y en una cámara separada, pues se ha visto que el emplear celdas de una sola cámara puede incrementar el desempeño de la celda[2]. En este caso el cátodo se coloca directamente en contacto con el aire. Se utilizaron láminas y tubos de acrílico, de 6 mm de grosor y 5.5 cm de diámetro, respectivamente. Para el ánodo se utilizó un electrodo de papel grafito Toray tipo S (E-Tek). Para el cátodo se utilizó un electrodo de carbón rígido conteniendo 0.35 mg/cm2 de platino como catalizador (E-Tek). Para conectar el circuito se utilizó alambre de platino (Sigma Chemical) pegado a los electrodos con resina epóxica de grafito (Electrosynthesis). Ambos discos fueron de 4.5 cm de diámetro, por lo que el área del cátodo y ánodo en todas las celdas fue de 0.001385 m2. El lado con platino se orientó hacia el interior de la celda y el otro lado quedó expuesto al aire. El cátodo de la celda se sujetó al acrílico con 6 tornillos y foamy como aislante (Figura 2).
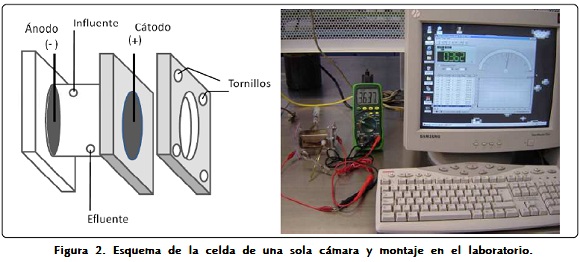
A tres de las celdas (40, 80 y 120 mL de capacidad) se les colocó una resistencia de 1000 Ω. La separación entre los electrodos fue de 2.8, 5.5 y 8.2 cm para las celdas de 40, 80 y 120 mL, respectivamente. Se construyó otra celda adicional de un volumen de 75 mL, sin resistencia. Esta celda se fabricó con la finalidad de obtener una colonización óptima para después realizar los análisis microscópicos correspondientes para la identificación bacteriana del dispositivo. También fue utilizada como control para determinar la contribución eléctrica de agua residual esterilizada, de los nutrientes y de todo el sistema en conjunto.
Para la operación de las celdas se utilizó agua residual de la planta de tratamiento del Campus Juriquilla de la UNAM, adicionada con una solución de acetato de sodio con una concentración de 100 mg/L. El ánodo se colonizó con las bacterias presentes en el agua residual. El pH se mantuvo entre 7 y 8 durante todo el experimento y se trabajó a temperatura ambiente (entre 14 y 23°C).
Análisis fisicoquímicos
El consumo de la materia orgánica se evaluó a través de la DQO y el carbono orgánico disuelto (COD). La cuantificación de la DQO se realizó según la técnica de la APHA[8]. El análisis para la determinación de Carbono Orgánico disuelto se realizó en un equipo TOC-5050Auto Sampler (Total Organic Carbon Analyzer) marca Shimadzu. Para la preparación de las muestras para dicha medición fue necesario llevarlas a un proceso de centrifugación a 3500 rpm por un tiempo de 7 min, una filtración con papel filtro de microfibra de vidrio (Whatman) y, posteriormente, la acidificación de las muestras añadiéndoles 35 μl de HCl 2M. Cada prueba se realizó por triplicado.
Cálculos
El voltaje se midió en línea con un multímetro Minipa ET-2231 conectado a una tarjeta de adquisición de datos y almacenados en una computadora. La corriente eléctrica (I) fue calculada en relación a la resistencia (R) y el voltaje (V) por medio de la ley de Ohm. La potencia generada (P) se obtuvo al multiplicar la intensidad por el voltaje. Para poder hacer comparaciones con otros trabajos, se calculó la densidad de potencia dividiendo P entre el área superficial del ánodo. El pH fue utilizado para el control del sistema.
Resultados y discusión
Evaluación de la puesta en marcha de la celda
La celda tipo H fue operada por tres semanas. Los electrodos se colonizaron paulatinamente. Después de una semana se observó una biopelícula sobre el ánodo y la degradación de materia orgánica se produjo en alrededor de 8 h. Se encontró que se producía una correcta colonización del ánodo aplicando una resistencia de 1000 Ω.
La concentración promedio de la DQO alimentada fue de 2268 mg/L y una COD inicial de 812 mg/L. Bajo estas condiciones se encontró una eliminación de materia orgánica del 80% en 8h y con un voltaje máximo producido de 462 mV (Figura 3). Se observó que la producción de voltaje aumentó a medida que la materia orgánica fue degradada, pasando por un máximo. La densidad de potencia máxima fue de 14 mW/m2, baja si se compara con las reportadas por otros autores[3,9] de hasta 500 mW/m2.

Durante el arranque se observó la acidificación de la cámara del ánodo. Una vez que el sistema se estabilizó, se llevó a cabo una cinética con el seguimiento de este parámetro. La Figura 4 muestra que a medida que la materia orgánica se consume, el ánodo se acidifica, lo que en parte explica la caída en la producción de voltaje ya observada. Con estos resultados se concluyó que después de una semana y con resistencia de 1000 O fue posible colonizar adecuadamente el electrodo. Sin embargo, el principal problema operacional fue la acidificación del ánodo que trajo como consecuencia una baja en la producción de energía. Este resultado nos llevó a la decisión de trabajar con otro tipo de celda.

Evaluación del funcionamiento de las CCM
Se realizó un experimento para demostrar que efectivamente las celdas de combustible microbianas usadas en la investigación generan energía eléctrica a partir de la transformación del agua residual y no simplemente por una reacción electroquímica. Para ello, se llevaron a cabo tres cinéticas con diferentes condiciones de alimentación. Para cada una de ellas se midió el voltaje generado por al menos 18 h (1100 min). Todas las pruebas se realizaron con una resistencia de 1000 Ω.
En primer lugar, una celda virgen sin ánodo colonizado, fue alimentada con sales minerales en agua desmineralizada (prueba N). Para la segunda prueba, la celda se alimentó con agua residual centrifugada (para eliminar la mayor parte de las bacterias), acetato y nutrientes (Prueba N+AR). Finalmente, se colonizó el ánodo por una semana y se determinó la cinética de generación de voltaje agregando agua residual, acetato y nutrientes (Prueba N+AR+B). Los resultados se presentan en la Figura 5.

Se observó que para las tres condiciones hubo generación de voltaje. El mínimo fue para el caso de la celda sin bacterias y sales minerales y el máximo se obtuvo en la celda colonizada. La celda que contenía exclusivamente sales minerales generó un voltaje constante de alrededor de 50 mV. Este valor puede ser considerado como una línea base y cuya aportación es posible por las reacciones meramente electroquímicas.
La cinética para la prueba N+AR tuvo dos comportamientos. Primero el voltaje se incrementó de manera constante y después de 600 min, éste fue constante. Así el voltaje pasó de 40 mV a alrededor de 100 mV en 600 min. Es posible que este aumento en el voltaje haya sido debido al crecimiento microbiano. Cabe recordar que el agua residual fue centrifugada solamente. Al cabo de estos primeros 600 min, las bacterias contenidas se reprodujeron, contribuyendo a la generación de electricidad. Se observó que la mayor producción de voltaje fue obtenida cuando la celda funcionó con el ánodo colonizado (Prueba N+AR+B). Se obtuvieron alrededor de 600 mV durante 18 h. A partir de los resultados anteriores se evidenció que las bacterias realmente contribuyen significativamente a la generación de electricidad.
Evaluación de cinéticas de voltaje en las celdas a diferentes distancias del electrodo
Se evaluó el voltaje generado por tres CCM bajo las mismas condiciones, excepto el volumen que varió (40, 80 y 120 mL) y con ello la distancia entre electrodos, ya que todas las celdas tenían la misma geometría. Para ello, el ánodo de cada celda fue colonizado por, al menos, tres semanas para cada celda. Se realizaron las pruebas cinéticas cuando la generación de voltaje fue constante en el tiempo para cada lote. Cada cinética se realizó por triplicado. La alimentación de las celdas fue con una solución de 100 mg/L de acetato de sodio en agua residual.
El pH se midió al principio y al final de cada cinética y se mantuvo entre 7 y 8 en todos los casos.
La Figura 6 presenta los resultados obtenidos para cada celda. Se puede observar que para el caso de las celdas de 40 y 80 mL no existen diferencias significativas en cuanto al voltaje obtenido, ni al tiempo durante el cual éste estuvo en su máximo valor. Sin embargo, al utilizar la celda de 120 mL, el voltaje obtenido fue mayor, así como el tiempo durante el cual fue mantenido. Es decir, se generó voltaje máximo de 540, 530 y 760 mV con una duración de 1390, 1480 y 8540 min para las celdas de 40, 80 y 120 mL, respectivamente.

Estudios preliminares han demostrado que la alimentación de celdas microbianas con agua residual es benéfica para una colonización satisfactoria de bacterias generadoras de electricidad y, como consecuencia a esto, la generación de energía debido a la transferencia de electrones171. Se piensa que la distancia entre electrodos en una celda puede ser un factor que interfiera en el comportamiento de la misma, ya que la transferencia de electrones se puede ver afectada por dicha distancia. Los estudios realizados mostraron que bajo las condiciones empleadas, la cantidad de agua procesada fue más significativa que la separación entre los electrodos, pues justamente la diferencia entre los volúmenes de las celdas fue el largo del tubo.
Con los datos obtenidos por las cinéticas de las tres celdas se calculó la intensidad de la corriente eléctrica, la potencia y la densidad de potencia expresada tomando en cuenta el área superficial del ánodo, en mW/m2, y la potencia volumétrica, tomando en consideración el volumen de la celda, en W/m3. De igual manera se calculó la potencia generada en el tiempo que duró cada lote. Los resultados se encuentran agrupados en la Tabla I.

Se puede observar que la mayor densidad de potencia se obtuvo con la celda de 120 mL. No se encontró una diferencia significativa entre las celdas de 40 y 80 mL. Lo anterior indica que el volumen de la celda no tiene una influencia sobre la densidad de potencia obtenida. Los valores encontrados en este estudio son similares a los reportados en la literatura, por ejemplo, para un volumen de celda de 30 mL se obtuvo una densidad de potencia de 261 mW/ m2 usando una resistencia menor de 200 Ω[10]; con una celda de 70 mL y usando lactato como sustrato[11] se obtuvo una densidad de 290mW/m2. Liu y Logan[12], utilizaron una celda de 180 mL con y sin membrana de intercambio de protones. La densidad de potencia obtenida fue de 262 ± 10 y 494 ± 21 mW/m2 con y sin membrana, respectivamente.
Al analizar la potencia volumétrica es claro que la distancia entre electrodos afecta de una manera significativa. A mayor separación de electrodos, menor es la potencia volumétrica obtenida. Esto nos indica que el diseño deberá mejorarse para producir una mayor potencia por unidad de volumen tratado. Es evidente que al tratar más agua, se obtiene una mayor cantidad de energía-hora, como es el caso de la celda de 120 mL. Es posible que, a pesar de tener una menor potencia volumétrica, la polarización de los electrodos ocurre en menor grado en la CCM de mayor volumen. De esta manera, se puede explicar el hecho de que a mayor separación de electrodos la celda tuvo un mayor tiempo de funcionamiento.
Análisis de la degradación del sustrato en celdas
La Figura 7 muestra la cinética de la degradación del sustrato, medido como carbono orgánico total (COT), para las tres CCM. El promedio de la degradación del carbono de las celdas fue del 71%. En todos los casos la remoción del sustrato fue acompañada de generación de voltaje. Es interesante observar cómo el máximo de voltaje se obtiene justo después de una rápida disminución de materia orgánica. Pasada esta etapa, la velocidad de remoción de materia orgánica disminuye, al igual que la generación de electricidad. Para el caso de la celda de 120 mL, se observa (Figura 7C) que esta primera etapa de rápida remoción ocurre en 2000 min, mientras que para los otros dos casos solamente dura 250 min. Es decir, una separación mayor de los electrodos causa que la materia orgánica se degrade más lentamente, aumentando el tiempo durante el cual la celda genera electricidad. Los resultados anteriores sugieren que es necesario mejorar el diseño de la celda, de tal modo que los electrodos no se polaricen, pero a su vez que la densidad de potencia obtenida por área superficial sea la máxima.
Conclusiones
Se evaluó la puesta en marcha de las celdas de combustible microbianas y la influencia de la separación de los electrodos y el volumen de la celda. A partir de los resultados es posible concluir que fue posible generar electricidad por medio de CCM alimentadas con agua residual en lote.
La materia orgánica fue degradada simultáneamente durante la producción de electricidad. Se removió hasta el 70% del carbono orgánico presente en el agua alimentada. Para el arranque de las celdas fue necesario colonizar el ánodo por al menos tres semanas. Se construyeron celdas de una sola cámara y sin membrana de intercambio protónico. El aumento de distancia entre los electrodos no causó un efecto negativo en la generación de electricidad, pues en la mayor separación (celda de 120 mL) se alcanzó un voltaje máximo de 660 mV, mientras que para las celdas de 40 mL y 80 fue de 540 mV y 532 mV, respectivamente. La mayor densidad de potencia se obtuvo con la celda de mayor volumen y separación entre electrodos (392 ± 5 mW/m2). Sin embargo, en relación con la potencia volumétrica, se observó que a medida que aumenta la separación entre electrodos ésta disminuye, obteniéndose 4.5 ± 0.06 W/m3 para la celda con mayor separación. La mayor potencia-h (77. 3 W-h) se produjo con la celda de mayor separación entre electrodos. Lo anterior sugiere que se debe optimizar la geometría de la celda. Se está trabajando en un nuevo diseño.
Agradecimientos
Se agradece a la DGAPA-UNAM por el apoyo financiero a través del proyecto PAPIIT IN104710 para la realización de este proyecto.
Referencias
1. Logan, B. Exoelectrogenic bacteria that power microbial fuel cells. Nature Reviews. 7, 375-381 (2009). [ Links ]
2. Fan, Y., Hu, H. & Liu. H. Enhanced coulombic efficiency and power density of air-cathode microbial fuel cells with an improved cell configuration. J. Power Sour. 171, 348-354 (2007). [ Links ]
3. Liu, H., Ramnarayanan, R. & Logan, B.E. Production of electricity during wastewater treatment using a single chamber microbial fuel cell. Environ. Sci. Technol. 38, 2281-2285 (2004). [ Links ]
4. Rabay, K., Clauwaert, P., Aelterman, P. & Verstraete, W. Tublar Microbial Fuel Cells for Efficient Electricity Generation. Environ. Sci. Technol. 39, 8077-8082 (2005). [ Links ]
5. Min, B., Kim, J.R., Oh, S. E., Regan J. M. & Logan, B. E. Electricity generation from swine wasterwater using Microbial Fuel Cells. Water Research, 39, 4961-4968 (2005). [ Links ]
6. Chae, K., Choi, M., Lee, J.. Kim, K & Kim, I. S. Effect of different substrates on the performance bacterial diversity and bacterial viability in MFC. Biosource Technology, 100, 3518-3525 (2009). [ Links ]
7. Du, Z., Li, H. & Gu, T. A state of the art review on microbial fuel cells: A promising technology for wastewater treatment and bioenergy. Biotechnology Advances, 25, 464-482 (2007). [ Links ]
8. APHA, AWWA and WPCF. Standard Methods for the Examination of Water and Wastewater, 21st ed. (Eaton, A.D. Clesceri, A.E., Rice EW and Greenberg, A.E. ed.), American Public Health Association, American Water Works Association and Water Environment Federeation (Washington D.C, 2005). [ Links ]
9. Liu, H., Cheng, S., Huan, L. & Logan, B.E. Sacle-up of membrane-free single-chamber microbial fuel cells. J. Power Sour. 179, 274-279 (2008). [ Links ]
10. Surya, G.K., et al. Inoculation procedures and characterization of a membrane electrode assemblies for microbial fuel cells. J. Power Sour. 195, 111-117 (2010). [ Links ]
11. Yang, S., Jia, B. & Liu, H. Effects of the Pt loeding side and cathode- biofilm on the performance of a membrane-less and single-chamber microbial fuel cell. Bioresour. Tech. 100, 1197-1202 (2009). [ Links ]
12. Liu, H. & Logan, B.E. Electricity generation using an air-cathode single chamber microbial fuel cell in the presence and absence of a proton exchange membrane. Environ. Sci. Technol. 38, 4040-4046 (2004). [ Links ]
Información sobre los autores
Germán Buitrón
Germán Buitrón es Ingeniero Químico egresado de la Facultad de Química de la UNAM, cursó la maestría y el doctorado en Ingeniería del tratamiento de aguas en el Instituto Nacional de Ciencias Aplicadas de Toulouse, Francia, obteniendo el grado en 1993. Actualmente es Investigador Titular "C" de tiempo completo en el Laboratorio de Investigación en Procesos Avanzados de Tratamiento de Aguas de la Unidad Académica Junquilla, Qro., del Instituto de Ingeniería de la UNAM. Es investigador Nacional Nivel II del Sistema Nacional de Investigadores. Su línea de investigación está enfocada al área de Tratamiento Biológico de Aguas Residuales Industriales y Valorización de Residuos. Tiene más de 280 publicaciones en revistas y una constante participación en congresos sobre su especialidad; alrededor de 65 informes de proyectos de investigación patrocinados. Ha impartido cerca de 40 cursos y diplomados, dirigido la tesis de 52 estudiantes para obtener el grado de licenciatura, maestría y doctorado.
Jaime Pérez
Jaime Pérez es Maestro en Biotecnología por la Universidad Autónoma Metropolitana y Biólogo egresado de la Facultad de Ciencias de la UNAM. Actualmente es Técnico Académico del Laboratorio de Investigación en Procesos Avanzados de Tratamiento de Aguas de la Unidad Académica Junquilla, Qro., del Instituto de Ingeniería de la UNAM. Tiene 18 publicaciones en revistas y ha participado en varios congresos.














