Introducción
Stevia rebaudiana es una planta de la selva subtropical del alto Paraná, nativa de las laderas montañosas de Paraguay, donde los pobladores la han utilizado como edulcorante y en herbolaria (Dacome et al., 2005; Prakash et al., 2008; Anton et al., 2010). El sabor dulce intenso en las hojas de esa especie se debe a la presencia de glucósidos diterpenoides, de los cuales esteviósido y rebaudiósido A están en proporción mayor. El poder endulzante de estos compuestos es 150 a 300 veces mayor que la sacarosa (Midmore y Rank, 2002; Liu et al., 2010) y sin contenido calórico (Anton et al., 2010). Por esto, su demanda para endulzar alimentos y bebidas ha aumentado (Brandle y Telmer, 2007; Durán et al., 2012). En México existen condiciones ambientales para el cultivo de S. rebaudiana (Ramírez-Jaramillo et al., 2011) y puede ser rentable.
Los estudios sobre nutrición mineral de estevia son escasos (Das et al., 2007); las investigaciones han evaluado la fertilización química (Jaitak et al., 2008; Jarma et al., 2010). Los sustratos con contenido alto de materia orgánica e inoculación de microrganismos aumentan los metabolitos secundarios (Brandt, y Møgaard, 2001) y mejoran el crecimiento de las plantas. El aumento del uso de los biofertilizantes (principalmente con microrganismos) ha permitido disminuir el uso de hasta 69 589 t de fertilizantes químico, lo que redujo 22.7 mil t de CO2 entre 2014 y 2015 (SAGARPA, 2016).
La hoja de estevia es el órgano con mayor concentración de esteviósidos (Gardana et al., 2010) y su contenido está influido principalmente por las horas luz, etapa fenológica y cultivar (Madan et al., 2010). Ciertas prácticas agronómicas, como la fertilización (Das et al., 2007) y aplicación de microorganismos endomicorrízicos (Portugal et al., 2006), incrementan la absorción de nutrimentos, principalmente P, mejoran la síntesis de metabolitos secundarios (Riipi et al., 2002) y pueden afectar la concentración de flavonoides e isoflavonoides (Das et al., 2008; Hanan et al., 2008).
Las condiciones ambientales de la costa de Chiapas, México, difieren de las del sitio de origen de Stevia y su persistencia como cultivo tiende a disminuir. Así, surge la posibilidad de aplicar brasinoesteroide exógeno, que es una hormona que induce diversas respuestas en las plantas, como favorecer la polarización de la membrana celular y aumentar la resistencia al estrés biótico y abiótico (Singh y Shono, 2005; Reyes et al., 2008).
Esta investigación tuvo como objetivo identificar la influencia de Rhizophagus intraradices y Azospirillum brasilense combinados con brasinoesteroide en los cambios morfológicos, fisiológicos y bioquímicos de Stevia rebaudiana Bert.
Materiales y Métodos
Descripción del experimento
La investigación se desarrolló en un vivero en la primavera de 2015, en el Campo Experimental de la Facultad de Ciencias Agrícolas, Campus IV, Huehuetán, Chiapas, localizado en el entronque carretera costera y Estación Huehuetán, municipio de Huehuetán, Chiapas (15° 00’ y 15° 30’ N, 94° 30’ y 95° 00’ O, altitud de 44 m y temperatura mínima y máxima de 15 y 38 °C). El suelo usado, del grupo de los fluvisoles eútricos, se mezcló con arena de río lavada (1:1). La textura del sustrato fue areno-migajosa (Bouyoucos, 1962), con 80.7 % arena, 13.3 % limo, 5.8 % arcilla, 2.6 % materia orgánica (Walkley-Black, 1934), conductividad eléctrica de 0.05 ds m-1, 5 Meq 100g-1 de capacidad de intercambio catiónico, pH 5.7, 0.13 % de N (cuantificado con Micro-Kjeldahl; Irigoyen et al., 1992), P 14.2 mg kg-1 (evaluado por colorimetría), K++ 64.2 mg kg-1, Ca++ 474 mg kg-1 (determinados por espectrofotometría atómica, Thermo Fisher Scientific, modelo 400 ¼), Mg++ 58.0 mg kg-1 y Na++ 102.5 mg kg-1.
Esquejes de S. rebaudiana Bert. de la variedad Morita 2 se obtuvieron de una plantación, a 10 km del sitio experimental, de plantas vigorosas y sin daños aparentes por insectos o enfermedad. Los esquejes con longitud de 10±2 cm y 60 d de edad se obtuvieron del tercio superior de la planta y se transportaron sumergidos en agua estéril para su siembra. Seis kg de la mezcla de suelo, sin esterilizar, se colocó en bolsas de plástico negro (calibre 700) con perforaciones en la base para drenaje. Los tratamientos fueron: 1) A. brasilense, 2) R. intraradices, 3) A. brasilense más R. intraradices, 4) Brasinoesteroide, 5) R. intraradices más brasinoesteroide, 6) A. brasilense más brasinoesteroide, 7) A. brasilense, R. intraradices más brasinoesteroide y 8) testigo (solo suelo). Cuatro g del inóculo de cada microorganismo, en dependencia del tratamiento, se depositaron en la cavidad donde se colocaría el esqueje al momento del trasplante. El brasinoesteroide (2 mg L-1) se aplicó 28 d después de la siembra y luego cada 14 d.
La planta hospedante de R. intraradices fue Brachiaria decumbens Stapf en suelo estéril, la colonización alcanzó 95 % en raíces y suelo. Este sustrato se usó como inóculo; cuando se aplicó contenía 40 esporas g-1 de suelo más propágulos. El inóculo de A. brasilense se obtuvo del Laboratorio de Microbiología de Suelos de la Benemérita Universidad Autónoma de Puebla (México), al momento de la inoculación presentaba 910X6 células g-1, este se impregnó en la turba como sustrato. El brasinoesteroide CIDEF-4 soluble (Natura del Desierto, S. A. de C. V. en México) tenía 80 % de contenido esteroidal y 10 % i.a., no es tóxico y es compatible con fertilizantes, insecticidas y fungicidas.
El diseño experimental fue completamente al azar con siete repeticiones por tratamiento. La unidad experimental fue una maceta con una planta. Los análisis de N, P, rebaudiósido A y esteviósido se determinaron en hojas deshidratadas con cuatro repeticiones. Los riegos se hicieron con agua destilada. Noventa días después de la siembra se cosecharon las hojas y se determinó su biomasa y contenido de N, P y edulcorantes.
Número de hojas, número de ramas, biomasa y área foliar
El número de hojas y ramas totales se contabilizó; la biomasa seca de las estructuras de la planta se midió en balanza analítica (0.1 mg; Ohaus, NJ, USA), después de deshidratarlos en una estufa, con aire circulante, a 75-80 °C. El área foliar se registró en cm2 con un integrador de área foliar (LI-COR, LI 3100, USA).
Contenido de edulcorantes en hoja
Los esteviósidos, rebaudiósido A y esteviol se extrajeron de hojas deshidratadas a 60 °C y trituradas en un molino eléctrico. Los compuestos se determinaron por HPLC (Agilent Technologies 1200 Series, California, USA), en columna Zorbax CDB C-18 analítica de 4.6X150 mm y 5 (m de tamaño de partícula, según el método descrito por Hashimoto y Moriyasu (1978), en el Laboratorio de Fitoquímica del Colegio de Postgraduados, Montecillo, México.
Contenido de N y P
El contenido de N y P se determinó en el vástago, el N con el método Microkjeldahl y el P con el método de Olsen et al. (1954) en un espectrofotómetro (Thermo Fisher Scientific Modelo 400 ¼), en el laboratorio de Suelo, Agua y Planta de la Facultad de Ciencias Agrícolas de la Universidad Autónoma de Chiapas, Huehuetán Chiapas, México.
Colonización micorrízica en raíz
La colonización se cuantificó únicamente en los tratamientos con R. intraradices, con la técnica de Phillips y Hayman (1970) en 100 segmentos de raíz, con 1.5-1.6 cm de longitud, y en microscopio óptico con objetivo de inmersión (100 X).
Análisis estadístico
El diseño experimental fue completamente al azar y los datos se analizaron mediante ANDEVA, con el procedimiento GLM de SAS (versión 9.0), y las medias se compararon con la prueba de Tukey (p≤0.05). Los valores en porcentaje se transformaron a arco-seno para el análisis estadístico.
Resultados y Discusión
El número mayor de hojas (p≤0.05) se registró con la mezcla de R. intraradices y brasinoesteroide. La inoculación de los dos microorganismos solos y coinoculados más brasinoesteroide aumentó entre 5 y 13 % el número de hojas respecto al testigo. Los microorganismos y el brasinoesteroide separados no modificaron el número de hojas respecto al testigo (Cuadro 1).
Cuadro 1 Características de desarrollo de plantas de Stevia rebaudiana Bert. inoculadas con microorganismos más brasinoesteroide, cultivadas en un suelo fluvisol-eútrico del Soconusco, Chiapas, México.
| Tratamiento | Número | Peso seco (g planta-1) | Área foliar (cm2 planta-1) |
|||
| Hojas | Ramas | Raíz | Tallo y ramas | Lámina foliar | ||
| R. intraradices | 317±7.8 c | 6.71±0.35 bc | 1.57±0.08 bcd | 4.43±0.05 e | 4.76±0.14 cd | 1173±47 cd |
| A. brasilense | 310±10.7 c | 5.86±0.26 bc | 1.75±0.05 abc | 4.98±0.18 cde | 5.33±0.20 bc | 1084±23 d |
| R. intraradices ×A. brasilense | 373±9.9 b | 6.00±0.30 bc | 1.95±0.10 ab | 6.22±0.15 b | 5.97±0.17 ab | 1390±48 b |
| Brasino-esteroide† | 339±9.9 bc | 5.71±0.47 cd | 1.94±0.10 abc | 5.88±0.19 bc | 4.70±0.19 cde | 1179±30 cd |
| Brasino-esteroide ×R. intraradices | 516±9.0 a | 11.29±0.42 a | 2.05±0.08 a | 7.31±0.22 a | 6.21±0.18 a | 1728±58 a |
| Brasino-esteroide ×A. brasilense | 246±6.1 d | 3.86±0.26 d | 1.52±0.12 cd | 4.99±0.11cde | 3.91±0.15 e | 1151±20 d |
| Brasino-esteroide ×R. Intraradices×A. Brasilense | 344±8.1 bc | 7.71±0.56 b | 1.64±0.10 abc | 5.57±0.30 bcd | 5.00±0.25c | 1356±50 bc |
| Testigo | 328±10.5 c | 6.57±0.57 bc | 1.15±0.07 d | 4.72±0.29 ed | 4.11±0.17 de | 1152±54 d |
| CV¶ | 6.9 | 16.5 | 14.6 | 9.8 | 9.9 | 9.1 |
†Brasinoesteroide CIDEF-4. ¶CV: coeficiente de variación (%). Medias con distinta letra en una hilera son estadísticamente diferentes (Tukey, p≤0.05).
El aumento en el número de hojas por inoculación con R. intraradices permite sugerir que la absorción de nutrimentos y agua por el sistema radical incrementó, ya que al aumentar el crecimiento del micelio de estos hongos les permite actúan como extensión de la raíz (Leigh et al., 2009) y favorecer cambios en su fisiología (Barea et al., 2002). El incremento en el número de hojas coincidió con el observado en especies perennes, como Theobroma cacao L. (Aguirre-Medina et al., 2007), Coffea arabica L. (Sánchez et al., 2005), Coffea canephora (Pierre) ex Froehner (Ibarra-Puón et al., 2014) y Tabebuia donnell-smithii Rose (Aguirre-Medina et al., 2014).
El brasinoesteroide también favoreció el crecimiento de la hoja y el número de ramas. Esto se debería a cierto estrés, de acuerdo con Núñez y Mazorra (2001) quienes registraron esta respuesta en otras especies en temperaturas tropicales. En nuestro estudio el estrés pudo deberse al cambio de temperatura del sitio de origen austral de estevia (15 y 30 °C) y la del sitio de estudio (hasta 38 °C). El brasinoesteroide es promotor del crecimiento mediante el aumento de la elongación y división celular (Salgado et al., 2008; Clouse, 2011), inductor de termo-tolerancia en Bromus inermis (Wilen et al., 1995) y en tomate (Solanum lycopersicum Lam.) (Sing y Shono, 2005).
La micorrización de R. intraradices en combinación con el brasinoesteroide promovió (p≤0.05) la acumulación de biomasa respecto a los otros tratamientos; fue 44 y 24 % mayor que en el tratamiento con R. intraradices y con brasinoesteroide. La micorrización se ha relacionado con el transporte de nutrientes y agua de lugares donde la raíz no puede explorar (Sylvia, 2005). La inoculación con R. intraradices en asociación con brasinoesteroide incrementó el área foliar (1728±58 cm2 por planta) más que el tratamiento con R. intraradices más A. brasilense (1390±48 cm2 por planta) y que con brasinoesteroide más R. intraradices más A. brasilense (1356±50 cm2 por planta); estos resultados contrastaron con los valores del testigo (1152±54 cm2 planta-1). El número de ramas y el peso de raíz mostraron coeficientes de variación mayores que las demás variables; pero no alcanzaron el 20 % permisible estadísticamente en estudios en campo. Esto indica que el uso de microrganismos y la aplicación de esteroide son eficientes para modificar la fisiológica de estevia.
El crecimiento de las plantas aumenta al combinar las bacterias asociativas, como Azospirillum, y los hongos micorrízicos (Miller y Jastrow 2000). Este efecto se observó en parcelas de validación de maíz y frijol en México (Aguirre-Medina, 2006; Trabelsi y Mhamdi, 2013). El testigo tuvo la biomasa menor, fue 55 % menor que la del mejor tratamiento.
El incremento inicial de la biomasa en la hoja de S. rebaudiana con R. intraradices influyó en el aumento en la biomasa total durante todo su desarrollo. Las hojas son fuente principal de fotosintatos para otros órganos de la planta, por lo que su incremento y persistencia favorecen la tasa de asimilación neta y relativa de crecimiento. Cuando los hongos micorrízicos favorecen la nutrición de las plantas la tasa fotosintética mejora (Wright et al., 2005). Este hecho, según Milthorpe y Moorby (1982), establece una relación positiva entre el suministro de nutrimentos minerales y la tasa de fotosíntesis, la cual influye en todo el complejo fotosintético.
Contenido de edulcorantes
Las plantas de S. rebaudiana inoculadas con R. intraradices en presencia de brasinoesteroide presentaron significativamente (p≤0.05) más esteviósido (35.8±1.76) que los otros tratamientos. En el mismo grupo estadístico estuvieron el tratamiento con los dos microorganismos más el brasinoesteroide (32.2±1.12) y con A. brasilense sin combinar (29.7±1.28). (Cuadro 2). Los hongos microrrízicos arbusculares incrementan la absorción de nutrientes, principalmente P, que es parte esencial de moléculas como uridin difosfato glucosa que es donadora de glucosa en la síntesis de los glucósidos de diterpeno (Shibata et al., 1995; Richardson et al., 2009).
Cuadro 2 Contenido de edulcorantes en hojas de Stevia rebaudiana Bert. inoculada con R. intraradices, A. brasilense y aspersión foliar de brasinoesteroide.
| Tratamientos | Mg g de peso seco-1 | |||
| Esteviósido | Rebaudiósido A | Esteviol | Total edulcorantes | |
| R. intraradices | 21.5±0.76 d | 17.7±0.90 a | 1.6±0.12 a | 40.9±1.47 b |
| A. brasilense | 29.7±1.28 abc | 26.3±6.66 a | 1.1±0.66 a | 57.2±7.78 ab |
| R. intraradices ×A. brasilense | 25.8±1.56 cd | 17.4±3.19 a | 5.0±0.98 a | 48.2±4.12 ab |
| Brasinoesteroide† | 27.2±1.14 bcd | 21.9±5.72 a | 1.6±0.96 a | 50.8±5.32 ab |
| Brasinoesteroide ×R. intraradices | 35.8±1.76 a | 27.9±2.23 a | 4.5±1.20 a | 68.4±4.84 a |
| Brasinoesteroide ×A. brasilense | 29.4±1.06 bc | 29.5±3.61 a | 4.2±1.18 a | 63.2±5.10 ab |
| Brasinoesteroide ×R. intraradices×A. brasilense | 32.2±1.12 ab | 35.1±7.84 a | 1.5±0.88 a | 68.8±9.41 a |
| Testigo | 25.0±1.4 cd | 17.8±0.60 a | 1.5±0.90 a | 44.9±2.00 b |
| CV¶ | 2.6 | 37.8 | 68.9 | 20.2 |
†Brasinoesteroide CIDEF-4. ¶CV (%): coeficiente de variación. Medias con distinta letra en una hilera son estadísticamente diferentes (Tukey, p≤0.05).
Azospirillum aumenta el desarrollo radical de la planta hospedante mediante las hormonas producidas y la fijación del N (Bashan y De Bashan, 2010) necesario para el crecimiento normal de las plantas (Jarma et al., 2010).
Las plantas en presencia de los hongos endomicorrízicos pueden modificar su contenido de esteviósidos e isoflavonoides (Hanan et al., 2008). Portugal et al. (2006) observaron concentración mayor de esteviósido (72 mg por planta) en plantas de estevia inoculadas con R. intraradices, en comparación con las plantas testigo (16 mg planta-1) sin inocular. En el presente caso, los valores mayores de esteviósido representaron 50 % con R. intraradices más brasinoesteroide.
El coeficiente de variación mostró variabilidad alta del contenido de rebaudiósido A y esteviol y la diferencia entre los tratamientos no sugieren una relación en su biosíntesis; es decir, la correlación del contenido de esteviosidos y el de rebaudiósidos no es significativa, aunque los glucósidos comparten camino metabólico con el rebaudiósido A (Madan et al., 2010). Los contenidos bajos del esteviol mostraron CV alto; pero, resaltaron los contenidos de las plantas inoculadas con microrganismos y brasinoesteroide (5.0±0.98, 4.5±1.2, 4.2±1.18).
Las plantas micorrizadas generalmente absorben cantidades mayores de micronutrimentos, como Mn (Pacovsky et al., 1985), que es cofactor de enzimas que intervienen en la síntesis del ácido entkaurenoico. Este es el precursor de los principales edulcorantes, como el esteviósido en estevia (Jarma et al., 2010); además, S, Cu, Zn and Fe (Habte y Aziz, 1985).
Jarma et al. (2010) señalaron que el esteviósido puede variar de 3 a 8 % en el tejido seco de las hojas de estevia. Las diferencias estadísticas se presentaron solamente con el esteviosido y el valor mayor se registró con la aplicación de brasinoesteroide más R. intraradices (p≤0.05) con los microorganismos inoculados solos, más el brasinoesteroide.
El contenido de edulcorantes, nutrientes y biomasa aumentó con la aplicación de brasinoesteroide. Esto indica la posibilidad de que las plantas de estevia estén estresadas, posiblemente por la temperatura de la región de estudio. Sing y Shono (2005) trataron plantas de jitomate con 24 epibrasinolida y reportan mayor tolerancia a 38 °C y mayor eficiencia fotosintética en comparación con las plantas tratadas a 25 °C.
Contenido de N y P
Las plantas inoculadas con cada microorganismo o su combinación presentaron contenido de N mayor en comparación con las plantas testigo y cuando se aplicó brasinoesteroide (Figura 1). El contenido de N aumentó y fue estadísticamente diferente del testigo (p≤0.05) al inocular A. brasilense más el brasinoesteroide. A. brasilense induce crecimiento radical en la planta hospedera como resultado de la producción de fitohormonas (Hungria et al., 2004), como ácido indolacético (Dobbelaere et al., 2003; Bashan y de Bashan, 2010), que modifica la morfología e incrementan la biomasa radical (Lalitha et al., 2011). Los hongos endomicorrízicos transportan N a través de la hifa desde sitios del suelo que son inaccesibles para la raíz (Hodge 2003). La inoculación con hongos endomicorrzicos en cultivo de Phaseolus sp., (Tajini y Drevon, 2012), Coffea arabica L. (Aguirre-Medina et al., 2011) y Cedrela odorata L. (Aguirre-Medina et al., 2014) mostró resultados similares. El contenido mayor de P en el tejido vegetal se registró en el tratamiento con A. brasilense y al adicionar brasinoesteroide (p≤0.05). Otros estudios han demostrado que las plantas micorrizadas absorben eficientemente el P del suelo en comparación con las plantas no colonizadas (Andrade et al., 2009) de regiones del suelo más allá de la zona de agotamiento alrededor de la raíz (Wright et al., 2005).
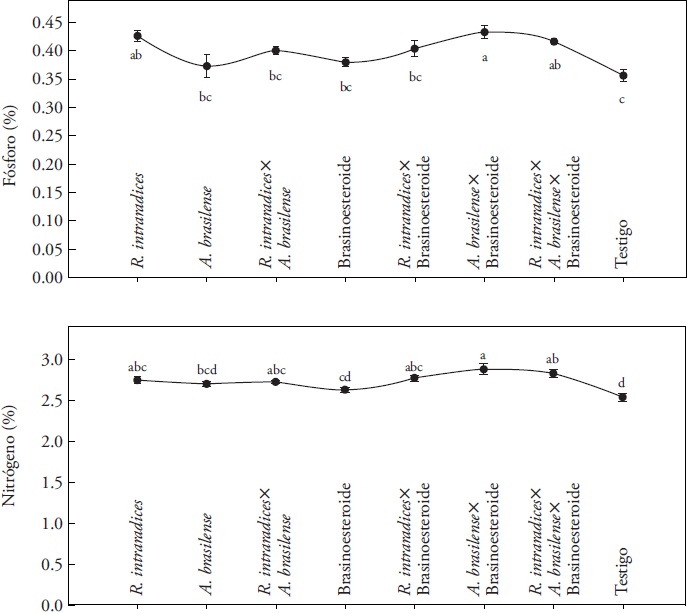
Figura 1 Porcentaje de fósforo (P) y nitrógeno (N) en hojas de S. rebaudiana Bert. biofertilizada con R. intraradices, A. brasilense y aplicación foliar de CIDEF-4 (brasinoesteroide) en condiciones de vivero (n=4) ± error estándar. Letras diferentes en cada tratamiento (N o P) son estadísticamente diferentes (p≤0.05). CV=2.6 % para N y CV=5.8 % para P.
La colonización radical de todas las plantas inoculadas R. intraradices fue alta. En promedio, la colonización fue de 83 al 90 %. En el caso del testigo sin aplicación del hongo endomicorrízico la colonización radical fue 52 %. La colonización radical en el tratamiento testigo y en el tratamiento con brasinoesteroide o A. brasilense seguramente se debe a micorrizas nativas que se encuentran en el sustrato.
Conclusiones
Plantas de S. reabudiana inoculadas y en presencia de brasinoesteroide, en modalidad diferente de asociación, mostraron cierto aumentos del área foliar y contenido de esteviosido, rebaudiósido y esteviol. El contenido de N y P aumentó con R. intraradices inoculado solo y más brasinoesteroide.











 texto en
texto en 


