Introducción
Los mecanismos para eliminar un contaminante hidrófobo del suelo son movilización y solubilización (Edwards et al., 1991; West y Harwell, 1992; Mulligan, 2005; Vreysen y Maes, 2005). La movilización depende de la capacidad del tensioactivo de disminuir la tensión superficial y facilitar que la disolución de lavado arrastre el contaminante (Cameotra y Makkar, 2010). Las moléculas de tensioactivo reducen la tensión interfacial en el sistema aceite/agua y hacen que aumente el ángulo de contacto del contaminante con el suelo, se reducen las fuerzas capilares que los mantienen unidos y se facilita la eliminación del aceite (Moldes et al., 2011). La solubilización tiene lugar por encima de la concentración micelar crítica (CMC), momento a partir del cual el tensioactivo forma micelas en el interior de las cuales queda retenido el contaminante, de modo que la cantidad de aceite eliminada aumentará con la concentración de tensioactivo. La solubilización depende tanto del tensioactivo como del grado de contaminación de la matriz sólida, y puede no ser significativo en el proceso de remediación cuando la contaminación es muy elevada (Abdul et al., 1990; Urum y Pekdemir, 2004).
Una gran cantidad de residuos industriales, como los aceites sintéticos y combustibles, los aceites de cocina y metales pesados procedentes de envases metálicos encontrados en los residuos domésticos, son la causa principal de la contaminación del suelo, ríos y lagos, provocando la destrucción de hábitats en casos extremos (Solans y Gadea 2015, Reglamento (UE) Nº1357/2014). Por ejemplo, la contaminación de suelos y aguas subterráneas causada en gasolineras por la naturaleza de los lubricantes, gasolinas o gasóleos tiene gran importancia debido a su magnitud y el impacto negativo que produce debe evaluarse con cuidado.
Dentro de estos residuos está el aceite quemado de motor, que por su peligrosidad para el medio ambiente, es uno de los principales residuos sometido a una estricta regulación (Solans y Gadea 2015, Reglamento (UE) Nº1357/2014). La mayoría de los hidrocarburos causantes de la contaminación ambiental son muy insolubles en agua y generan uniones hidrofóbicas a determinadas superficies, como las rocas, por lo cual su eliminación es muy difícil, ya que los microorganismos que pueden degradarlos no pueden acceder a ellos por no estar biodisponibles. Por esto, en el campo de la biorremediación se intenta encontrar microorganismos productores de sustancias biosurfactantes que favorezcan la biodisponibilidad de estos hidrocarburos (Banat et al., 2000; Ortíz-Hernández et al., 2001; Youssef et al., 2007; Yañez-Ocampo et al., 2009, 2011, 2013; Vecino et al., 2015b).
Los biosurfactantes son compuestos anfifílicos de origen microbiano con altas propiedades tensioactivas que permiten reducir el impacto ambiental causado por diversos residuos liberados al medio ambiente como los hidrocarburos (Moldes et al., 2011). En comparación con los surfactantes producidos por síntesis química, los biosurfactantes son menos tóxicos que sus homólogos derivados del petróleo (Levison, 2009). Debido a su biodegradabilidad y biocompatibilidad, los biosurfactantes se estudian en varios campos industriales (Kourkoutas et al., 2004; Banat et al., 2010; Reis et al., 2013): en la industria farmacéutica (Rodrigues et al., 2004; Cameotra y Makkar, 2010), cosmética (Gharaei-Fathabad, 2011; Vecino et al., 2017), en el tratamiento de aguas residuales (Perez-Ameneiro et al., 2015), así como en la biorremediación de suelos contaminados con hidrocarburos (Desai y Banat, 1997; Banat et al., 2010; Damasceno et al., 2012; Moldes et al., 2011; 2013).
Vecino et al. (2014a, 2014b, 2014c, 2015a) evaluaron y patentaron los licores de lavado de maíz como fuente para obtener biosurfactantes de bajo coste y propusieron un proceso para la extracción y caracterización de estos compuestos tensioactivos que se pueden aplicar en distintos sectores industriales. La ventaja de estos biosurfactantes, comparados con sus homólogos, es que son económicamente competitivos con los surfactantes químicos porque su producción no requiere ningún proceso fermentativo controlado, y se producen de forma espontánea en un corriente residual procedente de la industria del maíz.
El objetivo de este estudio fue evaluar la capacidad del biosurfactante extraído de los licores de lavado de maíz, para la eliminación de aceite quemado de motor, sobre un suelo arenoso. Esta es la primera vez que se evalúa este biosurfactante como agente limpiador de aceite sobre suelo y se espera que los resultados permitan establecer las condiciones idóneas para su uso como surfactante natural, de origen renovable, en vertidos industriales.
Materiales y Métodos
Suelo y contaminante
El suelo arenoso se obtuvo de una playa de la Costa Gallega, del Noroeste de España, que se mezcló con aceite quemado de motor de coche de un taller automovilístico local (Vigo, España).
Extracción del biosurfactante a partir de los licores de lavado de maíz
El biosurfactante contenido en los licores de lavado de maíz (CSL) se extrajo con cloroformo en tres etapas (Vecino et al., 2015): 1) una extracción líquido-líquido a 65 ºC utilizando una relación CSL/cloroformo de 1/2 (v:v) durante 1 h; 2) luego, la mezcla permaneció 24 h en un embudo de decantación para permitir alcanzar el equilibrio, la separación de la fase acuosa y la fase orgánica que contiene el biosurfactante; 3) el cloroformo fue destilado y recuperado, y se obtuvo un extracto de biosurfactante concentrado que se diluyó en agua para obtener la disolución limpiadora.
Evaluación de la capacidad del biosurfactante para formar emulsiones con el aceite quemado de motor
La capacidad emulsionante del biosurfactante obtenido desde licores de lavado de maíz para formar emulsiones se calculó en función de dos variables, EV (% volumen de emulsión relativo) (ecuación 1) y ES (% estabilidad del biosurfactante para mantener la emulsión cuando se mezclan aceite con agua) (ecuación 2). Las variables que miden la capacidad emulsionante del biosurfactante (EV y ES) se registraron 30 d con las ecuaciones de Neufeld y Zajic (1984) y Das et al. (1998). Para ello, una muestra de 2 mL de aceite quemado se puso en una disolución de BS a la CMC (200 mg L-1), se agitó 2 min en un vortex, se estabilizó 72 h y se cuantificó el EV y el ES. El cálculo de EV se basa en el porcentaje de emulsión formada entre la fase oleosa y la fase acuosa, respecto al volumen total. Para ello se toman los valores de la altura de emulsión, de la altura total de ambas fases y la sección transversal de tubo (ecuación 1). ES es la relación entre EV a un tiempo determinado y EV a tiempo 0 (ecuación 2):
Test de desplazamiento de aceite
El test de desplazamiento de aceite por el biosurfactante indica su capacidad para solubilizar el aceite. Para realizar este test se depositaron 20 mL de agua en una placa Petri, se adicionaron 40 (L de aceite quemado de motor, y sobre el aceite se adicionaron 80 (L de disolución de biosurfactante por encima de la CMC. Además, como testigo se prepararon otros dos experimentos en los cuales se adicionó agua o una disolución de dodecil sulfato sódico (SDS) (detergente usado en la limpieza de tanques petrolíferos, obtenido por síntesis química) a su CMC (2365 mg L-1). Aquella disolución limpiadora que logre desplazar en mayor medida el aceite sobre el agua y que muestre un mayor diámetro de desplazamiento tendrá mayor capacidad como disolución limpiadora.
Medida de la tensión superficial
La tensión superficial de la disolución de biosurfactante, así como de los testigos realizados con agua, antes y después del lavado de la arena, se midieron con un tensiómetro superficial (KRUSS K6, España) equipado con un anillo de platino 1.9 cm (método del anillo de Du Noüy). Las medidas se realizaron por triplicado a temperatura ambiente.
Pruebas de lavado del suelo contaminado a escala de laboratorio
Para estas pruebas se pesaron 5 g de suelo arenoso contaminado con aceite quemado de motor de coche con un contenido de aceite de 0.25 g (50,000 ppm) presente en este suelo. Los experimentos de lavado a escala de laboratorio se realizaron en discontinuo, en matraces Erlenmeyer de 250 mL, a temperatura ambiente en un agitador orbital a 150 rpm. La relación sólido / líquido establecida entre el suelo contaminado y las disoluciones limpiadoras fue entre 1:10 y 1:30 (p:v). Las disoluciones limpiadoras se prepararon con biosurfactante dos veces por debajo de la CMC (BS/2) o a la CMC (BS). El tiempo de limpieza se fijó en 6 h.
Tras el lavado de la arena se separó la disolución limpiadora mediante filtración, utilizando un embudo de placa porosa, cuantificando el aceite extraído en la disolución limpiadora mediante análisis gravimétrico y para ello se tomó 1 mL de la disolución limpiadora y permaneció 48 h en estufa a 100 ºC.
La arena descontaminada y filtrada se sometió a un proceso de extracción utilizando acetona en un dispositivo Soxhlet (Nahita. Heating mantles. Mod 655. Navarra-España), para cuantificar el aceite que permaneció en la arena, el cual tiene que ser complementario al aceite extraído en las disoluciones limpiadoras.
Proceso de extracción del aceite remanente en el suelo arenoso
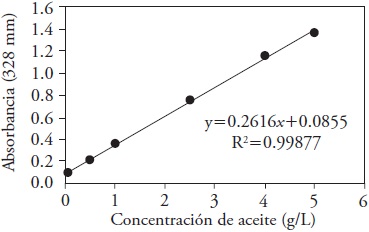
Para la extracción del aceite remanente en la arena con el Soxhlet, la arena tratada se introdujo en un cartucho de celulosa, y la acetona se colocó dentro de una manta calefactora a 65 ºC (temperatura mayor que la de ebullición de la acetona, de 56 ºC), lo cual permitió su evaporación. El dispositivo Soxhlet incluye un sistema de condensación que permite pasar a la acetona de estado vapor a estado líquido, arrastrando en su caída al aceite remanente en la arena. Este dispositivo funcionó por 1 h, después se retiró el cartucho del Soxhlet, se tomó una muestra de la acetona que contenía el aceite residual en la arena y se midió a 328 nm en un espectrofotómetro de doble haz (Jasco Mod. V-650, España). La relación entre la concentración de aceite en la acetona y la absorbancia medida a 328 nm fue lineal (Figura 1), y así se obtuvo la ecuación de la concentración de aceite en relación con la absorbancia.
Cálculo de la eficacia del proceso de extracción
La eficacia de extracción (EE) se define de acuerdo con la ecuación (3) como el porcentaje del aceite eliminado de la arena:
donde A0 y A1 representan los gramos iniciales y finales de aceite presente en la arena, respectivamente.
Resultados y Discusión
Evaluación de la capacidad emulsionante y dispersante del biosurfactante sobre aceite quemado de motor
Tras el proceso de extracción se obtuvo un extracto biosurfactante con un rendimiento de 8±0.5 g extracto kg-1 de CSL con 50 % en sólidos, aunque este rendimiento puede sufrir variaciones pequeñas entre lotes porque los licores de lavado de maíz son fermentados espontáneamente en condiciones no controladas, si se supone un residuo industrial.
El extracto obtenido se disolvió en agua por encima de su CMC (Figura 2), y CMC es la concentración de surfactante que puede reducir al máximo la tensión superficial del agua. A la CMC (200 mg L-1) o por encima de esta, el biosurfactante puede mantener la tensión superficial del agua constante en valores cercanos a 40 mN m-1, punto donde el biosurfactante empieza a formar micelas con capacidad para rodear a aquellas moléculas no solubles en agua, lo que facilita su movilización y solubilización.

Figura 2 Aspecto de la disolución de biosurfactante extraído de los licores de lavado de maíz, solubilizado en agua.
Una vez establecida la CMC del biosurfactante se preparó una disolución limpiadora con una concentración de biosurfactante a la CMC (BS) o a la mitad de la CMC (BS/2) y se evaluó su capacidad para estabilizar emulsiones aceite/agua. El biosurfactante a la CMC (BS) pudo emulsionar el aceite con el agua en su totalidad en comparación con el sistema agua/aceite en ausencia de biosurfactante (Figura 3). Esta emulsión fue estable durante más de un mes, periodo durante el cual se evaluó su estabilidad.

Figura 3 Sistema aceite/agua estabilizado y emulsionado con biosurfactante procedente de los licores de lavado de maíz (izquierda), comparado con un sistema aceite/agua sin biosurfactante (derecha).
El biosurfactante obtenido de los licores de lavado de maíz dispersó el aceite y lo desplazó en mayor medida hacia los bordes de la placa, en comparación con el detergente de origen sintético, SDS, lo que indica una mayor capacidad del biosurfactante para extraer y solubilizar el aceite (Figura 4).
Pruebas de lavado del suelo arenoso contaminado con aceite quemado de motor de coche
La eficacia del proceso de extracción logrado con el biosurfactante y extraído desde los licores de lavado de maíz fue notablemente mayor que la alcanzada con agua como testigo, sobre todo cuando la disolución limpiadora se formuló con concentraciones de biosurfactante en torno a la CMC (Figura 5).
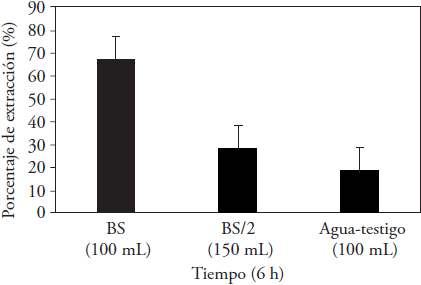
Figura 5 Porcentajes de extracción de aceite, alcanzados con el biosurfactante obtenido de los licores de lavado de maíz después de 6 h de tratamiento comparados con agua (testigo).
Concentraciones de biosurfactante alrededor de la CMC, definidas como BS, presentaron alrededor de 67 % de extracción de aceite, mientras que al reducir la concentración de biosurfactante a la mitad de su CMC, definidas como BS/2, el porcentaje de extracción de aceite fue 28 %. Aunque el volumen de la disolución limpiadora aumentó, los resultados alcanzados fueron similares a los obtenidos con la disolución limpiadora testigo consistente en agua.
Los resultados obtenidos en nuestro estudio con BS son mejores que los reportados por Vreysen y Maes (2005) de 50 % y 20 % de extracción de aceite diésel usando el tensioactivo Tergitol NP-10. Moldes et al. (2011) usaron un biosurfactante producido por Lactobacillus pentosus, y eliminaron 58.6 % de octano después de 15 d de contacto entre el BS y el suelo contaminado.
Esto permite considerar que las causas de los peores resultados obtenidos por debajo de la CMC en nuestro estudio, podrían deberse a que en tales concentraciones el biosurfactante no forma micelas que rodeen a las moléculas de aceite, ni favorece la movilización y solubilización del aceite presente en el suelo arenoso.
En la Figura 6 se muestran los valores de tensión superficial alcanzados en las distintas disoluciones limpiadoras, tras el tratamiento de la arena contaminada. En los experimentos en los que se usaron 100 mL de disolución limpiadora la relación sólido/líquido fue 1:20 (p:v), mientras que con 150 mL dicha relación fue 1:30 (p:v). La tensión superficial menor (37 mN m-1) se observó en la disolución limpiadora con la concentración mayor de biosurfactante (200 mg L-1), pero la disolución limpiadora BS/2 con 100 mg L-1 de biosurfactante tiene una tensión superficial superior (46 mN m-1), lo que explica su menor capacidad de limpieza en comparación con la disolución limpiadora BS, y la tensión superficial aproximada de la disolución limpiadora a base de agua (denominada agua testigo) fue 60 mN m-1 (Figura 6).
Moya-Ramírez et al. (2014) durante el tratamiento de un suelo arenoso con 10 g L-1 de un surfactante sintético (G600) demostraron que al aumentar la temperatura se alcanza mayor eficacia en el proceso de extracción. Estos autores observaron extracciones menores del 20 % a temperatura ambiente, y hasta casi 40 % cuando la temperatura aumentó hasta 65 ºC. El uso de temperaturas en torno a 65 ºC no hacen factible este proceso a nivel industrial, principalmente en procesos de extracción in situ, ya que el costo energético y de los equipos para dicho proceso sería muy elevado. En comparación con detergentes naturales Moya-Ramirez et al. (2014) usaron un biosurfactante producido por B. subtillis y obtuvieron mejores porcentajes de limpieza que los obtenidos con el surfactante sintético G600, aunque concentraciones mayores de biosurfactante causaron rendimientos menores. Pero la extracción alcanzada con el biosurfactante usado por dichos autores fue inferior al 40 %, para 45 ºC, y es menor al obtenido con el biosurfactante evaluado en nuestro estudio (67 %) a temperatura ambiente (25 ºC).
Conclusiones
El biosurfactante extraído de los licores de lavado de maíz pudo solubilizar el aceite quemado de motor en agua y desplazó al mismo en mayor medida que el SDS. Concentraciones de biosurfactante en torno a la CMC muestran buenas propiedades como agente limpiador de suelos arenosos contaminados. Por lo tanto, este detergente natural se podría usar en vertidos industriales, de carácter hidrofóbico, en sustitución de agentes limpiadores de origen no renovable.











 texto en
texto en