Introducción
El selenio (Se) es un microelemento esencial para los animales porque forma parte de la selenocisteína, que es un aminoácido de proteínas óxido reductoras (Stock y Rother, 2009). El consumo deficiente de Se altera el metabolismo de las hormonas tiroideas y la respuesta inmune, provoca patologías musculares y desórdenes reproductivos (Hefnawy y Tórtora-Pérez, 2010). La inclusión de Se en la dieta, el uso de comprimidos intraruminales y las soluciones inyectables son prácticas recomendadas en las regiones con deficiencia del microelemento (Hernández-Calva y Ramírez-Bribiesca, 2006; Revilla-Vázquez et al., 2008).
Los rumiantes requieren de 0.1 a 0.3 mg kg-1 MS de Se (NRC, 2001; NASEM, 2016), el requerimiento varía con el peso vivo y el tipo de dieta (NRC, 2007). Los ovinos y caprinos son susceptibles a la deficiencia del microelemento (Ramírez-Bribiesca et al., 2001; Ramírez-Bribiesca et al., 2004), porque los microorganismos ruminales reducen la forma inorgánica a formas poco disponibles (Se elemental y selenuro) para el rumiante, como mecanismo de conservación de energía y para evitar la selenosis (Nancharaiah y Lens, 2015), o lo incorporan en proteína microbiana como selenoaminoácidos (Mainville et al., 2009; Panev et al., 2013). El efecto del Se adicionado en la fermentación ruminal y el uso de nutrientes con concentraciones cercanas a las requeridas ha sido variable (Serra et al., 1994; Kim et al., 1997; Del Razo-Rodriguez et al., 2013).
Ovinos en etapas fisiológicas diferentes han recibido dietas con Se en concentraciones superiores a la máxima tolerable (5 mg kg-1 MS; NRC, 2005). El suministro de 10, 20 y 40 mg Se kg-1 MS, como selenito de sodio, no provocó selenosis ni efectos negativos en el peso vivo de ovinos (Cristaldi et al., 2005; Davis et al., 2006a; Davis et al., 2006b; Davis et al., 2008); pero, la información del efecto de concentraciones altas de Se en la fermentación ruminal y degradación de la materia seca (DMS) es limitada (Datt et al., 2013; Eun et al., 2013).
Por lo anterior, la hipótesis fue que el Se, adicionado como selenito de sodio, en concentraciones superiores a la máxima tolerable para rumiantes afecta la fermentación in vitro y la DMS. Por tanto, el objetivo fue evaluar el efecto del Se en la producción de gas, CH4, pH, DMS y concentración de ácidos grasos volátiles (AGV) y nitrógeno amoniacal (N-NH3), durante la fermentación in vitro de heno de avena.
Materiales y Métodos
Localización
El estudio se realizó en los laboratorios de Nutrición Animal y de Análisis Especiales, del Instituto de Ciencias Agropecuarias de la Universidad Autónoma del Estado de Hidalgo (UAEH), en Tulancingo de Bravo, Hidalgo, México.
Tratamientos
Los tratamientos fueron: testigo, Se20, Se40, Se60 y Se80, que correspondieron a la cantidad de Se adicionado al sustrato (0, 20, 40, 60 y 80 mg Se kg-1 MS). Cada tratamiento tuvo siete repeticiones independientes y la unidad experimental fue un frasco con 500 mg de sustrato. La concentración del microelemento en cada tratamiento se obtuvo a partir de una solución base con 99 mg Se L-1 (220 mg de selenito de sodio grado alimenticio; 45 % de Se 1000 mL-1); 500 µL de soluciones con 20, 40, 60 y 80 mL aforadas a 100 mL se adicionaron a los frascos, según el tratamiento y agua destilada para el testigo.
Fermentación in vitro
La fermentación in vitro se realizó con la técnica de producción de gas (Theodorou et al., 1994). El medio de cultivo contenía 225 mL de solución amortiguadora (4 g de NH4HCO3 (Meyer) y 35 g de NaHCO3 (Meyer), en 1000 mL), 225 mL de solución macromineral (5.7 g de Na2HPO4 (Meyer), 6.2 g de KH2PO4 (Meyer) y 0.6 g de MgSO4 • 7H2O (Sigma), en 1000 mL), 100 mL de líquido ruminal y 450 mL de agua destilada, por cada 1000 mL. Además, se agregaron 100 µL de una solución micromineral (13.2 g de CaCl2 • 2H2O (Sigma), 10 g de MnCl • 4H2O (Sigma), 1 g de CoCl • 6H2O (Meyer) y 8 g de FeCl3 (Meyer), en 100 mL), 1.2 mL de resazurina al 0.1 % y una solución reductora (0.57 g de Na2SO4 y 4 mL de NaOH 0.1 N, en 100 mL), en proporción 2 mL: 60 mL del medio. Los componentes del medio se mezclaron con agitación, a 39 °C y flujo constante de dióxido de carbono (CO2).
El líquido ruminal se obtuvo de dos ovejas con cánulas (Suffolk x Rambouillet, 2 años de edad), se filtró a través de tres capas de manta de cielo y se mantuvo a 39 °C hasta su uso. Las ovejas se alimentaron con heno de avena (libre acceso) y 500 g d-1 de alimento comercial con 15 % de proteína cruda. La colocación quirúrgica de las cánulas fue autorizada por el Comité Institucional de Ética para el Cuidado y Uso de Animales de Laboratorio de la UAEH. Los cuidados antes y después de la cirugía se realizaron conforme a la Norma Oficial Mexicana NOM-062-ZOO-1999, que establece las especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio (DOF, 2001).
La fermentación del sustrato (partícula de 1 mm, humedad de 13.5 % y PC de 9.4 %) se realizó en frascos de vidrio transparente (120 mL de capacidad y boca de 20 mm). 40 mL del medio de cultivo se agregaron a cada frasco con flujo constante de CO2 por 15 s. El sellado hermético de los frascos se obtuvo con tapones de silicón y casquillos de aluminio colocados con una engarzadora manual (Wheaton, E-Z Crimper, USA). La incubación fue a 39 °C en baño María (Thermo Scientific, 2864, USA) por 72 h. Tres frascos sin sustrato (blancos) se incluyeron para medir el volumen de gas producido por la digesta del inóculo; este se restó al producido por la fermentación de las muestras.
Producción de gas y CH4
El volumen parcial de gas se registró, por desplazamiento de agua (Ramirez-Bribiesca et al., 2011) 1, 2, 3, 4, 5, 7, 9, 12, 24, 32, 48 y 72 h después de la incubación y sirvió para calcular el volumen acumulado de gas (VAG; mL g-1 MS). Las variables de la cinética de la producción de gas fueron V: volumen máximo (mL g-1 MS), S: tasa de producción (h-1) y L: tiempo de retardo (h); estas se calcularon con el modelo estadístico de Schofield y Pell (1995) Va = V/(1 + e2-4S(t-L)) con el procedimiento NLIN de SAS® (SAS Institute Inc., 2012).
Las muestras de CH4 se extrajeron de dos frascos por tratamiento con una jeringa desechable (5 mL y aguja de 21 G x 32 mm), antes de la lectura de las 9, 12, 24, 32 y 48 h de incubación. Las muestras se almacenaron en frascos de vidrio transparente (15 mL de capacidad y boca de 20 mm), que se llenaron previamente con solución salina saturada (6 N, pH 2 ajustado con HCl concentrado y rojo de metilo como indicador), sellados herméticamente con tapón de silicón y casquillo de aluminio. La muestra se inyectó en los frascos a través del tapón, permitiendo el desplazamiento de la solución a través de una aguja. Las muestras se conservaron en refrigeración (4 °C) con los frascos invertidos hasta su análisis.
La concentración de CH4 se determinó en 200 µL de la muestra inyectados en un cromatógrafo de gases (Perkin Elmer, Autosystem XL, USA), equipado con metanizador, detector de ionización de flama (FID) y columna capilar (Elite Plot Q 30 m x 0.53 mm, Series GC; USA). Las condiciones del análisis fueron 200 °C en el detector e inyector y 50 °C en el horno; 5 min fue el tiempo de corrida. La concentración se calculó mediante una curva estándar construida con concentraciones crecientes de CH4 (30, 50 y 100 %) y se utilizó para calcular el volumen acumulado de CH4.
DMS y análisis de AGV y N-NH3
Al final de la fermentación, las muestras se mantuvieron 2 h a 4 °C para detener la actividad microbiana. El pH se registró con potenciómetro (Hanna Instruments, HI 2211, Rumania). La DMS se estimó con la MS no degradada y recuperada después de centrifugar el contenido de los frascos a 20 980 x g, por 10 min (Hermle, Z 326 K; Alemania) y secar el residuo a 65 °C, por 72 h en un horno (Terlab, TH-45DM, México). La fórmula fue: DMS = [(PSM - PSMR) / PSM] * 100; donde PSM: peso seco de la muestra (g) y PSMR: peso seco de la materia residual (g).
La concentración de AGV en los medios se determinó por cromatografía de gases a las 72 h de incubación (Erwin et al., 1961). Para ello, una muestra de 800 µL del contenido líquido de los frascos se mezcló con 200 µL de ácido metafosfórico al 25 % p/v (J. T. Baker). La mezcla se centrifugó a 17 000 x g por 15 min (Thermo Scientific, PICO 17, Alemania) y el sobrenadante se refrigeró a 4 °C hasta su análisis. El cromatógrafo (HP, Agilent 6890, USA) estuvo equipado con una columna capilar de 0.25 mm x 30 m (HP-FFAP, Agilent, USA) y las temperaturas fueron 140, 250 y 240 °C para el horno, detector e inyector, respectivamente. El gas acarreador fue N a 10 psi y el flujo de aire e H2 fueron 350 y 35 mL min-1. La muestra que se inyectó fue 1 µL.
La concentración de N-NH3 se determinó por colorimetría (Weatherburn, 1967) en un espectrofotómetro UV/visible (Jenway, 6305, Reino Unido). Para ello, 20 µL del sobrenadante utilizado para AGV se mezclaron con 1 mL de fenol (50 mg Na2Fe(CN)5NO•2H2O (Meyer) y 10 g de fenol (Fermont), en 1000 mL) y 1 mL de hipoclorito de sodio (7.5 g de NaOH (Meyer), 21.3 g de Na2HPO4 anhidro (Meyer) y 15 mL de hipoclorito de sodio al 5 %, en 1000 mL). Las muestras se diluyeron con 5 mL de agua destilada después de 30 min de incubación a 37 °C en baño María (Thermo Scientific, 2864, USA) y se leyeron a 630 nm.
Análisis estadístico
El diseño experimental fue completamente al azar con medidas repetidas. Los datos de todas las variables se analizaron con el procedimiento MIXED de SAS® (SAS Institute Inc., 2012), considerando en el modelo estadístico al tratamiento como efecto fijo (el tiempo se consideró también como efecto fijo para VAG y CH4) y a la unidad experimental, repetición y error experimental como efectos aleatorios. Las medias de cuadrados mínimos se obtuvieron con LSMEANS; la comparación de medias se realizó para variables con efecto de tratamiento significativo utilizando PDIFF y el comportamiento lineal y cuadrático se determinó con ESTIMATE. El análisis de medidas repetidas se realizó con el enunciado TYPE=SP(POW). El nivel de significancia fue p ≤ 0.05.
Resultados y Discusión
La producción de gas ocurre a consecuencia de la degradación de los carbohidratos por los microorganismos ruminales y los productos resultantes son AGV, CO2 y CH4. El Se adicionado afectó VAG a las 24 y 72 h de incubación (p ≤ 0.05; Figura 1). Las medias disminuyeron linealmente a las 12, 24 y 32 h, y su disminución fue cuadrática a las 48 y 72 h (p ≤ 0.05) con concentración mayor del microelemento (Figura 2). Las diferencias entre medias se observaron desde las 12 h de incubación, momento en que el VAG con Se60 fue menor que el generado en los otros tratamientos (p ≤ 0.05). Después, las diferencias definieron las concentraciones que afectaron la producción de gas; los tratamientos Se60 y Se80 produjeron menos VAG (entre 11 y 6.9 %) a las 48 y 72 h de incubación (p ≤ 0.05), sin diferencia entre ellos a las 72 h (p > 0.05). Datt et al. (2013) obtuvieron resultados similares con adición de selenito de sodio a una mezcla de paja de arroz y concentrado (40:60), durante la fermentación; ellos observaron producción menor de gas con 60 y 70 mg Se kg-1 MS, a las 24 y 48 h de incubación, respecto a concentraciones menores del microelemento.
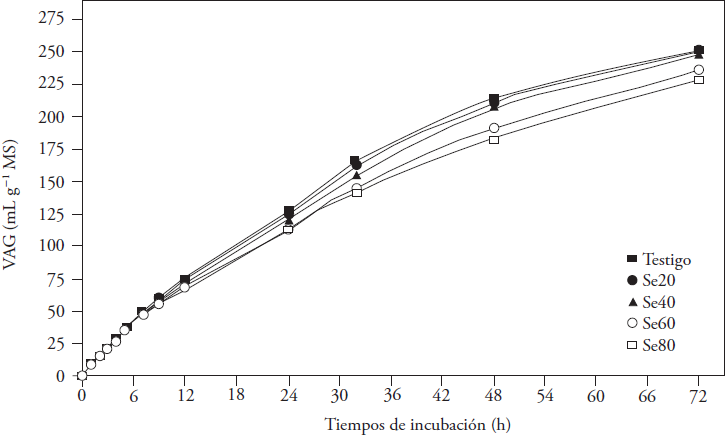
Figura 1 Volumen acumulado de gas (VAG) generado en la fermentación in vitro de heno de avena por 72 h, con la adición de selenito de sodio (testigo: 0, Se20: 20, Se40: 40, Se60: 60 y Se80: 80 mg kg-1 MS).
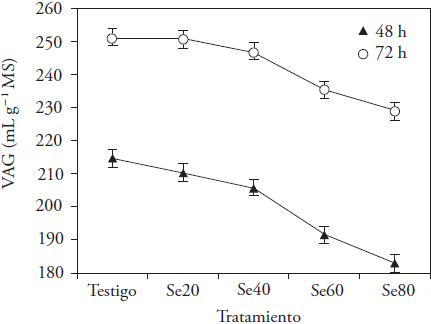
Figura 2 Cambios en el volumen acumulado de gas (VAG) generado en la fermentación in vitro de heno de avena a las 48 y 72 h de incubación, con la adición de selenito de sodio (testigo: 0, Se20: 20, Se40: 40, Se60: 60 y Se80: 80 mg kg-1 MS).
El efecto del tratamiento se observó también en la cinética de producción de gas, en V y S (p ≤ 0.05), y sus medias disminuyeron linealmente con el aumento de Se (p ≤ 0.05); esto no ocurrió con L (p = 0.07; Cuadro 1). El valor de las variables con Se60 y Se80 fue similar entre sí, pero menor que el de los otros tratamientos (excepto Se60 respecto a Se40). Estos resultados permiten inferir que las concentraciones de Se superiores a 40 mg kg-1 MS afectan la fermentación in vitro del heno de avena y, por tanto, la actividad microbiana, porque la cinética de producción de gas refleja la actividad microbiana en los medios de cultivo (Schofield et al., 1994).
Cuadro 1 Variables de la cinética de producción de gas y volumen acumulado de metano (CH4) obtenidas por fermentación in vitro de heno de avena, por 72 h, con adición de selenio (Se).
| Variable/tiempo | Tratamientos | EE | ||||
| Testigo | Se20 | Se40 | Se60 | Se80 | ||
| Variables de la cinética de producción de gas | ||||||
| V (mL g-1 MS) †¶ | 244.0a | 243.0a | 240.5a,b | 229.1b,c | 221.2c | 4.3 |
| S (mL h-1) †¶ | 0.0246a | 0.0241a | 0.0235a,b | 0.0227b | 0.0220b | 0.0005 |
| L (h) | 3.00 | 3.11 | 3.32 | 2.93 | 1.53 | 0.51 |
| Volumen acumulado de CH4 (mL g-1 MS) | ||||||
| 32 h ¶ | 6.0 | 5.8 | 5.7 | 4.6 | 3.9 | 0.61 |
| 48 h †¶ | 9.5a | 8.2a | 9.3a | 7.8a,b | 6.4b | 0.61 |
a,b,c Medias con distinta letra en una hilera son diferentes (p ≤ 0.05). Testigo: 0, Se20: 20, Se40: 40, Se60: 60 y Se80: 80 mg Se kg-1 MS; EE: error estándar de la media; V: volumen máximo; S: tasa de producción; L: tiempo de retardo; MS: materia seca. †Efecto de tratamiento (p ≤ 0.05). ¶Tendencia lineal de las medias (p ≤ 0.05).
El CH4 se produce durante la fermentación de carbohidratos en el rumen por la actividad de arqueas como Methanobrevibacter ruminantium, M. gottschalkii, Methanosphaera spp, Methanimicrococcus spp y Methanobacterium spp (Hill et al., 2016; Yang et al., 2016). Las enzimas microbianas implicadas en la producción y utilización de gases de efecto invernadero contienen cofactores metálicos (Glass y Orphan, 2012); el Se es parte de la formato deshidrogenasa que participa en la formación de CH4 (Stock y Rother, 2009).
El efecto de tratamientos en el volumen acumulado de CH4 se observó a las 48 h de incubación (p ≤ 0.05), pero no a las 32 h (p = 0.06), y las medias disminuyeron linealmente con el incremento en la concentración de Se en ambos tiempos (p ≤ 0.05). Se80 produjo volumen de CH4 similar al obtenido con Se60 (p > 0.05), pero menor al de los otros tratamientos (p ≤ 0.05; Cuadro 1). Con 50 mg Se kg-1 MS (selenato de sodio) adicionado durante la fermentación in vitro de heno de pasto ovillo (Dactylis glomerata), en un sistema de cultivo continuo de doble flujo, no se observaron cambios en la concentración de CH4 (p = 0.10) (Eun et al., 2013). Esto indica que la producción in vitro de CH4 con concentraciones altas de Se puede estar asociada con la concentración y fuente del microelemento y a la técnica utilizada.
Los tratamientos afectaron el pH de los medios a las 72 h de incubación (p ≤ 0.05; Cuadro 2). Con Se40, Se60 y Se80 el pH fue similar (p > 0.05), pero fue mayor que en Se20 y el testigo (p ≤ 0.05). El efecto de tratamientos no se observó en DMS (p = 0.07) ni en la concentración total de AGV (p = 0.10), acetato (p = 0.07), propionato (p = 0.27), butirato (p = 0.06) y N-NH3 (p = 0.64); pero, con una concentración mayor de Se las medias (excepto propionato y N-NH3) disminuyeron linealmente (p ≤ 0.05). Estos resultados muestran relación con la disminución en la producción de gas con el incremento del Se; además, indican que la producción in vitro de AGV tiene correlación positiva con la degradabilidad de la MS y con la producción de gas (p < 0.05; Getachew et al., 2004).
Cuadro 2 pH, degradación de la materia seca (DMS) y concentración de ácidos grasos volátiles (AGV) y nitrógeno amoniacal (N-NH3) obtenidos por fermentación in vitro de heno de avena por 72 h, con la adición de selenio (Se).
| Variable | Tratamientos | EE | ||||
| Testigo | Se20 | Se40 | Se60 | Se80 | ||
| pH †¶ | 6.74a | 6.75a | 6.77a,b | 6.81b | 6.82b | 0.02 |
| DMS (%)¶ | 61.0 | 61.7 | 60.8 | 59.7 | 57.8 | 0.91 |
| AGV total (mMol L-1) ¶ | 46.4 | 47.0 | 46.1 | 44.5 | 39.7 | 1.81 |
| Acetato (mMol L-1) ¶ | 30.4 | 30.6 | 29.9 | 28.8 | 25.8 | 1.12 |
| Propionato (mMol L-1) | 13.0 | 13.4 | 13.3 | 13.0 | 11.5 | 0.64 |
| Butirato (mMol L-1) ¶ | 3.0 | 3.0 | 2.9 | 2.8 | 2.4 | 0.13 |
| N-NH3 | 8.5 | 9.9 | 8.8 | 8.3 | 8.6 | 0.76 |
a,b Medias con distinta letra en una hilera son diferentes (p ≤ 0.05). Testigo: 0, Se20: 20, Se40: 40, Se60: 60 y Se80: 80 mg Se kg-1 MS; EE: error estándar de la media; MS: materia seca. †Efecto de tratamiento (p ≤ 0.05). ¶Tendencia lineal de las medias (p ≤ 0.05).
El efecto de la adición de concentraciones altas de Se en la DMS y los productos generados no está definido completamente y podría depender de la concentración y fuente de Se, y de la técnica de análisis utilizada. Kim et al. (1997) adicionaron in vitro 2 mg Se kg-1 MS, a partir de selenito de sodio; ellos no detectaron cambios en la concentración total de AGV, pero observaron una proporción mayor de butirato y menor de acetato. Eun et al. (2013) adicionaron 50 mg Se kg-1 MS, utilizando selenato de sodio, pero no encontraron cambios en pH, concentración de AGV y N-NH3. Xun et al. (2012) reportaron cambios positivos en DMS, concentración total de AGV y de N-NH3 y relación acetato:propionato con la adición de 4 mg Se kg-1 MS, a partir de levadura enriquecida y nano partículas con Se en un estudio in situ.
Existen bacterias y arqueas que utilizan selenato y selenito como aceptores finales de electrones durante su respiración anaerobia y forman nanoesferas, que es una forma insoluble de Se. Esta reducción es un mecanismo para prevenir selenosis (Nancharaiah y Lens, 2015). Al respecto, Eun et al. (2013) indicaron que las bacterias ruminales se adaptan a concentraciones altas del microelemento, porque detectaron crecimiento de bacterias reductoras de selenato al adicionar 50 mg Se kg-1 MS en el medio. Esto permite explicar porque el suministro de 40 mg Se kg-1 MS en ovinos no provocó selenosis ni cambios en el peso vivo (Davis et al., 2008). Sin embargo, la producción de masa bacteriana tiene correlación negativa (p < 0.05) con la concentración de Se en líquido ruminal (Kim et al., 1997), por lo cual la actividad bacteriana puede también disminuir con el aumento en la concentración del microelemento. Así, es posible inferir que las bacterias se adaptaron a las concentraciones de 20 y 40 mg Se kg-1 MS, lo que mantuvo la fermentación constante y la DMS sin cambios.
Conclusiones
La actividad microbiana durante la fermentación in vitro de heno de avena se mantuvo constante con 20 y 40 mg Se kg-1 MS, y disminuyó con 60 y 80 mg Se kg-1 MS. El Se agregado no afectó la degradación de materia seca, la concentración de AGV y N-NH3, aunque mostró reducción lineal en estas variables. Parece que 40 mg Se kg-1 MS es el límite máximo que garantiza la actividad microbiana sin afectar la fermentación ni la degradación in vitro de la materia seca de heno de avena.











 texto en
texto en 


