Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agrociencia
versión On-line ISSN 2521-9766versión impresa ISSN 1405-3195
Agrociencia vol.44 no.2 Texcoco feb./mar. 2010
Protección vegetal
Determinación de residuos de malatión y malaoxón en mango de las variedades Ataulfo y Tommy Atkins producidos en Chahuites, Oaxaca
Determination of residues of malathion and malaoxon in mango varieties Ataulfo and Tommy Atkins produced in Chahuites, Oaxaca
Casibe Fuentes–Matus1,*, Salvador Vega y León1, Gilberto Díaz–González1, Mario Noa–Pérez2, Rey Gutiérrez–Tolentino1
1 Universidad Autónoma Metropolitana. Unidad Xochimilco. Departamento de Producción Agrícola y Animal. Calzada del Hueso No. 1100, Colonia Villa Quietud, Delegación Co–yoacán 04960, México D.F. *Autor responsable: (vianii05@yahoo.com.mx).
2 Universidad de Guadalajara. Centro Universitario de Ciencias Biológicas y Agropecuarias Km 15.5 Carretera Guadalajara–Nogales, Las Agujas, Nextipac, Zapopan, Jalisco, México.
Recibido: Enero, 2009.
Aprobado: Agosto, 2009.
Resumen
El plaguicida órgano fosforado malatión y su metabolito malaoxón causan efectos nocivos en la salud de los humanos que consumen alimentos contaminados con estas moléculas. Se estudió la presencia de residuos de malatión y malaoxón en mangos (Mangifera indica) de las variedades Ataulfo y Tommy Atkins producidos en el municipio de Chahuites, estado de Oaxaca, durante el periodo de su cosecha en 2007. Se usó un sistema de extracción con acetato de etilo en matriz acuosa, y determinación analítica mediante cromatografía gas–líquido con detector termoiónico específico (TSD). Se determinó la concentración de residuos de malatión y malaoxón para cada variedad mediante el muestreo a los 1, 30 y 60 d después de una aplicación de malatión (520 g i. a. de malatión ha–1), en cumplimiento con la norma fitosanitaria (NOM–023–FITO) para el combate de la mosca mexicana de la fruta (Anastrepha Itidens) en los días 1 (TI) y 30 (T2), y dos aplicaciones de malatión para el día 60 (T3). Se usaron mangos testigos de ambas variedades, tomados de huertos libres de aplicación del plaguicida por 10 años. En 75 % y 95.6 % de las muestras (n=12) de las variedades Ataulfo y Tommy Atkins se detectó presencia de malatión. En 83.3 % de las muestras (n=12), para ambas variedades se detectaron residuos del metabolito malaoxón. No se observó degradación de ambos plaguicidas una vez presentes en el fruto, hasta el día 60 del estudio. Además, las medias de los residuos aumentan en el tiempo tres de estudio (T3) en ambas variedades, luego de dos aplicaciones de malatión.
Palabras clave: cromatografía de gases, malatión, malaoxón, mangos, residuos.
Abstract
The organophosphate pesticide malathion and its metabolite malaoxón cause harmful effects on the health of humans that consume foods contaminated with these molecules. The presence of residues of malathion and malaoxón was studied in mangos (Mangifera indica) of the varieties Ataulfo and Tommy Atkins produced in the municipality of Chahuites, state of Oaxaca, during the harvest period of 2007. The extraction system used ethyl acetate in aqueous matrix, and analytic determination by means of liquid gas chromatography with thermionic specific detector (TSD). The concentration of residues of malathion and malaoxón was determined for each variety through sampling at 1, 30 and 60 d after having applied malathion (520 g i. a. of malathion ha–1), in compliance with the phytosanitary norm (NOM–023–FITO) for the control of the Mexican fruit fly (Anastrepha ludens) on days 1 (T1) and 30 (T2), and two applications of malathion for day 60 (T3). Control mangos of both varieties were used, taken from orchards free of pesticide application for 10 years. The presence of malathion was detected in 75 % and 95.6 % of the samples (n=12) of the varieties Ataulfo and Tommy Atkins. Residues of the metabolite malaoxón were detected in 83.3 % of the samples (n=12) in both varieties. No degradation was observed of either pesticide once it was present in the fruit until day 60 of the study. Furthermore, the means of the residues increased in time three of the study (T3) in both varieties, after two applications of malathion.
Key words: gas chromatography, malathion, malaoxón, mangos, residues.
INTRODUCCIÓN
En las plantaciones de mango el malatión se usa para controlar la mosca de la fruta (Anastrepha sp.) (CICOPLAFEST, 2003). El monocultivo es una forma de producción agrícola que ha generalizado el uso de agrotóxicos, cayendo en la dualidad daño–beneficio (Coscolia, 1993). El impacto ambiental provocado por los plaguicidas afecta a todos los organismos vivos, al persistir en el ambiente mucho tiempo después de su aplicación; también provoca daños a los humanos y su habitat al contaminar suelos, el aire, mantos freáticos y dañar su macro y micro fauna (EPA, 2006; Rassoulzadegan y Akyurtlaki, 2002).
Los plaguicidas organofosforados como el malatión, paratión metílico presentan poder residual bajo, pero toxicidad elevada. Los síntomas por contaminación aguda en humanos son: salivación abundante, bradicardia, miosis, hiperemia, parálisis vasomotora, sudoración excesiva, temblores, falta de coordinación muscular, visión borrosa, color amarillento en la piel, convulsiones, debilitamiento de la memoria, opresión en el pecho, respiración ruidosa, calambres abdominales y musculares, daños genéticos que provocan malformaciones y deficiencias mentales (FAO/WHO, 1997; ATSDR, 2003; EPA, 2006.
México tiene normas fitosanitarias que no coinciden con las establecidas por el protocolo del Codex Alimentario FAO/WHO, con las normas de la EPA, de los EE.UU., en cuanto al límite máximo de residuos (LRM) permitidos para malatión en mango hasta el 2007– Además, el país carece de un programa temporal o permanente rutinario obligatorio para monitorear todos o una parte de los productos agrícolas, para consumo interno o para mercado de exportación.
La normatividad vigente de la CICOPLAFEST (2003) establece el límite máximo de residuos (LMR) para el malatión en mangos de 8.0 µg g–1. El Codex Alimentario de la FAO/WHO (2006) propone 1.0 µg g–1 para el LMR de ese plaguicida en frutas con hueso, y la EPA (2006) establece 0.2 µg g–1 como LMR de malatión en mango. El Codex Alimentario de la FAO/OMS (2006) y la EPA (2006) consideran aditivos los residuos de malatión a los residuos de su metabolito principal, malaoxón, para establecer el LMR del malatión en mango.
México es uno de los principales productores y exportadores de mango en el mundo, por lo que es deseable conocer la residualidad del malatión en mangos de las variedades Ataulfo y Tommy Atkins, que son las de mayor exportación (SAGARPA, 2003), así como su efecto en el control de la mosca de la fruta, y con base en ello establecer las medidas precautorias pertinentes para favorecer la comercialización de esta fruta en mercados nacionales e internacionales.
La determinación de residuos de plaguicidas organofosforados en alimentos vegetales se realiza usando el tiempo de retención para la identificación cualitativa y al área del pico cromatográfico para determinación cuantitativa (CENAM, 2004). El método más usado es cromatografía de gases acoplada al detector de nitrógeno–fósforo.
Los insecticidas organofosforados tienen una función preponderante como plaguicidas fitosanitarios, a pesar de su problemática toxicológica (FAO/WHO, 1997; FAO/OMS, 1999). La aplicación periódica de malatión al árbol y fruto con compuestos de elevado poder de penetración puede provocar la aparición de residuos cuya importancia toxicológica debe ser evaluada regular y normativamente (Calonge, 2002).
El monitoreo de la presencia de residuos de plaguicidas en alimentos para determinar el grado de exposición de la población humana, es crucial. El control rutinario de residuos de plaguicidas debe realizarse para moléculas de síntesis reciente, y para aquellas donde se ha determinado su restricción o prohibición (Calonge, 2002; Richter et al. 2001; Durmusoglu, 2003).
En insectos, mamíferos y vegetales, el malatión es convertido a su metabolito malaoxón (vía oxidación del grupo P=S a P=O); en insectos y mamíferos el oxón es el metabolito activo inhibidor de la colinesterasa (ATSDR, 2003; EPA, 2006; FAO/WHO, 2006). El malatión comercial no es una molécula pura y está asociada a impurezas inherentes al proceso de producción de la molécula principal y a metabolitos secundarios como el malaoxón; por tanto, los métodos de detección deben considerar lo anterior y realizar su análisis como un complejo de moléculas (Montenegro, 2001). Así, en el 2006 la EPA considera aditivos los residuos de malatión y malaoxón en mango y reconsidera fijar el LMR del malatión, al pasar de 8.0 a 0.2 µg g–1 en esta fruta. El malatión es degradado vía mecanismos físico–químicos, en particular por hidrólisis, fotolisis y por biodegradación ambiental, en o dentro de organismos vivos (ATSDR, 2003; EPA, 2006; FAO/WHO, 2006). Es evidente que los informes actuales no pueden considerarse definitivos y por tanto el debate sobre el tema continúa.
El propósito del presente estudio fue determinar la concentración de los residuos de malatión y malaoxón en mangos de las variedades Ataulfo y Tommy Atkins, luego de una y dos aplicaciones de malatión.
MATERIALES Y MÉTODOS
Localización de la zona de trabajo
La presente investigación se realizó con muestras de dos variedades de mangos, Tommy Atkins y Ataulfo (cosecha 2007), de dos áreas experimentales ubicadas en el municipio de Chahuites, Oaxaca, México a 16° 17' 17.59" N y 94° 11' 35.06" O, con promedios anuales de 27.4 °C de temperatura y 1010.4 mm de precipitación (SMN, 2002).
Para la toma de muestras, cada área experimental se dividió en 16 bloques y un área por bloque de 2304 m2. Cada bloque estaba formado por 16 árboles frutales separados simétricamente por 12 m entre sí. Los árboles incluidos en la muestra fueron seleccionados al azar, así como los bloques y las muestras de mangos se tomaron al azar de cada árbol.
La dosis fue 1 L ha–1 de Lucathión 50–E (Química Lucava S. A. de C. V.), equivalente a 520 g de ingrediente activo de malatión ha–1 en cumplimiento con la norma fitosanitaria (NOM–023–FITO) para controlar la mosca mexicana de la fruta (Anastrepha ludens) por aplicación. Para determinar residuos de malatión se recolectaron 12 muestras de cada variedad en abril (T1), mayo (T2) y junio (T3) del 2007, luego de una aplicación de malatión en abril y mayo y dos aplicaciones en junio, tomando 4 muestras por periodo de muestreo por cada variedad, en total 24 muestras. Este mismo procedimiento se aplicó para las muestras testigo de mangos, Ataulfo y Tommy Atkins, cultivados sin aplicar de plaguicidas, recolectadas de un huerto testigo en el mismo municipio, el cual tenía un mínimo de 10 años sin aplicación de plaguicida.
Preparación de muestras
Las muestras de mango recolectadas de los huertos experimentales se trasladaron en una hielera a 4 °C al laboratorio y se congelaron, para su conservación, a –20 °C. Se retiraron de la cámara fría y fueron descongeladas a temperatura ambiente para iniciar su análisis. Las muestras fueron cortadas en pequeños pedazos (cascara y pulpa), excepto la semilla, y trituradas y homogeneizadas en una licuadora (PAM, 1999; IUPAC, 2002).
Extracción de plaguicidas
Se usó el método de extracción recomendado por Ricardo et al. (2000), para lo cual se tomaron alícuotas de 50 g de muestras homogeneizadas a las que se adicionaron 100 mL de acetato de etilo y 50 g de sulfato de sodio anhidro. La mezcla se maceró en licuadora a velocidad alta por 3 min, se decantó el líquido a través de un embudo que contenía sulfato de sodio anhidro, repitiendo la extracción del residuo con 100 mL de acetato de etilo. Una vez reunidos los extractos, permanecieron en evaporador rotatorio de vacío a menos de 50 °C hasta un volumen final.
Condiciones cromatográficas
El análisis de malatión se realizó en un cromatógrafo de gases VARIAN CP 3800 con automuestreador 8410 y columna SPB–608 de 25 m x 0.53 mm de diámetro interno y 0.25 µm de espesor de fase (Supelco, Bellefonte, CA).
Para determinar malatión se usó un detector TSD a 300 °C y corriente de cama de 3.2 A. Las condiciones cromatográficas fueron: volumen de muestra inyectado, 1 µL en modo split–splitless a 300 °C. El horno se programó así: 200 °C (2 min) con rampa de 10 °C min–1, hasta 290 °C (5 min), con tiempo de corrida de 16 min. Para calcular la concentración se usó el programa de procesamiento y adquisición de datos GALAXIE CROMATO–GRAPHY WORKSTATION versión 1.9.3.2., mediante el método del estándar externo, con niveles de concentración de 0.01, 0.1,0.5 y 1.0 µg g–1 de malatión. El gas usado como acarreador móvil fue N (4.5 mL min–1, con 0.5 % desviación), según las recomendaciones de Noa et al. (2005).
Diseño experimental y análisis estadístico
El diseño experimental fue de bloques completamente al azar, con mediciones repetidas y arreglo factorial con interacción. Se realizó un análisis de varianza, la prueba de Tukey (p<0.05) para comparación de medias, así como regresión lineal para correlacionar la concentración residual contra el número de aplicaciones usando el programa SYSTAT 9 (Zar, 1999).
RESULTADOS Y DISCUSIÓN
La recuperación para malatión fue 87–9 % (CV 2.5 % –9.5 %) y para malaoxón 87.6 % (CV de 2.5 % –5–2 %), concordando con el protocolo establecido por la AOAC (2005) para la recuperación de residuos de plaguicidas. Se obtuvieron tiempos de retención de 6.1 y 6.6 min (Figura 1) para malaoxón y malatión, en los tres niveles de concentración (0.25, 0.05 y 1.0 µg g–1). Se evaluó lalinealidad del método considerando las curvas de calibración mediante los estándares de trabajo en concentraciones 0.01, 0.1, 0.5 y 1.0 µg g–1 para malaoxón y malatión. El valor para el coeficiente de correlación fue 0.99 en malatión y en malaoxón, lo que mostró la linealidad del método.
En el Cuadro 1 se observa que luego de la primera aplicación de malatión los valores de residuos del plaguicida fueron 0.004 a 0.06 µg g–1 (abril, T1) y 0.001 a 0.03 µg g–1 (mayo, T2); y 3.1 a 7.1 µg g–1 luego de dos aplicaciones en junio (T3) para la variedad Ataulfo. Sin embargo, para las mismas aplicaciones de malatión se obtuvieron valores diferentes para la variedad Tommy Atkins: 0.0061 a 0.108 µg g–1 (abril, T1), de 0.005 a 0.095 µg g–1 (mayo, T2), y de 6.19 a 7–76 µg g–1 luego de dos aplicaciones en junio (T3). En 75 % y 95–6 % de las muestras de las variedades Ataulfo y Tommy Atkins, se detectó presencia de malatión. Considerando lo dispuesto en la normatividad de la EPA (2006), 25 % de las muestras analizadas (n=12) rebasan el LMR 0.2 µg g–1 de malatión en mangos en las dos variedades estudiadas.
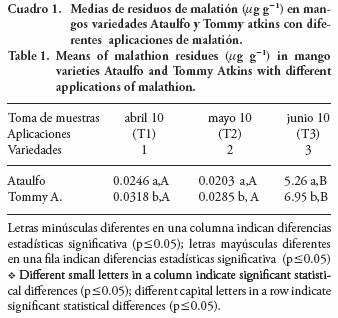
La media de los residuos para la primera aplicación mostró diferencia significativa con respecto a la media de los residuos, luego de dos aplicaciones en la misma variedad. Además hubo diferencia significativa en las medias entre variedades para la primera y la segunda aplicación (Figura 2). Ninguna muestra testigo resultó positiva para malatión.

Malatión es el plaguicida más comúnmente detectado en los productos alimenticios, en 18 % de 936 alimentos con inspección sanitaria (FDA, 1992). Según Jensen et al. (2003), malatión es el tercer compuesto que contribuye a la toxicidad en la dieta de la población danesa con 12 % del total de residuos tóxicos, mientras que Saeed et al. (2005) encontraron residuos de plaguicidas organofosforados en 12.5 % de muestras vegetales analizadas.
En fresa, 95–4 % de las muestras estudiadas estuvieron por debajo de los LMR de malatión (Guerrero, 2003). Calonge et al. (2002), en muestras de manzanas y peras, y Sanchez et al. (2005), en guayaba, detectaron presencia de malatión pero no se rebasó el LMR, lo que es diferente a lo encontrado en la presente investigación. En México, Salas et al. (2003) reportan 29 % a 50 % de muestras contaminadas, con organofosforados en cuatro marcas de leches, mientras que Hussain et al. (2002) reportan residuos de otros organofosforados en mango, sin incluir al malatión, pero los valores no rebasan el LMR de estos plaguicidas. Según Aldana et al. (2008) elmalatiónse encuentra en 97 % de muestras de nopal fresco, pero el nivel de residuos fue menor al LMR establecido para hortalizas.
Para el malaoxón, luego de la primera aplicación de malatión se obtuvieron valores de 0.002 µg g–1 (abril, T1 y mayo, T2), y 0.004 a 0.06 µg g–1 luego de dos aplicaciones en junio (T3) para la variedad Ataulfo (Cuadro 2). Para la variedad Tommy Atkins los valores fueron similares: 0.002 8g g–1 (abril, T1 y mayo T2) luego de la primera aplicación y 0.11 a 0.13 µg g–1 en junio (T3) luego de dos aplicaciones de malatión (Cuadro 2).

En 83–3 % de las muestras (n=12) y para ambas variedades, se detectaron residuos del metabolito malaoxón. La media de los residuos de malaoxón para la primera aplicación del malatión mostró diferencia significativa con respecto a la media luego de dos aplicaciones en la misma variedad. No hubo diferencia significativa en las medias entre variedades para una aplicación, pero la diferencia si fue significativa luego de dos aplicaciones. Hernández et al. (2002) informan la detección de residuos de malaoxón en algunas muestras de diversas frutas pero no hubo correlación entre la disminución y la presencia de malaoxón. Ninguna muestra testigo resultó positiva para malaoxón.
CONCLUSIONES
El 25 % de las muestras analizadas (n=24) rebasan el LMR propuesto por la EPA y el Codex Alimentario FAO/WHO de 0.2 y 1.0 µg g–1, de malatión en mangos de las variedades estudiadas luego de dos aplicaciones de malatión, considerando aditivos los residuos de la molécula principal y su metabolito malaoxón. El análisi estadístico sugiere que a mayor número de aplicaciones de malatión, mayor concentración residual de ambas moléculas para las dos variedades. En 83–3 % de las muestras (n=24) para ambas variedades, se detectaron residuos del metabolito malaoxón en las dos variedades.
LITERATURA CITADA
AOAC. 2005. Official Methods of Analysis. Guidelines for Collaborative study. Procedures to Validate Characteristics of a Method of Analysis. Appendix D. United States, p: 1–12. [ Links ]
Aldana M., M., M. Garcia M., G. Rodriguez O., M. Silveira G., y A. Valenzuela Q. 2008. Determinación de insecticidas organofosforados en nopal fresco y deshidratado. Rev. Fitotec. Mex. 31 (2): 133–139. [ Links ]
ATSDR. 2003. Toxicological profile for malathion. Agency for Toxic Substances and Disease Registry. Public Health Service. U.S. Deparment of Health and Human Services. 327 p. [ Links ]
Calonge M., Y. Pérez–Pertejo, C. Ordoñez, R. Reguera, y D. Ordoñez. 2002. Determinación de residuos de siete insecticidas organofosforados en frutas mediante cromatografía de gases con detector de nitrógeno–fósforo y confirmación por espectrometría de masas. Rev. Toxicol. 19 (1): 55–60. [ Links ]
CENAM. 2004. Guía técnica sobre trazabilidad en cromatografía de gases (CG) y cromatografía de líquidos de alta resolución (CLAR). CENAM. México. pp:1–72. [ Links ]
CICOPLAFEST. 2003. Catálogo Oficial de Plaguicidas. SAGARPA. México. 480 p. [ Links ]
Coscolla, R. 1993. Residuos de Plaguicidas en Alimentos Vegetales. Mundi–Prensa. Madrid. 205 p. [ Links ]
Durmusoglu, E. 2003. Market basket monitoring of some organophosphorus pesticides on apple and strawberry in Izmir Province. Turkey. Archiv fur Lebensmittelhygiene 54 (1): 16–19. [ Links ]
EPA. 2006. Registration Eligibility Decision (RED) for Malathion. United States Environmental Protection Agency. United States. 195 p. [ Links ]
FAO/WHO. 1997. Pesticide Residues in Food (Malathion). Joint meeting of the FAO panel of experts on Pesticide Residues in Food and the Enviroment and the WHO Core Assessment Group. Lyon, France, pp: 1– 43. [ Links ]
FAO/OMS. 1999. Codex Alimentarius, Programa conjunto FAO/OMS sobre Normas Alimentarias. Roma, Italia. 76 p. [ Links ]
FAO/OMS. 2006. Codex Alimentarius. Programa conjunto FAO/OMS sobre Normas Alimentarias. Roma, Italia. 160 p. [ Links ]
FAO/WHO. 2006. Pesticide Residues in Food. Joint meeting of the FAO panel of experts on Pesticide Residues in Food and the Enviroment and the WHO Core Assessment Group. Rome, Italy. 400 p. [ Links ]
FDA, U.S. 1992. Residue monitoring 1991. J. Assoc. Anal. Chem. 75 (1): 135A–157A. [ Links ]
Guerrero A., J. 2003. Estudio de residuos de plaguicidas en frutas y hortalizas en áreas específicas de Colombia. Agron. Colombiana 21 (3): 198–209. [ Links ]
Hernández T. M., F. Egea G., M. Castro C., M. Moreno F., and J. Martínez V. 2002. Residues of methamidofos, malathion and methiocarb in greenhouse crops. J. Agric. Food Chem. 50(5): 1172–1177. [ Links ]
Hussain S., T. Masud, and K. Ahad. 2002. Determination of pesticides residues in selected varieties of mango. Pakistan J. Nutr. 1 (1): 41–42. [ Links ]
IUPAC. 2002. Harmonized guidelines for single–laboratory validation of methods of analysis. Pure Applied Chemistry. United States. 74 (5) : 835–855. [ Links ]
Jensen, R, A. Petersen, and K. Granby. 2003. Cumulative risk assessment of the intake of organophosphorus and carbamate pesticides in Danish diet. Food Additive Contaminants 20 (8): 776–785. [ Links ]
Montenegro, R. 2001. Informe sobre los riesgos sanitarios y ambientales del malatión. Red de acción en plaguicidas y sus alternativas para América Latina. Córdoba, Argentina, pp: 1–37. [ Links ]
Noa P., M., N. Pérez F., G. Díaz G., y S. Vega L. 2005. Cromatografía de gases y de líquidos de alta resolución. Aplicación en el análisis de alimentos. México. Universidad Autónoma Metropolitana– Xochimilco, División de Ciencias Biológicas y de la Salud. Núm. 57. Serie Académicos. 326 p. [ Links ]
PAM. 1999. Pesticide Analytical Manual. Volumen I, Chapter 3. U.S. Food and Drug Administration. 132 p. [ Links ]
Rassoulzadegan, M., and N. Akyurtlaki. 2002. An investigation on the toxic effects of malathion (organophosphate insecticide) on the Daphnia magna Straus, 1820 (Crustacea, Cladocera). Turk J. Zool. 26 (1): 349–355. [ Links ]
Ricardo M., B. Suárez, L. Nela, y M. García. 2000. Métodos de Análisis de Residuos de Plaguicidas. Centro de información y documentación de sanidad vegetal. La Habana, Cuba. 295 p. [ Links ]
Richter, E., F. Hoefler, and M. Linkerhaegner. 2001. Determining organophosphorus pesticides in food using accelerated solvent extraction with large sample sizes. LC–GC 19 (4): 408–412. [ Links ]
Saeed, T., N. Sawaya, N. Ahmad, and S. Rajagopal. 2005. Organophosphorus pesticide residues in the total diet of Kuwait. Arabian J. Sci. Eng. Kuwait 30 (1): 3–15. [ Links ]
SAGARPA. 2003. Servicio de Información Agroalimentaria y Pesquera. http://www.siap.gob.mx/ (consultado 12 enero 2007). [ Links ]
Salas, H., M. González, M. Noa, N. Pérez, G. Díaz, R. Gutiérrez, H. Zazueta, and I. Osasuna. 2003. Organophosphorus pesticide residues in Mexican comercial pasteurized milk. J. Agrie. Food Chem. 51 (15): 4468–4471. [ Links ]
Sánchez, J., G. Ettiene, I. Buscema, y D. Medina. 2005. Persistencia de los insecticidas organofosforados malathion y chlorpiryphos en guayaba (Psidium gtiajava L.). Rev. Fac. Agron. Luz 22: 62–71. [ Links ]
SMN. 2002. Normales climatológicas 1971–2000. Servicio Metereológico Nacional. http://www.smn.cna.gob.mx/climatologia/normales/estacion/oaxaca/NORMAL20328.TXT (consultado 20 enero 2007). [ Links ]
Zar, J. 1999. Biostatistical Analysis. Fourth ed. Printice Hall. New Jersey. 663 p. [ Links ]














