INTRODUCCIÓN
El cáncer es una de las principales causas de morbilidad y mortalidad en el mundo, casi una de cada seis defunciones se debe a esta enfermedad. Los cánceres de mama y de cuello uterino se ubican entre los primeros lugares como causa de muerte por tumores en la población del sexo femenino (OMS, 2015). La detección temprana del cáncer de cérvix ha reducido el índice de mortalidad, sin embargo, un importante porcentaje de casos tratados con cirugía, radioterapia y quimioterapia pueden resurgir y llevar incluso a metástasis originando nuevos y más agresivos tumores; la vacuna anti VPH ya es aplicada en algunos países, pero es un tratamiento profiláctico que no cubre la totalidad de serotipos oncogénicos (Bonanni et al., 2015). La investigación en productos naturales ha dado origen a gran parte de los fármacos utilizados en la actualidad, los esfuerzos para descubrir drogas anticancerígenas nuevas se han intensificado en el mundo y aproximadamente el 60% de principios empleados son de origen natural, especialmente de plantas (Alonso-Castro et al., 2011; Chavan, Damale, Shamkuwar, & Pawar, 2013; Gordaliza, 2007; Shaikh, Shrivastava, Apte, & Navale, 2016). En este trabajo se realizó una investigación con los miembros de la Cooperativa Tosepan Titataniske de las plantas medicinales recomendadas por pobladores de la comunidad de Cuetzalan del Progreso, eligiéndose las que podrían presentar actividad contra el cáncer de cérvix evaluándose tanto la actividad citotóxica, como la reducción en el tamaño y proliferación de tumores in vitro de células SiHa de los extractos acuosos e hidroalcohólicos.
MÉTODOS
Investigación y selección del material vegetal
Se solicitó a las mujeres que forman parte de la cooperativa, un listado con las plantas que ocupan de manera tradicional en el tratamiento de diversos padecimientos, con los datos: nombre común de la planta, su abundancia, forma de reproducción y usos; las plantas fueron seleccionadas de acuerdo a lo reportado en este listado y al uso tradicional, composición química y actividad biológica reportada en la bibliografía, para lo que se consultaron diferentes fuentes sobre la región (Cifuentes & Ortega, 1990; Flora Medicinal de México II y III, 1994; M. Martínez, 1979). Las partes aéreas de las plantas se recolectaron en la región de Cuetzalan del Progreso Puebla, México con la ayuda de miembros de la cooperativa Tosepan Titataniske y fueron identificadas en el Herbario de la Benemérita Universidad Autónoma de Puebla.
Preparación de extractos
Las hojas de cada planta se limpiaron y desinfectaron para posteriormente secarse a 40°C en horno eléctrico y fueron molidas y extraídas por maceración a temperatura ambiente, protegidas de la luz; para ambos extractos se empleó una proporción planta/disolvente del 10%; los extractos acuosos se pusieron en agitación continua de 150 rpm en un agitador orbital durante 24 h (Azmir et al., 2013; Betancourt, Saez, Granados, Salazar, & Ossa, 1999), y los extractos hidroalcohólicos (tinturas) se obtuvieron con etanol al 70% durante siete días (Saldierna, Suárez, García, & Rodríguez, 2001). Después del tiempo de maceración los extractos se esterilizaron por filtración con una membrana de 0.22 mm (discos de nylon Gelman Sciencies, Northampton, UK) manteniéndose en condiciones de esterilidad y oscuridad a -20°C, fueron llevados a sequedad en rotaevaporador para el cálculo de los rendimientos, estos se reportaron en porcentaje (%) m/m de extracto crudo.
Ensayos de citotoxicidad
Citotoxicidad de extractos en cultivos adherentes de células SiHa
La línea celular SiHa (carcinoma cervical con papilomavirus tipo 16) se mantuvo en medio mínimo esencial de Eagle´s (MEM) suplementado con 10% de suero fetal bovino (SFB), 1000 UI de penicilina, 100 µg /mL de estreptomicina e incubadas a 37°C en atmósfera húmeda con 95% de humedad. Una proporción de 1 X 104 células /pozo se depositaron en placas para cultivo celular de 96 pozos con MEM a las condiciones antes mencionadas y se incubaron durante 24 h, después de transcurrido este tiempo el medio se cambió por medio fresco con concentraciones de cada extracto desde 0.1 a 100 µg/mL (concentraciones diferentes fueron empleadas en este rango de concentración) y se incubaron por 72 h más. La citotoxicidad/ viabilidad celular fue determinada con sales de tetrazolio (MTT) siguiendo la metodología convencional para este método (Wang et al., 2015). Los resultados fueron expresados como porcentaje de viabilidad celular o como índice de citotoxicidad 50 (IC50), que es la concentración que inhibió el 50% del crecimiento celular; estos valores se estimaron por regresión lineal a partir de las curvas de dosis-respuesta para cada extracto, empleándose el programa KyPlot v 2.0. El quimioterapeútico Bleomicina (100 µg/mL) se usó como control positivo de citotoxicidad y el control negativo fueron células cultivadas bajo las mismas condiciones, pero sin los extractos vegetales (sin tratamiento), al control negativo para los experimentos con los extractos hidroalcohólicos se adicionó la cantidad de etanol corres-pondiente a la máxima concentración experimental empleada.
Actividad sobre los tumores in vitro
Condiciones de cultivo para el aislamiento y formación de clonas tumorales
El método para el cultivo de las clonas tumorales fue adaptado de Freshney, 1991. El medio de cultivo se preparó con 0.5 mL de agarosa al 2% y 0.5 mL de medio MEM 2X a temperatura de 45°C, esta mezcla se vertió en placas para cultivo celular de 24 pozos, 24 h antes de colocar las células. Las monocapas de células SiHa fueron cosechadas usando tripsina 0.1 M y buffer de fosfatos (PBS), se diluyeron a una concentración de 1 X 105 células/mL en MEM 2X por pozo. Un volumen igual de carboximetilcelulosa (CMC) estéril al 2.72% fue adicionada y mezclada con las células en suspensión y posteriormente la mezcla se colocó en los pozos que contenían previamente el medio agarosa-MEM (suplementado con SFB y antibióticos) preparado, las placas se incubaron a 37°C en atmósfera húmeda con 5% de CO2 y se mantuvieron así hasta observar las clonas tumorales (dos semanas), adicionándose 0. 5 mL de la mezcla agarosa-MEM cada tercer día. Las clonas tumorales se aislaron del medio cuando fueron visibles y posteriormente se depositaron en cajas de cultivo celular para formar monocapas que fueron empleadas para los cultivos de actividad antitumoral (Freshney, 1991).
Inhibición en el crecimiento del tumor in vitro
La inhibición del crecimiento del tumor in vitro se realizó colocando 1 X 104 UFC tumorales (células SiHa)/500 µL MEM-CMC 2X (1:1); con concentración de los extractos desde 0.1-100 µg/mL en placas para cultivo celular de 24 pozos con el medio semisólido agarosa-MEM y se incubaron bajo las mismas condiciones de cultivo durante 96 h, transcurrido este tiempo, las colonias tumorales (tumores in vitro) fueron removidas delicadamente por aspiración, y se disgregaron con tripsina; la viabilidad de las mismas se determinó con el ensayo MTT; adicionalmente el tamaño del tumor formado se determinó por micrografía empleando el software Image Tool 3. Todas las pruebas se llevaron a cabo por triplicado en tres experimentos biológicamente independientes.
RESULTADOS
Selección de plantas y extractos obtenidos
La tabla 1 muestra el listado de 88 plantas recabado por los miembros de la cooperativa TOSEPAN Titataniske de Cuetzalan, Puebla, que incluye nombre científico y referencias sobre la actividad biológica mencionada de acuerdo a la bibliografía. En ella se destacan cuatro plantas recomendadas para el tratamiento del cáncer: árnica, espinoso, huichin y sábila; de la sábila, el árnica y el huichin existen investigaciones previas sobre esta actividad bajo metodologías semejantes (El-Shemy et al., 2010; Kim, Kacew, & Lee, 1999; Quintero, Pelcastre, & Solano, 1999; Via et al., 2015). Con la búsqueda bibliográfica se seleccionaron tres plantas de acuerdo a su empleo tradicional, composición química y actividad farmacológica reportada (Cifuentes & Ortega, 1990; Flora Medicinal de México II y III, 1994; M. Martínez, 1979), siendo las plantas para el estudio: la caña de venado clasificada como Costus pulverulentus (número de espécimen 12211), originaria de México a Centroamérica y oeste de Sudamérica, asociada a bosque tropical perennifolio; el espinoso clasificado como Sechium edule (número de espécimen 17447), originario de México en climas cálido, semicálido, semiseco y templado; cojón de gato clasificado como Tabernaemontana alba (número de espécimen 31 423), originaria de México y Centroamérica que se desarrolla en clima cálido; y Ocma, que se clasificó como Vernonia patens (número de espécimen 12 130), originaria de México y norte de Sudamérica, presente en climas cálido, semicálido y templado (Cifuentes & Ortega, 1990; Flora Medicinal de México II y III, 1994; M. Martínez, 1979). Los especímenes fueron reservados en el Herbario del Jardín botánico de la BUAP.
Tabla 1 Listado de plantas de uso medicinal recomendadas por miembros de la Cooperativa Tosepan Titataniske, Cuetzalan del Progreso, Puebla.
| Planta | Disponibilidad/Forma de reproducción | Uso medicinal | Nombre científico (referencias sobre estudios de actividad biológica) |
|---|---|---|---|
| 1. Ajenjo | abundante / mata | bilis (té) | Artemisia absinthium L. (W. Ahmad, Hasan, Abdullah, & Tarannum, 2010; Govind, 2011) |
| 2. Ajo | abundante / semilla | tos, bronquitis | Allium sativum L. (Sultana, Khan, Safhi, & A. Alhazmi H., 2016) |
| 3. Ala de murciélago | poco / camote o guia | riñones (té) | Passiflora coriacea Juss. (UNAM, 2009a). No existen reportes que corroboren este uso |
| 4. Albahacar | abundante / vara | mal aire, cólico menstrual | Ocimum basilicum (Ghafari et al., 2018; Rodrigues et al., 2016) |
| 5. Arnica | poco / semilla | lavar las heridas, desinflamar, artritis y cicatrizar | Arnica montana / Heterotheca inuloides (Hostanska, Rostock, Melzer, Baumgartner, & Saller, 2012; Rodríguez-Chávez et al., 2017) |
| 6. Asonate | abundante / vara | mal de aire y limpias | Brickellia veronicifolia Kunth (UNAM, 2009b). No existen reportes que corroboren este uso |
| 7. Astzomiate | abundante / vara o semilla | ojeadas | Barkleyanthus salicifolius (Kunth) Rob. et. Brett. (UNAM, 2009q). No existen reportes que corroboren este uso |
| 8. Bayetilla | abundante / vara o semilla | lavar heridas, dolor de estómago (te), cicatrización, hemorragias, gastritis (agua de uso con huichin) | Hamelia patens (A. Ahmad, Pandurangan, Singh, & Ananad, 2012) |
| 9. Verbena | abundante / semilla | bilis | Verbena officinalis L. (Tiwari, 2008) |
| 10. Bugambilia | abundante / vara | tos (té) | Bougainvillea glabra (Alonso-Castro et al., 2012; Elumalai, Eswaraiah, Madhavi, & Ali, 2012) |
| 11. Pelo de elote | abundante / semilla | dolor de riñón | Estigma maydis (Sukandar, Sigit, & Adiwibowo, 2013; Vijitha & Saranya, 2017) |
| 12. Cacaloxochit | poco / tallo | dolor de riñón, colitis | Plumeria acutifolia (Alhozaimy, Al-Sheddi, & Ibrahim, 2017) |
| 13. Calahuala | abundante / camote | riñones, mal de orín | Phlebodium aureum (L.) J. Smith (UNAM, 2009c). No existen reportes que corroboren este uso |
| 14. Cana de venado | abundante / raiz | riñones y mal de orín | Costus pulverulentus (UNAM, 2009r). No existen reportes que corroboren este uso |
| 15. Cana morada | NR / semilla | riñones , mal de orín (té) | Saccharum officinarum L. (UNAM, 2009d). No existen reportes que corroboren este uso |
| 16. Cebolla | abundante / semilla | hemorragia de menstruación (hervida con sal), tos, dolor de oído | Allium cepa (Amir, Dhaheri, Jaberi, Marouqi, & Bastaki, 2011; Augusti, 1996) |
| 17. Cempasuchil | poco / semilla | bilis | Tagetes erecta L. (Gopi, Elumalai, & Jayasri, 2012) |
| 18. Cuetexiquit | abundante / raíz o semilla | calambres, bilis | No existen reportes para esta planta |
| 19. Chanclan | abundante / rama | recaídas | No existen reportes para esta planta |
| 20. Chilillo | abundante / vara | sarna | Alchemilla procumbens Rose (UNAM, 2009e). No existen reportes que corroboren este uso |
| 21. Durazno | abundante / semilla | curar heridas y baños | Prunus persica L. Batsch (Aziz & Rahman, 2013; Gasparotto et al., 2014) |
| 22. Encino | corteza / semilla | curar heridas y baños | Género Quercus (Aroonrerk & Kamkaen, 2009; Güllüce et al., 2004) |
| 23. Epazote | abundante / semilla o vara | desparasitante, control de plagas, sazonar comidas | Chenopodium ambrosioides L. (Kliks, 1985; Monzote et al., 2006) |
| 24. Espinosilla | abundante / vara | fiebre, gripa, tos, recaídas | Loeselia mexicana (Lam) Brandgee (UNAM, 2009f). No existen reportes que corroboren este uso |
| 25. Espinoso | abundante / semilla | cáncer | Sechium edule (Laure, Faca, Izumi, Padovan, & Greene, 2006; Monroy-Vázquez et al., 2009) |
| 26. Estafiate | poco / rama | dolor de estómago, susto | Artemisia ludoviciana (Zavala-Sánchez, Pérez-Gutiérrez, Pérez-González, Sánchez-Saldivar, & L. Arias-García, 2002) |
| 27. Hierbabuena | abundante / vara o raíz | desparasitante, dolor de estómago, cólicos, partos, sazonar comida, tos, gripa, diarrea (con canela), lechada | Mentha piperita L. (Saharkhiz et al., 2012; Vidal et al., 2007) |
| 28. Hierba del cancer | abundante / rama | heridas | Cuphea aequipetala Cav (Palacios-Espinosa et al., 2014; Waizel-Bucay, Martínez-Porcayo, Villarreal-Ortega, Alonso. Cortés, & A. Pliego-Castañeda, 2003) |
| 29. Hierba dulce | abundante / vara | hemorragia, cólico menstrual | Lippia dulcis Trev. (UNAM, 2009g). No existen reportes que corroboren este uso |
| 30. Hoja de aguacate | abundante / semilla | mal de aire (hojas), inflamación, paperas (huesos molidos) | Persea americana (Idris, Ndukwe, & Gimba, 2009; Owolabi, Coker, & Jaja, 2010) |
| 31.Hoja de cafe | abundante / semilla | calmante de nervios, presión | Coffea arabica L. (Godos et al., 2014) |
| 32. Hoja de guayabo | abundante / semilla | diarrea | Psidium guajava L. (Kamath, Rahul, Ashok, & Lakshmi, 2008) |
| 33. Hoja de limon | abundante / semilla | calmante de nervios | Citrus limon (L.) Burm. F. (Cherng-Wei, Wen-Sung, Chi-Tang, & Lee-Yan, 2013) |
| 34. Hoja de maracuya | abundante / semilla | calmar nervios | Passiflora edulis sims (Li et al., 2011) |
| 35. Hoja de naranja | abundante / semilla | infección y empacho, para granos | Citrus sinensis (L.) Osbeck (Milind & Dev, 2012) |
| 36. Hoja santa | abundante / vara | curar heridas y baños | Piper sanctum (Miq.) Schlechtendal (UNAM, 2009h). No existen reportes que corroboren este uso |
| 37. Huele de noche | abundante / semilla | susto y balo general | Cestrum nocturnum L. (Pérez-Saad & Buznego, 2008) |
| 38. Huichin | abundante / vara | curar heridas, infecciones (té), desinflamar, fiebre, riñones | Verbesina persicifolia D.C. (Via et al., 2015) |
| 39. Izote | poco / tallo | diabetes, mal de oído | Yucca elephantipes Regel (Cruz & Andrade-Cetto, 2015) |
| 40. Jarilla | abundante / rama | bilis | Barkleyanthus salicifolius (Kunth) Rob. & Brett. (M. Domínguez et al., 2005) |
| 41. Jengibre | poco / camote | descongestionar vías respiratorias, dolor de reumas | Zingiber officinale Roscoe (Badoni, Kumar, Combrinck, & Viljoen, 2015) |
| 42. Kouapajxiuit o Santa Elena | abundante / raíz o semilla | desparasitante para lombrices, piquete de víbora (semilla) | Spigelia palmeri Rose (UNAM, 2009i). No existen reportes para esta actividad |
| 43. Laurel | NR / semilla | congestiones | Litsea glaucescens Kunth (López-Romero et al., 2018) |
| 44. Lengua de ciervo | poco / guía | riñones, mal de orín | Tectaria heracleifolia (Willd.) Underw. (UNAM, 2009j). No existen reportes que corroboren este uso |
| 45. Limon | abundante / semilla | para las heridas | Citrus limon (L.) Burm. F. (UNAM, 2009k). No existen reportes que corroboren este uso |
| 46. Malva | poco /semilla | desinflamar | Malva parviflora L. (Bouriche, Meziti, Senator, & Arnhold, 2011) |
| 47. Maltantzin morado, blanco, chino | abundante / vara o raíz | susto, pelotillas | Scutellaria guatemalensis (A. M. A. Martínez et al., 2001). No existen reportes que corroboren este uso |
| 48. Manzanilla | abundante / semilla | dolor de estómago, vista, desinflamar | Matricaria recutita L. (Gupta, Mittal, Bansal, Khokra, & Kaushik, 2010) |
| 49. Mejorana | poco / vara | cólicos, resfriado del estomago | Origanum majorana L (Al-Howiriny et al., 2009) |
| 50. Menta | poco / planta completa | diarrea y cólicos | Mentha spicata (Moosavy & Shavisi, 2013) |
| 51. Mirto | abundante / rama | dolor de oído y cabeza, bilis, baño para parturientas | Salvia microphylla Kunth y Salvia coccinea Juss (UNAM, 2009l). No existen reportes que corroboren este uso |
| 52. Mozote, Mozote morado | abundante / semilla | susto | Bidens pilosa L. (UNAM, 2009m). No existen reportes que corroboren este uso |
| 53. Muicle | abundante / tallo o rama | alferecía | Justicia spicigera Schl. (UNAM, 2009n). No existen reportes que corroboren este uso |
| 54. Nopal | NR / nopal | diabetes | Opuntia ficus-indica (L.) Miller (Osuna-Martínez, Reyes-Esparza, & Rodríguez-Fragoso, 2014) |
| 55. Ogma | abundante / semilla | disentería | Vernonia patens Kunth (Pérez-Amador, Ocotero, Benítez, & Jiménz, 2008) |
| 56. Omequelite | abundante / vara, semilla o raíz | quemaduras, después del parto, tos, resfriado, baños, hemorragia nasal, vapores vaginales | Piper auritum Kunth (F. Domínguez, Lozoya, & Simon, 2007) |
| 57. Oregano | abundante / vara o semilla | bronquitis, mal de ojo | Origanum vulgare L. (Amber, Adnam, Tariq, & Mussarat, 2017) |
| 58. Pagua | poco / semilla | paperas | Persea schiedeana (Villavicencio & Pérez, 2006) |
| 59. Peonia | poca / semilla | alferecía en té con rosa blanca | No se posee suficiente información |
| 60. Pimienta | abundante / semilla | bronquitis | Piper dioica (Sindhu & Manorama, 2014). No existen reportes que corroboren este uso |
| 61. Plátano gineo | poco / camote | alforre de los niños | Musa sapientum L. (Lucas, Dumar, & Cárdenas V.C.A., 2013). No existen reportes que corroboren este uso |
| 62. Poleo | NR / hoja | dolor de estomago | Mentha pulegium L. (Darvishi et al., 2014) |
| 63. Raíz de milpa morada | NR / semilla | alferecía | Zea mays L., variedad morada (Pedreschi & Cisneros-Zevallos, 2007). No existen reportes que corroboren este uso |
| 64. Romero | abundante / vara | para saumar | Rosmarinus officinalis L (Okoh, Sadimenko, & Afolayan, 2010). No existen reportes que corroboren este uso |
| 65. Rosa de Castilla | abundante / tallo | fiebre, purga, dolor de cabeza, limpiar la vista y derrame de ojos | Rosa gallica L. (Bonjar, 2004) |
| 66. Ruda | abundante / rama | bilis, tos, aire, cólicos | Ruta graveolens L. (García, Martínez, Ortega, & Castro, 2010; Saeidinia et al., 2016) |
| 67. Sabila | poca / camote | desinflamar, erisipela, cicatrización, principios de cáncer, diabetes (con nopal), caída de pelo | Aloe vera L. (Singh, Sharma, Kumar, & Dudhe, 2010) |
| 68. Secapalo | poca / guía | susto | Género Struthanthus (Leitão, Moreira, Almeida, & Guimarães, 2013). No existen reportes que corroboren este uso |
| 69. Sauco | abundante / rama | ojeada, mal de ojo | Sambucus mexicana Presl (UNAM, 2009o). No existen reportes que corroboren este uso |
| 70. Suape | abundante / rama | cólicos | No existen reportes para esta planta |
| 71. Tabardillo | abundante / rama | cólicos | Piqueria trinervia Cav (Esparza, Bye, Meckes, Torres-López, & M. Jiménez-Estrada, 2007) |
| 72. Tacechinolxihuit | abundante / semilla o raíz | sarampión, viruela | No existen reportes para esta planta |
| 74. Talamat | abundante / raíz | bronquitis, baños, disentería | Desmodium incanum DC. (Hao et al., 2015). No existen reportes que corroboren este uso |
| 75. Talocma | abundante / rama | ataques | No existen reportes para esta planta |
| 76. Tepocihyac | abundante / raíz o semilla | disentería | No existen reportes para esta planta |
| 77. Te cedron | poco / rama | diarrea | Aloysia triphylla Brett. (Ali, El-Beltagi, & Nasr, 2011) |
| 78. Tiricia | poco / tallo | susto | No existen reportes para esta planta |
| 79. Tzopelitcxihuil | poco / raíz | dolor de estomago | No existen reportes para esta planta |
| 80. Violeta | abundante / rama | estreñimiento | Viola odorata L. (Akhbari, Batooli, & Kashi, 2011) |
| 81. Xalcuahuit | abundante / semilla | infección intestinal | No existen reportes para esta planta |
| 82. Xalxocot tzinaca | abundante / semilla | disentería | No existen reportes para esta planta |
| 83. Xomet | abundante / tallo | mal aire | No existen reportes para esta planta |
| 84. Yoloxochitl | poco /semilla | dolor de corazón | Talauma mexicana DC. (Waizel-Bucay, 2002) |
| 85. Zacapale | abundante / semilla | susto | Cuscuta jalapensis Sch. (UNAM, 2009p). No existen reportes que corroboren este uso |
| 86. Zanahoria | NR / semilla | vista | Daucus carota L. (Da Silva, 2014) |
| 87. Zapote blanco | poco / semilla | presion | Casimiroa edulis Llave y Lex (Awaad et al., 2011) |
| 88. Zapote negro | abundante | sarna | Diospyros digyna Jacq (Leonti, Vibrans, Sticher, & Heinrich, 2001) |
Los rendimientos para los extractos tanto acuosos como hidroalcohólicos después de la evaporación de los solventes se presentan en la tabla 2, como puede verse los rendimientos más altos se obtuvieron con las maceraciones hidroalcohólicas.
Actividad citotóxica sobre cultivos adherentes de células SiHa
Extractos acuosos
Al exponer los cultivos celulares adherentes a los extractos acuosos se observó que los extractos de C. pulverulentus y V. patens incrementaron la proliferación celular en 11.11% y 48.6%, respectivamente; a la concentración de 10 µg/mL, en relación a las células sin tratamiento; las células tratadas no muestran cambios morfológicos visibles (fig. 1-B y 1-E) al comparase con las células no tratadas (fig. 1-A). Los extractos de S. edule y de T. alba inhibieron levemente la proliferación; S. edule aumentó el crecimiento celular a las concentraciones de 1 µg/mL (23.6%) y 10 µg/mL (43.4%), sin embargo, a 100 µg/mL reduce el crecimiento en 11.3% observándose a esta concentración células dañadas y en menor número (fig. 1-C); T. alba mostró un efecto inhibitorio de 15.8% a la concentración de 100 µg/mL mostrando en la micrografía una menor densidad celular con células desprendidas (fig. 1-D). La bleomicina presentó un máximo de disminución de la proliferación celular a la concentración de 100 µg/mL de 41.6%, observándose al microscopio daño celular severo con muy disminuido número de células (fig. 1-F). En la tabla 3 se pueden observar los valores de viabilidad celular resultantes.
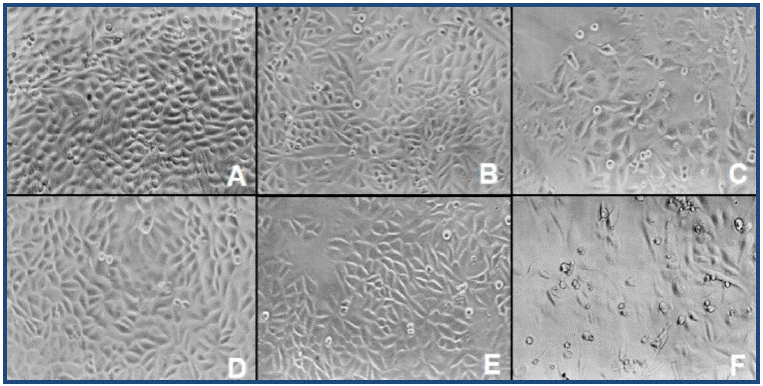
Fig. 1 Micrografías por contraste de fase para las células SiHa tratadas con los extractos acuosos (concentración de 100 µg/mL): células no tratadas (A), C. pulverulentus (B), S. edule (C), T. alba (D), V. patens (E). Se observan cambios morfológicos para S. edule y T. alba con una reducción en el número de células; en las células expuestas a Bleomicina (F) se observa daño celular importante con abundante detrito celular y disminuido número de células; para C. pulverulentus y V. patens no existen cambios aparentes (Magnificación 200X).
Tabla 3 Actividad de los extractos acuosos a diferentes concentraciones en la viabilidad de células SiHa. La concentración de 0 µg/mL corresponde a células sin tratamiento (control negativo).
| Extracto acuosos | Viabilidad celular (%) ± DE a diferentes concentraciones (µg/mL) | ||||
|---|---|---|---|---|---|
| 0 | 0.1 | 1 | 10 | 100 | |
| C. pulverulentus | 100 ± 5.06 | 103 ± 3.3 | 108.6 ± 0.6 | 111.11 ± 2.2 | 108.6 ± 2.0a |
| S. edule | 100 ± 3.0 | 103 ± 16.5 | 123.6 ± 3.8 | 143.4 ± 11.2 | 88.7 ± 5.3b |
| T. alba | 100 ± 1.64 | 105 ± 1.04 | 98.4 ± 1.1 | 94 ± 3.3 | 84.2 ± 3.9b |
| V. patens | 100 ± 10.3 | 125 ± 6.8 | 143.6 ± 8.9 | 148.6 ± 7.9 | 115.7 ± 5.7a |
DE = desviación estándar
a, b = Letras diferentes indican diferencia significativa con p < 0.05.
Extractos hidroalcohólicos
Todos los extractos hidroalcohólicos disminuyeron la viabilidad de las células SiHa de una manera dosis dependiente, resultando en la muerte de la población celular del 50 % o más a la concentración de 100 µg/mL dependiendo de la planta empleada (tabla 4). El efecto citotóxico de los extractos vegetales sobre las células SiHa se observa en la microscopía (fig. 2-B a 2-E), este efecto no fue producido por la adición de etanol al medio de cultivo (fig. 2-A). El índice de citotoxicidad 50 % (IC50) determinado para cada extracto fue de 16.5 µg/mL para S. edule, 54.8 µg/mL para T. alba, 69.1 µg/mL para V. patens y 90.2 µg/mL para C. pulverulentus. A la concentración de 100 µg/mL S, edule, T. alba y V. patens presentan prácticamente el mismo valor de citotoxicidad, C. pulverulentus tuvo la menor actividad (tabla 4).
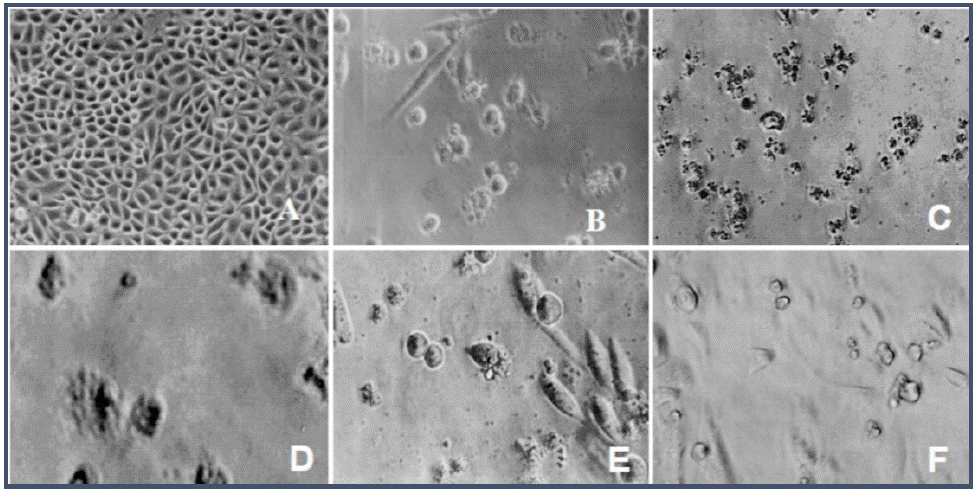
Fig. 2 Micrografías por contraste de fase de células SiHa tratadas con los extractos hidroalcohólicos (100 µg/mL): se observan células muertas; algunas con aumento de tamaño y citólisis (D), redondeadas y desprendidas de la monocapa y con abundante detrito celular (B, C, E): Células no tratadas (A), C. pulverulentus (B), S. edule (C), T. alba (D) y V. patens (E). El efecto más citotóxico se presenta en las células expuestas a S. edule y T. alba; la Bleomicina (F) también muestra efecto citotóxico (magnificación 200x).
Tabla 4 Actividad citotóxica de los extractos hidroalcohólicos en células SiHa a 100 µg/mL y valor de IC50 determinado para cada planta.
| Extracto hidroalcohólico | Viabilidad celular (%) ± DE a dosis de 100 µg/mL | IC50 (µg/mL) ± DE |
|---|---|---|
| C. pulverulentus | 47.9 ± 2.1a | 90.2 ± 4.64* |
| S. edule | 10.1 ± 5.6b | 16.5 ± 2.5** |
| T. alba | 11.75 ± 2.1b | 54.8 ± 3.9*** |
| V. patens | 15.8 ± 0.8b | 69.1 ± 6.9**** |
DE = desviación estándar
a, b, c, d = Letras diferentes indican diferencia significativa con p < 0.05
*,**,***,**** = Diferente número de asteriscos indican diferencia significativa con p < 0.05
Efecto de los extractos en el crecimiento de los tumores in vitro
Extractos acuosos
La capacidad de los extractos de las plantas para reducir el tamaño del tumor se ensayó mediante la reproducción de un ensayo clonogénico antiguo que favorece el desarrollo y crecimiento de tumores in vitro (Freshney, 1991). Los extractos acuosos de T. aba y V. patens fueron probados sobre las clonas tumorales de las células SiHa en el medio de cultivo semisólido. Los extractos acuosos fueron seleccionados por sus efectos contrarios en los cultivos en monocapa (para T. alba citotoxicidad y para V. patens incremento de la proliferación celular). Los resultados corroboran el efecto de ambos extractos en las células adherentes, como puede observarse en la tabla 5 el extracto acuoso de T. alba disminuyó la proliferación (tamaño) de las clonas en los tumores y en el caso de V. patens la proliferación del tumor se incrementó. La determinación de viabilidad celular con MTT para los tumores muestra una reducción del 13.6 % para T. alba e incremento de 111% para V. patens a 100 µg/mL.
Tabla 5 Actividad de extractos acuosos en la proliferación de clonas en los tumores in vitro. La concentración de 0 µg/mL corresponde a células sin tratamiento (control negativo).
| Extracto acuoso | Viabilidad celular (%) ± DE a diferentes concentraciones (µg/mL) | ||||
|---|---|---|---|---|---|
| 0 | 0.1 | 1 | 10 | 100 | |
| T. alba | 100 ± 0.04 | 106.5 ± 0.06 | 126.6 ± 0.01 | 90.08 ± 0.02 | 86.4 ± 0.04a |
| V. patens | 100 ± 0.66 | 108 ± 1.5 | 128 ± 2.1 | 137.5 ± 0.97 | 211 ± 2.05b |
DE = desviación estándar
a, b = Letras diferentes indican diferencia significativa con p < 0.05.
Extractos hidroalcohólicos
Todos los extractos hidroalcohólicos redujeron el tamaño y la proliferación del tumor in vitro sin presentar diferencia significativa entre ellos a la concentración de 100 µg/mL; sin embargo, el extracto de V. patens presentó actividad desde la concentración de 1 µg/mL (40% de disminución de la viabilidad) que se mantuvo a las concentraciones de 10 µg/mL y 100 µg/mL; S. edule disminuyó en 25.7% la proliferación del tumor a la concentración de 10 µg/mL y de 39.6% para la concentración de 100 µg/mL; los extractos de C. pulverulentus y T. alba redujeron en 31.3% y 32.9%, respectivamente la viabilidad del tumor a la concentración de 100 µg/mL (tabla 6).
Tabla 6 Actividad de los extractos hidroalcohólicos a diferentes concentraciones en la viabilidad de clonas en los tumores in vitro. La concentración de 0 µg/mL corresponde a las células no tratadas.
| Extracto hidroalcohólico | Viabilidad celular (%) ± DE a diferentes concentraciones (µg/mL) | ||||
|---|---|---|---|---|---|
| 0 | 0.1 | 1 | 10 | 100 | |
| C. pulverulentus | 100 ± 6.25* | 124.7 ± 6.9* | 80.5 ± 6.0* | 106.8 ± 6.7*a | 69.6 ± 5.7**,d |
| S. edule | 100 ± 8.4* | 88.2 ± 2.7* | 94.4 ± 3.4* | 74.3 ± 2.7**b | 60.4 ± 1.3***d |
| T. alba | 100 ± 7.5* | 94.4 ± 2.5* | 106.8 ± 5.3* | 111.4 ± 6.3**a | 68.1 ± 2.8**d |
| V. patens | 100 ± 7.7* | 88.2 ± 3.4* | 60.4 ± 3.1** | 63.5 ± 2.9**c | 71.2 ± 3.02**a |
DE = desviación estándar
a, b, c, d = Letras diferentes en las columnas indican diferencia significativa con p < 0.05 entre los extractos a las concentraciones señaladas.
*, **, *** = diferente número de asteriscos en una misma fila indican diferencia significativa con p < 0.05 entre las dosis evaluadas para el mismo extracto.
En la figura 3 se observan los tumores in vitro expuestos a dosis de 10 µg/mL de cada extracto, hay una disminución de tamaño en los tratados con V. patens con respecto a las demás plantas, los datos obtenidos con el programa Image Tool, fueron: 4044.7 + 368.5 pixeles (tumor sin tratamiento) 7871.33 + 368.5 pixeles (C. pulverulentus), 2073.33 + 197.9 pixeles (S. edule), 5816.33 + 191.3 (T. alba) y 842.67 + 113.52 (V. patens); la tabla 7 presenta los porcentajes determinados para el tamaño de los tumores con respecto al control negativo.
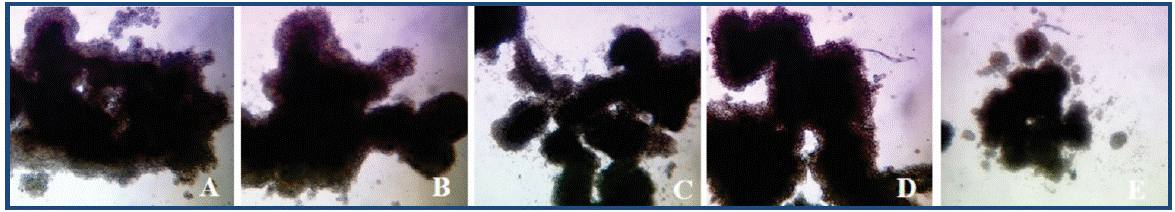
Fig. 3 Reducción del tamaño del tumor in vitro : Los ensayos clonogénicos fueron desarrollados como se mencionó previamente, las células SiHa se trataron con los extractos hidroalcohólicos por tres días (10 µg/mL). El tamaño del tumor muestra una notable reducción con V. patents (E), seguido por S. edule (C); para C. pulverulentus y T. alba (D) no se observa disminución comparando con el control negativo (A). Las micrografías fueron obtenidas con microscopio estereoscópico (Magnificación 20X).
Tabla 7 Porcentajes de tamaño con respecto al control negativo de los tumores in vitro crecidos en presencia de los extractos hidroalcohólicos a la concentración de 10 µg/mL
| Extracto hidroalcohólico | Porcentaje del tamaño de tumor in vitro respecto al Control negativo (%) ± DE |
|---|---|
| Control negativo | 100 ± 9.11a |
| C. pulverulentus | 194.6 ± 2.4bc |
| S. edule | 51.3 ± 9.6d |
| T. alba | 143.8 ± 11ac |
| V. patens | 20.8 ± 13.5d |
DE = desviación estándar
a, b, c, d = Letras diferentes indican diferencia significativa con p < 0.05
Comparando los resultados de viabilidad y tamaño de los tumores in vitro, podemos notar que no existe una correspondencia exacta en cuanto a los porcentajes, sin embargo, si existe un patrón de comportamiento, esto sugiere que al determinar la viabilidad tomamos en cuenta a las células vivas, mientras que en el tamaño las células pueden quedar ocultas dentro del tumor y a medida que el tumor se desarrolla el contacto de las células con el extracto disminuye.
DISCUSIÓN
Tres de los cuatro extractos acuosos probados (C. pulverulentus, S. edule y V. patens) indujeron un incremento en la proliferación celular a las concentraciones menores de 0.1, 1 y 10 µg/mL, este comportamiento ha sido observado también en otros trabajos (Itharat et al., 2004; Whelan & Ryan, 2003) y puede deberse a un efecto estimulante de compuestos de naturaleza terpenoide como las saponinas los fitoestrógenos y los fitoesteroides que a concentraciones bajas inducen la proliferación celular pero al incrementarse la reducen (Leyva, Navarro-Tovar, Loredo-Carrillo, & Santos, 2011). A la concentración de 100 µg/mL los extractos acuosos de S. edule y T. alba presentaron baja actividad citotóxica. Tomando en cuenta los valores de IC50 determinados y comparándolos con la bibliografía, podemos considerar que los extractos hidroalcohólicos de las cuatro plantas poseen potencial para el tratamiento del cáncer, Estrada et al., 2013 considera que valores de IC50 < 100 µg/mL en extractos crudos son candidatos para el aislamiento de metabolitos con acción antitumoral (Estrada, López, Márquez, Martínez, & Márquez, 2013), mientras que Suffness y Pezzuto en 1990 establecen como parámetro valores de IC50 < 30 µg/mL (Suffness & Pezzuto, 1990), los extractos hidroalcohólicos de C. pulverulentus, T. alba y V. patens presentaron valores de IC50 menores a 100 µg/mL, mientras que el de S. edule es menor a 30 µg/mL. De las cucurbitáceas, familia botánica a la que pertenece S. edule se han aislado proteínas (Dhiman, Gupta, Sharma, Gill, & Goyal, 2012; Ibrahim, Shalaby, El-Gengaihi, & Rizk, 1999; Jayaprakasam, Seeram, & Nair, 2003; Poma, Marcozzi, Cesare, Carmignani, & Sapano, 1999; Rajasree, Sibi, Francis, & William, 2016) inhibidoras de proteasas y proteínas tipo RIP (proteínas inhibidoras de ribosomas) en semillas (Laure et al., 2006; Wu, Chow, & Lin, 1998), ambas poseen potencial anticancerígeno, los frutos del chayote mostraron actividad citotóxica en células L929 y HeLa a concentraciones de IC50 de 2.22 y 2.68 mg/mL respectivamente, las fracciones del extracto metanólico de los frutos tuvieron en células L929 valores de IC50 menores (0.047 mg/mL), el análisis fitoquímico mostró la presencia de ácidos grasos saturados e insaturados (Monroy-Vázquez et al., 2009); los extractos alcohólicos del fruto de diferentes variedades de chayote entre ellas: virens levis, nigum xalapensis y nigrum spinosum presentan metabolitos con actividad antiproliferativa y citotóxica, diferentes híbridos de Sechium edule (Jacq.) Sw. favorecen su efecto a partir de la modificación de su metabolismo secundario (Monroy-Vázquez et al., 2009; Uriostegui, 2014).
Costus pulverulentus (Costaceae) mostró la menor actividad citotóxica con un IC50 de 90.2 µg/mL, en el extracto alcohólico de los tallos se ha identificado campesterol, stigmasterol, β-sitosterol, ácido vanílico, entre otros con un moderado efecto anticonceptivo y antiinflamatorio; este mismo extracto mostró una baja citotoxicidad en células PC-3 de carcinoma de próstata con una IC50 de 179 + 23.2 µg/mL (Alonso-Castro et al., 2016), valores de IC50 mayores que para las células SiHa, en el extracto hexánico crudo se observó potencial antioxidante y antitopoisomerasa (Niño, Correa, Cardona, & Marino, 2011) que podrían contribuir a la citotoxicidad mostrada en este estudio. El extracto de V. patens de la familia Compositae mostró una IC50 de 69.1 µg/m, miembros de este mismo género han sido reportados por su actividad citotóxica, V. guineensis presenta actividad citotóxica sobre células de linfoma y sarcoma de Kaposi del 100% a concentraciones 8 µg/mL, induce apoptosis y reduce el tamaño de tumores (40%) inducidos en ratones nude (Toyang, Toyang, & Toyeng, 2012), podemos destacar que en los tumores in vitro desarrollados en nuestra investigación V. patens fue la que produjo el efecto inhibitorio mayor a menor concentración; V. amygdalina ha sido ampliamente estudiada por su actividad en células de cáncer de mama (MCF-7, MDA-MB-231) el extracto etanólico presentó concentraciones de IC50 de 56 µg/mL y 46 µg/mL, respectivamente, sugiriéndose un arresto del ciclo celular (Wong, Woo, Hsu, & Tan, 2013), en otro estudio el extracto acuoso presentó IC50 de 5.67 + 2 µg/mL para las células MCF-7 (Howard, Johnson, Pervin, & Izevbigie, 2015), los resultados para estas muestran mayor actividad que los obtenidos para las células SiHa, lo que puede deberse al tipo celular y a la especie. El extracto hidroalcohólico de T. alba (Apocynaceae) tuvo una concentración de IC50 de 54.8 µg/mL, los efectos citotóxicos de algunos miembros de esta familia han sido probados con diferentes líneas celulares de cáncer humano (Itharat et al., 2004; Kuo et al., 1999) y una importante actividad antioxidante ha sido reportada para este género (Moussa, Emam, Diab, Mahmoud, & Mahmoud, 2011); T. catharinensis produjo citólisis con extractos obtenidos con fluídos supercríticos a la concentración de 25 µg/mL con disminución de la proliferación de células tumorales (mama, pulmón, melanoma, colon, próstata y riñón) del 50% (Pereira, Carvalho, & Meireles, 2006), monoterpenos indol alcaloides aislados de T. elegans indujeron apoptosis aproximadamente del 40% a las 24 h de incubación en células de HuH-7 de hepatoma humano (Mansoor, Ramalho, Mulhovo, Rodrigues, & Ferreir, 2009). No existen reportes asociados a la actividad citotóxica de T. alba, y V. patens por lo que este estudio sería el primer reporte acerca de su actividad citotóxica con un valor de IC50 dentro de los valores establecidos por el NCI.
CONCLUSIONES
Los extractos hidroalcohólicos de las plantas seleccionadas de acuerdo a su uso tradicional, a la composición química y a la actividad biológica: C. pulverulentus, S. edule, T. alba y V. patens, poseen potencial antitumoral por lo que se recomienda la caracterización química para determinar el principio activo y la evaluación de la capacidad antitumoral in vivo.











 nueva página del texto (beta)
nueva página del texto (beta)


