Introducción
Las plantaciones del género Pinus spp en Brasil ocupan 1,6 millones de hectáreas, los estados de Santa Catarina y Paraná son los mayores productores del país, juntos, suman 76% de toda la producción nacional (Indústria Brasileira de Árvores [IBÁ], 2020). Las especies de Pinus como Pinus ellioti, P. tadea, P. caribaea, P. oocarpa, P. patula, P. maximinoi, P. greggii, P. tecunumanii, P. kesiya, son las más cultivadas en el territorio brasileño (Shimizu y Sebbenn, 2008). Las utilidades de estas especies se extienden en la producción de celulosa de fibras largas, tableros aglomerados (Carvalho et al., 2014b), carbón vegetal y briquetas (Mendoza et al., 2012; Oliveira et al., 2017), madera aserrada (Murara Junior et al., 2013), resina (Lopes, 2008) y corteza como sustrato para la producción de plantas u ornamentación de jardines (Neto et al., 2005; Suguino et al., 2011).
Los taninos producidos de forma natural a partir de metabolitos secundarios en vegetales pueden ser encontrados en corteza, hojas, duramen y raíces de los árboles, estos se pueden dividir en dos grandes grupos, los hidrolizables y los condensables (Volz y Clause, 2001; Zhou y Du, 2019). Estos compuestos son muy utilizados en la industria del cuero, en la producción de colorantes, polímeros, fungicidas y bebidas, en la detección de proteínas y alcaloides en laboratorio, en la industria farmacéutica, en el tratamiento de agua y como adhesivos para la producción de tableros aglomerados de madera (Gonçalves et al., 2008; Gonçalves et al., 2017; Kim et al., 2007; Monteiro et al., 2005; Mori et al., 2003; Rahman et al., 2014; Vieira et al., 2014).
Las substancias fenólicas en las plantas pueden alcanzar 40% de masa seca de la corteza en determinadas especies arbóreas, existen especies que poseen potencial para la extracción de compuestos tánicos a escala industrial (Trugilho et al. 2003; Carvalho et al., 2014a). Cada especie vegetal se comporta de modo diferente en relación con el rendimiento y calidad de los taninos, los cuales están asociados a la forma de extracción, esta puede ser con agua (Trugilho et al., 1997), sulfito de sodio (Carvalho et al., 2014a; Tahir et al., 2002; Vieira et al., 2011), bisulfito de sodio, sulfato y carbonato de sodio (Santiago et al., 2019), metabisulfito e hidróxido de sodio (Vázquez et al., 2001). Este proceso puede ser realizado aplicando diferentes temperaturas de acuerdo con lo indicado en diferentes investigaciones desarrolladas por Vieira et al. (2014), Rodrigues et al. (2015), Nath et al. (2017), Sartori et al. (2018) y Medeiros et al. (2018). Existen pocos estudios relacionados con la extracción de taninos a partir de la corteza de pino mediante termomodificación.
Objetivos
Teniendo en cuenta lo expuesto anteriormente, el objetivo de este estudio estuvo fue basado en evaluar la extracción de taninos de la corteza de pino mediante tratamiento térmico, para determinar el contenido y calidad de taninos extraídos en diferentes condiciones de temperatura.
Materiales y métodos
Materiales y preparación de la materia prima
Una mezcla de corteza de Pinus spp fue proporcionada por una empresa localizada en la región central del Estado de Paraná, Brasil, la cual utiliza la corteza como sustrato (in situ) comercial para la producción de plántulas de orquídeas. Las cortezas fueron fragmentadas para su dimensión comercial en tamaños de 2 cm × 2 cm. El delineamiento experimental para la extracción de taninos está representado en la tabla 1, en ella se muestran los métodos aplicados para la termomodificación de la corteza y para la evaluación de los compuestos tánicos.
Tabla 1 Tratamientos térmicos aplicados a los residuos de corteza de Pinus spp.
| Tratamiento | Condiciones térmicas de las cortezas |
| I | Corteza sin tratamiento térmico (testigo) |
| II | Corteza a 60 °C en proceso seco durante 50h |
| III | Corteza a 120 °C a vapor durante 10 h |
| IV | Corteza adherida al tronco y sometida a 120 °C a vapor durante 10 h |
Extracción de taninos
Las cortezas inicialmente fueron secadas al aire libre y posteriormente fragmentadas en molino de martillo para obtener partículas menores que permitieran la extracción de taninos. Estas partículas fueron trituradas en molino Willey con tamices de 0,8 mm y el material resultante fue homogeneizado y separado por tamices con dimensiones de abertura entre 0,42 mm y 0,25 mm (mallas granulométricas 40 y 60), Luego, las partículas fueron almacenadas en ambiente con condiciones controladas de 25 °C de temperatura y 65% de humedad relativa.
Para potencializar la extracción de taninos de la corteza de pino se utilizó agua destilada y sales de sulfito de sodio (Na2SO3) y carbonato de sodio (Na2CO3), ambas en una proporción de 5% en relación con la masa seca de la corteza. El proceso de extracción fue realizado en un equipo de reflujo con un matraz volumétrico y un condensador por dos horas, con una relación corteza/licor de 1:15 (p/v), 10 g de corteza y 5% de sal en 150 mL de agua destilada. Luego fue usado un filtro de vidrio sinterizado con placa porosa número 2 sobre un recipiente vacío y se determinaron los contenidos de taninos y otras sustancias extraíbles, a partir del número de Stiasny (NS) y la reactividad ultravioleta (Vieira et al., 2011; Almeida, 2010). Del extracto filtrado, se tomó una muestra de 50 mL para determinar la cantidad de polifenoles reactivos del licor mediante el índice de Stiasny, a partir de la adición de 4 mL de formaldehido (37%) y 1 mL de ácido clorhídrico (HCl). Esta solución fue mantenida en una manta térmica sobre reflujo durante 30 min.
La absorción del extracto (reactividad) se realizó empleando un espectrofotómetro UV (Bel, UV-M51) de 280 nm, se usó 1 mL del material filtrado, diluido en 200 mL de agua destilada; esta solución se sometió a las lecturas de tamaño de ondas determinadas para el ensayo. La reactividad de los taninos fue calculada mediante la relación entre las diferencias de la absorción del extracto antes y después de la reacción de “Stiasny” (Ec. 1)
donde:
RUV: reactividad ultravioleta
A a : absorción antes de la adición de formaldehído y ácido clorhídrico
A d : absorción después de la adición de formaldehído y ácido clorhídrico
El contenido de extractivos totales fue determinado a partir de la diferencia de masa contenida en 25 mL del extracto, después de ser secado en estufa a 103 ºC ± 2 ºC y obtener una masa constante. El porcentaje de taninos fue obtenido mediante el producto del número de Stiasny y por el contenido de extractivos totales. A partir de la diferencia entre el contenido de extractivos y de taninos se puede estimar el porciento de otras sustancias extraíbles.
Propiedades tecnológicas del tanino como adhesivo
El tratamiento con mayor rendimiento de tanino fue sometido a dos procesos subsecuentes de extracción en autoclave vertical (con capacidad de 75 L) durante dos horas. Posteriormente, el extracto fue filtrado con filtro de vidrio sintetizado con placa porosa número 2 y llevado para secado previo en estufa a temperatura de 60 °C, luego en secado completo en estufa a 103 °C ± 3 °C durante ocho horas.
El proceso descrito anteriormente fue realizado para obtener el material seco y macerado en un recipiente de cerámica. El material triturado fue tamizado en una malla de 53 µm de abertura (malla granulométrica 270) para obtener el tanino puro en polvo. Luego, fue preparada una solución de 45% de extractos tánicos homogeneizadas con agua destilada para subsecuentes análisis de las propiedades tecnológicas (pH, densidad, viscosidad, tiempo de gel, contenido de sólidos) con el propósito de utilizarlo como adhesivos para la manufactura de tableros aglomerados de madera y otros materiales lignoce-lulósicos.
Para el análisis de pH de las soluciones, se usó un potenciómetro pH (Alfakit, AT 355), la medición fue después de 3 min de contacto con el adhesivo en ambiente climatizado a 25 °C. La densidad fue obtenida utilizando un recipiente de volumen conocido, mediante la relación entre la masa del adhesivo y el volumen del recipiente conocido.
Por su parte, la viscosidad fue determinada mediante un viscosímetro rotativo digital de mesa (Marte, MVD-8), adecuado a 2-3-4 y con rotación de 60 min-1 en 150 mL de la solución. El tiempo de gel fue determinado a partir de 10 g de la solución de extractos tánicos con la adición de 20% de formaldehído con base en el contenido de sólidos, en baño maría a 90 °C hasta el cambio de fase. Este proceso corresponde con la polimerización o gel time del adhesivo durante un tiempo determinado. También fue evaluado el contenido de sólidos, este se realizó mediante el secado de una muestra de 1,0 g del adhesivo en estufa en condiciones de temperatura de 102 °C ± 3 °C durante tres horas. El porcentaje de solidos fue calculado a partir de la relación de la masa seca final por la masa húmeda inicial. En este proceso fueron realizadas tres repeticiones y evaluadas para cada propiedad indicada anteriormente.
Estadística aplicada
Las propiedades tecnológicas de los extractos tánicos fueron evaluadas mediante un delineamiento casualizado con tres repeticiones. La normalidad fue evaluada de acuerdo con la prueba de Kolmorogov - Sminov y la homogeneidad de varianza de los datos por la de Kruskal-Wallis. Los valores medios fueron evaluados mediante la prueba de Dunnet (p < 0,05).
Resultados y discusión
Caracterización química de la corteza de pino
Los valores medios obtenidos para cada uno de los ensayos desarrollados en la investigación están representados en la tabla 2. De manera general, la adición de sales proporcionó los mejores resultados en relación con el contenido de taninos extraídos de la corteza de pino, valores entre 14,06% y 20,55% para Na2SO3, y valores entre 17,60% y 20,56% para el Na2CO3, mientras que para la extracción con agua destilada se obtuvieron valores entre 4,04% y 4,97%.
Tabla 2 Valores medios del contenido de extractivos, taninos y no taninos, número de Stiasny y reactividad por el método ultravioleta.
| Método de Extracción | Contenido de extractivos (%) | Número de Stiasny (NS) | Tanino (%) | No tanino (%) | Reactividad UV (%) | |
| Corteza sin tratamiento térmico (testigo) |
|
|
|
|
|
|
| Corteza a 60ºC proceso seco por 50 h |
|
|
|
|
|
|
| Corteza a 120 ºC a vapor por 10 h |
|
|
|
|
|
|
| Corteza adherida al tronco a 120 ºC a vapor por 10 h |
|
|
|
|
|
|
Se observó que los contenidos de taninos con la adición de carbonato de sodio fueron superiores a los valores obtenidos con la adición de sulfito de sodio. Resultados publicados por Santiago et al. (2019) en la extracción de taninos a partir de corteza de eucalipto demuestran que el Na2CO3 presenta una mayor eficiencia en el proceso de extracción en comparación con el sulfato de sodio.
Estudios realizados por Ferreira et al. (2009) y Vieira et al. (2014), en cuanto a los contenidos de extractivos en corteza de Pinus oocarpa mediante el uso de sulfito de sodio, obtuvieron valores medios entre 30,1% y 32,49%, estos valores fueron superiores a los encontrados en este estudio (20,55%), lo cual puede estar dado por el posible efecto de los procesos térmicos utilizados antes de la extracción.
Los tratamientos térmicos con menores contenidos de extractivos fueron los más eficientes en la obtención de los extractos tánicos. En comparación con el testigo, el tratamiento térmico a 60 °C con agua destilada presentó mayor eficiencia en el contenido de extractos tánicos, dado que estos últimos presentaron valores entre 4,04% y 4,27%.
Los resultados muestran que, a partir de la adición de sales, se puede favorecer la solubilidad de los polifenoles en comparación con las extracciones obtenidas a partir de agua. Con excepción del tratamiento IV, los valores mayores de número de Stiasny (NS) en los diferentes tratamientos térmicos fueron obtenidos con la adición de carbonato de sodio. Valores similares fueron encontrados por Vieira et al. (2014) en extractos de corteza de Pinus oocarpa con la adición de sulfito de sodio a 5%.
Los valores NS encontrados en los diferentes métodos de extracción, con excepción del tratamiento térmico a 120 °C, fueron inferiores a los encontrados por Vásquez et al. (2001), cuyos valores medios obtenidos a partir de diferentes concentraciones de hidróxido de sodio en corteza de Pinus pinaster variaron entre 81,2% y 96,5%.
De modo general, los tratamientos térmicos favorecen la obtención de valores menores de NS, con excepción del tratamiento térmico IV. Esto demuestra que la eficiencia de temperaturas de 120 °C en la obtención de taninos para la corteza adherida al tronco es baja. El tratamiento donde fue aplicada temperatura de 120 °C directamente sobre las cortezas presentó menores valores de NS y fue el más eficiente en la remoción de extractos tánicos. Estas condiciones permiten que sea utilizado para la producción de plantas ornamentales ya que el tanino, por ser un metabolito secundario de carácter fenólico (Lima et al., 2007), puede actuar como inhibidor del crecimiento radicular debido a los efectos alelopáticos (Fan et al., 2003).
La adición de carbonato de sodio y sulfito de sodio solubilizó mayores cantidades de extractivos. Además, los mayores contenidos de extractivos de NS y taninos se encontraron en las extracciones con carbonato de sodio, con excepción del tratamiento IV. Sin embargo, se encontraron mayores cantidades de sustancias extraíbles (azúcares solubles), las cuales pueden influir negativamente en la aplicación de adhesivo (Marra, 1992).
Los resultados obtenidos, en relación con el tratamiento testigo, muestran diferencias respecto a los contenidos de taninos encontrados. Por ejemplo, se obtuvo 10,77% de taninos extraídos con 5% de sulfito de sodio; estos valores son inferiores a los encontrados por Vieira et al. (2014) y Ferreira et al. (2009) con medias de 22,5% y 31,6%, respectivamente, utilizando también 5% de sulfito de sodio en corteza de Pinus oocarpa. La diferencia entre los valores obtenidos en esta investigación y los publicados por los autores citados puede estar relacionada con la heterogeneidad de la mezcla del material estudiado (residuo).
Al analizar el contenido de sustancias extraíbles (no taninos) de la muestra testigo con la adición de 5% sulfito de sodio, el valor obtenido (4,74%) fue superior al encontrado en las mismas condiciones por Vieira et al. (2014) en corteza de Pinus oocarpa (2,9%). Estos resultados fueron similares a los obtenidos por Ferreira et al. (2009), quienes encontraron valores promedio de 4,77% en cuatro variedades de la especie Pinus caribaea.
Los resultados obtenidos en relación con la reactividad de los polifenoles por el método UV muestran valores inferiores de reactividad en aquellos tratamientos donde fue aplicada temperatura de 60 ºC y 120 °C (solamente agua destilada en la extracción). En los demás métodos fue evidente una elevada reactividad de los polifenoles obtenidos con la adición de carbonato de sodio y sulfito de sodio.
Los valores de la reactividad UV de los compuestos tánicos con la adición de 5% de sulfito de sodio, fueron semejantes a los obtenidos por Carvalho et al. (2014b), quienes encontraron para Pinus caribaea var. bahamensis valores de reactividad de 95,4%. Por su parte, Vieira et al. (2014) en corteza de Pinus oocarpa encontraron valores medios de 99,53%, los cuales son próximos a los obtenidos en este trabajo (entre 91,64% y 96,83%). Teniendo en cuenta estos resultados, se puede inferir que para los tratamientos donde se aplicó vapor a 120 °C directamente sobre las cortezas adheridas al tronco, se pueden obtener los mayores rendimientos en todos los parámetros.
Evaluación de las propiedades tecnológicas de los adhesivos
Los resultados muestran que el menor porcentaje de contenido de sólido fue encontrado con la extracción de taninos a partir de carbonato de sodio (19,16%), los cuales tienen diferencias estadísticas en relación con los demás adhesivos. Los valores de contenido de sólidos del adhesivo a base de tanino de la corteza de Pinus spp. extraído con sulfito de sodio (43,53%) no mostró diferencias estadísticas para los valores obtenidos en relación con el adhesivo comercial de Acacia mearnsii (39,98%) (Tabla 3). Esto indica una buena solubilidad de los materiales evaluados. De acuerdo con Almeida (2010), los porcentajes ideales de contenidos de sólidos en adhesivos a base de tanino deben variar entre 44% y 55%. Por su parte, Vieira et al. (2014) obtuvieron valores inferiores del contenido de sólidos en adhesivos al substituir parte de las resinas sintéticas por extracto tánico de Pinus oocarpa, indicando interferencia del tanino en el contenido de sólidos de los adhesivos.
Tabla 3 Valores medios del contenido de sólidos, densidad y tiempo de formación de gel de los adhesivos.
| Adhesivos / Dilución en agua destilada | Contenido de sólidos (%) | Densidad (g/cm3) | Tiempo de gel (min) |
| Acacia mearnsii comercial a 45% | 39,98 b* | 9,09 b | 6’18” b |
| Mezcla de corteza de pino / Na2CO3 a 23% | 19,16 a | 8,74 b | 0’46” a |
| Mezcla de corteza de pino / Na2SO3 a 45% | 43,53 b | 7,56 a | 1’05” a |
*Promedios en cada columna con la misma letra, no difieren estadísticamente por la prueba de Dunnet (p ≥ 0,05).
El adhesivo de la corteza de pino con 5% de sulfito de sodio y formulación de 45% de tanino presentó menor valor de densidad (7,56 g/cm3), mientras que el adhesivo comercial no se diferenció estadísticamente del adhesivo obtenido (9,09 g/cm3). En cuanto al tiempo de formación de gel, el tanino comercial se diferenció estadísticamente de los adhesivos obtenidos en este estudio, presentando valor medio de 6 min y 18 s. Ambos adhesivos obtenidos a partir de la corteza de Pinus sp. presentaron valores de formación de gel próximos a 1 min. Es importante tener en cuenta esos criterios en la fase de colado y en el proceso productivo de tableros y aglomerados, ya que pueden determinar el tiempo operacional de la etapa productiva a escala industrial.
En estudios realizados por Carvalho et al. (2014b) se evalúa el tiempo de formación de gel obtenido de la corteza de Pinus caribaea var. bahamensis, estos autores obtuvieron buenos resultados para un tiempo de 1 min y 10 s, valores próximos a los encontrados en este estudio. Además, el tiempo de gel para los adhesivos de la corteza de Pinus caribaea también presentó valores inferiores en comparación con el tiempo de gel de adhesivo comercial. Teniendo en cuenta la evaluación del incremento de tanino natural en adhesivos sintéticos, es posible inferir que los extractos tánicos, obtenidos de corteza de Pinus spp o de acacia negra pueden reducir el tiempo de gel de los adhesivos.
En la figura 1 se presentan los valores medios de pH y viscosidad de los adhesivos, con significancia por el análisis de variancia (p < 0,05). La adición de carbonato de sodio en el proceso de extracción del tanino en autoclave elevó el valor de pH del adhesivo, lo cual representa una diferencia estadística en los valores obtenidos en relación con el adhesivo comercial.
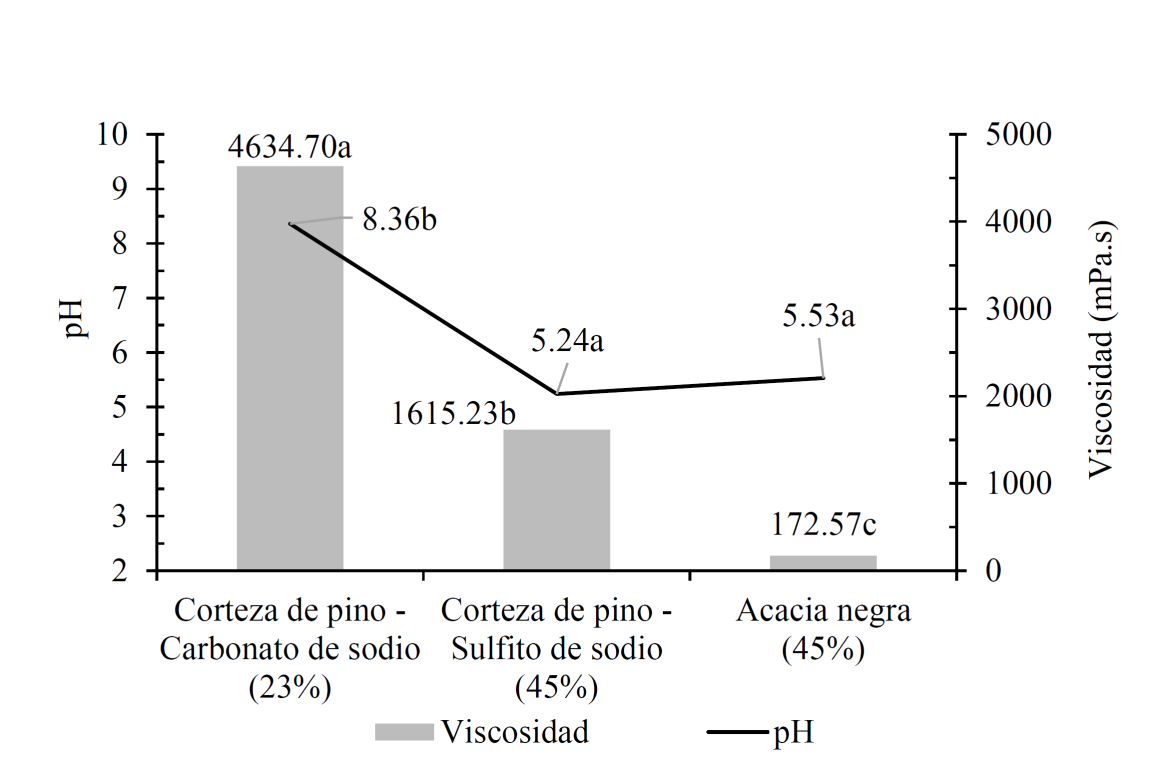
*Promedios con la misma letra para las propiedades distintas, no difieren estadísticamente por la prueba de Dunnet
Figura 1 Valores medios de pH y viscosidad de los adhesivos.
Se considera que el tanino es naturalmente ácido, esto permite inferir que la extracción con carbonato de sodio conduce a la producción de adhesivos con menores índices de pureza, esto puede retardar el proceso de curado del adhesivo durante la manufactura de tableros aglomerados debido a que la acidez interfiere en la reacción de condensación del tanino con el formaldehido (Vieira et al., 2014), además de interferir en la viscosidad del adhesivo (Vásquez et al., 2009; Carvalho et al., 2014b).
Los valores de pH del adhesivo obtenidos con sulfito de sodio no presentaron diferencias estadísticas en relación con el tanino comercial, presentando carácter ácido (pH 5,24). Esta condición puede explicar la menor viscosidad del adhesivo en comparación con el adhesivo de carácter básico (pH 8,36) obtenido con el carbonato de sodio.
Los valores mayores de viscosidad fueron encontrados en los adhesivos obtenidos con el carbonato de sodio (4634,7 mPa·s). De acuerdo con Gonçalves y Lelis (2009) y con Brito (1995), la viscosidad con valores superiores a 1500 mPa·s tiende a disminuir la eficiencia del proceso de colado de tableros de madera, lo cual afecta la capacidad de distribución, humedad y adhesión del adhesivo, además de la funcionalidad tecnológica de los tableros. Por lo tanto, ambos adhesivos presentan valores de viscosidad no deseables. Es importante destacar que las unidades flavonoides que componen las moléculas de taninos son diferentes para aquellos provenientes de acacia negra y de corteza de Pinus oocarpa (Vieira et al., 2014), como fue observado en los valores de viscosidad y pH.
Estudios realizados por Carvalho et al. (2014b) evalúan el incremento de extractos tánicos de Pinus caribaea var. bahamensis en adhesivos de Acacia mearnsii con tres niveles de porcentaje (90:10; 80:20; 75:25), se puede observar una tendencia en el aumento de la viscosidad a partir del incremento del tanino obtenido de Pinus sp. (180,1 mPa·s; 190,2 mPa·s y 196,8 mPa·s), a pesar de no presentar diferencias estadísticamente significativas.
A partir de estudios realizados por diferentes investigadores relacionados con el tema, se puede inferir que los valores de viscosidad elevada en extractos tánicos conducen a una menor fluidez en los adhesivos naturales en comparación con los sintéticos. Esto se debe a los fenoles de las moléculas de tanino que presentan alto peso molecular y fuerte atracción electrostática (puentes de hidrógeno) entre los polifenoles y sus interacciones con los azúcares solubles contenidos en el extracto, lo cual forma agregados moleculares que no se rompen con la simple dilución en agua (Pizzi y Mittal, 1994).
Conclusiones
La aplicación de vapor durante 10 h a 120 °C, directamente en los troncos con corteza, presentó una baja eficiencia en la remoción de extractos tánicos, siendo diferente la eficiencia para las cortezas fragmentadas y sometidas a 120 °C a vapor durante 10 h.
La adición de 5% de carbonato de sodio proporcionó mayores rendimientos en contenidos de extractivos, taninos y sustancias extraíbles (no taninos). Sin embargo, el extracto acuoso fue el que presentó carácter alcalino, mayor viscosidad y menor tiempo de formación de gel.
La adición de 5% de sulfito de sodio mostró eficiencia en la remoción de extractivos tánicos, además de proporcionar un adhesivo con menor viscosidad, carácter ácido y mayor contenido de sólido.











 nueva página del texto (beta)
nueva página del texto (beta)



