Introduction
Le bois, contrairement à la plupart des autres matériaux, est une ressource renouvelable disponible en vaste quantité (Walinder, 2006). La couleur du bois est particulièrement intéressante pour la fabrication de matériaux orientés vers les marchés où les clients exigent du bois avec des caractéristiques de perception esthétique bien définies.
Marchal et Mothe (1994) ont établi une hiérarchie des critères de choix exprimés par des consommateurs et des professionnels du bois français (bois de chêne): la clarté et l'homogénéité de la teinte se classent juste après la nodosité et l'orientation du débit. A part cet aspect d'apparence, la couleur a été mise en relation avec la stabilité dimensionnelle et les propriétés mécaniques du matériau (Bekhta et Niemz, 2003), en même temps qu'elle reflète les changements physico-chimiques que le bois a suivis lors d'un procédé. La couleur est aussi liée à la capacité du bois à résister l'attaque fongique (Gierlinger et al., 2004). Les substances phénoliques du bois ont été mises en relation avec les tonalités rougeâtre des bois et l'activation/inactivation des surfaces des planchettes, ce qui est important pour les fabricants de placage et contreplaqué (Sandoval, 2008).
McGinnes et Rosen (1984); Kubinsky et Ifju (1973), ont étudié l'influence de la température sur la couleur de la sève du bois et ont conclu que les extractibles sont des pigments très important dans les fluides (sève du bois) qui suivent des altérations au cours d'un traitement thermique.
Thompson, Kozak et Evans, (2005) ont étudié la modification thermique de la couleur sur l'aulne rouge (Alnus rubra Bong), et ont émis l'hypothèse que la couleur de cette espèce thermiquement modifiée dépend de l´intensité des réactions qu'engendre les chromophores orange/rouge sur le bois, qui permettent le noircissement thermique du bois. Okino et al., (2015) ont étudié la relation entre la couleur et la résistance à la pourriture du bois de feuillus, car les extractibles peuvent protéger le bois de toute dégradation biologique. L'influence des groupes phénoliques sur la résistance à la dégradation du bois a aussi été démontrée pour le duramen du pin (Harju et al., 2003). Aydin et Colakoglu (2005) ont signalé que certains changements de la couleur naturelle du bois surviennent à la suite de réactions chimiques (extractibles phénoliques) et de la présence d'enzymes dans le bois. Par conséquent, l'inactivation des enzymes pourrait être une solution contre la discoloration du bois.
Le séchage du bois de feuillus pose plus de problèmes au niveau des changements de couleur par rapport au bois résineux. Les espèces de bois de feuillus sont plus sensibles à la discoloration (Alexiadis, Cohen, Kozak et Avramidis, 2007). De plus, en ce qui concerne les bois de feuillus de grande valeur sur le marché européen, certaines caractéristiques d'apparence telles que la couleur et son l'homogénéité sont des critères très importants (Sandoval-Torres, Marc, Jomaa et Puiggali, 2010). Dans le Tableau 1, nous résumons les principales causes de discoloration dans le bois.
La chimie du bois du chêne
La dégradation ou altération du bois est un sujet complexe car il s'agit d'un mélange de trois polymères naturels (cellulose, hémicellulose et lignine) et des extractibles existants dans le bois (White et Dietengerger, 2001). La céllulose est un polymère linéaire d'unités de glucose cyclique de configuration β (le groupement hydroxyle fixé au premier atome de carbone, à l'endroit où le cycle se ferme, est situé au dessus du plan du cycle), reliées par des liaisons (1-4). Dans le bois, le degré de polymérisation de la cellulose (poids moléculaire de la cellulose / poids moléculaire du glucose) est compris entre 5000 et 10000. Un degré de polymérisation de 10000 correspond à une chaîne d'une longueur de 5 µm.
Les hémicelluloses sont, comme la cellulose, des polysaccharides (polymères de sucres). Ces deux constituants forment la fraction désignée sous le nom de holocellulose. Les hémicelluloses sont construites à partir de plusieurs unités différentes de sucres. Leurs chaînes sont plus courtes que celle de la cellulose et elles portent des ramifications. On distingue les pentosanes et les hexosanes. La lignine est un polymère tridimensionnel amorphe de nature phénolique. Elle diffère d'une essence à l'autre, notamment de par sa teneur en unités guaïacyles et syringyles. Les feuillus contiennent environ 25% de lignine et les résineux 30%. Enfin, le terme d'extractibles recouvre de nombreux composés qui peuvent être extraits du bois par des solvants polaires ou apolaires. La teneur et la composition des extractibles varient fortement d'une essence à l'autre, les essences tropicales en contenant généralement plus que les bois issus des zones tempérées (Trouy-Triboulot et Triboulot, 2012).
La teneur et la composition des extractibles varient fortement d'une essence à l'autre, les essences tropicales en contenant généralement plus que les bois issus des zones tempérées. Parmi les extractibles, la vescalagine et la castalagine représente plus de 50% des ellagitanins dans le bois de chêne. En fait, près de 10% du duramen du bois de chêne (sec) européen (Quercus robur L. et Q. petraea (Matt.) Liebl.) contient des ellagitanins extractibles constitués d'acide ester hexahydroxydiphe et du glucose. Les ellagitanins sont des molécules solubles à l'eau, et fortement oxydables et astringentes. Toutes les propriétés mentionnées ont des effets antioxydants et anti-radicaux sur ces produits, ce qui explique certaines substitutions nucléophiles, qui jouent un rôle dans la discoloration du bois.
La formation des chromophores est à l'origine des changements de la couleur des matériaux lignocellulosiques, puisque la couleur est directement affectée par ces groupes (Hon et Shiraishi, 2000). La formation des substances colorées à partir d'un composé phénolique oxydé avec de l'air et la formation des substances de couleurs foncées produits de l'hydrolyse des hémicelluloses ont été généralement considérées comme étant les causes principales de la décoloration (Charrier, Haluk et Janin, 1992 ; Charrier, Haluk et Metche, 1995; McMillen 1975). Lorsque les substances chromophores sont hydrosolubles, ces matériaux s'accumulent à la surface et altèrent la coloration des bois. La formation des groupes chromophores des pulpes ligno-cellulosiques requiert la présence d'une structure d'hydrate de carbone (Beyer, Koch et Fischer, 2006).
Le traitement par la chaleur, que ce soit dans des conditions de sécheresse ou d'humidité, provoque une altération dans la couleur du bois. Cependant, peu d'articles ont relevé ces informations dans des conditions de séchage sous vide par contact.
Materiel et méthodes
À partir d'une grume de chêne d'environ 100 ans, nous avons obtenu des morceaux de bois frais. Pour chaque expérience de séchage des disques de bois frais ont été utilisés (7,0 cm de diamètre, 2,5 cm d'épaisseur). Les échantillons de bois sont des disques de bois de coeur de chêne (Quercus pedoncularis), l'aubier a été écarté dans cette étude, la concentration en composants polyphénoliques étant plus importante dans le cœur de chêne.
Tous les disques ont été protégés de la lumière, emballés dans un film plastique et gardés au congélateur afin d'éviter les dégradations enzymatiques et les processus d'oxydation. Les échantillons de bois seront stockés entre -20 °C à -24 °C pendant un à deux mois. Trois niveaux de températures (46 °C, 61 °C et 70 °C) et un niveau de pression (6 kPa - 10 kPa ; 60 mBar-100 mBar) ont été associés pour le séchage sous vide.
Equipement expérimental
Le dispositif expérimental (Fig. 1) est une chambre à vide où la pression est réglée entre deux valeurs : Pmin (6 kPa ; 60 mBar) et Pmax (10 kPa ; 100 mBar). Le chauffage provient d'une résistance noyée dans une plaque d'aluminium afin d'homogénéiser la distribution de la chaleur dans la zone de contact. Les capteurs de température ont été placés à trois emplacements suivant l'épaisseur du disque de bois. Un de ces capteurs a été placé à 3 mm à proximité de la plaque, un autre au centre du disque et le troisième à 3 mm en dessous de la surface d'évaporation. Pour chaque expérience, l'historique des trois températures est enregistré.

Figure 1 Séchoir sous Vide: 1) balance de précision Ohaus Navigator avec interface RS-232; 2) capteur de pression Edwards, et contrôleur de pression Edwards; 3) Thermocouples, résistance, plaque chauffante et porte échantillon; 4) contrôleur de température WEST 6100.
La régulation de la pression permet de maintenir celle-ci entre deux valeurs de consigne (P-, et P+). L'évolution de la pression autour de ces deux points fait apparaître deux régimes, l'un passif et l'autre actif. Un régime actif pendant lequel la pompe à vide est en fonctionnement (chute de pression) et pendant lequel l'évaporation en surface est étroitement lié au débit de la pompe. Cet effet de pompage est visible sur l'évolution de la masse de l'échantillon où l'on observe une diminution brusque chaque fois que la pompe à vide est en fonctionnement.
Dans un souci de maîtriser les conditions d'expérimentation, nous avons mis en place ce dispositif expérimental. Dans le domaine industriel, le bois est empilé entre deux plaques d'aluminium à l'intérieur desquelles circule de l'eau chaude. Ces plaques sont reliées par des flexibles au circuit principal. La chaleur se transmet donc au bois par contact direct, tandis que le vide est maintenu durant tout le cycle de séchage.
La particularité de ce travail est que nous exposons une surface du bois à la plaque chauffante et l'autre à l'atmosphère (vide), donc nous pouvons ainsi étudier deux effets de séchage sur un échantillon. Les surfaces du bois exposés à la plaque chauffante sont dans la direction radiale. Cette orientation est normale dans l'industrie du bois.
Mesure de la couleur du bois
La mesure objective de la couleur d'un objet consiste à déterminer d'une part, la valeur de la luminosité L* (variant de 0 à 100), en utilisant la réflectance globale de cet objet en comparaison avec celle d'un étalon blanc de référence, et d'autre part, les coordonnés chromatiques a (+ ou -, sur un axe rouge-vert) et b (+ ou -, sur un axe bleu-jaune). Ces trois valeurs permettent de repérer le point de couleur correspondant à l'objet mesuré dans le système CIELAB 1976. A partir de ces trois coordonnées sont également calculés un angle de teinte h* (angle de couleur) par rapport au cercle chromatique, et une saturation C* de cette teinte (Janin et al., 2001; Forintek, 2006), nous parlons alors de système CIELCh.
Pour l'échantillonnage de sciure de bois de chaque disque de bois, et afin d'obtenir un matériau le plus homogène possible, nous avons brossé la surface du disque très doucement pour éviter l'échauffement du matériau. Nous avons brossé la surface exposée à l'air de l'enceinte et les surfaces qui ont été chauffés directement par la plaque. De chaque surface, nous avons raboté le bois jusqu'à 5 mm de profondeur. Pour chaque échantillon on obtient environ 5 g de poudre lesquels sont gardés dans un flacon bien fermé, protégé de la lumière et placé au congélateur jusqu'aux analyses.
À partir des poudres tamisées à 100 μm (Fig. 2) et à l'aide d'un colorimètre, les paramètres L*, a* et b* des poudres ont été enregistrés (4-7 répétitions par échantillon). Dans le système CIELCh, C* est zéro au centre de cet espace, la valeur augmente quand C* se déplace du centre vers l'extérieur. L'angle de teinte h* est exprimé en degrés: 0° exprime +a (rouge), 90° exprime b* (jaune), 180° -a*(vert), et 270° -b*(bleu). A partir des paramètres L*, a* et b*, on peut donc calculer C*.
Après chaque expérience, nous avons mesuré les paramètres des couleurs selon le système Cielab (Communication Minolta), en utilisant un Colorimètre Minolta avec un illuminant C, D65.
Les spectres infrarouges (ftir)
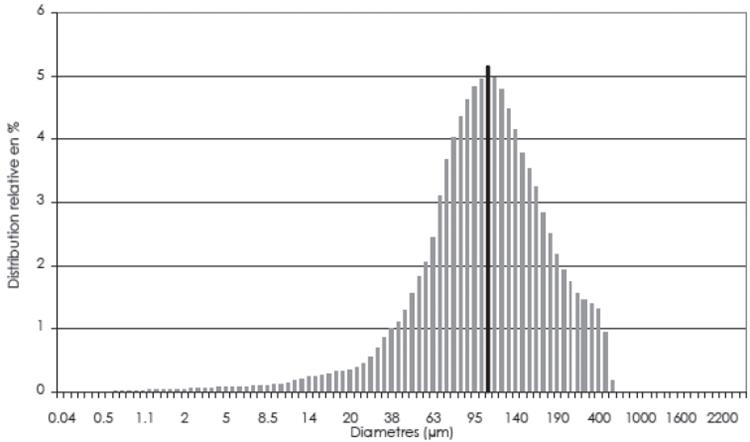
Les Spectres Infrarouge à Transformée de Fourier des échantillons de bois ont été obtenus avec un spectromètre Bruker EQUINOX 55 (Bruker Optics Inc, Ettlingen, Allemagne), sur la gamme 400 cm-1-4000 cm-1 et une résolution de 4 cm-1, les spectres sont enregistrés selon le mode de réflexion (R%). Dans un souci d'homogénéisation des échantillons de poudre de bois, nous avons passé les sciures du bois destinées à l'analyse FT-IR dans un tamis à 100 micromètres. Une analyse granulométrique par diffraction laser a été pratiquée en utilisant l'éthanol comme liquide porteur. La distribution relative des particules est présentée dans la (Fig. 2), celles-ci possèdent un diamètre moyen de 103 μm. Trente scans ont été accumulés avant la Transformation Fourier. D'après (Pandey et Pitman, 2003), une ligne de base a été utilisée pour le calcul des aires correspondant au groupe carbonyle (1741 cm-1), le dit point d'intensité correspondant à la bande de vibration de valence de la liaison C=O. Nous avons utilisé cette méthode proposée par (Pandey et Pitman, 2003).
Le dosage du potentiel antioxydant
Pour doser le potentiel antioxydant il est nécessaire d'obtenir un extrait de ces poudres. Pour ceci un solvant adéquat est utilisé. Dans ce travail il s'agit d'un mélange éthanol/eau (1/1; v/v). La mesure du potentiel antioxydant et le suivi des processus d'oxydation sont abordés ici globalement en déterminant l'aptitude de l'extrait à piéger des radicaux modèles, et donc à ralentir ou inhiber les réactions d'oxydations radicalaires. Ceci implique la création de radicaux. Dans la méthode AAEAC (Acide Ascorbic Equivalent Antioxidant Capacity), l'activité antioxydante totale d'une molécule est déduite de sa capacité à inhiber le radical ABTS•+, obtenu à partir de l'ABTS(sel d'ammonium de l'acide 2,2-azinobis-(3-éthylbenzothiazoline-6-sulfonique)) comparativement à un antioxydant de référence : l'acide ascorbique (Vitamine C). Le radical ABTS•+, en contact avec un donneur de H• conduit à l'ABTS+ et à la décoloration à 734 nm de la solution.
Lors de chaque expérience de séchage, de la poudre de bois homogène est obtenue par tamisage des sciures à la cuillère à thé (0.06 g bois sec). Chaque échantillon de poudre est mis en suspension dans 50 ml d'un solvant (eau-éthanol, 1/1) et placé dans un sonicateur pendant 15 min. Le surnageant est ensuite récupéré, il va constituer l'extrait qui sera analysé. L'action du sonicateur améliore l'extraction des composés d'intérêt, et a l'avantage d'être plus simple et rapide que l'utilisation du soxhlet. Les résultats obtenus ont montrés que cette technique d'extraction était cependant discriminante.
La densité optique de l'ABTS•+ en solution aqueuse est fixée initialement à 0.70 ± 0.02. À 1960 μl d'ABTS•+ sont ajouté 40 μl d'extrait (dilué 5 fois). La solution est ensuite agitée (vortex) pendant 30s puis la mesure de la densité optique (DO) à 734 nm est effectuée à 1 min et 15 min après avoir ajouté l'extrait. Huit déterminations sont effectuées pour chaque échantillon, chaque échantillon appartenant à un procédé de séchage. Plus la densité optique diminue plus le potentiel antioxydant est important.
Nous avons choisit de présenter les résultats du potentiel après 15 minutes de réaction, car ce temps correspond à la décoloration maximale des radicaux libres crées (ABTS+•). Ce temps a été déterminé par une étude cinétique de la réaction de piégeage (Re et al., 1999).
Resultats et discussion
Les cinétiques de séchage à partir des six expériences réalisées au cours de ce travail sont montrées dans la (Fig. 3).
Des profils des températures lors d'une expérience de séchage sous vide à 60 °C, sont exposés dans la (Fig. 4). Une diminution de la pression permet d'atteindre le point d´ébullition de l´eau à basse température. Car le vide permet de sécher ces matériaux qui d'ordinaire n'acceptent pas de hautes températures. Durant le séchage sous vide, nous sommes en présence d'un faible taux d'oxygène. Nous pouvons donc dire aux vues des premiers résultats que les réactions d'oxydation peuvent être réduites dans ces conditions de séchage et la modification de la couleur du bois par la chaleur peut s'expliquer principalement par la production et/ou la destruction des groupes chromophores par effet thermique.
Il a été clairement établi que les hémicelluloses sont détériorées par la chaleur provoquant une modification du bois ; les températures doivent être cependant élevées, T >200 °C. Nous avons également mesuré les changements de couleur des surfaces exposés à la plaque chauffante et à l'air de l'enceinte, puisque selon les principes de phénomène de transport, les produits chimiques tels que les sucres, les phénols, les antioxydants et autres substances étrangères auraient pu être transportés du centre à la couche de la surface par l'évaporation de l'eau, où ils peuvent être ensuite modifiés par les conditions de séchage.
La Figure 5 montre que la luminosité et la saturation de la couleur du bois sont proportionnelles. L'augmentation de la saturation et de la luminosité peuvent être liées à la dégradation thermique des extractibles (ellagitanins principalement). La luminosité peut être expliquée par une perte en composés phénoliques. La chaleur aussi peut modifier directement la couleur du bois en provoquant l'hydrolyse et l'oxydation de composants en bois. En autre, la discoloration des chênes a été étudié par Kollman, Keywerth et Kubler, (1951), et Wassipaul et Fellner, (1987), ils ont constaté qu'une humidité au-dessus de 70% facilite l'apparition des discolorations.
Il est bien connu que les extraits du bois de chêne ont des propriétés antioxydants qui peuvent restreindre les changements de couleur pendant le séchage, ces propriétés limitant les dégradations causées par l'oxygène et les radicaux libres (Hon et Minemura, 2000). Parmi les extractibles, les tanins ont des structures phénoliques qui peuvent être dégradés par effets thermiques et par l'oxygène. Ils peuvent par conséquence produire des composés de discoloration. Dans le cas du chêne, la participation des gallotanins et des éllagitanins a été bien identifiée dans les processus de discoloration (Haluk, Schloegel et Metche, 1991; Charrier, 1992; Koch, 2008; Zahri, 2007). Par ailleurs, la vescalagine et la castalagine subissent des réactions qui produisent des composés chromophores au cours du séchage. D'après Zhentian (2002), la vescalagine et la castalagine (éllagitanins) jouent le rôle principal de la discoloration au cours du séchage. Il a été montré que la vitesse de dégradation des éllagitanins est affectée par la température, l'oxygène et le pH; la température étant le paramètre le plus important.
Zanetti (2000), a étudié l'évolution de la couleur du bois de chêne sessile (Quercus petraea (Matt.) Liebl.) par photodégradation. Il a observé au cours d'un cycle de vieillissement de 500 heures à l'aide d'un spectrocolorimètre deux phénomènes: dans un premier temps un assombrissement accompagné d'un jaunissement, ainsi qu'une augmentation de la saturation de la couleur; dans un deuxième temps une baisse de la saturation, un rougissement et une augmentation de la luminosité du bois.
La dégradation des éllagitanins est un phénomène difficile à contrôler, car ceux-ci sont constitués de composants hydrolysables, qui en présence d'eau libre et de chaleur peuvent produire de l'acide gallique, de l'acide ellagique et du glucose. Ces acides peuvent aussi jouer un rôle de catalyseurs de réactions, ce qui complique la compréhension des phénomènes contrôlant les changements de couleur des bois. Les produits de l'hydrolyse des éllagitannines sont moins chromophores que les constituants d'origine (Hemingway et Hillis, 1971). L'acide ellagique peut donner lieu à une décarboxylation, et à des produits d'oxydation. Donc, nous pensons que la dégradation des éllagitanines correspond à des réactions d'hydrolyse qui en absence d'oxygène (sous vide) ne polymérise pas, et donc ne conduisent pas à des produits fortement chromophores. Nous pensons alors la dégradation que nous observons est une phase intermédiaire (cassure des éllagitanines) de l'évolution de ces composés. Les composants phénoliques sont des substances à tonalité rougeâtre, et dans l'espace de couleur leur dégradation concorde avec une tonalité jaune. Même si l'on travaille à basse température, la couleur des bois peut être altérée à partir de 43 °C (Yeo et Smith, 2004). En théorie, la réactivité de l'oxygène est plus élevée en présence d'eau libre (W>Wpsf). C'est pourquoi quelques travaux ont essayé d'élucider les mécanismes de discoloration du bois en amont du point de saturation de la fibre.
Le jaunissement peut être provoqué par une dégradation des composés phénoliques. La forte présence jaune sur la couche décolorée de la surface pourrait être due en partie au composants tels que les extractibles phénoliques. Le jaunissement du bois est lié à la formation des groupes contenant de l'oxygène, tels que les groupes carbonyles, et le peroxyde d'hydrogène. Afin de pouvoir confirmer la présence de groupes carbonyles, nous avons eu recours aux analyses de la Spectroscopie Infrarouge à Transformée de Fourier.
Néanmoins, l'altération de la couleur du bois n'est pas un sujet totalement compris ce qui nous a amené dans ce travail à explorer et analyser la relation entre le potentiel antioxydant et les groupes carbonyles. Il se peut que les ellagitanins subissent une oxydation et des réactions de polymérisation durant le séchage et participent à la formation des groupes chromophores. Les extractibles ont des propriétés antioxydantes qui peuvent limiter le changement de couleur durant le processus de séchage, ces dites propriétés limitant les dommages causés par les radicaux libres.
Par rapport à la technique de spectroscopie infrarouge, nous avons mesuré l'intensité des bandes à 1740 cm-1/1750 cm-1, et le rapport existant avec les potentiels antioxydants et les paramètres de l'espace CIELab. Le pic 1740 cm-1/1750 cm-1 est mis en relation avec la formation de composants chromophores C=O liés à l'oxydation des structures phénoliques (Zahri et al., 2007). Dans la Figure 6 nous présentons les spectres infrarouges du chêne lors du séchage sous vide à plaques.
Dans la Figure 7, nous présentons les valeurs du potentiel antioxydant et l'intensité C=O. Le Delta du potentiel antioxydant représente la différence entre le potentiel initial et le potentiel final pour chaque échantillon. Nous pouvons remarquer que le Delta du potentiel antioxydant augmente en même temps que C=O augmente. Le potentiel antioxydant est lié au contenu des extractibles car les groupes phénoliques sont des antioxydants puissants. Parmi les extractibles antioxydants, les ellagitanins et les gallotanins sont les plus importants. Les ellagitanins contribuent à la formation de l'oxydation des produits (groupes chromophores); ce fait a été confirmé par une présence plus importante d'entités carbonyles dans les surfaces de bois identifiés par spectroscopie. Les ellagitanins peuvent être hydrolysables en présence d'eau libre et de chaleur, même à basse température, par conséquent, il est possible de produire de l'acide gallique, de l'acide ellagique et du glucose durant le processus de séchage.
Conformément à ces résultats, nous pouvons dire que la capacité antioxydant et les pics à 1741 cm-1 sont directement en corrélation puisqu'une perte plus importante du potentiel antioxydant correspond à une présence plus importante en carbonyle plus importante (groupes chromophores). On peut donc supposer que la couleur du bois de chêne européen thermiquement modifiée est le résultat de la production et/ou destruction des groupes chromophores. L'effet de la température sur le potentiel antioxydant est démontré dans la Figure 8. La perte en puissance antioxydante augmente avec la température. Les composés phénoliques sont de couleur rougeâtre, la dégradation des ellagitanins provoque donc une couleur jaunâtre du bois par effet thermique. L'augmentation de la saturation et de la luminosité peut être liée à la dégradation thermique des extractibles (principalement les ellagitanins).
D´après la Figure 9, la luminosité est toujours plus forte dans les surfaces en contact avec la source de chaleur. Par conséquent on pourrait penser que l'augmentation de la luminosité est provoquée par l'effet d'une température plus importante du coté de la plaque (le bois étant dans ce cas directement en contact avec la plaque chauffante - sous vide continu à plaques).
Dans son travail, Grekin (2007) mentionne que la teinte rouge des bois du pin est associée avec la teneur en composants extractibles des bois, et que la tonalité jaune est associée à la photochimie des bois (en particulier à la présence de lignine). Il attribue le jaunissement du bois à la formation de groupes qui contiennent de l'oxygène, comme les groupes carbonyles, carboxyles, et peroxyde d'hydrogène, des observations que nous avons également remarqués.
Au vu des résultats expérimentaux, et étant donné la complexité des phénomènes et des réactions, la forte variabilité de la composition chimique et de la teneur en eau du matériau, il nous parait difficile d'établir une conclusion définitive à partir des analyses en colorimétrie. Cependant cette augmentation de la luminosité peut être liée aux états intermédiaires des substances, c´est-à-dire à des réactions intermédiaires (cassure des éllagitanines).
En théorie, le bois de feuillus est séché au-dessus de 60 °C et 65% d'humidité, nous avons donc recours au séchage sous vide pour que le bois soit chauffé par la plaque chauffante. Durant les opérations de séchage, les réactions entraînent la libération des composés organiques volatils (COV). Les dits composés peuvent catalyser les réactions chimiques sur la surface du bois; les réactions chimiques sont donc un phénomène complexe.
Conclusion
L'augmentation de la saturation et de la luminosité peuvent être liées à la dégradation thermique des ellagitanins durant le séchage sous vide à plaques. Une augmentation des groupes chromophores C=O dans le bois de chêne durant le processus de séchage est fortement liée au facteur température. La dégradation thermique des composés phénoliques est suivie d'une perte de la capacité antioxydant et on peut noter une tendance au jaunissement de la couleur du bois. L'intensité des groupes chromophores C=O augmente à mesure que la température augmente. Les extractibles (ellagitanins), qui sont des composés phénoliques, et les émissions de composés organiques volatils, ont donc une grande influence sur la luminosité des surfaces du bois. La discoloration durant le processus de séchage du bois implique la formation de substances colorées (tels que les chromophores) à partir des composés antioxydants extractibles.
La dégradation des ellagitanins peut contribuer à la formation des produits d'oxydation ; cette théorie a été appuyée par une plus importante intensité de la bande de vibration de valence de la double liaison C=O (groupe carbonyle) des surfaces du bois. Les ellagitanins sont des composés antioxydants mais ils sont hydrolysables en présence d'eau libre et de chaleur, il est donc ensuite possible de diminuer les quantités en acide gallique, acide ellagique et glucose durant le séchage. Dans nos échantillons, le potentiel antioxydant diminue à mesure que le pic 1741 cm-1 augmente. Ce fait est lié à la formation des produits d'oxydation (oxydation des ellagitanins), conséquence directe de la chute du potentiel antioxydant.
Nous avons demontré que la luminosité des surfaces du bois augmente à mesure que la température de séchage augmente, nous pouvons donc suggérer une vitesse d'évolution intermédiaire de la couleur (cassure des éllagitanines) puisque les groupes carbonyles augmentent à mesure que le potentiel antioxydant diminue.
Les différentes conditions de séchage sous vide et la particularité de notre dispositif expérimental permettent d'obtenir des résultats assez intéressants, peu de travaux ayant ont été orientés vers l'étude de l'altération de la couleur dans une opération de séchage sous vide à plaque.
D'après les résultats énoncés, nous pouvons donc dire que le séchage sous vide par contact réduit les dommages thermiques infligés au bois. Néanmoins les solutions apportées à ce problème restent cependant limitées.











 nueva página del texto (beta)
nueva página del texto (beta)