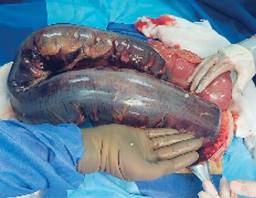
Introducción
El término “vólvulos” proviene del latín volvere (ˈvɔl.ve.re/) que significa giro. La torsión de un segmento del tracto alimentario fue descrita por primera vez en 1550 en el papiro de Ebers; la primera descripción del vólvulo sigmoideo fue hecha por Rokitansky en 1836.1,2
Por definición, un vólvulo es la torsión de un órgano a través de un eje, sobre su pedículo vascular; en el caso del vólvulo sigmoides esto ocasiona la formación de un asa cerrada en la cual existe compromiso de la circulación sanguínea, la causa principal es un fallo o laxitud de la fijación peritoneal, llámese punto fijo a las adherencias cecales, masa abdominal, útero gestacional, adenopatías, etcétera.3
Los vólvulos del tracto gastrointestinal siguen siendo una etiología importante del abdomen agudo, no por su frecuencia, sino por la gravedad de las complicaciones que conlleva, por lo cual es imperativo un diagnóstico precoz.3 Los casos más frecuentes son los vólvulos de ciego y sigmoides.4 Si la circulación mesentérica se ve comprometida o la distensión colónica compromete la irrigación, se desarrolla isquemia que concluye en necrosis en caso de diagnóstico tardío con translocación bacteriana masiva y sepsis.
Epidemiología
El vólvulo del sigmoides constituye la tercera causa de obstrucción colónica (10%),3 con una incidencia variable, que tiene una tendencia mayor en regiones de India, África y países del Medio Oriente, pero relativamente más baja en Estados Unidos, Australia, Nueva Zelanda y países de Europa Occidental. Más de 95% de los casos involucran colon sigmoides.5 De 50 a 80% de los vólvulos de sigmoides son la etiología más común de oclusión intestinal en países en desarrollo.6 En países occidentales se suele presentar en pacientes de la sexta a la octava década de la vida con padecimientos médicos crónicos, incapacidad neuropsicológica o estreñimiento. En estudios recientes se reporta una prevalencia 2:1 de vólvulo sigmoideo en hombres, principalmente en pacientes de edad avanzada (mayores de 70 años) y 3:1 de vólvulo cecal en mujeres jóvenes (menores de 60 años).1,7
Existen dos picos de mayor incidencia: el primero es de la primera a la tercera década de la vida por malformaciones intestinales desde el proceso embrionario, ejercicio excesivo o mesenterio común para intestino delgado y grueso; el segundo pico de 60 a 79 años, asociado a constipación crónica, obstrucción distal y trastorno neurocognitivo mayor.8
Etiología y fisiopatología
La etiología del vólvulo es multifactorial, se produce generalmente en pacientes con factores predisponentes, como un colon sigmoides redundante, fallo en la fijación normal del mesenterio, íleo, dietas ricas en fibra, estreñimiento crónico, distensión por gases, posturas anormales en niños con parálisis cerebral, la enfermedad de Chagas con megacolon y malrotaciones en el proceso embrionario.3 En un estudio de casos y controles, realizado por Akinkuotu y colaboradores,9 se encontró un aumento significativo de la longitud del mesosigmoides en pacientes que necesitaron intervención quirúrgica.
En el sigmoides, una rotación de 180 grados es considerada fisiológicamente normal, sin embargo, un giro mayor a estos grados deriva en complicaciones como obstrucción, isquemia, necrosis y, por consiguiente, perforación. Durante el vólvulo sigmoideo, la distensión colónica causa incremento en la presión intraluminal que resulta en disminución de la perfusión capilar, lo que ocasiona isquemia mural, agravada por la oclusión venosa mesocólica por el fenómeno mecánico de compresión y rotación axial.1
La isquemia temprana de la mucosa conlleva translocación bacteriana y ésta a producción de gas, lo que aumenta la distensión colónica y la afección sistémica. Si la torsión no es revertida en un periodo temprano, se crea un círculo vicioso que lleva a necrosis, posible perforación y posteriormente a síndrome de isquemia-reperfusión, lo que resultará en un estado de choque distributivo.10
Diagnóstico
El cuadro más común se presenta en pacientes mayores de 60 años y bajo tratamiento psiquiátrico que causa constipación crónica, esto aunado a los factores de riesgo (Tabla 1).1,6,10 Se presenta con dolor abdominal de tipo cólico, náusea, vómito y constipación; suele haber distensión abdominal, grados variables de sensibilidad, ruidos peristálticos disminuidos o aumentados y ámpula rectal vacía a la exploración digital, aunque un porcentaje puede cursar como asintomáticos inicialmente. El 33% de los pacientes presenta la triada del vólvulo de sigmoides, emesis, dolor tipo cólico con constipación y distensión abdominal.1 De 30 a 40% de los pacientes va a presentar antecedente de oclusión intestinal.8 La duración de los síntomas puede ser de algunas horas hasta varios días.
Tabla 1: Factores de riesgo para vólvulos -diferencial-.
| Sigmoides | Colónico |
|---|---|
| Constipación crónica | Constipación crónica |
| Oclusión recurrente | Dieta alta en fibra |
| Dependencia a laxantes | Uso frecuente de laxantes |
| Enfermedad de Hirschsprung | Antecedente quirúrgico abdominal |
| Diabetes mellitus | Falla en proceso embriológico |
| Antecedente neuropsiquiátrico | Embarazo |
| Estadio en cama prolongado | Antecedente de cirugía pélvica |
| Enfermedad de Chagas (megacolon) | Colonoscopia |
| Internamiento en instituciones médicas |
La presentación de emergencia suele ser con peritonitis o choque relacionados con isquemia o perforación y con una frecuencia de 25 hasta 35% de pacientes con vólvulo sigmoideo.7
En la radiografía simple, la clave diagnóstica para el vólvulo sigmoideo es el colon dilatado sin haustras, con forma de “U” invertida y localizado en la línea media con dirección hacia los cuadrantes superiores. El signo del “grano de café” se produce debido a la imagen central creada por el contacto de las paredes mediales del asa volvulada y las paredes laterales que dan lugar a los bordes del grano (Figura 1).3 Sin embargo, sólo el 60% de los pacientes se logra diagnosticar mediante radiografía abdominal. La presencia de neumatosis lineal sugiere perforación inminente por necrosis intestinal; la presencia de aire libre sugiere perforación intestinal.11
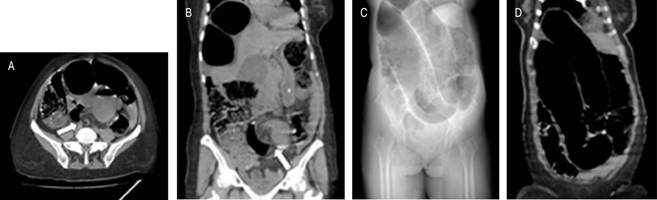
Figura 1: Tomografía axial computarizada simple en la cual se evidencia signo característico del vólvulo sigmoideo de “imagen de whirlpool” (flecha) en corte axial (A) y coronal (B). Se evidencia signo característico de vólvulo sigmoideo en “grano de café” (C y D).
El estudio de elección es la tomografía computarizada debido a su sensibilidad de 100% y especificidad > 90%, debido a que permite crear reconstrucciones multiplanares que facilitan el diagnóstico definitivo.1 Los hallazgos son superiores a los de la radiografía simple; los signos específicos tanto de la tomografía como de la radiografía para vólvulos sigmoideo y colónico se muestran en la Tabla 2.3,11 No obstante, hasta 25% de los pacientes no presentaron estos signos característicos (Figura 1).
Tabla 2: Signos radiológicos del vólvulo.
| Vólvulo sigmoideo | Vólvulo colónico | |
|---|---|---|
| Radiografía abdominal | Asa intestinal dilatada con niveles hidroaéreos | Distensión de asa que se extiende de cuadrante superior derecho a epigastrio o cuadrante superior izquierdo |
| Signo de “grano de café” | Un solo nivel hidroaéreo | |
| Ausencia de gas en ámpula rectal | ||
| Tomografía axial computarizada | Asa intestinal dilatada con ausencia de haustra | Dilatación de colon |
| Signo de whirlpool: torsión del mesenterio y vasos mesentéricos | Dilatación focal de aire con haustra en cuadrante superior izquierdo | |
| Signo de “pico de pájaro” | Signo de whirlpool: torsión del mesenterio y vasos mesentéricos | |
| Signo de “grano de café” | ||
| Signo de “X”: el entrecruzamiento de asas intestinales en el sitio de torsión | Signo de “pico de pájaro” | |
| Signo de “pared dividida”: por grasa mesentérica que se invagina en pared intestinal | Signo de “X”: el entrecruzamiento de asas intestinales en el sitio de torsión |
Enema contrastado: la imagen característica de “papel doblado” o de “pico de pájaro” en el punto donde se forma el vólvulo.11 Su utilidad como método diagnóstico terapéutico se explicará más adelante.
La elevación de lactato en casos de afección isquémica o datos propios de sepsis, en caso de ésta, suelen ser los únicos cambios en el perfil bioquímico. De igual forma, se debe solicitar biometría hemática, electrólitos, examen general de orina y prueba inmunológica de embarazo para toda mujer en edad fértil, así como fosfatasa alcalina y pruebas de función hepática que incluyan conteo de bilirrubina, amilasa y lipasa en todo dolor abdominal para descartar alguna otra patología.
Tratamiento
El diagnóstico oportuno en pacientes estables permite múltiples opciones diagnóstico-terapéuticas quirúrgicas, endoscópicas o intervencionistas, ya sean transitorias o definitivas. Dentro del tratamiento para el vólvulo sigmoideo no complicado, el primer paso es realizar una colonoscopia diagnóstica terapéutica para valorar la viabilidad sigmoidea, así como también la detorsión del mismo.1 Si hay imágenes sugestivas de necrosis, datos bioquímicos de isquemia o el recurso endoscópico no es accesible, el paciente amerita cirugía de urgencia (Figura 2).
Tratamiento no quirúrgico y endoscópico
El tratamiento inicial en cuadros sin perforación o isquemia es la detorsión endoscópica, que es efectiva en 60 a 95% de los casos, puede realizarse con sigmoidoscopia o colonoscopia flexible, usualmente se deja una sonda de descompresión por uno a tres días para mantener la reducción, permitir la descompresión continua y facilitar la preparación mecánica del colon en caso de ser necesario; con el manejo endoscópico exclusivo se ha documentado una mortalidad de 6.4%, una recurrencia a largo plazo de 43 a 75% de los pacientes y una recurrencia durante la misma hospitalización de 3 a 5%.7 En términos generales, ofrece una posibilidad terapéutica transitoria para pacientes inestables y con riesgo preoperatorio elevado, así como beneficio de preparación colónica y optimización de condiciones generales previo a un tratamiento definitivo.
La colostomía percutánea endoscópica es una opción prometedora que ha demostrado baja morbimortalidad y que se indica en pacientes con alto riesgo anestésico en quienes no sea posible la utilización de anestesia general. Se necesitan estudios a largo plazo y con mayor cantidad de pacientes que avalen esta recomendación.1
El colon por enema persiste como una opción viable, tradicionalmente indicado en pacientes sin inestabilidad hemodinámica ni necesidad de cirugía urgente, necrosis o perforación. Tiene una tasa de éxito de 69%, aunque alta morbilidad (23%), mortalidad (6.4%) y recurrencia de 43-75%, si se compara con la endoscopia flexible con una tasa de éxito de 76% y recurrencia de 25, 0.3 y 6%, respectivamente. No se considera una alternativa de primera elección de tratamiento en la actualidad debido a estos resultados.2
La sigmoidoscopia está indicada en pacientes hemodinámicamente estables; permite evaluar la viabilidad del colon y lograr la devolvulación con un índice de éxito de 70-95%, morbilidad de 4% y mortalidad de 3%. Se prefiere la endoscopia flexible por sobre la rígida.12 Después de la descompresión se coloca una sonda rectal por hasta 72 horas; en la actualidad, el consenso es realizar manejo quirúrgico resectivo-electivo de dos a cinco días después de la devolvulación endoscópica, por las altas tasas de recidiva (45-71%) en manejo endoscópico exclusivo, además de una mortalidad de 9 a 36% durante las mismas.12,13
La pexia de colon con colostomía percutánea es un procedimiento relativamente nuevo, descrito inicialmente en 1990 y que tradicionalmente se usa en pacientes geriátricos con alguna contraindicación para anestesia general o un ASA > a 3; consiste en la fijación colónica a la pared abdominal mediante la realización de una colostomía endoscópica.12 En un estudio de 2019, en Japón, con ocho pacientes y un seguimiento de 22.8 meses no se registró recidiva, sin embargo, no se cuenta con estudios multicéntricos, muestras grandes o estudios en población obesa para evaluar su aplicación en una población occidental.14
La detorsión endoscópica no será posible en 5 a 22% de los pacientes y requerirán tratamiento quirúrgico de emergencia. De 5 a 25% de los pacientes tendrán isquemia, perforación, peritonitis o choque séptico como presentación inicial, por lo que requerirán cirugía de emergencia.7
Tratamiento quirúrgico
En casos que se presenten inicialmente con signos o síntomas de isquemia o perforación intestinal el tratamiento indicado será quirúrgico (Figura 2); también en los pacientes que se observe isquemia avanzada de la mucosa y perforación, o perforación inminente, durante la endoscopia, se deberá abortar el procedimiento e implementar manejo quirúrgico de emergencia,7 con base en tres técnicas quirúrgicas esenciales: 1) detorsión y plicatura del mesenterio, 2) resección intestinal y anastomosis, 3) procedimiento de Hartmann,2 pero en pacientes con condiciones favorables para una anastomosis segura el tratamiento de elección es la resección con anastomosis primaria.
Según las guías de la American Society for Gastrointestinal Endoscopy, la intervención quirúrgica es el manejo indicado en los pacientes que presentan peritonitis, isquemia, perforación, deterioro clínico o diámetro cecal mayor de 12 cm, en pacientes con intestino isquémico o perforado se ha encontrado una mortalidad de hasta 44%. En pacientes con datos de alarma no se debe realizar devolvulación del intestino para prevenir síndrome de reperfusión, en estos casos se debe realizar resección del área volvulada en su misma posición.11,15
Algunas clasificaciones sobre los procedimientos quirúrgicos para el tratamiento del vólvulo sigmoideo los dividen en resectivos y no resectivos. Para decidir la técnica a realizar resultan de gran importancia las condiciones generales del paciente y las condiciones locales del colon.
No resectivo
En la actualidad, se reservan para casos en los que existe viabilidad del segmento afectado, en pacientes con alto riesgo preoperatorio o condiciones de inestabilidad transoperatoria, o como medida paliativa en pacientes con menor esperanza de vida y cuando el recurso endoscópico no es viable.
La sigmoidopexia tiene la ventaja de que no se requiere de preparación de colon para su realización, sin embargo, la tasa de recidiva con este procedimiento es de 22%16 y se asocia con 3% de mortalidad.1
La mesosigmoidoplastía, originalmente descrita por Tiwary y Prasad en 1979, es un procedimiento no resectivo y está indicado en casos en los que el colon sigmoides aún es viable durante el evento quirúrgico; se encuentra actualmente en desuso debido a su alto índice de recidivas. Consiste en una incisión longitudinal del mesosigmoides y un cierre en forma transversal.3 Se ha registrado una morbilidad postoperatoria baja con tasas de infección de herida quirúrgica de 2.7% y de íleo postquirúrgico de 8%, una mortalidad reportada entre 0-11%, relacionada a las comorbilidades del paciente y no al procedimiento quirúrgico, y una tasa de recurrencia hasta del 80%.17
La extraperitonealización del sigmoides, descrita por primera vez en 1970 como una alternativa segura para el vólvulo sigmoideo agudo y no complicado, se usó para prevenir recurrencias en pacientes jóvenes y sanos; consiste en la creación de un bolsillo entre el peritoneo y la fascia del músculo recto posterior, que exterioriza el colon sigmoides a través de una abertura peritoneal en la corredera parietocólica izquierda; el abordaje suele ser con una incisión paramedia y se suelen aproximar los bordes del peritoneo al colon con suturas absorbibles para evitar la herniación de asas del intestino delgado en ella. Se asocia con tasas mínimas de morbilidad y mortalidad, se dice que esta técnica previene con éxito la recurrencia del vólvulo, incluso cuando existe una dilatación generalizada del colon, por lo que ofrece una opción viable dentro de la población geriátrica o con comorbilidades mayores.18
Resectivas
Los tratamientos quirúrgicos resectivos se dividen a su vez en reconstitutivos y no reconstitutivos (procedimiento de Hartmann); estos últimos son sugeridos en pacientes que presentan inestabilidad hemodinámica, acidosis, hipotermia o coagulopatía;15 sin embargo, en la actualidad se considera el tratamiento estándar a la resección colónica con restauración de la continuidad.16
Los procedimientos resectivos establecidos se realizan en dos tiempos y comprenden dos variantes técnicas: 1) la resección sigmoidea en un primer tiempo mediante técnica de Rankin-Mikulicz complementada con cierre extraperitoneal de la colostomía, y 2) la resección sigmoidea con colostomía y bolsa de Hartmann complementada con la anastomosis intraperitoneal del colon en un segundo tiempo. La resección del asa sigmoidea afectada suele ser suficiente extensión de la resección colónica, no obstante, se debe considerar colectomía subtotal en casos asociados a atonía colónica, doble vólvulo o megacolon.1 La resección de intestino infartado se debe realizar sin distorsión y con mínima manipulación para prevenir la liberación de endotoxinas, potasio y bacterias a la circulación general, así como para prevenir perforación colónica.7
Se recomienda la colostomía si hay condiciones adversas locales o sistémicas, o si la experiencia del cirujano es limitada.1 La maduración de un estoma colónico permite la derivación del tránsito intestinal, toda vez que permite la fijación del asa volvulada a la pared abdominal como medida preventiva para la evitar una recidiva en la torsión de la misma.
En el caso de vólvulo se recomienda la creación de estoma con doble lumen, ya que previene recurrencias futuras del vólvulo, así como la monitorización adecuada del tránsito colónico y la restauración más simple de la continuidad intestinal como un procedimiento electivo retardado,1 encontrando las siguientes alternativas:
En asa: en la cual una luz es utilizada para descarga fecal mientras que la otra funciona como fístula mucosa, al evitar así la elevación de la presión intraabdominal; requiere un corte transversal de 50% del diámetro del asa.
Doble estoma: se puede usar después de resección, y presenta dos luces, una en la cual se descarga materia fecal y la otra por donde se descarga mucosidad conocida como fístula mucosa, en este caso se realiza corte completo de intestino y separación por segmento de piel.
Bloch-Paul-Mikulicz (escopeta): se realiza después de resecar segmento de colon, posteriormente se unen los cabos entre sí a nivel de la cara posterior, lo que da una luz para desecho fecal y una fístula mucosa.
Descrito inicialmente por Henri Albert Hartmann en 1923 para el manejo del cáncer colorrectal, el procedimiento de Hartmann consiste en una sigmoidectomía sin restauración de la continuidad intestinal, con colostomía terminal en el cuadrante inferior izquierdo, con cierre primario del muñón rectal que preserva la posibilidad de una restauración eventual de la continuidad intestinal.17
En contexto del vólvulo sigmoideo se indica cuando hay isquemia colónica con peritonitis fecal, inestabilidad hemodinámica o malas condiciones generales del paciente,17 así como en casos de vólvulo bajo con necrosis colónica que se extienda a la unión rectosigmoidea y que hace imposible brindar el segmento colónico hasta la piel.1 Los puntos clave del procedimiento involucran: a) definición de los márgenes de resección; b) disección retrógrada desde el sigmoides hacia la flexura esplénica por la línea blanca de Toldt; c) apertura del retroperitoneo y exposición del uréter izquierdo; d) identificación de la vena mesentérica inferior; e) identificación de los nervios hipogástricos para su preservación; f) control del tallo vascular mesentérico inferior o hemorroidal superior; g) liberación del mesosigmoides y resección intestinal; y h) cierre del muñón distal y maduración de estoma terminal.
Resección con anastomosis primaria
La anastomosis primaria se realiza generalmente en los casos donde el colon es viable, no hay inestabilidad hemodinámica, coagulopatía, acidosis o hipotermia, lo que conserva los principios básicos para una anastomosis exitosa que incluyen márgenes proximal y distal bien vascularizados, libres de enfermedad activa y de tensión. La anastomosis también debe ser hemostática y circunferencialmente hermética, y, de ser posible, realizada en un paciente con nutrición aceptable y enfermedades sistémicas controladas. Es con el propósito de satisfacer dichas condiciones, que los procedimientos transitorios menos invasivos han ganado auge en años recientes, con un procedimiento definitivo retardado, bajo las mejores condiciones locales y generales del paciente, lo que constituye el procedimiento de elección en el contexto de cirugía electiva para prevenir episodios recurrentes de vólvulos sigmoideos.7
Para la anastomosis manual, de gran complejidad para la anastomosis colorrectal, se prefiere el uso de una capa de puntos continuos con material monofilamento de lenta absorción, ya que se asocia con menor reacción tisular y menor riesgo de infección; un buen ejemplo son las suturas a base de polidioxanona de absorción lenta, larga preservación de la fuerza tensil y baja adherencia bacteriana.19 A pesar de que la técnica de anastomosis intestinal manual no está debidamente estandarizada (distancia de intersutura, distancia de la sutura al borde anastomótico, tensión de la sutura, etcétera), la manufactura clásica de la pared posterior, seguida del cierre de la pared anterior con puntos de Cushing o Connel Mayo, con o sin refuerzo con una segunda línea de sutura con puntos invaginantes de Lembert tiene resultados satisfactorios.19 No se ha encontrado diferencia estadísticamente significativa a favor de los puntos continuos en comparación con puntos interrumpidos con base en el porcentaje de fuga de anastomosis o de fuerza tensil de la misma.20
La anastomosis mecánica se apoya de herramientas para realizar un cierre hermético mediante grapeo de todas las capas intestinales, lo que ayuda a optimizar el tiempo quirúrgico. La más utilizada es la engrapadora circular para anastomosis término-terminal o término-lateral, con la presencia de tres líneas de grapas direccionales a distinto nivel para realizar mejor hermeticidad, menor estrés tisular y mejor perfusión de los bordes anastomóticos.21 Pueden reforzarse con una capa de sutura manual con puntos hemostáticos invaginantes. Diversos estudios apoyan la teoría de que no existe diferencia significativa entre la anastomosis manual versus la anastomosis mecánica, ya que ambas resultan en una cicatrización aceptable y adecuada fuerza tensil, con similar tasa de fuga anastomótica.4
Además, se han descrito factores de seguridad para la anastomosis mecánica, los cuales son:
Revisión de los rodetes anastomóticos para asegurar que se encuentren íntegros.
Que ambos cabos del colon se encuentren perfectamente unidos.
Reforzar la anastomosis con parche de epiplón o de serosa.
Realización de la prueba neumática, que consiste en la aplicación de clamp intestinal en la porción proximal de la anastomosis, al llenarse a continuación la cavidad con solución fisiológica, y posteriormente se insufla aire por el recto verificando la permeabilidad de la anastomosis.
Si se identifican sitios de fuga, éstos serán reparados con puntos invaginantes.
Para el seguimiento, se han propuesto diversos métodos de monitorización. La proteína C reactiva (PCR), reactante de fase aguda con vida media de 19 horas, empleado en un método de medición seriada -CRP ratio- ha demostrado un factor predictivo negativo de 97% a los tres, cuatro y cinco días postoperatorios con un corte menor o igual a 1.5 veces su valor basal. Un valor por arriba de este corte sugiere la realización de una tomografía contrastada para el diagnóstico oportuno de fuga anastomótica con una sensibilidad de 73% y especificidad de 91%. La limitante de este tipo de estudios al evaluar la fuga de anastomosis es la falta de un verdadero método de referencia, no contar con mediciones de PCR al ingreso del paciente ni con mediciones diarias, no tener grupo control y no disponer de estudios de imagen en todos los pacientes.22,23 La taquicardia, fiebre, leucocitos y en general la evolución postoperatoria tórpida con un alto índice de sospecha siguen jugando un papel importante en el diagnóstico oportuno de la fuga anastomótica.
La derivación fecal a través de una ileostomía en asa o colostomía proximal, de mayor uso en la cirugía oncológica, ofrece protección para una anastomosis colorrectal de alto riesgo desde un aspecto técnico. Los pacientes con ileostomía de protección demostraron una tasa de complicaciones significativamente más alta en estomas de alto gasto que los pacientes con colostomías, mientras que los pacientes con colostomía presentaron mayor tasa de complicaciones en cuanto a infección de herida, eventración contenida del abdomen y reconstitución del tránsito intestinal.24-26
Complicaciones
Son las propias de la obstrucción en asa cerrada: isquemia, necrosis, perforación o estrangulación (Figura 3). En algunos pacientes en los que la sigma es redundante, el mesenterio elongado y el pedículo estrecho, puede haber asas del intestino delgado que envuelvan al pedículo de tal manera que sean arrastradas por el giro del vólvulo y se produzca una isquemia de intestino delgado, a esta asociación se le llama nudo íleo sigmoideo que se encuentra en 5-8% de los vólvulos de sigmoides.3
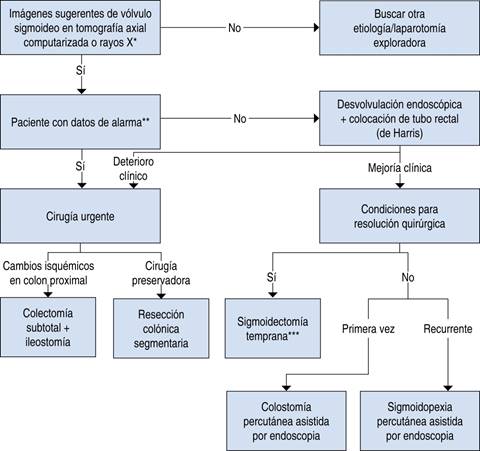
Figura 3: Toma de decisiones terapéuticas con respecto a hallazgos y clínica de paciente con dolor abdominal. * Ver imágenes radiológicas en Tabla 2. ** Datos de peritonitis o perforación. *** Durante mismo internamiento hospitalario o a la brevedad para prevenir recurrencia.
La presencia de comorbilidades severas (enfermedad pulmonar obstructiva crónica, hipertensión arterial sistémica, enfermedad isquémica cardiaca, falla cardiaca, diabetes, falla renal crónica, hemiplejía y Parkinson), así como la presencia de choque, duración prolongada de los síntomas y la combinación del vólvulo colónico e ileal fueron significativamente asociados con el riesgo de necrosis colónica. No se demostró relación entre la edad del paciente y la necrosis colónica.1
La necrosis colónica y la peritonitis son los dos principales factores de riesgo para mortalidad.1
Las complicaciones anastomóticas (fuga, sangrado postoperatorio, estenosis, etcétera) requieren una segunda intervención con una incidencia de hasta 50% de estoma permanente.17
La dehiscencia de la anastomosis (DA) se define como aquella manifestación clínica que incluye la salida de contenido intestinal y/o gases a través de un drenaje, de la herida principal o la fístula a un órgano vecino, y los hallazgos de una reintervención por una peritonitis localizada (colección) o generalizada secundaria a una filtración de la anastomosis (generalmente registrada como dehiscencia).
El periodo crítico en la aparición de fallos anastomóticos se sitúa entre el tercer y quinto día postquirúrgico, que es el momento en el que la sutura tiene menor resistencia. Durante este periodo se produce una disminución en la cantidad de colágeno de la submucosa que coincide además con una situación de precariedad en la vascularización, ambos hechos parecen ser la causa de esa menor fuerza en la anastomosis. La incidencia global de esta complicación en cirugía colorrectal varía entre 3.4 y 6%, cifra que se eleva hasta 15% si se analiza específicamente la anastomosis colorrectal baja luego de una resección anterior.24
Los factores de alto riesgo para fuga anastomótica son: sexo masculino, desnutrición, enfermedad cardiovascular grave, uso de esteroides, historia de abuso de alcohol, transfusión sanguínea perioperatoria, edad avanzada, obesidad y pacientes con antecedente de radiación pélvica, en estos se puede considerar una ileostomía de protección.25
Entre los estudios que utilizaron selectivamente un estoma disfuncional están los de Gastinger y colegas, quienes realizaron un estudio multicéntrico retrospectivo de un total de 2,729 pacientes, donde 881 recibieron un estoma y 1,848 no; no encontraron diferencias en las tasas generales de fuga anastomótica entre los dos grupos, pero encontraron una tasa de intervención quirúrgica significativamente más baja en los pacientes que tenían un estoma protector.27
La presencia de un colon proximal dilatado incrementa el riesgo de fuga anastomótica postoperatoria.1 Oren y colaboradores encontraron que no había diferencia significativa de mortalidad entre el procedimiento de Hartmann (22%) versus la resección con anastomosis (19%) en los pacientes que se sometieron a cirugía por un vólvulo complicado. El riesgo de fuga anastomótica y estancia hospitalaria fueron similares entre laparoscopia y laparotomía.
Pronóstico
En pacientes con gangrena se ha demostrado una mortalidad de 11 a 60%, mientras que en pacientes sin gangrena se reduce a menos de 10%, la recurrencia de vólvulos en pacientes que no se sometieron a cirugía es de 84% y varía en su presentación de horas a semanas.11
Existen factores a tomar en cuenta a favor de no restaurar el tránsito intestinal, tales como puntaje ASA > III, edad > 75 años, presencia de neoplasia, paciente renuente e imposibilidad para acceder al muñón rectal, entre otros, lo que representa de 8-12% de todos los pacientes ostomizados.17
Para la reconexión anastomótica se prefiere la vía laparoscópica, ya que presenta menos complicaciones graves (falla multiorgánica, reoperación), infección (sepsis, choque séptico, abscesos intraabdominales), menor mortalidad (12%), menor porcentaje de fuga anastomótica (1.2%) y menos complicaciones parietales, junto con menor estancia hospitalaria (1.5 días); sin embargo, la disponibilidad del recurso laparoscópico apropiado y un cirujano experimentado deben ser factores que se deben considerar al momento de elegir el método de restitución del tránsito.17
Conclusión
El vólvulo de sigmoides representa una entidad de urgencia, cuyo diagnóstico oportuno permite esquematizar cada caso a fin de ofrecer un tratamiento escalonado desde lo mínimamente invasivo, para favorecer una transición segura hasta los procedimientos resectivos definitivos en las mejores condiciones posibles. No obstante, es de gran importancia conocer el gran arsenal de procedimientos transitorios de los que el cirujano general puede echar mano en pacientes inestables o con comorbilidades mayores, y que no se benefician de un procedimiento invasivo con larga duración y riesgo postoperatorio.











 nueva página del texto (beta)
nueva página del texto (beta)