Introducción
La obesidad y el sobrepeso han presentado un aumento progresivo en las últimas tres décadas, tanto en países desarrollados como en los que no lo son, aplicándose a dicho fenómeno la denominación de “pandemia”.1
En la Encuesta Nacional de Salud y Nutrición 2016 en nuestro país, la prevalencia combinada de sobrepeso y obesidad en adultos mayores de 20 años fue de 72.5% en ambos sexos. El rango de obesidad fue más elevado en mujeres, 38.6 versus 27.7% en hombres. El grupo de edad más afectado se encuentra entre los 40-49 años; sin embargo, los grados más altos de obesidad se observan en personas entre 50-59 años.2 Jalisco ocupa el décimo lugar con 28.50%, seguido de los estados fronterizos del norte con 37.8%, siendo éstos los más afectados del país.3
La cirugía bariátrica se ha convertido en la mejor opción de tratamiento para la obesidad mórbida. Regularmente mantiene una pérdida de peso sostenida con resolución o control de sus comorbilidades, tales como diabetes tipo 2 (DM), hipertensión arterial (HTA), hiperlipidemia, osteoartritis y la apnea del sueño.4-10
La incidencia de la DM ha alcanzado proporciones realmente alarmantes en nuestro país, donde existen 13.26 millones de personas con esta enfermedad, las cuales están estrechamente relacionadas con obesidad.3
Buchwald y cols. en un metaanálisis con 22,000 pacientes observaron que la técnica de Scopinaro (switch duodenal) controla 98.9% de los casos de la DM, el bypass gástrico en Y de Roux (BPGYR) 83%, la gastroplastía vertical en 71% y con la banda ajustable sólo 50%, demostrando que la cirugía bariátrica es una alternativa efectiva para el tratamiento de la obesidad y sus comorbilidades a mediano y largo plazo.10 Otro estudio retrospectivo en pacientes operados por obesidad mostró una disminución de la mortalidad causada por enfermedades cardiovasculares y cáncer en un seguimiento de 7.1 años.9
La obesidad actúa como un precursor del síndrome metabólico, el cual es una etapa crucial para muchas enfermedades que muestran inflamación crónica y contribuye en desórdenes como la artritis, la esteatohepatitis no alcohólica (sin inflamación: NAFLD, con inflamación: NASH), el cáncer, las enfermedades cardiovasculares, la muerte prematura, el asma y la enfermedad de Alzheimer debido a las respuestas inflamatorias excesivas y prolongadas.11,12 Estudios previos demuestran que la inflamación sistémica en sujetos obesos posterior a un procedimiento bariátrico se reduce de manera significativa13 y es una alternativa de tratamiento con bajo riesgo de morbilidad y mortalidad.14
Los procedimientos bariátricos se dividen en dos tipos: los gástrico-restrictivos y los gástrico-restrictivos y malabsortivos. Actualmente, de los restrictivos el que más se usa es la gastrectomía vertical en manga o manga gástrica (GVM). La banda gástrica ajustable laparoscópica (BGAL) ha perdido popularidad por los resultados reducidos y las complicaciones postoperatorias que presenta.15
La GVM se introdujo inicialmente como el primer paso del procedimiento de switch duodenal, pero ahora se utiliza como un procedimiento independiente. Gran parte de la curvatura mayor del fondo y cuerpo gástrico se extirpan, dejando un estómago tubular, lo que da lugar a cambios endocrinos benéficos importantes. Debido a la sencillez de la técnica y a la pérdida de peso aceptable que produce, su práctica en la actualidad tiene una tendencia cada vez mayor.15
El bypass gástrico se introdujo en la década de los años 70 y desde entonces se han hecho varias modificaciones a la técnica con mejores resultados a corto y largo plazo. La versión más común es la reconstrucción en Y de Roux laparoscópico (BPGYR).15
La cirugía bariátrica actualmente es el mejor método para controlar la obesidad y sus comorbilidades, desafortunadamente son pocos los estudios en la población mexicana. Por lo tanto, en el presente estudio se evaluaron los efectos a corto plazo (12 meses) de la cirugía bariátrica en el control de la obesidad y algunas de sus enfermedades comórbidas asociadas.
Material y métodos
Tipo de estudio: de cohorte prospectivo.
Sujetos
Se hizo un seguimiento de corto plazo de 12 meses de los pacientes ingresados a la clínica de cirugía bariátrica sometidos a cirugía de obesidad de manera electiva durante el periodo comprendido entre el 1o de noviembre de 2009 y el 30 abril de 2016 en el Hospital Civil de Guadalajara “Fray Antonio Alcalde” (HCGFAA). Se evaluaron 160 pacientes de los 162 pacientes operados hasta el 30 de abril de 2016, los cuales habían completado un seguimiento a 12 meses con cuatro controles de las variables establecidas (preoperatorio, tres, seis y 12 meses). Por lo tanto, se trabajó con una muestra por conveniencia. Se excluyeron dos pacientes, una por defunción a los tres meses de postoperatorio por embolismo cerebral y otro paciente operado de derivación biliopancreática en el que no se llevó un seguimiento adecuado.
La edad promedio fue de 34 años. De éstos, 108 fueron sometidos a BPGYR y 36 a GVM, todos por vía laparoscópica. Se realizaron los procedimientos de acuerdo con el protocolo multidisciplinario de la Clínica de Cirugía Bariátrica del HCGFAA y con la Norma Oficial Mexicana NOM-008-SSA3-2010.16
Se incluyeron pacientes con una edad mayor o igual a 18 años, con un IMC (kg/m2) mayor de 35 y valorados por el grupo multidisciplinario (nutrición, psicología, cardiología, neumología y endocrinología). Para determinar si los pacientes eran candidatos a BPGYR o GVM se tomó en cuenta su IMC, la coexistencia de enfermedades metabólicas, cardiacas, respiratorias, osteoartritis (principalmente de columna, cadera, rodillas y tobillos) y enfermedad por reflujo gastroesofágico. Los criterios de inclusión para el procedimiento de GVM fueron: edad entre los 18 y 25 años, sin coexistencia de enfermedades metabólicas, sin hernia hiatal ni reflujo gastroesofágico. Además, en este procedimiento se incluyó un paciente con un IMC mayor de 50 kg/m2, asociado a un problema cardiorrespiratorio severo. Aunque a dicho paciente se le practicó inicialmente GVM, varios meses más tarde, cuando logró perder peso y mostró una mejoría importante de su condición cardiorrespiratoria (revalorado por neumología y cardiología), se sometió a cirugía de conversión, de GVM a BPGYR. A los pacientes con IMC de 35 a 40 kg/m2 con enfermedad comórbida asociada o un IMC mayor de 40 kg/m2 sin comorbilidad se les practicó BPGYR.
Mediciones
Cada paciente fue evaluado antes de la cirugía y a los tres, seis y 12 meses posteriores a la misma. Las variables que se midieron fueron: peso, IMC (kg/m2), glucosa sérica con ayuno de 12 horas, hemoglobina glicosilada, insulina sérica, urea, creatinina, proteína C reactiva, colesterol, triglicéridos, enzimas hepáticas: fosfatasa alcalina (FA), transaminasa glutámico-pirúvica/alanina transaminasa (TGP/ALT), transaminasa glutámica oxalacética/alanina aminotransferasa (TGO/AST) y gamma glutamil transpeptidasa (GGT), y presión arterial. Se consideraron como rangos normales de las variables séricas medidas los actualmente vigentes en el laboratorio del Hospital Civil de Guadalajara “FFA”. El peso, la estatura y la presión arterial fueron medidos por dos de los investigadores con una báscula digital marca FECA® y con el esfigmomanómetro de la Clínica de Cirugía Bariátrica del HCGFAA, los cuales fueron calibrados cada seis meses.
Procedimiento
Todos los pacientes fueron atendidos en la consulta de primera vez, donde se les abrió expediente y número de registro. Posteriormente fueron evaluados por los departamentos de cirugía, psicología y nutrición de la clínica de cirugía bariátrica. Después de obtener los estudios iniciales se discutió en forma multidisciplinaria la elección del procedimiento quirúrgico a realizarse según los criterios anteriormente expuestos. Finalmente, previa valoración por endocrinología, cardiología y anestesiología, los pacientes fueron programados para cirugía.
En el periodo postoperatorio el seguimiento clínico, psicológico y nutricional fue llevado a cabo de acuerdo con el protocolo establecido en la Clínica de Cirugía Bariátrica del HCGFAA.
Análisis estadístico
Las variables fueron capturadas en una base de datos electrónica y se sometieron a un análisis estadístico utilizando el programa SPSS (versión 21.0; IBM Corp., Armonk, NY, EUA). Las variables de estudio cualitativas se presentan en frecuencias y/o porcentajes, mientras que las cuantitativas se presentan con medidas de tendencia central (medias) y dispersión (desviación estándar). Posteriormente, con la finalidad de determinar si existían diferencias tanto entre los tipos de cirugía (GVM y BPGYR) como entre los valores preoperatorios y los obtenidos por los pacientes a los tres, seis y 12 meses de la cirugía, se realizó un análisis de varianza de parcelas divididas (2 × 4), el cual combina comparaciones entre grupos (tipos de cirugía) e intragrupo (tiempos). Además, para conocer el sentido de las diferencias se realizaron análisis post hoc, los cuales fueron ajustados con el método de Bonferroni. Se consideró un nivel de significancia p < 0.05.
Consideraciones éticas: los aspectos éticos en este estudio se basan en el Reglamento de la Ley General de Salud en Materia de Investigación para la Salud y en la declaración de Helsinki de 1975 y sus enmiendas, así como los códigos nacionales e internacionales vigentes para las buenas prácticas en la investigación, autorizándose con el número de Registro del Comité de Ética en Investigación 044/11, y del Comité de Investigación 002/15.
Resultados
Presentamos resultados a corto plazo de nuestra experiencia en los primeros 6.6 años de actividad en la Clínica de Cirugía Bariátrica del HCGFAA. Se incluyeron 160 pacientes con evaluación completa preoperatoria y seguimiento a los tres, seis y 12 meses. Las variables estudiadas de los pacientes en el periodo preoperatorio se presentan en la Tabla 1.
Tabla 1: Variables de estudio en el prequirúrgico de bypass gástrico en Y de Roux y gastrectomía vertical en manga.
| BPGYR* | GVM** | |
|---|---|---|
| IMC*** | 46.7 ± 8.5 | 43.1 ± 9.9 |
| Hb glucosilada | 7.1 ± 1.7 | 6.4 ± 1 |
| Glucosa | 134.8 ± 64.2 | 108.8 ± 29.4 |
| Insulina plasmática | 22.7 ± 10.9 | 24.4 ± 11.9 |
| Urea | 28.7 ± 9.1 | 24.9 ± 7.3 |
| Creatinina | 0.83 ± 0.24 | 0.77 ± 0.15 |
| Colesterol | 198.67 ± 52.8 | 185.8 ± 49.1 |
| Triglicéridos | 166.4 ± 83.3 | 161.3 ± 50.1 |
| Proteína C reactiva | 8.82 ± 4.5 | 7.8 ± 4.4 |
| Fosfatasa alcalina | 100.2 ± 49.4 | 70.6 ± 11.7 |
| TGO/AST | 62.7 ± 59.7 | 57.1 ± 52.2 |
| GGT | 49.4 ± 33 | 45 ± 38.1 |
| TGP/ALT | 63.3 ± 60.8 | 59 ± 55 |
* BPGYR = Bypass gástrico en Y de Roux.
** GVM = Gastrectomía vertical en manga.
*** IMC = Índice de masa corporal.
Pérdida de peso e índice de masa corporal (kg/m2)
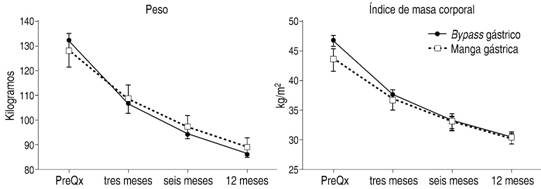
El grupo de BPGYR (108 casos) tuvo un peso promedio inicial (PPI) de 132.42 kg y al año sólo de 86.55 kg, con un IMC promedio inicial de 46.82 (kg/m2) y al año de 30.65 kg/m2, lo que significó que perdieron en promedio 45.86 kg (34.63%) de su peso inicial. Los 52 pacientes operados de manga gástrica tenían un PPI de 128.57 kg y al año de 89.20 kg, con un IMC promedio inicial de 43.69 (kg/m2) y al año de 30.43 kg/m2, por lo que perdieron en promedio 39.36 kg (30.62%) del peso preoperatorio.
Los ANDEVA mostraron que, aunque no se encontraron diferencias significativas en estas variables entre los dos tipos de cirugía (GVM y BPGYR), se obtuvo una reducción significativa después de la cirugía en todos los periodos registrados (Figura 1).
Variables bioquímicas relacionadas con el metabolismo de la glucosa
Se observó que 37 (23.12%) pacientes prediabéticos (glicemia entre 100-124 mg/dl), de los cuales a 30 se les practicó BPGYR y a siete GVM. A los 12 meses sólo cuatro (10.81%) pacientes continuaron siendo prediabéticos, tres en el grupo de BPGYR y uno en el de GVM. Se detectaron 54 (33.75%) pacientes con DM, de los cuales a 45 se les practicó BPGYR y a nueve GVM. A los 12 meses sólo un (1.85%) paciente del grupo con BPGYR mostró diabetes persistente; es decir, continuó con glucemia en ayunas con niveles iguales o mayores de 126 mg/dl.
Se determinaron los niveles de insulina sérica inicial sólo en 76 pacientes. De éstos, 37 (48.68%) tuvieron hiperinsulinemia inicial, los cuales usualmente presentaban glicemia inicial elevada.
Sólo a 90 pacientes se les determinaron los niveles de hemoglobina glicosilada inicial, de los cuales 64 (71.11%) la tuvieron elevada. A los 12 meses todos los pacientes presentaron niveles normales.
Finalmente, los ANDEVA indicaron que en los niveles de glucosa, hemoglobina glicosilada (HbA1c) e insulina plasmática no se encontraron diferencias significativas entre los tipos de cirugía (GVM y BPGYR). Sin embargo, tanto la glucosa como la hemoglobina glicosilada mostraron después de la cirugía una reducción significativa y gradual con el tiempo. En la insulina plasmática sólo se observó una tendencia no significativa de dicha reducción a través del tiempo (p < 0.091) (Figura 2).
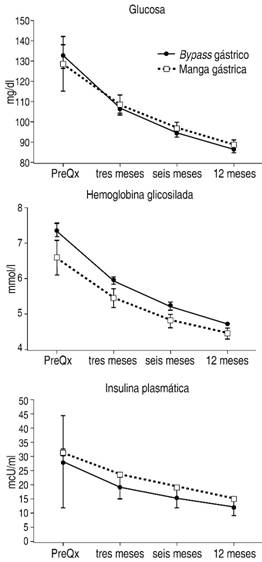
Figura 2: Niveles de glucosa, hemoglobina glicosilada e insulina plasmática (X ± EEM) antes de la cirugía por BPGYR y GVM y a los tres, seis y 12 meses postquirúrgicos. Tanto la glucosa (F3,396 = 28.79, p < 0.000, µ2 = 0.179, n = 134) como la hemoglobina glicosilada (F3,246 = 101.976, p < 0.000, µ2 = 0.554, n = 135) mostraron después de la cirugía una reducción significativa y gradual a través del tiempo. En la insulina plasmática sólo se encontró una tendencia no significativa de dicha reducción a través del tiempo (F3,183 = 2.950, p < 0.091, µ2 = 0.046, n = 136).
Variables bioquímicas relacionadas con la función renal
Hasta el momento no se ha establecido un protocolo dirigido a tratar pacientes con obesidad y disfunción renal, aunque se detectaron en el preoperatorio 25 pacientes (15.63%) con urea y/o creatinina alteradas, pero al año todos alcanzaron sus niveles normales.
En los ANDEVA no se encontraron diferencias significativas entre los tipos de cirugía en los niveles de urea y creatinina. Aunque en la urea hubo después de la cirugía una reducción significativa y gradual con el paso del tiempo, sólo se observó un cambio entre la medida prequirúrgica y el control postquirúrgico a los tres meses, no habiendo diferencias significativas entre seis y 12 meses (Figura 3).
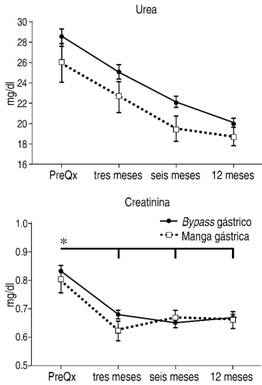
Figura 3: Niveles de urea y creatinina (X ± EEM) antes de la cirugía por BPGYR y GVM y a los tres, seis y 12 meses postquirúrgicos. En el caso de la urea todas las diferencias en el tiempo son significativas (F3,399 = 101.751, p < 0.000, µ2 = 0.433, n = 135), mientras que en la creatinina sólo entre la medida prequirúrgica y las tres medidas posteriores a la cirugía (F3,402 = 18.384, p < 0.000, µ2 = 0.121, n = 136).
Colesterol y triglicéridos
En relación con los lípidos, únicamente se tomó en cuenta las determinaciones de colesterol o triglicéridos totales y se consideró a un paciente con dislipidemia cuando tenía uno o ambos parámetros elevados. De esta manera, se detectaron 76 (55%) pacientes con lípidos alterados y a los 12 meses solamente un paciente (0.62%) persistió con triglicéridos elevados y todos corrigieron sus niveles de colesterol.
En los ANDEVA no se encontraron diferencias significativas entre los tipos de cirugía. No obstante, como se describe en la Figura 4, en los niveles de ambos lípidos hubo una reducción significativa y gradual después de la cirugía.
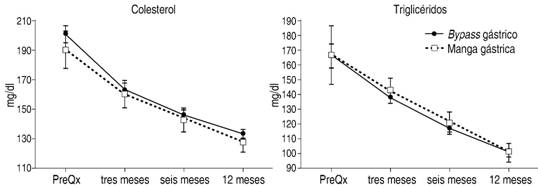
Figura 4: Niveles de colesterol y triglicéridos (X ± EEM) antes de la cirugía por BPGYR y GVM y a los tres, seis y 12 meses postquirúrgicos. Todas las diferencias en el tiempo son significativas entre sí (colesterol: F3,327 = 89.572, p < 0.000, µ2 = 0.451, n = 111; triglicéridos: F3,321 = 38.325, p < 0.000, µ2 = 0.264, n = 109).
Proteína C reactiva
En la evaluación preoperatoria 37 pacientes tenían la proteína C reactiva elevada y a los 12 meses, sólo tres mantuvieron dicha elevación; estos pacientes fueron los mismos que mostraron inflamación y fibrosis hepática. En los ANDEVA no se apreciaron diferencias significativas entre los dos tipos de cirugía ni en las mediciones preoperatorias ni postoperatorias.
Perfil hepático
Antes de la cirugía, la fosfatasa alcalina se observó alta en 56 (35%) casos, la TGP/ALT en 59 (36.8%) casos, la TGO/AST en 54 (33.7%) casos y la GGT en 52 (32.5%) casos. En 69 (43.13%) pacientes se detectó disfunción hepática; es decir, tenían elevada al menos una de las enzimas. A los 12 meses se logró medir las variables hepáticas en 142 pacientes, de los cuales sólo 13 (9.15%) continuaron con una o más enzimas elevadas. De éstos, tres tuvieron diagnóstico de inflamación y fibrosis grado 2 (NASH), dos de ellos remitieron con tratamiento farmacológico y uno evolucionó a cirrosis.
En los ANDEVA se observó que en ninguna de las variables del perfil hepático hubo diferencias significativas entre los tipos de cirugía. No obstante, como se describe en la Figura 5, los niveles de fosfatasa alcalina, TGP/ALT, TGO/AST y GGT mostraron una reducción significativa gradual después de la cirugía.
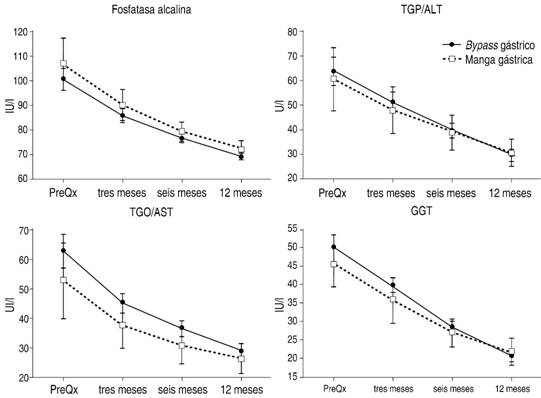
Figura 5: Niveles fosfatasa alcalina, TGP/ALT, TGO/AST y GGT (X ± EEM) antes de la cirugía por BPGYR y GVM y a los tres, seis y 12 meses postquirúrgicos. Todas las diferencias en el tiempo son significativas entre sí. (Fosfatasa alcalina: F3,390 = 47.825, p < 0.000, µ2 = 0.269, n = 132; TGP/ALT: F3,396 = 39.150, p < 0.000, µ2 = 0.229, n = 134; TGO/AST: F3,396 = 37.147, p < 0.000, µ2 = 0.220, n = 134, y GGT: F3,399 = 89.450, p < 0.000, µ2 = 0.397, n = 135).
Presión arterial
Antes de la cirugía 67 (41.8%) pacientes tenían HTA, mientras que a los 12 meses sólo continuaron con la presión arterial elevada siete (4.93%) con una resolución de 89.56%. Los ANDEVA indicaron que no hubo diferencias significativas en la presión arterial entre los tipos de cirugía, pero tanto en la presión sistólica como diastólica se observó una reducción significativa y gradual hasta los seis meses después de la cirugía (Figura 6).
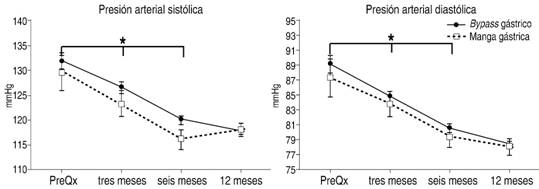
Figura 6: Presión sistólica y diastólica (X ± EEM) antes de la cirugía por BPGYR y GVM y a los tres, seis y 12 meses postquirúrgicos. Las diferencias en el tiempo son significativas entre la evaluación prequirúrgica y las evaluaciones a los tres y seis meses postoperatorios. (Presión sistólica: F3,396 = 30.233, p < 0.000, µ2 = 0.186 y presión diastólica: F3,396 = 39.920, p < 0.000, µ2 = 0.195 (* p < 0.001) n = 134).
Discusión
La cirugía bariátrica realizada en un programa multidisciplinario con cirujanos certificados ha demostrado ser un procedimiento seguro y eficaz en la pérdida del exceso de peso de las personas con obesidad mórbida, al igual que en el control de las alteraciones metabólicas, de la presión arterial, respiratorias, osteoarticulares, fertilidad en las mujeres jóvenes y en general cambia la expectativa de vida en lo social, laboral, sexual y da lugar a una elevación muy significativa de la autoestima.6,8,10,13,15 La pérdida de peso dependerá también de la reeducación en la forma de alimentarse, en lo posible incorporar actividad física al nuevo estilo de vida y llevar un seguimiento estrecho en los primeros meses hasta alcanzar las metas establecidas por el grupo bariátrico multidisciplinario.
Los resultados a corto plazo de nuestra experiencia demuestran que tanto el BPGYR como la GVM son dos procedimientos quirúrgicos adecuados para el tratamiento de la obesidad mórbida y las enfermedades asociadas en los pacientes que acuden al HCGFAA. Aunque ambos tipos de cirugía fueron efectivos para disminuir el exceso de peso y las enfermedades comórbidas de los pacientes obesos, se continuará con el seguimiento de los mismos para conocer sus efectos a largo plazo.
Por otra parte, es importante destacar que los pacientes sometidos a bypass tenían mayor peso e IMC inicial y que el porcentaje de pérdida de peso a un año fue mayor en este grupo, pero no hubo una diferencia estadísticamente significativa entre los grupos (Figura 1). Los resultados a un año en este estudio concuerdan con lo que se ha descrito en la literatura.8,10,17-21
La pérdida de peso después de un procedimiento bariátrico está condicionada por una restricción importante en la ingesta calórica; sin embargo, en los procedimientos mal absortivos y mixtos se altera la secreción de diversas hormonas gastrointestinales que regulan el eje entero-insular, conocidas como incretinas, principalmente el péptido insulinotrópico dependiente de glucosa (GIP), el péptido similar al glucagón 1 (GLP-1), la grelina y péptido YY, entre otras, resultando en un aumento en la secreción de insulina y una mejoría a nivel celular en la sensibilidad a ésta.10,13,15 Estudios en humanos y en animales han demostrado que el BPGYR modifica la composición de la microbiota, factor que influye en la pérdida de peso con este procedimiento. La microbiota tiene un papel importante en el almacenamiento de energía, por lo que participa en el desarrollo de la obesidad.22
De los pacientes en el preoperatorio 56.87% tenía glucemias arriba de 100 mg/dl, pero sólo a 54 (33.75%) casos se les consideró como diabéticos (nivel de > 126 mg/dl) con niveles de insulina plasmática elevados mayores de 23 µU/ml y de 6% de HbA1c. Al final sólo una paciente (1.85%) con bypass gástrico persistió con glicemias en un rango de 200 a 300 mg/dl, misma que a las tres semanas del periodo postoperatorio dejó de requerir insulina y continuó bajo tratamiento con metformina. Lo anterior indica un control de la DM en 98.15% de nuestros pacientes operados con bypass gástrico. De los 91 casos que tuvieron glucemias mayores de 100 mg/dl, sólo cuatro (4.39%) quedaron en el rango de prediabéticos.
A este respecto, en el metaanálisis de Buchwald y cols. (2004) se documentó la resolución de la DM en 83.7% en pacientes operados con BPGYR.10 El mismo autor, en otro metaanálisis efectuado 10 años después con pacientes operados con BPGYR, encontró que 84.2% mostraron control de la DM.17 Otros estudios recientes reportan resolución de la DM entre 92 y 86% de los casos.6,8,13 Sin embargo, existe una gran cantidad de reportes (algunos con muestras pequeñas) en los que la remisión de la diabetes mellitus fluctúa de 10023 a 38.2%24 de los casos. Los resultados discrepantes en estos estudios pueden depender del tipo de cirugía, del tiempo de evolución de la diabetes, del periodo de seguimiento de los sujetos y de la fecha de cohorte.
Otro factor de riesgo cardiaco y metabólico frecuentemente asociado a la obesidad son las altas concentraciones de lípidos en sangre. Con fines prácticos únicamente tomamos en cuenta como variables los niveles altos de colesterol o triglicéridos totales y consideramos como “dislipidemia” a los pacientes que tenían uno o ambos elevados. De esta manera se detectó que 55% de los pacientes tenían dislipidemia y que a los 12 meses sólo 0.62% continuó con lípidos alterados. Así que puede afirmarse que la cirugía bariátrica es una excelente alternativa para normalizar los lípidos en sangre en los pacientes obesos. En el metaanálisis de Buchwald (2004)10 se analizaron 1,985 pacientes con dislipidemia entre cirugías restrictivas y mixtas y se presentó una resolución media de 85.62%, de los cuales los mejores resultados fueron con la derivación biliopancreática (99.5%), el BPG en segundo lugar (93.6%) y los resultados más bajos fueron con la banda gástrica ajustable (71.1%); en este metaanálisis no se evaluó la efectividad de la gastrectomía en manga. En un metaanálisis más reciente de Li J y cols. (2016)25 se analizaron 14 estudios comparativos que en conjunto sumaban 1,269 pacientes (BPG versus MG). Los autores observaron el control de las dislipidemias en 95% en el grupo de bypass gástrico. Otros reportes recientes tienen resultados muy similares.6,17,19,26
A pesar de que todos los pacientes con obesidad padecen esteatosis hepática, no todos muestran inflamación. Nuestro estudio reveló que cerca de 85% de los pacientes tenían inflamación; es decir, esteatohepatitis no alcohólica (NASH). Con la cirugía solamente tres pacientes no revirtieron la inflamación. Dos de éstos fueron sometidos a tratamiento médico y clínicamente (con laboratorio y elastografía) se observó que detuvieron el proceso inflamatorio; el tercer paciente desarrolló cirrosis. Varias publicaciones han comprobado que la cirugía bariátrica reduce el grado de esteatosis, inflamación y fibrosis hepática.27,28 Hafeez y Ahmed encontraron 12 reportes con 576 pacientes obesos con NASH, una remisión de inflamación y fibrosis entre 83 y 50%.29
Antes de la cirugía se detectaron 67 (41.8%) de 160 pacientes con HTA y al año siete (4.93%) continuaron con esta condición, lo que significa que nuestra población tuvo una resolución de la HTA al año de 89.56%. Estos resultados están por arriba de los referidos en el metaanálisis de Buchwald y cols.10 en el grupo de bypass, ya que sólo 75.4% de los pacientes remitieron y 87.1% mejoraron. Por el contrario, nuestros resultados fueron inferiores a los reportados en el metaanálisis reciente de Li y cols., quienes reportan una resolución de 95% de los casos en su grupo de BPG.25
De 28 pacientes que presentaron apnea de sueño solamente un paciente que al inicio pesaba 258 kg persistió con el problema a los 12 meses. Se le practicó MG y a los dos años se llevó a cabo cirugía de conversión (BPGYR), con la que controló aún más su peso y se resolvió su problema respiratorio después de dos años. Los dos metaanálisis antes mencionados reportan un promedio de resolución de 95% de los problemas respiratorios, principalmente con el BPGYR.10,25
De igual forma, de los 22 pacientes que se detectaron con problema de osteoartritis de columna, cadera, tobillos o rodillas, sólo una persistió y tuvo que ser derivada a ortopedia para el manejo quirúrgico de las rodillas.
Finalmente, comentamos que se detectaron 25 pacientes que presentaron urea o creatinina elevada en el preoperatorio, aunque ninguno que necesitara tratamiento dialítico. Estos pacientes mostraron al año cifras normales en dichas variables.
Conclusiones
Se logró conocer los resultados a corto plazo de la cirugía bariátrica en 160 pacientes intervenidos quirúrgicamente en el Antiguo Hospital Civil de Guadalajara con BPGYR y GVM.
La cirugía bariátrica es una alternativa de tratamiento segura para el control de la obesidad y sus comorbilidades, principalmente de la DM, dislipidemias, NASH, HTA y en general controla el síndrome metabólico con una disminución del riesgo de muerte temprana.
Nuestros resultados mostraron concordancia con los obtenidos en la literatura internacional actual.
Consideramos que es indispensable establecer un grupo multidisciplinario con protocolos de manejo actualizados y la participación de cirujanos calificados para obtener buenos resultados.
Aunque nuestros resultados son muy alentadores en todas las variables medidas hasta el cierre de la evaluación, esperamos continuar en el futuro con el seguimiento y evaluación de los pacientes para determinar los efectos de la cirugía bariátrica a largo plazo.











 nueva página del texto (beta)
nueva página del texto (beta)