Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Cirujano general
versão impressa ISSN 1405-0099
Cir. gen vol.33 no.3 Ciudad de México Jul./Set. 2011
HISTORIA DE LA CIRUGÍA
Unidad de Microcirugía: 30 años de experiencia clínica, entrenamiento continuo e investigación
Microsurgery unit: 30 years of clinical experience, continuous training and research
Luis Padilla, Jesús Tapia-Jurado, Jonathan Goldberg, Takeshi Landero, Pilar Carranza, Mauricio Di Silvio
Unidad de Microcirugía, Servicio de Cirugía Experimental Centro Médico Nacional ''20 de Noviembre'', Instituto de Seguridad y Servicios Sociales para los Trabajadores del Estado (ISSSTE) y Unidad de Microcirugía, Departamento de Cirugía, Escuela de Medicina, Universidad Nacional Autónoma de México (UNAM)
Correspondencia: Dr. Luis Padilla M.D.
Millet Núm. 83-206, Col. Extremadura Insurgentes, México D.F. 03740
E-mail: lpadilla@issste.gob.mx padilu@servidor.unam.mx
Recibido para publicación: 9 abril 2011
Aceptado para publicación: 11 mayo 2011
Resumen
Se describen 30 años de actividades clínicas, entrenamiento e investigación en dos Unidades de Microcirugía. El Servicio de Cirugía Experimental del Centro Médico Nacional (CMN) ''20 de Noviembre'' del ISSSTE y el Departamento de Cirugía de la Facultad de Medicina de la UNAM, ambos de la Ciudad de México; participando en 121 casos clínicos resueltos con técnicas microquirúrgicas en 7 diferentes especialidades.
En el ISSSTE, de 1977 a 2007, se han impartido 104 cursos de ''Microcirugía vascular'' y entrenado a 453 cirujanos y residentes de especialidades quirúrgicas. En la UNAM, de 1984 a 2007 se han entrenado 364 alumnos en 67 cursos.
Desde 1979 hemos estudiado experimentalmente microprótesis vasculares de origen biológico o sintético de 1 y 2 mm de diámetro, en sustitución de segmentos de aorta y vena cava en rata, generando seis publicaciones. Desde 1996 estamos trabajando el fenómeno de ''angiogénesis'' como tratamiento de miembros inferiores con isquemia crítica. Con base en los trabajos previos, el Comité de Investigación y Ética del CMN aprobó un protocolo de investigación en pacientes con dicha patología, acumulando a la fecha 26 extremidades con trasplante de células endoteliales progenitoras, derivadas de la médula ósea, aplicadas por inyección intramuscular y por vía venosa distal a nivel de vena safena. Del 2004 al 2009 se han amputado 5 extremidades y salvamento de 21; los resultados del estudio se encuentran en evaluación para su publicación.
Los hospitales con programas de formación de residentes en especialidades quirúrgicas, deben contar con laboratorio de microcirugía para entrenamiento básico, continuo y diseño de protocolos de investigación, ofreciendo a los pacientes soluciones con técnicas microquirúrgicas.
Palabras clave: Microcirugía vascular, entrenamiento continuo, investigación, angiogénesis.
Abstract
We describe 30 years of clinical, training and research activities in two Microsurgery Units. The Experimental Surgery Service of the National Medical Center ''20 de Noviembre'' from the ISSSTE (Mexican Health and Welfare Institute for government employees) and the Department of Surgery of the School of Medicine, UNAM (National Autonomous University of Mexico), both located in Mexico City, participating in 121 clinical cases resolved with microsurgical techniques in seven different specialties.
At the ISSSTE, from 1977 to 2007, 104 courses on ''Vascular Microsurgery'' have been given and 453 surgeons and residents have been trained in surgical techniques. At the UNAM, from 1984 to 2007, 364 students have been trained in 67 courses.
Since 1979, we have experimentally studied vascular microprostheses of biological or synthetic origin of 1 to 2 mm in diameter in substitution of aorta and cava vein segments in rats, giving rise to six publications. Since 1996, we have been studying the ''angiogenesis'' phenomenon as treatment for lower extremities with critical ischemia. Based on previous studies, the Ethics and Research Committee of the ISSSTE-Medical Center approved a research protocol in patients with that pathology, accumulating, until this date, 26 extremities with bone marrow-derived stem cells, applied through intramuscular injection and through distal venous route at the level of the saphenous vein. From 2004 to 2009, five extremities have been amputated and 21 have been saved; the results of the study are being evaluated for publication.
Hospitals with programs for the training of residents in surgical specialties must have a laboratory of microsurgery for the basic and continuous training and for the design of research protocols, to be able to offer solutions to the patients with microsurgical techniques.
Key words: Vascular microsurgery, continuous training, research, angiogenesis.
Introducción
La microcirugía es ampliar o magnificar un campo operatorio utilizando sistemas ópticos (lupas, telelupas, microscopio de operaciones o lente para cirugía endoscópica) -lo que nos permite una disección y reparación de tejidos con una mayor calidad y precisión.
La microcirugía no es una especialidad, es una técnica quirúrgica que debe ser dominada por todos los especialistas en cirugía (cirugía general, cirugía vascular, cirugía reconstructiva, urología, neurocirugía, cirugía pediátrica, ginecología, ortopedia etcétera).
El entrenamiento en microcirugía requiere de cursos bien estructurados que ofrezcan al alumno conocimientos teóricos, demostraciones microquirúrgicas por un profesor experto y repeticiones de las técnicas bajo supervisión.
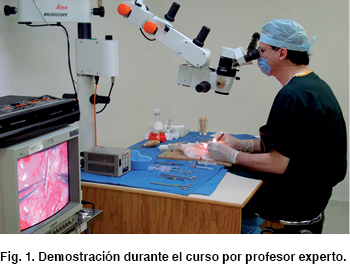
Es indispensable que cada alumno cuente con ''su microscopio'', ''su charola de microinstrumentos'', microsuturas y ratas de laboratorio (Figura 1). Una unidad de microcirugía de calidad debe ofrecer además videos de procedimientos microquirúrgicos básicos, experimentales y de casos clínicos, además de libros y revistas actualizados. Desafortunadamente no todas las instituciones hospitalarias que tienen programas de formación de especialistas cuentan con laboratorios de cirugía experimental y unidades de microcirugía.
En este artículo describimos 30 años de actividades clínicas, de entrenamiento e investigación en dos unidades de microcirugía -el Servicio de Cirugía Experimental del Centro Médico Nacional ''20 de Noviembre'' del Instituto de Seguridad y Servicios Sociales para los Trabajadores del Estado (ISSSTE) desde 1977 y el Departamento de Cirugía de la Facultad de Medicina de la Universidad Nacional Autónoma de México (UNAM) desde 1984.
En julio de 1976, se llevó a cabo el IV Congreso de la International Microsurgical Society (IMS) en el Instituto Nacional de Nutrición ''Salvador Zubirán'' de la Ciudad de México, organizado por el Dr. Federico Chávez Peón, entonces Jefe de la Unidad de Trasplantes y Microcirugía Experimental (Figura 2), el congreso fue realizado con éxito en el auditorio del hospital, pero lo que dejó mayor huella entre los cirujanos mexicanos fue el ''Surgical Skill Station'' de demostraciones de microcirugía experimental que se implementó en cinco mesas, donde el Dr. Sun Lee (padre de la microcirugía experimental)1 (Figura 3) y otros pioneros de la microcirugía realizaron anastomosis de aorta, derivación portocava, trasplante renal, trasplante cardíaco y trasplante hepático en ratas. El impacto fue tan grande que un grupo de cirujanos mexicanos le solicitaron al Dr. Chávez Peón que diseñara un curso con el Dr. Sun Lee, el cual fue llevado a cabo del 21 al 28 de noviembre de 1976.

Este curso motivó a que varios de los alumnos del Dr. Lee organizaran en sus laboratorios de cirugía experimental, de diferentes unidades hospitalarias, programas de entrenamiento en microcirugía, destacando el Dr. Trifón de la Sierra, el Dr. Alberto Chousleb, el Dr. Mauro Loyo y el Dr. Rubén Cortés.
Entrenamiento en microcirugía vascular y casos clínicos
Nosotros iniciamos nuestro Curso de ''Microcirugía vascular'' en el Centro Médico Nacional ''20 de Noviembre'' en la Ciudad de México en junio de 1977, con el apoyo del entonces Jefe del Servicio de Cirugía Experimental, Dr. Armando Valle, el cual fue impartido a cinco Jefes de Servicios Quirúrgicos, quienes a su vez enviaron a sus médicos de base y residentes a entrenarse en el laboratorio con la idea de poder desarrollar aplicaciones clínicas de la microcirugía.
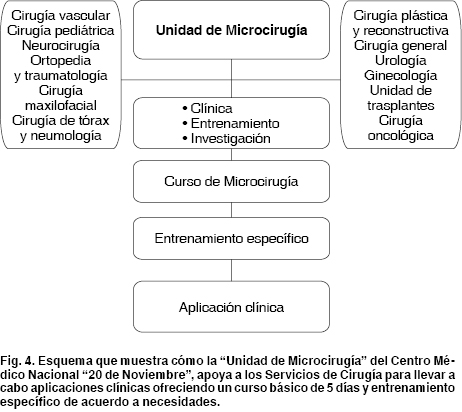
Desde entonces inicia el concepto de ''Unidad de Microcirugía'' con la idea de apoyar a todos los servicios quirúrgicos del hospital con el fin de resolver casos clínicos con técnicas de microcirugía, ofreciendo un curso básico de cinco días y un programa de entrenamiento continuo específico de acuerdo a la necesidad clínica, además de apoyar en los procedimientos de urgencias (Figura 4). En 30 años, nuestra unidad de microcirugía ha participado directamente en 121 casos clínicos en siete diferentes especialidades, disminuyendo su frecuencia a medida que se multiplica la capacidad de nuestros cirujanos y residentes entrenados (Cuadro I).

En vista de la gran demanda hacia la microcirugía como destreza, en agosto de 1984 iniciamos el mismo programa de ''Microcirugía vascular'' en el Departamento de Cirugía de la Facultad de Medicina de la UNAM con el apoyo inicial del Dr. Alberto Chousleb y ahora con el Dr. Jesús Tapia.
Nuestro Curso de Microcirugía se imparte tres veces al año en el Centro Médico Nacional ''20 de Noviembre'' del ISSSTE y cuatro en la Facultad de Medicina de la UNAM, teniendo duración de cinco días; durante el primer día se desarrollan temas teóricos como: Historia de la microcirugía, aplicaciones experimentales y clínicas de la microcirugía, técnicas de microanastomosis vasculares y anatomía, biología y manejo de la rata de laboratorio. También durante el primer día se llevan a cabo dos demostraciones quirúrgicas por un profesor experto No. 1: Manejo anestésico de la rata y laparotomía exploradora con disección de aorta y cava y No. 2: Microsuturas en cartilla de entrenamiento (lámina de látex) con magnificación con microscopio de operaciones, iniciando de menor a mayor aumento y con material de sutura de mayor a menor calibre.
El segundo día se demuestra la técnica de anastomosis de aorta abdominal término-terminal, con material de sutura de 8 y 9 ceros. Seguida de dos repeticiones por la mañana y dos por la tarde.
El tercer día se hace la demostración de la técnica de anastomosis de vena cava abdominal término-terminal, con material de 9 y 10 ceros. Y repitiendo el modelo de aorta abdominal término-terminal antes de intentar la repetición de vena cava en cuatro ocasiones como mínimo.
El cuarto día se demuestra la técnica de anastomosis de arteria iliaca-iliaca término-lateral con 10 ceros y antes de intentar la anastomosis de iliacas, se repite el modelo de anastomosis de aorta abdominal término-terminal.
Finalmente el quinto día demostramos a los alumnos las técnicas de anastomosis de arteria y vena femorales con material de sutura de 10 ceros. Igual que los días anteriores se inician las repeticiones con anastomosis de aorta y después los vasos femorales. Como evaluación final solicitamos a los alumnos que realicen una anastomosis de aorta abdominal término-terminal para poder aprobar el curso y recibir el diploma de reconocimiento (Cuadro II).

Sólo aceptamos cinco alumnos por curso con el fin de otorgar asesoría de calidad y que cada uno cuente con su microscopio de operaciones y charola de instrumentos.
Las demostraciones microquirúrgicas las llevamos a cabo en una mesa especial con microscopio de operaciones, conectado a un monitor para que los alumnos observen todos los detalles de la técnica y tengan facilidades de grabación (Figura 1).
Para apoyar el desarrollo de las sesiones prácticas y que los alumnos pudieran consultar los detalles de las técnicas; en 1983 editamos un ''Manual de microcirugía'' que en la actualidad sigue siendo de utilidad.2
En un periodo de 30 años hemos impartido 104 cursos de ''Microcirugía vascular'' y entrenado 453 cirujanos y residentes de especialidades quirúrgicas en el Centro Médico Nacional ''20 de Noviembre'' del ISSSTE y en la Facultad de Medicina de la UNAM en 23 años, 67 cursos con 364 alumnos (Figura 5).

Investigación microquirúrgica
Desde 1979, nuestro grupo tuvo interés por estudiar experimentalmente con microprótesis vasculares de origen biológico o sintético de 1 y 2 mm de diámetro, utilizando como modelo la sustitución de segmentos de aorta y vena cava en la rata. La justificación de la línea de investigación está fundamentada en la necesidad de contar con este material para resolver casos de microcirugía clínica en ausencia de venas autólogas necesarias para restablecer la circulación arterial y venosa de colgajos libres, reimplantes y trasplantes de tejidos.
En el cuadro III mostramos seis publicaciones en el periodo de 1983 a 1996, que reportan los resultados en permeabilidad de materiales como microprótesis de origen bovino tratadas con pepsina-dialdehído y ficina-dialdehído, politetrafluoroetileno y arterias umbilicales humanas tratadas con glutaraldehído.3-8

Durante el desarrollo del trabajo experimental, en el que utilizamos microprótesis de origen biológico con tubos de fibrocolágena,8 llamó nuestra atención la red vascular externa de neoformación durante la preparación y disección del tubo de silastic en el tejido celular subcutáneo de la rata, por lo que iniciamos una revisión bibliográfica sobre el fenómeno de angiogénesis '' in vitro '' e '' in vivo '' y encontramos que los grupos de investigación de Symes9 Baffour10 e Isner,11 demostraron que, aplicando citocinas como el factor estimulante beta de crecimiento de fibroblastos (bFGF) y el factor estimulante de crecimiento de las células endoteliales (VEGF) por vía intramuscular en conejos con isquemia experimental en miembros inferiores, lograban la proliferación de vasos de neoformación (angiogénesis).
En 1994, Jackson12 reporta que, agregando heparina y colágena tipo I a un cultivo de células endoteliales, éstas se reproducen y forman tubos capilares '' in vitro ''. En nuestro laboratorio imitamos la técnica de Jackson, pero a nivel de músculo isquémico en miembros inferiores de la rata, formando un túnel muscular fibrocolágeno receptor de células endoteliales y heparina; logrando angiogénesis significativa.13
Asahara14 demuestra que las células mononucleares derivadas de la médula ósea (CD34+) tienen la capacidad de transformarse en células endoteliales progenitoras e inducir angiogénesis.
Utilizando un modelo de isquemia muscular en ratas, nuestro grupo demostró que puede inducirse angiogénesis efectiva al trasplantar células mononucleares derivadas de la medula ósea (células endoteliales progenitoras) en túneles fibrocolágenos, utilizándolos como ''andamiaje'' para facilitar la sobrevida y la diferenciación celular.15 En otro estudio experimental, utilizando cánidos con isquemia muscular en la extremidad inferior, corroboramos que movilizando las células endoteliales progenitoras de la medula ósea a la sangre periférica, posterior a la aplicación del factor estimulante de colonias de granulocitos (G-CSF), filgastrin (Neupogen-Roche) y trasplantándolas en túneles fibrocolágenos se incrementa significativamente la angiogénesis, comparado al trasplante celular sin G-CGF.16
Con estos antecedentes experimentales en animales, obtuvimos la autorización de los Comités de Investigación y Ética del Centro Médico Nacional ''20 de Noviembre'' para iniciar un estudio experimental en seres humanos.
En una primera etapa clínica realizamos el trasplante celular en ocho extremidades inferiores con isquemia crítica de siete pacientes a través de túneles musculares fibrocolágenos; obteniendo las células endoteliales progenitoras de la sangre periférica por citaféresis después de haber movilizado las células de la médula ósea con G-CSF. El resultado inicial fue de mejoría clínica significativa en cinco extremidades y mala evolución en tres, que mejoraron su perfusión vascular proximal pero desarrollaron necrosis de ortejos; interpretamos que en estos tres pacientes el trasplante no logró que las células llegaran a los vasos capilares digitales.
Revisando la bibliografía encontramos dos trabajos clave para desarrollar nuestra nueva hipótesis experimental. El grupo de Gross17 emboliza islotes pancreáticos por vía venosa portal hacia los sinusoides hepáticos, logrando producción de insulina con control de la diabetes y Bartsch18 inyecta células mononucleares en el músculo y por vía intraarterial femoral en pacientes con isquemia de miembros inferiores logrando buenos resultados. Tomando estas ideas (Cuadro IV) diseñamos una técnica de trasplante celular que permite llegar a los vasos capilares digitales a través de la vena safena distal en el pie y evitar la gangrena de ortejos.

Antes de aplicar clínicamente este procedimiento, desarrollamos un estudio experimental en 30 ratas divididas en tres grupos; demostrando mayor grado de angiogénesis en el grupo de trasplante de células endoteliales progenitoras por vía venosa distal.19
En una segunda etapa, a 18 pacientes con isquemia crítica de miembros inferiores que cumplieron con los criterios de inclusión, les aplicamos 300 μg de G-CSF subcutáneos cada 24 horas durante 5 días. El quinto día por medio de citaféresis aislamos 60 ml de concentrado celular por extremidad 1 × 108/ml. células conteniendo CD34+ y CD133+. Los 18 pacientes fueron divididos en dos grupos:
Grupo 1. Nueve pacientes que recibieron el trasplante celular por vía intramuscular.
Grupo 2. Nueve pacientes que recibieron el trasplante celular por vía intramuscular y por vía venosa safena distal.
La evaluación de estos 18 pacientes se está llevando a cabo, analizando el estado clínico de la extremidad (claudicación, dolor en reposo, úlcera, gangrena) temperatura, índice brazo tobillo, presión de primer ortejo, presión parcial de oxígeno, láser Doppler y angiografía; los resultados de este estudio serán motivo de análisis y publicación.
Conclusión
Es importante que hospitales con programas de formación de residentes en especialidades quirúrgicas, cuenten con laboratorio de microcirugía para poder desarrollar cursos de entrenamiento básico y continuo, así como facilidades para diseñar protocolos de investigación y con esto estar en condiciones de ofrecer a los enfermos soluciones con técnicas microquirúrgicas.
REFERENCIAS
1. Lee SH, Fisher B. Portocaval shunt in the rat. Surgery 1961; 50: 668-672. [ Links ]
2. Padilla SL, Valle GA. Manual de microcirugía. Editorial Salvat. México, 1983. [ Links ]
3. Padilla SL, Valle GA, Sánchez CR. Trasplante en ratas de arterias bovinas pretratadas con enzimas proteolíticas Arch Inst Cardiol Méx 1983; 53: 91-98. [ Links ]
4. Padilla L, Sastre N, Chousleb A, Di Silvio M, Contreras M, Manzano B, et al. Polytetrafluoroethylene microprosthesis in the venous system of the rat. J Reconstr Microsurg 1987; 3: 159-163. [ Links ]
5. Padilla L, Valle A, Carrillo H, Di Silvio M, Contreras M, Viniegra F, et al. Polytetrafluoroethylene microprosthesis in the arterial system of the rat. J Reconstr Microsurg 1987; 4: 33-37. [ Links ]
6. Padilla SL, Chousleb KA, Di Silvio LM, Viniegra RF, Shultze RA, Sánchez CR, et al. Injertos vasculares biológicos para microcirugía. Rev Fac Med UNAM 1990; 33: 11-18. [ Links ]
7. Padilla SL, Chousleb KA, Rocha HG, Di Silvio LM, Viniegra RF, Vázquez CJ, et al. Microprótesis de politetrafluoroetileno de pared delgada. Rev Méx Angiol 1991; 19: 14-19. [ Links ]
8. Padilla SL, Carrillo-Soto IA, García GMV, Valdés GR. Angiogénesis inducida por túneles fibrocolágenos. Cir Gen 1996; 18: 123-128. [ Links ]
9. Pu LQ, Arekat Z, Brassard R, Symes JF. Demonstration of significantly enhanced neovascularitization by angiogenic stimulation in the ischemic limb. Surg Forum 1992; 43: 368-370. [ Links ]
10. Baffour R, Berman J, Garb JL, Rhee SW, Kaufman J, Friedman P. Enhanced angiogenesis and growth of collaterals by in vivo administration of recombinant basic fibroblast growth factor in a rabbit model of acute lower limb ischemia: dose-response effect of basic fibroblast growth factor. J Vasc Surg 1992; 16: 181-191. [ Links ]
11. Bauters C, Asahara T, Zheng LP, Takeshita S, Bunting S, Ferrara N, et al. Site-specific therapeutic angiogenesis after systemic administration of vascular endothelial growth factor. J Vasc Surg 1995; 21: 314-25. [ Links ]
12. Jackson CJ, Giles I, Knop A, Nethery A, Schrieber L. Sulfated polysaccharides are required for collagen. Induced vascular formation. Exp Cell Res 1994; 215: 294-302. [ Links ]
13. Padilla SL, Figueroa BS, De León D, Carrillo SI, King-MAC, Schalch LP, et al. Angiogénesis inducida por colágena polivinilpirrolidona y heparina en el músculo isquémico. Cir Cir 1999; 67: 59-65. [ Links ]
14. Asahara T, Murohara T, Sullivan A, Silver M, van der Zee R, Li T, et al. Isolation of putative. Progenitor endothelial cells for angiogenesis. Science 1997; 275: 964-967. [ Links ]
15. Padilla SL, Krötzsch E, Schalch LP, Figueroa BS, Miranda A, Rojas E, et al. Administration of bone marrow cells into surgically induced fibrocollagenous tunnels induces angiogenesis in ischemic rat hindlimb model. Microsurgery 2003; 23: 568-574. [ Links ]
16. Padilla L, Krötzsch E, De La Garza AJ, Figueroa S, Rodríguez-Trejo J, Avila G, et al. Bone marrow mononuclear cells stimulate angiogenesis when transplanted into surgically induced fibrocollagenous tunnels: results from a canine ischemic hindlimb model. Microsurgery 2007; 27: 91-97. [ Links ]
17. Goss JA, Soltes G, Goodpastor SE, Barth M, Lam R, Brunicardi FC, et al. Islet transplantation: the radiographic approach. Transplantation 2003; 76: 199-203. [ Links ]
18. Bartsch T, Falke T, Brehm M, Zeus T, Kögler G, Wernet P, Strauer BE. Intra-arterial and intramuscular transplantation of adult, autologous bone marrow stem cells. Novel treatment for therapy-refractory peripheral arterial occlusive disease. Dtsch Med Wochenschr 2006; 131: 79-83. [ Links ]
19. Padilla SL, Rodríguez-Trejo J, Escoto SJ, Flores CJDD, Rodríguez Ramírez N, Krötzsch GE, et al. Trasplante de células mononucleares progenitoras derivadas de médula ósea por vía endovenosa retrógrada distal para inducir angiogénesis en miembros inferiores con isquemia. Cir Gral 2009; 31: 213-218. [ Links ]














