Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista mexicana de ciencias geológicas
versão On-line ISSN 2007-2902versão impressa ISSN 1026-8774
Rev. mex. cienc. geol vol.29 no.2 Ciudad de México Ago. 2012
Datos isotópicos (δ13C, δ18O) de la fauna pleistocénica de la Laguna de las Cruces, San Luis Potosí, México
Isotopic data (δ13C, δ18O) of the Pleistocene fauna from Laguna de las Cruces, San Luis Potosí, Mexico
Victor Adrián Pérez–Crespo1*, Joaquín Arroyo–Cabrales2, Luis M. Alva–Valdivia3, Pedro Morales–Puente4 y Edith Cienfuegos–Alvarado4
1 Posgrado en Ciencias Biológicas, Universidad Nacional Autónoma de México, Ciudad Universitaria, Del. Coyoacán, 04150, México, D.F., México.
2 Laboratorio de Arqueozoología M. en C. Ticul Álvarez Solórzano, Subdirección de Laboratorios y Apoyo Académico, INAH, Moneda 16 Col. Centro, 06060, México, D.F., México.
3 Laboratorio de Paleomagnetismo, Instituto de Geofísica, Universidad Nacional Autónoma de México, Ciudad Universitaria, Del. Coyoacán, 04150, México, D.F., México.
4 Instituto de Geología, Universidad Nacional Autónoma de México, Circuito de la Investigación Científica S/N, Ciudad Universitaria, Del. Coyoacán, 04150 México, D.F., México. * vapc79@gmail.com
Manuscrito recibido: Junio 20, 2011.
Manuscrito corregido recibido: Noviembre 4, 2011.
Manuscrito aceptado: Noviembre 8, 2011.
RESUMEN
Por medio de los marcadores biogeoquímicos δ13Cy δ18O, se determinó la dieta y el hábitat de tres mamíferos extintos, Camelops hesternus, Equus sp. y Mammuthus columbi encontrados en Laguna de las Cruces (San Luis Potosí, México). Las comparaciones realizadas entre ellos indican que no existen diferencias en cuanto a su dieta, siendo clasificados como organismos con dieta mixta C3/C4. Camelops hesternus fue el que presentó el mayor consumo de plantas C4, mientras que Mammuthus columbi y Equus sp. incluían más plantas C3 en su dieta. Estas pequeñas diferencias en su alimentación explicarían su coexistencia en el sitio, el cual fue un pastizal con algunos árboles, durante el Pleistoceno Tardío.
Palabras clave: Camelops hesternus, Equus sp. Mammuthus columbi, dieta, hábitat, partición de recursos, México.
ABSTRACT
Using bioegeochemical markers δ13C and δ18O, we determined the diet and habitat of three extinct mammals: Camelops hesternus, Equus sp. and Mammuthus columbi, found in Laguna de las Cruces (San Luis Potosí, México). The statistical comparisons assayed among them showed that there are not differences in their diet since all of them may be classified as C3/C4 mixed feeders. Camelops hesternus used to have the major consumption of C4 plants, meanwhile Mammuthus columbi and Equus sp. ate more C3plants. Those little differences in their feeding habits should explain their coexistence them at the site, that was a grassland with some trees, during Late Pleistocene.
Key words: Camelops hesternus, Equus sp. Mammuthus columbi, diet, habitat, resource partition.
INTRODUCCIÓN
En la Laguna de las Cruces (San Luis Potosí, México) durante el Pleistoceno Tardío (Rancholabreano) coexistieron el camello (Camelops hesternus), el caballo (Equus sp.) y el mamut de las praderas (Mammuthus columbi) (Alvarez, 1982). Basado en la morfología dental, se ha asumido que estas especies tenían hábitos alimentarios y de hábitat similares ya que, por presentar molares hipsodontos, se les ha considerado como mamíferos pacedores y habitantes de pastizales o praderas (McDonald y Pelikan, 2006; Johnson et al., 2006a).
Sin embargo, la presencia de molares hipsodontos no significa necesariamente que un organismo se alimente exclusivamente de pastos; por ejemplo se ha observado que las cebras actuales son capaces de consumir, sin problemas, hojas de árboles (Beaver y Brussard, 2004). Pérez–Crespo et al. (2009) usando la razón isotópica 13C/12C presente en el esmalte dental de 14 especímenes de caballo y uno de mamut del yacimiento de Cedral (San Luis Potosí), encuentran que aunque ambos animales consumían importantes cantidades de plantas C4 (pastos), también incluían en su dieta plantas C3 (hojas de árboles o arbustos) corroborado esto por el registro palinológico que indica la presencia de pastos y árboles en la zona. En el caso de la Laguna de las Cruces, el análisis isotópico realizado en cuatro especímenes de mamut revela que estos individuos, en promedio, exhibían una dieta mixta C3/C4 (Pérez–Crespo, 2007); sin embargo, dado que en Laguna de las Cruces solo se analizó anteriormente una especie de herbívoro, el propósito de este trabajo es evaluar la dieta y el hábitat de otros herbívoros, C. hesternus y Equus sp., presentes en Laguna de las Cruces (San Luis Potosí) y comparar si las tres especies de herbívoros de esta localidad tienen los mismos hábitos alimentarios y de hábitat, como se ha propuesto (Kurtén y Anderson, 1980) o estos cambian.
Isótopos estables de carbono y oxígeno
Existen tres formas de evaluar la dieta y el hábitat en especies extintas, los estudios basados en el actualismo biológico, los análisis morfofuncionales y el empleo de los marcadores biogeoquímicos (Nieto y Rodríguez, 2003). Estos últimos se basan en la cuantificación de las proporciones de 13C/12C, 18O/16O y 15N/14N presentes en el apatito del esmalte (δ13C, δ18O) o el colágeno del hueso (δ13C, δ15N, δ18O) (Land et al., 1981; Koch et al., 1998; Ferannec y MacFadden, 2000; MacFadden et al., 2004; Feranec, 2005; Pérez–Crespo et al., 2010a).
En el caso del carbono, éste se halla presente en la atmósfera en forma de CO2, siendo las plantas los primeros seres vivos en incorporarlo, por medio de las vías fotosintéticas C3 (ciclo Hatch–Slack), C4 (ciclo Calvin–Benson) y CAM (Metabolismo Ácido Crasuláceo) (O'Leary, 1988; Farquhar et al., 1989; Ricalde y Andrade, 2009). En el caso de las plantas C3, presentes en árboles y arbustos dicotiledóneos principalmente y, en algunos pastos de zonas frías (Medrano y Flexas, 2001), el primer producto que se obtiene al fijar una molécula de CO2 es la ribulosa–bifosfato–carboxilasa y estas plantas exhiben valores de δ13C entre –22‰ y –35‰ con una media de –26%o (Koch et al., 1989; Lee–Thorp et al., 1989;Cerling et al.,1997).
Por otro lado, para las plantas C4, las cuales son principalmente pastos y algunos árboles y arbustos dicotiledóneos de zonas cálidas (Cerling, 1999; Stowe y Teeri, 1978), la primera molécula obtenida por medio de la fotosíntesis es la fosfoenol–piruvato–carboxilasa, siendo los valores de δ13C de estas plantas de –10‰ a –14‰ con una media de –12% (Bender, 1971; Smith y Epstein, 1971; Keeley y Rundel, 2003). La ultima vía, la CAM, propia de plantas suculentas como las agaváceas, bromelias y cactáceas, produce valores de δ13C que están dentro del intervalo de los de las plantas C3 y C4 (–10‰ a –30‰), lo que las hace indistinguibles de las otras dos vías fotosintéticas (Andrade et al., 2007).
El δ13C de las plantas se incorpora a los tejidos de los herbívoros, por lo que se puede inferir el tipo de plantas con el que el animal se alimentó; así en el caso del apatito del esmalte dental, el δ13C es incorporado por medio del HCO3 de la sangre proveniente del CO2 (Schwarcz, 2000; Martínez del Río y Wolf, 2005); esta reacción es controlada por la temperatura corporal, lo que provoca, que en mamíferos de talla mediana y grande exista un incremento de 14% en los valores de δ13C del apatito del esmalte dental (Cerling y Harris, 1999). Por lo que, usando la clasificación alimentaría de los herbívoros propuesta por Hofmann y Stewart (1972), y modificada por MacFadden y Cerling (1996), se tiene para los animales cuya principal fuente de alimento son las plantas C3 (ramoneadores), valores de –9‰ a –19‰; los que consumen plantas C4 (pacedores) muestran valores de 2‰ a –2‰; aquellos que usan ambos tipos de plantas (dieta mixta) exhiben valores de –2‰ a –9‰.
El oxígeno, en cambio, ingresa a los organismos principalmente por el agua que es bebida y, en menor medida por el agua de los alimentos, así como el que es inhalado, y se encuentra en equilibrio con el oxígeno que es perdido por el sudor, la orina, las heces y la exhalación (Bryant y Froelich, 1996; Koch et al., 1994; Koch., 2007). Dado que el oxígeno ingerido proviene del agua de la precipitación, la cual se halla afectada por la altitud, la latitud, la cantidad de precipitación que cae en una zona y principalmente, por la temperatura (Dansgaard, 1964; Castillo et al., 1985), la composición isotópica del oxigeno en el esmalte dental es usada para inferir aspectos paleoclimáticos y paleoecológicos (Ayliffe et al., 1992; Fricke y O'Niel, 1996; Sánchez, 1997; Sponheirmer y Lee–Throp, 1999; Harris y Cerling, 2000; Levin et al., 2006).
Contexto geográfico y geológico
Laguna de las Cruces se encuentra al oeste del poblado de Salinas en el estado de San Luis Potosí, México (22°43'N y 102°01'W) (Mirambell, 1982; Figura 1). Se realizaron excavaciones arqueológicas controladas, encontrándose restos óseos de M. columbi, Equus sp., C. hesternus y el bisonte Bison bison, infiriéndose que dicho conjunto faunistíco perteneció a la Edad de Mamíferos Rancholabreana (Pleistoceno Tardío) por la presencia del bisonte, acotada entre 120, 000 y 10, 500 años antes del presente (Bell et al., 2004); sin embargo no existe datación alguna que permita determinar con exactitud la edad a la que pertenecen. La estratigrafía local de los sedimentos se encuentra representada por calizas, lutitas del Cretácico y, sobre éstas, rocas ígneas, suelos rojos, turbas y sedimentos lacustres (Figura 2), siendo en estos últimos donde fueron encontrados los restos fósiles (Flores, 1982; Reyes, 1982).


MATERIALES Y MÉTODOS
Preparación de muestras
Los molares usados fueron encontrados en la misma capa estratigráfica, por lo que puede asumirse que son contemporáneos (Álvarez, 1982), y están bajo resguardo de la Colección Paleontológica del Laboratorio de Arqueozoología, Subdirección de Laboratorios y Apoyo Académico, Instituto Nacional de Antropología e Historia con números de catálogo DP2024, DP2027, DP2028, DP2029, DP–2030 (camellos); DP2100, DP2106, DP2121, DP2125 y DP2131 (caballos). Por medio de un taladro Dremel provisto de una fresa de dentista de carburo, se extrajo una muestra (10 mg) cerca en la parte inferior de los molares (raíz) y siguiendo el método propuesto por Feranec y MacFadden (2000); antes de comenzar a extraer el esmalte, los molares fueron limpiados con alcohol y una espátula. En el caso de los mamuts, los valores de δ13C y δ18O fueron tomados de Pérez–Crespo (2007).
Las muestras se prepararon con la técnica descrita por Koch et al. (1997). Una vez extraído el esmalte, éste se pulverizó en un mortero de ágata con pistilo y se tamizó con objeto de obtener un polvo fino. Se le agregaron 10 ml de agua oxigenada al 30% y se mantuvo allí por dos horas; posteriormente el agua se descartó y la muestra se enjuagó tres veces con agua destilada. Una vez concluido el enjuague, se agregó una solución buffer o amortiguadora de ácido acético y acetato de sodio 1 M, dejándose reposar durante nueve horas. Posteriormente la solución se decantó y las muestras volvieron a ser lavadas con agua destilada tres veces. Este pretratamiento elimina cualquier carbonato exógeno que pueda alterar los valores isotópicos de δ13C del esmalte dental (Koch et al., 1997), por lo que no se analizaron las alteraciones diagenéticas.
Finalmente, se les agregó alcohol etílico y se dejaron secar en horno a 90 °C durante 12 horas. Las muestras fueron enviadas al Laboratorio Universitario de Geoquímica Isotópica del Instituto de Geología de la UNAM (LUGIS) y las proporciones isotópicas de éstas fueron medidas en un espectrómetro de Masas Finnigan MAT 253, con sistema dual de introducción de muestras y un equipo auxiliar Gas Bench con un automuestreador GC Pal y plancha de aluminio con termostato acoplado al espectrómetro de masas.
Las medidas de δ18OVPDB y δ13CVPDB en los carbonatos se tomaron de acuerdo al procedimiento descrito por Révész y Landwehr (2002) a 25 °C, utilizando el Gas Bench. Se pesaron 0.6 mg de carbonato en tubos exentainer, utilizando una microbalanza Mettler Toledo MX5 con resolución de 0.000001 g y fueron colocados en una plancha de aluminio a 25 °C; a cada tubo se le inyectó Helio con 99.995% de pureza durante 10 minutos para eliminar el aire, utilizando una aguja de doble vía. Posteriormente se inyectaron 15 gotas de ácido ortofosfórico al 100% con una jeringa con llave. Con ello se liberó el CO2 que posteriormente fue analizado para determinar su composición isotópica, tanto de δ13C como de δ18O. Los resultados han sido expresados con la notación δ y con respecto del estándar internacional PDB (Pee Dee Belemnite Limestone), el cual es un carbonato de origen marino de la formación cretácica Peedee en Carolina del Sur (Craig, 1957). Los cálculos de la δ13CVPDB y la δ18OVPDB fueron obtenidos de acuerdo a las siguientes expresiones: δ13C=(13C/12Cmuestra/13C/12Cvpdb–1) × 1000 y δ18O= (18O/16Omuestra/18O/16Ovpdb–1) × 1000.
Como patrón de trabajo se utilizó un tanque de CO2 con una pureza de 99.998% y los resultados de δ18OVPDB y δ13CVPDB de los carbonatos, se normalizaron utilizando NBS–19, NBS–18 y LSVEC, a la escala VPDB de acuerdo con las correcciones descritas por Coplen (1988) y Werner y Brand (2001). Para esta técnica se tiene una desviación estándar de 0.2% para oxígeno y 0.2% para el carbono.
Análisis estadístico
Se determinaron la media y la desviación estándar de los valores obtenidos de δ13C y δ18O. En el caso de los valores de δ13C, se procedió a determinar el porcentaje de plantas C4 (X) consumido (%C4) usando la ecuación propuesta por Koch et al. (2004):
(100)δ13Cmuestra=(100–X)δ13C100%C3esmalte+(X)δ13C100%C4esmalte
en donde el valor de δ13C100%C3esmalte es de –12.5‰ y δ13C100%C4esmalte de 2.5‰, que corresponden a los estimados para el Pleistoceno Tardío (Koch, 2007).
Por medio de un Análisis de Varianza (ANOVA), se realizó una comparación entre los valores de δ13C y δ18O de C. hesternus, Equus sp. y M. columbi con objeto de detectar diferencias entre ellos. Para distinguir los grupos estadísticamente diferentes, se usó la Prueba de Tukey–Kramer de agrupamiento de medias (Hammer y Harper, 2006). Asimismo se compararon los valores de 513C de Camelops con estudios previos realizados con C. hesternus en Estados Unidos de America (E.U.A) (Koch et al., 1994, 2004) y, en el caso de los caballos, con los datos obtenidos por Pérez–Crespo et al. (2009) y Nunez et al. (2010) en Cedral y Terapa (México), respectivamente, para observar si mantenían la misma dieta que sus contrapartes estadounidenses y mexicanos o ésta tendía a cambiar por factores geográficos. El nivel de significancia usado en las pruebas estadísticas fue de p<0.05 y el programa usado fue NCCS & PASS (Hintze, 2004). Para inferir el tipo de hábitat en el cual habitaron estas especies, se realizó una comparación de los valores de δ13C y δ18O de estos taxa.
RESULTADOS
A continuación se muestran los resultados obtenidos de δ13C y δ18O para cada uno de los taxa de Laguna de las Cruces (Tabla 1). En el caso de C. hesternus, el promedio de δ13C de esta especie es de –2.0‰, con un valor mínimo que va de –3.6‰ a un máximo de 0.3‰, mientras que el valor promedio de δ18O es de –4.4‰ y se exhibe un intervalo que va de –5.1‰ a –3.5‰. La comparación realizada de los valores de δ13C con los ejemplares de E.U.A. muestran que existen diferencias significativas entre ambos grupos (p<0.013078*, gl: 5, F: 14.18).

M. columbi exhibe un valor promedio de δ13C de –3.0‰ con un intervalo de valores que va de –3.7‰ a –1.9‰, mientras que los valores de oxígeno muestran un promedio de –5.3‰ y un intervalo de –6.2‰ a –3.5‰.
Para Equus sp, los valores de δ13C muestran un intervalo de –7.3‰ a 0.8‰ con un promedio de –3.2‰ y el promedio para el δ18O es de –4.9‰ con un valor mínimo de –5.8‰ y máximo de –4.0 ‰: El ANOVA usado para comparar este conjunto con los caballos de Cedral y Terapa, indica que existen diferencias entre los valores de δ13C de los tres sitios (p<0.005974*, gl: 26, F: 6.28), sin embargo, la Prueba de Tukey muestra que Terapa es diferente al Cedral, pero los valores de δ13C de ambos sitios son estadísticamente semejantes a la Laguna de las Cruces (Tabla 2).

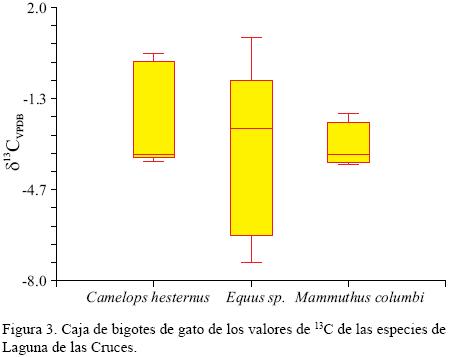
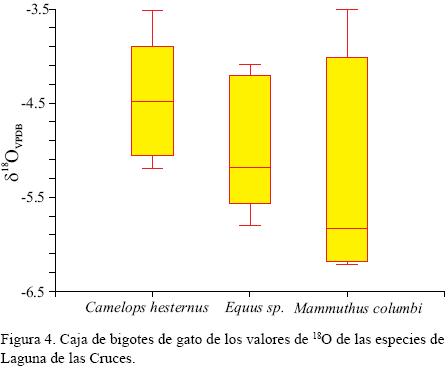
La comparación realizada con los valores de δ13C entre los taxa de Laguna de las Cruces, indica que no existen diferencias significativas entre ellos (p<0.671379, gl: 13, F: 1.20; Figura 3) al igual que los de δ18O (p<0.338848, gl: 13, F: 1.09, Figura 4). La comparación realizada entre los valores isotópicos de δ13C y δ18O entre los taxa muestra que estos dispersan a lo largo del gráfico (Figura 5).
DISCUSIÓN
Hábitos alimentarios
En promedio, la dieta de C. hesternus entra en la categoría de dieta mixta C3/C4 (%C4: 69.6%), con tres individuos que exhiben una dieta mixta C3/C4 y dos con una dieta exclusivamente pacedora C4. Los análisis morfológicos de las mandíbulas y los estudios de microdesgaste de los molares realizados por Dompierre (1995) y Semprebon y Rivals (2010), indican que esta especie era en promedio un organismo con dieta mixta, pero con individuos que presentaban dietas tanto ramoneadoras como pacedoras. Esto explicaría la diferencia encontrada con los individuos de E.U.A, quienes muestran una dieta mixta C3/C4, pero con un importante consumo de plantas C3 (%C4: 26.6%) en comparación con los de Laguna de las Cruces en donde el consumo de plantas C4 era mayor que el de C3.
En el caso de los caballos, también entran en la categoría dieta mixta C3/C4 (%C4: 61.4%), con un individuo con una dieta pacedora (%C4: 89.2%) y cuatro con dieta mixta C3/C4, incluyendo uno con un importante consumo de plantas C3 (%C4: 34.6 %), siendo esto similar a lo encontrado por MacFadden et al.(1999) y Hoppe et al. (2004) en EUA y Pérez–Crespo et al., (2009) en el Cedral (México). Sin embargo, la población de Terapa, ubicada en Sonora, muestra una dieta pacedora en comparación a la mostrada por la población de Laguna; Bravo–Cuevas et al. (2011) señalan que los caballos del Pleistoceno Tardío de Norteamérica poseían una dieta mixta con algunas poblaciones o individuos con dietas pacedoras, lo que indica que este taxa poseía una flexibilidad para incluir diversas cantidades de pastos u hojas de árboles, en sitios cuya vegetación era heterogénea, en su dieta, dependiendo de la disponibilidad de pastos en la zona. Así, en Terapa los pastos abundaban más que los árboles, por lo que su consumo fue mayor que en el Cedral y la Laguna de las Cruces (Pérez–Crespo et al., 2009; Nunez et al., 2010). Los mamuts también muestran una dieta mixta en promedio C3/ C4 (%C4: 62.8%), con un individuo con una dieta pacedora (%C4: 70.6%) y tres con una dieta mixta C3/C4, lo que es similar a lo encontrado con mamuts procedentes de Cedral y Tocuila (Pérez–Crespo et al., 2009 y 2010b).
Dado que la comparación realizada indica que las tres especies tenían las mismas preferencias alimentarias, debía existir algún mecanismo que evitaba la competencia por el alimento (Jaksic, 2001). Arsenault y Owen–Smith (2008) y van Wieren y Bakker (2008) han señalado que en el caso de los mamíferos pacedores africanos, los cuales tienen dietas similares, hay algunas diferencias en la manera de consumir diferentes partes de una misma planta, ingiriendo pequeñas cantidades de hojas de árboles o arbustos, lo que evita que las especies, compitan por el alimento.
En el caso de los ejemplares de Laguna de las Cruces, la especie que tiene el mayor consumo de plantas C4 es C. hesternus con un %C4 de 69.9 (δ13C: –2.0‰), seguida de M. columbi con un %C4 de 62.7% (δ13C:–3.0‰) y, finalmente el que tiene menor ingesta de plantas C4 es Equus sp. (%C4: 61.4; δ13C: –3.2‰). Así, C. hesternus era el más pacedor, tal como sucede con sus contrapartes actuales, los dromedarios, llamas y camellos (Pfister et al., 1989; Mengli et al., 2006); M. columbi posiblemente se alimentaba de herbáceas C4, frutos y hojas de los árboles como los elefantes actuales (Haynes, 1991; Owen–Smith, 1988) y Equus sp., consumía plantas C4 al mismo tiempo que ramoneaba los arbustos y las hojas bajas de los árboles como lo hacen los caballos y cebras actualmente (Beaver y Brussard, 2004; Álvarez–Romero y Medellín, 2005). Estas pequeñas diferencias evitaban una competencia directa por lo que pudieron coexistir en la misma zona, tal como sucede con los herbívoros africanos actuales.
Hábitat
Los valores de δ18O muestran una variación de 2‰ lo cual indica variaciones en la temperatura de hasta 10 ºC. Sin embargo, Caballero et al. (2010) señalan que en México, la temperatura durante el Máximo Glaciar descendió 6 ºC, por lo cual esta variación en los valores isotópicos de oxígeno, no puede ser debida a cambios en la temperatura ambiente, sino posiblemente a diferencias en la cantidad de precipitación que caía en la zona (efecto cantidad), pero también a patrones de migración (MacFadden,2005). En el caso de los mamuts, cuyo intervalo de valores es de 2.7‰, los análisis isotópicos de estroncio realizados por Pérez–Crespo et al. (2011) han demostrado que dos de estos individuos poseen valores de 87Sr diferentes a los otros dos, lo que indica que esta población estaba integrada por individuos de manadas distintas, mismos que pudieron provenir de sitios diferentes y, con ello, ingerir agua con composiciones isotópicas diferentes. Sin embargo, dado que sólo se analizó una especie usando el 87Sr, no se puede afirmar que las variaciones entre los valores isotópicos de δ18O observadas en los caballos (1.7‰) y en los camellos (1.7‰) puedan deberse también al movimiento de estos animales de un sitio a otro o debido al efecto cantidad. En la Figura 5 se puede observar que los caballos se distribuyen a lo largo de todo el gráfico, lo que indica que esta especie vivía en zonas de vegetación completamente abierta, pero también en zonas que tenían algún grado de cobertura arbórea, en cambio los camellos y mamuts preferían las zonas completamente abiertas.
El hábitat de estas especies debió haber sido una zona abierta, un pastizal semejante a las sabanas africanas, con pocos árboles, corroborado esto por la dieta mixta que presentaron estos organismos. Álvarez (1982) y Polaco (1982) indicaron que en la zona debió haber existido un pastizal o una pradera, basados las especies encontradas en este sitio; mientras que Johnson et al. (2006b) han señalado la existencia de un gran pastizal que, en el Pleistoceno Tardío, se extendió desde el Centro de Canadá hacia el Centro de México, lo que incluía a este sitio, que se ubica en la parte central de México; sin embargo, Metcalfe (2006) y Caballero et al. (2010), quienes compilan y analizan el registro palinológico del Centro de México, indican la presencia de bosques templados con pastizales, los cuales se desarrollaron en esta parte del país durante el Pleistoceno Tardío. Asimismo Bravo–Cuevas et al. (2011), con base en los herbívoros encontrados en la parte suroriental de Hidalgo, infirieren que en esta zona, durante el Pleistoceno Tardío, se desarrolló una vegetación abierta junto con áreas arboladas. Los datos isotópicos obtenidos de la fauna de Laguna sugieren un hábitat similar a lo propuesto para Hidalgo.
CONCLUSIONES
Los especímenes de caballo, camello y mamut que vivieron en Laguna de las Cruces, tuvieron una dieta mixta C3/C4 y un hábitat similar; sin embargo, existían pequeñas diferencias entre su régimen alimentario. Así, Camelops hesternus era el que tenía un mayor consumo de plantas C4, mientras que Equus sp. incluía en su dieta importantes aportes de plantas C3. Estas diferencias indican una partición en los recursos alimentarios entre estas especies y explican su coexistencia en el mismo sitio durante el Pleistoceno Tardío, el cual fue un pastizal con pocos árboles, como sugieren estudios previos.
AGRADECIMIENTOS
Al Consejo Nacional de Arqueología del INAH por el permiso para tomar las muestras de esmalte dental. Al Consejo Nacional de Ciencia y Tecnología y al Posgrado en Ciencias Biológicas UNAM por la beca de estudios otorgada al primer autor (# 200441). Al Laboratorio Universitario de Geoquímica Isotópica (LUGIS) del Instituto de Geología de la UNAM y a F. J. Otero y R. Puente M. por analizar las muestras. A los Drs. Juan Pablo Bernal Uruchurtu, Oscar Carranza Castañeda y Antonio García Alix por los comentarios que enriquecieron el presente manuscrito.
REFERENCIAS
Álvarez, T., 1982, Restos óseos animales localizados en las excavaciones, en Mirambell, L (ed.), Laguna de las Cruces, Salinas, S. L. P. Un sitio paleontológico del Pleistoceno final: México, D. F, Instituto Nacional de Antropología e Historia, 62–75. [ Links ]
Álvarez–Romero, J., Medellín, R.A., 2005, Equus burchellii. Vertebrados superiores exóticos en México: diversidad, distribución y efectos potenciales: Instituto de Ecología, Universidad Nacional Autónoma de México. Bases de datos SNIB –CONABIO, Proyecto U020, México, D. F: 7. [ Links ]
Andrade, J.L., de la Barrera, E., Reyes–García, C., Ricalde, M. F., Vargas–Soto, G., Cervera, J. C., 2007, El metabolismo ácido de las crasuláceas: Boletín de la Sociedad Botánica de México, 81, 37–50. [ Links ]
Arsenault, R., Owen–Smith, N., 2008, Resource partitioning by grass height among grazing ungulates does not follow body size relation: Oikos, 117, 1711–1717. [ Links ]
Ayliffe, L.K., Lister, A.M., Chivas, A.R., 1992, The preservation of glacial–interglacial climatic signatures in the oxygen isotopes of elephant skeletal phosphate: Paleogeography, Palaeoclimatology, Palaeoecology, 99,179–191. [ Links ]
Beaver, E.A., Brussard, P.F., 2004, Community–and landscape–level responses of reptiles and small mammals to feral–horse grazing in the Great Basin: Journal of Arid Environments, 59, 271– 297. [ Links ]
Bell, C.J., Lundelius Jr., E.L., Barnosky, A.D., Graham, R.W., Lindsay, E.H., Ruez Jr., D.R., Semken Jr., H.A., Webb, S.D., Zakrzewski, R.J., 2004, en Woodburne, M.O. (ed.), The Blancan, Irvingtonian, and Rancholabrean mammal ages, Late Cretaceous and Cenozoic mammals of North America: New York, Columbia University Press, 232–314. [ Links ]
Bender, M.M., 1971, Variations in the 13C/12C ratios of plants in relation to the pathway of photosynthetic carbon dioxide fixation: Phytochemistry, 10, 1239–1244. [ Links ]
Bravo–Cuevas, V.M., Jiménez–Hidalgo, E., Priego–Vargas, J., 2011, Taxonomía y habitos alimentarios de Equus conversidens (Perissodactyla, Equidae) del Pleistoceno Tardío (Rancholabreano) de Hidalgo, Centro de México: Revista Mexicana de Ciencias Geologícas, 28, 65–82. [ Links ]
Bryant, J.D., Froelich, P.N., 1996, A model f oxygen isotope fractionation in body water of large mammals: Geochimica et Cosmochimica Acta, 59, 4523–4537. [ Links ]
Caballero, M., Lozano–García, S., Vázquez–Selem, L., Ortega, B., 2010, Evidencias de cambio climático y ambiental en registros glaciales y en cuencas lacustres del Centro de México durante el último máximo glacial: Boletín de la Sociedad Geológica Mexicana, 62, 359–377. [ Links ]
Castillo, R., Morales, P., Ramos, S., 1985, El oxígeno–18 en las aguas meteóricas de México. Revista Mexicana de Física, 31, 637–647. [ Links ]
Cerling, T.E., 1999, Paleorecords of C4 plants and ecosystems, en Sage, R.F., Monson, R. K. (eds.), C4 plant biology: USA, Academic Press, 445–469. [ Links ]
Cerling, T.E., Harris, J.M., 1999, Carbon isotope fractionation between diet and bioapatite in ungulate mammals and implications for ecological and paleoecological studies: Oecologia, 120, 347–363. [ Links ]
Cerling, T.E., Harris, J.M., Ambrose, S.H., Leakey, M. G., Solounias, N, 1997, Dietary and environmental reconstruction with stable isotope analyses of herbivore tooth enamel from the Miocene locality of Fort Ternan, Kenya, Journal of Human Evolution, 33, 635–650. [ Links ]
Coplen, T.B., 1988, Normalization of oxygen and hydrogen isotope data: Chemical Geology, 72, 293–297. [ Links ]
Craig, H., 1957, Isotopic Standards for Carbon and Oxygen and correction factors for mass–spectrometric analysis of carbon dioxide: Geochimica et Cosmochimica Acta, 12, 133–149. [ Links ]
Dansgaard, W., 1964, Stable isotopes in precipitation: Tellus, 16, 436–468. [ Links ]
Dompierre, H., 1995, Observations on the diets of six late Cenozoic North American camelids: Camelops, Hemiauchenia, Palaeolama, Procamelus, Alforjas and Megatylopus. Toronto, Canada, University of Toronto, tesis doctoral, 190 pp. [ Links ]
Farquhar, G.D., Ehleringer, J.R., Hibick, K.T., 1989, Carbon isotope discrimination and photosynthesis: Annual Review Plant Physiology Plant Molecular Biology, 40, 503–537. [ Links ]
Feranec, R.S., 2005, Growth rate and duration of growth in the adult canine of Smilodon gracilis, and inferences on diet on the diet through stable isotopes analysis: Bulletin of the Florida Museum of Natural History, 45, 369–377. [ Links ]
Feranec, R.S., MacFadden, B., 2000, Evolution of the grazing niche in Pleistocene mammals from Florida: evidence from stable isotopes: Palaeogeography, Palaeoclimatology, Palaeoecology, 162, 155–169. [ Links ]
Flores, A. D., 1982, Análisis físicos y químicos de la Laguna de las Cruces, en Mirambell, L. (ed.), Laguna de las Cruces, Salinas, S. L. P. Un sitio paleontológico del Pleistoceno final: México, D. F, Instituto Nacional de Antropología e Historia, 35–58. [ Links ]
Fricke, H.C., O'Neil, J., 1996, Inter– and intra–tooth variations in the oxygen isotope composition of mammalian tooth enamel: Some implications for paleoclimatological and paleobiological research: Palaeogeography, Palaeoclimatology, Palaeoecology, 126, 91–99. [ Links ]
Hammer, Ø., Harper, D., 2006, Paleontological data analysis: USA, Blackwell Publishing, 351 pp. [ Links ]
Harris, J.M., Cerling, T.E., 2000, Dietary adaptations of extant and Neogene African suids: Journal Zoological London, 256, 45 –54. [ Links ]
Haynes, G., 1991, Mammoths, mastodonts and elephants. Biology, behavior, and the fossil record: USA, Cambridge University Press, 413 pp. [ Links ]
Hintze, J., 2004, NCSS and PASS: Number Cruncher Stastical System: Kaysville, Utha, www.ncss.com. [ Links ]
Hofmann, R.R., Stewart, D.R.M., 1972, Grazer or browser: a classification based on stomach structure and feeding habits of East Africa ruminants: Mammalia, 36, 226–240. [ Links ]
Hoppe, K.A., Amundson. R., Vavra, M., McClaran, M.P., Anderson, D.L., 2004, Isotopic analysis of tooth enamel carbonate from modern North America feral horses: implications for paleoenvironmental reconstructions: Palaeogeography, Palaeoclimatology, Palaeoecology, 203,299–311. [ Links ]
Jaksic, A. F., 2001, Ecología de comunidades: Chile, Ediciones Universidad Católica de Chile, 233 pp. [ Links ]
Johnson, E., Arroyo–Cabrales, J. Polaco, O., 2006a, Climate, environment, and game animal resources of the Late Pleistocene Mexican grassland, en Jiménez, L.J.C., González, S., Pompa y Padilla, J.A., Ortiz, P.F. (eds.), El hombre temprano en América y sus implicaciones en el poblamiento de la Cuenca de México: México D. F., Instituto Nacional de Antropología e Historia, 231–245. [ Links ]
Johnson, E., Politis, G., Gutierrez, M., Martinez, G., Miotti, L., 2006b, Grassland archaeology in the Americas. From the U.S. southern plains to the argentinean pampas, in Marrow, J.E., Gnecco, C. (eds), Paleoindian archeology. A hemispheric perspective: USA,. The University Press of Florida, 44–65. [ Links ]
Keeley, J.E., Rundel, P.W., 2003, Evolution of CAM and C4 carbon–concentrating mechanisms: International Journal Plants Science, 164 (suplemento 3), S55–S77. [ Links ]
Koch, P.L., 2007, Isotopic study of the biology of modern and fossil vertebrates, en Michener, R., Lajtha, K. (eds.), Stable isotopes in ecology and Environmental Science. Boston, Blackwell Publishing, 99–154. [ Links ]
Koch, P.L., Behrensmeyer, A.K., Fogel, M.L., 1989, The isotopic ecology of plants and animals in Ambroseli National Park, Kenya: Annual Report of the Director of the Geophysical Laboratory, Carnegie Institution of Washington, 1990–1991,163–171. [ Links ]
Koch, P.L., Fogel, M.L., Tuross, N., 1994, Tracing the diets of fossil animals using stable isotopes, en Lajtha, K., Michener, R. H. (eds.), Stable isotopes in Ecology and environmental Science: USA, Blackwell Scientific, 63–92. [ Links ]
Koch, P.L., Tuross, N., Fogel, M.L., 1997, The effects of sample treatment and diagenesis on the isotopic integrity of carbon in biogenic hydroxylapatite: Journal of Archaeological Science, 24, 417–429. [ Links ]
Koch, P.L., Hoppe, K.A., Webb, S.D., 1998, The isotopic ecology of late Pleistocene mammals in North America: Part 1. Florida: Chemical Geology, 152, 119–138. [ Links ]
Koch, P.L., Diffenbaugh, N.S., Hoppe, K.A., 2004,. The effects of late Quaternary climate and pCO2 change on C4 plant abundance in the south–central United States: Palaeogeography, Palaeoclimatology, Palaeoecology, 207, 331–357. [ Links ]
Kurtén, B., Anderson, E., 1980, Pleistocene mammals of North America: USA, Columbia University Press, 442 pp. [ Links ]
Land, L.S., Lundelius, Jr. E.L., Valastro, J.S., 1980, Isotopic ecology of deer bones: Paleogeography, Palaeoclimatology, Palaeoecology, 31, 143–152. [ Links ]
Lee–Throp, J.A., van der Merwe, N., Brain, C.K., 1989, Isotopic evidence for dietary differences between two extinct baboon species from Swartkrans: Journal of Human Evolution, 18, 183–190. [ Links ]
Levin, N.E., Cerling, T.E., Passey, B.H., Harris, J.M., Ehleringer, J.R., 2006, A stable isotope aridity index for terrestrial environments: Proceedings of National Academy Science, 30, 11201–11205. [ Links ]
MacFadden, B.J., 2005, Diet and habitat of toxodon megaherbivores (Mammalian, Notoungulata) from the late Quaternary of South and Central America: Quaternary Research, 64,113–124. [ Links ]
MacFadden, B.J., Cerling, T.E., 1996, Mammalian herbivore communities, ancient feeding ecology, and carbon isotopes: a 10 million–year sequence from the Neogene of Florida: Journal of Vertebrate Palaeontology, 16, 103–115. [ Links ]
MacFadden, B.J., Cerling, T.E., Harris, J.M., Prado, J.L.,1999, Ancient latitudinal gradients of C3/C4 grasses interpreted from stable carbon isotopes of New World Pleistocene horses (Equus) teeth: Global Ecology and Biogeography, 8,137–149. [ Links ]
MacFadden, B., Higgins, P., Clementz, M.T., Jones, D.S., 2004, Diets, habitat preferences, and niche differentiation of Cenozoic sirenians from Florida: evidence from stable isotopes: Paleobiology 30, 297–324. [ Links ]
Martínez del Rio, C., Wolf, B. O., 2005, Mass–balance models for animal isotopic ecology, in Starck, M.J., Tobias, W. (eds.), Physiological and ecological adaptations to feeding in vertebrates: New Hampshire, Science Publishers, 141–174. [ Links ]
McDonald, G.H., Pelikan, S., 2006, Mammoths and mylodonts: Exotic species from different continents in North America Pleistocene faunas: Quaternary International, 142–143, 229–241. [ Links ]
Medrano, H., Flexas., J., 2000. Fotorrespiración y mecanismos de concentración del dióxido de carbono, in Azcón–Bieto, J., Talón., M. (eds.), Fundamentos de Fisiología Vegetal. Madrid, McGraw–Hill Interamericana, 187– 201. [ Links ]
Mengli, Z., Williams, W.D., Guodons, H., Ye, J. 2006, Bactrian camel foraging behavior in a Haloxylon ammodendron (C. A. Mey) dessert of Inner Mongolia: Applied Animal Behavior Science, 99:330–343. [ Links ]
Metcalfe, S.E., 2006, Late quaternary environments ofthe Northern deserts and central trasnvolcanic belt of México: Annals of Missouri Botanical Garden, 92, 258–273. [ Links ]
Mirambell, L., 1982, Las excavaciones, en Mirambell, L. (ed.), Laguna de las Cruces, Salinas, S.L.P. Un sitio paleontológico del Pleistoceno final: Instituto Nacional de Antropología e Historia, 12– 18. [ Links ]
Nieto, M., Rodríguez, J., 2003, Inferencia paleoecológica en mamíferos cenozoicos: limitaciones metodológicas. Palaeocology inferences in cenozoic mammals: methodological constraints: Coloquios de Paleontología, 1, 459–474. [ Links ]
Nunez, E.E., MacFadden, B.J., Mead, J.I., Baez, A., 2010, Ancient forests and grasslands in the desert: Diet and habitat of Late Pleistocene mammals from Northcentral Sonora, Mexico: Palaeogeography, Palaeoclimatology, Palaeoecology, 297, 391–400. [ Links ]
O'Leary, M.H., 1988, Carbon isotopes in photosynthesis: Bioscience, 38, 328–336. [ Links ]
Owen–Smit, R.N., 1988, Megaherbivores. The influence of very large body size on ecology: United Kingdom, Cambridge University Press, 369 pp. [ Links ]
Pérez–Crespo, V.A., 2007, Reconstrucción paleoambiental de una comunidad pleistocenca en México usando isótopos estables (δ13C, δ18O): Oaxaca, México, Instituto Politécnico Nacional, Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional, tesis de,maestría, 65 pp. [ Links ]
Pérez–Crespo, V.A., Sánchez–Chillón, B., Arroyo–Cabrales, J., Alberdi, M. T., Polaco, J.O., Santos–Moreno, A., Benammi, M., Morales–Puente, P., Cienfuegos–Alvarado, E., 2009, La dieta y el hábitat del mamut y los caballos del pleistoceno tardío de El Cedral con base en isótopos estables (δ13C, δ18O): Revista Mexicana de Ciencias Geológicas, 26(2), 347–355. [ Links ]
Pérez–Crespo, V.A., Alva–Valdivia, L.M., Arroyo–Cabrales, J., Polaco, O.J., 2010a, Uso de los marcadores biogeoquímicos δ13C y δ18O en paleoecología de tetrápodos: Arqueo Ciencias, 5, 15–27. [ Links ]
Pérez–Crespo, V.A., Arroyo–Cabrales, J., Benammi, M., Santos–Moreno, A., Morett–A, L., Morales–Puente, P., Cienfuegos–Alvarado, E., 2010b, Carbon isotopic values of tooth enamel of Mammuthus columbi from Tocuila, State of México, México: Current Research in the Pleistocene, 27, 212–214. [ Links ]
Pérez–Crespo, V.A., Schaaf, P., Alva–Valdivia, L.M., Arroyo–Cabrales, J., 2011, Datos preliminares de la isotopía de estroncio aplicada a Mammuthus columbi procedentes de La Laguna de las Cruces (San Luís Potosi) (resumen), en XII Congreso Nacional de Paleontología, Puebla, Puebla, México, p. 108. [ Links ]
Pfister, J.A., San Martín, F., Rosales, L., Sisson, D.V., Flores, E., Bryant, F.C., 1989, Grazing behaviour of llamas, alpacas and sheep in the Andes of Peru: Applied Animal Behaviour Science, 23, 237–246. [ Links ]
Polaco, O.J., 1982, Identificación de restos óseos de Mamut, en Mirambell, L (ed.), Laguna de las Cruces, Salinas, S. L. P. Un sitio paleontológico del Pleistoceno final: México, D. F, Instituto Nacional de Antropología e Historia, 78–87. [ Links ]
Révész, K.M., Landwehr, J.M., 2002, δ13C and δ18O isotopic composition of CaCO3 measured by continuous flow isotope ratio mass spectrometry: statiscal evaluation and verification by application to Devils Hole core DH–11 calcite: Rapid Communications in Mass Spectrometry, 16, 2012–2114. [ Links ]
Reyes, C.M., 1982, Consideraciones sobre la geología del Cuaternario del área, en Mirambell, L (ed.), Laguna de las Cruces, Salinas, S. L. P. Un sitio paleontológico del Pleistoceno final:México, D. F, Instituto Nacional de Antropología e Historia, 22–31. [ Links ]
Ricalde, M.F., Andrade, J.L., 2009, La pitahaya, una delicia del trópico: Ciencia Revista de la Academia Mexicana de Ciencias, 60, 36–43. [ Links ]
Sánchez, B., 1997, Estudio de las variaciones climáticas durante el final del Neogeno a partir del análisis de δ18O (PO43–) en fósiles de mamíferos, en Calvo, J.P.,Morales, J. (eds.), Avances en el conocimiento del Terciario Ibérico: España, 197–200. [ Links ]
Schwarcz, H. P., 2000, Some biochemical aspects of carbon isotopic paleodiet studies, en Ambrose, S.H., Katzenberg, M. A. (eds.), Biochemical Approaches to Paleodietary Analysis: New York, Kluwer Academic/Plenum Publishers, 189–209. [ Links ]
Semprebon, G.M., Rivals, F., 2010, Trends in the paleodietary habits of fossil camels from Tertiary and Quaternary of North America: Paleogeography, Palaeoclimatology, Palaeoecology, 295, 131–145. [ Links ]
Smith, B.N., Epstein, S., 1971, Two categories of13C/12C ratios for higher plants: Plant Physiology, 47, 380–384. [ Links ]
Sponheirmer, M., Lee–Thorp, J.A., 1999, Oxygen isotopes in enamel carbonate and their ecological significance: Journal of Archaeological Science, 26, 723–728. [ Links ]
Stowe, L.G., Teeri, J.A., 1978, The geography distribution of C4 species of the dicotyledonae in relation to climate: The American Naturalist, 112, 609–623. [ Links ]
van Wieren, S.E., Bakker, J.P, 2008, The impact of browsing and grazing herbivores on biodiversity, en Gordon, J., Prinz, H.T (eds.), The ecology of browsing and grazing: USA, Springer, 263–292. [ Links ]
Werner, R.A., Brand, W.A., 2001, Referencing strategies and techniques in stable isotope ratio analysis: Rapid Communications in Mass Spectrometry, 15, 501–519. [ Links ]














