Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias geológicas
versión On-line ISSN 2007-2902versión impresa ISSN 1026-8774
Rev. mex. cienc. geol vol.26 no.3 Ciudad de México dic. 2009
Adsorción y mineralización de atrazina y relación con parámetros de suelos del DR 063 Guasave, Sinaloa
Adsorption and mineralization of atrazine and their relationship with soil parameters in the irrigation distict 063 Guasave, Sinaloa
Luis Carlos González–Márquez y Anne M. Hansen*
Instituto Mexicano de Tecnología del Agua, Paseo Cuauhnáhuac 8532, 62550 Jiutepec, Mor., México. * ahansen@tlaloc.imta.mx
Manuscrito recibido: Noviembre 20, 2008
Manuscrito corregido recibido: Mayo 2, 2009
Manuscrito aceptado: Mayo 8, 2009
RESUMEN
Se investigó el efecto de los parámetros del suelo en la atenuación natural de atrazina en muestras de suelo del distrito de riego 063 (DR 063). Se evaluó la adsorción y la mineralización del herbicida aplicando las guías recomendadas por la Organización para la Cooperación y el Desarrollo Económico (OCDE) y utilizando atrazina con trazador radiactivo (14C–atrazina). Los límites de confianza de 99% de la media para coeficientes de adsorción fueron 0.297–0.587 L kg –1 y para la vida media 2.0–5.8 años. Las isotermas de adsorción del herbicida fueron lineales y los coeficientes obtenidos están en el intervalo de los valores reportados en la literatura para adsorción de atrazina en suelos agrícolas. La mineralización del herbicida fue relativamente lenta, lo cual es un indicador de la falta microorganismos degradadores de este herbicida en las muestras de suelo, debido probablemente a que no ha sido aplicado en años recientes. Las muestras de suelo fueron caracterizadas por su contenido de arena, limo, arcilla, materia orgánica, nitratos y amonio, así como el pH, la conductividad eléctrica y la profundidad del suelo. El análisis de correlación entre la atenuación natural de atrazina y estas propiedades del suelo, muestran una relación negativa entre la adsorción y la profundidad del suelo, así como entre la mineralización de atrazina y el contenido de materia orgánica, la concentración de amonio y la conductividad eléctrica. Esto significa que la atrazina es más móbil debido a la menor adsorción del herbicida a mayor profundidad y la mayor persistencia con el incremento de la concentración de tales componentes. Estos resultados permitirán formular escenarios más realistas sobre la lixiviación de atrazina en suelos agrícolas.
Palabras clave: atenuación natural, región agrícola, vida media, materia orgánica, fertilizantes, salinidad.
ABSTRACT
The effect of soil properties on the natural attenuation of the herbicide atrazine was investigated in soil samples from the irrigation district 063. Adsorption and mineralization of atrazine in soils were evaluated using guidelines recommended by the Organization for Economic Cooperation and Development and radiolabeled (14C) atrazine. Confidence limits of 99% for mean of adsorption coefficients were 0.297–0.587 L kg–1 and for the half life 2.0–5.8 yr. Atrazine adsorption isotherms were linear and adsorption coefficients of the herbicide were in the range reported in the literature for agricultural soils. The mineralization of atrazine in the soil samples was slow, an indicator that soil microorganisms are not adapted to the herbicide. This may be due to a reduction in the application rate of atrazine. Soil samples were characterized for sand, silt, clay contents, as well as organic matter, nitrates, ammonium, pH, and electrical conductivity. The correlation analysis between the natural attenuation of atrazine and soil properties shows a negative relationship between adsorption and soil depth as well as between atrazine mineralization and organic matter, ammonium and electrical conductivity. This means that atrazine is more mobile due to its lower adsorption in deeper soils and more persistent due to the increase in concentrations of such components. The results obtained in this work will be useful in the formulation of better scenarios of atrazine lixiviation in agricultural soils.
Key words: natural attenuation, agricultural region, half life, organic matter, fertilizers, salinity.
INTRODUCCIÓN
La superficie utilizada para la agricultura en México varía entre 20 y 25 millones de hectáreas, de las cuales aproximadamente 3.5 Mha corresponden a 85 Distritos de Riego (CONAGUA, 2007a). Entre los diversos medios utilizados para el control de plagas y enfermedades que afectan la producción agrícola destacan los plaguicidas; en el año 2006 el consumo aparente de plaguicidas en México fue de 95,025 toneladas de las cuales el 47% correspondió a herbicidas (SENER, 2007).
Atrazina (2–cloro–4–etilamino–6–isopropilamino–1,3,5–triazina) es un herbicida ampliamente utilizado en zonas agrícolas de México; aproximadamente en 59% de los DR se aplica atrazina en dosis que van de 0.1 a 4 kg ha–1 año–1 (Villada–Canela, 2006). Pertenece al grupo de los herbicidas triazínicos y es usada para el control selectivo de malezas en cultivos de maíz y sorgo. En el DR 063 se ha aplicado una gran variedad de herbicidas, entre los cuales atrazina fue una de los más utilizados (SEMARNAP–IMTA, 2000).
Por ser un compuesto persistente, atrazina puede representar un riesgo para el ambiente y se asocia con riesgos para la salud, dado que se ha encontrado que llega a contaminar cuerpos de agua (Tappe et al., 2002; Gilliom et al., 2006). En agua, la atrazina se ha relacionado positivamente con cáncer de estómago (Van Leewen et al., 1999) y con afectación al sistema endocrino e inmune de ranas (Hayes et al., 2002; Brodkin et al., 2007). Este herbicida fue introducido al mercado nacional en el año de 1975 (SAGARPA, 2007). Sin embargo, como la atrazina aún no ha sido incluida en las guías ambientales y de salud, no se incluye en los programas de monitoreo de agua ni en los métodos analíticos rutinarios, por lo que se desconoce el destino ambiental de este herbicida en México. Caso contrario a los plaguicidas organoclorados y organofosforados, que se han detectado en agua, sedimentos y biota de ecosistemas costeros del estado de Sinaloa (Galindo–Reyes et al., 1999; González–Farías et al., 2002).
En estudios anteriores se ha encontrado que cambios en diversos componentes del suelo pueden favorecer o inhibir la adsorción y mineralización de atrazina en suelos: fertilizantes (Abdelhafid et al., 2000; Blume et al., 2004; Guillén–Garcés et al., 2007), pH (Weber, 1993 y 1995; Honeycutt y Schabacker, 1994; Houot et al., 2000; Tyess et al., 2006) y contenido de arcillas y de materia orgánica (M.O.) (Ben–Hur et al., 2003; Ling et al., 2005).
Con el fin de evaluar la capacidad de retención y persistencia de atrazina, diferentes autores han investigado los procesos de adsorción y degradación del herbicida en suelos agrícolas (Li et al., 1996; Socías–Viciana et al., 1999; Krutz et al., 2003; Dorado et al., 2003; Coquet 2003; Drori et al., 2005; Inoue et al., 2006). González–Márquez (2005) reporta una vida media (tiempo requerido para que la concentración de atrazina se reduzca a la mitad de su concentración inicial) de atrazina de 120 d para una muestra de suelo del DR 063, Guillén–Garcés et al. (2007) reportan vidas medias en suelos superficiales que van de 4.5 a más de 35 d, mientras que Márquez–Pacheco (2009) reporta vidas medias entre 0.8 y 1.12 años en perfiles de suelo del DR 063. Estudios realizados por Villada–Canela (2006) sobre los procesos de migración de atrazina en suelos de este distrito, indican que existe un riesgo de contaminación del agua subterránea por aplicación del herbicida, debido principalmente a la persistencia de atrazina y la poca profundidad de la zona vadosa. La adsorción y la mineralización de atrazina son los principales procesos involucrados en la atenuación natural de plaguicidas en suelos. Para poder formular escenarios más realistas sobre la lixiviación de atrazina en suelos agrícolas, en este trabajo se investiga el efecto de componentes, así como de la profundidad de suelos del DR 063, en la adsorción y la mineralización de atrazina, considerando datos generados en este trabajo, así como datos generados por Márquez–Pacheco (2009).
Área de estudio
El DR 063 se ubica en el norte del Estado de Sinaloa (Figura 1), cuenta con una superficie agrícola de 108,865 ha en los municipios de Guasave y Sinaloa de Leyva. Limita al norte con el municipio de Choix y con la Sierra Madre Occidental, al sur con el Golfo de California, al este con el DR 074 Mocorito y al oeste con la primera y segunda unidad del DR 075 (CNA–IMTA, 2001). Su localización geográfica está entre los meridianos 108°18'00'' y 108°42'00' de longitud Oeste y los paralelos 25°52'00'' y 25°37'00'' de latitud Norte, a una altitud promedio de 40 msnm (SARH, 1982; CONAGUA, 2007b).
El clima en la zona de influencia del DR 063 es seco sin excedente de humedad durante el año; cálido con régimen normal de calor e invierno benigno. La temperatura media anual es de 23.9 °C; las temperaturas máximas y mínimas son de 42.0 °C y 4.4 °C, respectivamente. La precipitación media anual oscila en los 409 mm y la evaporación media anual es de 2,202 mm (SARH, 1982).
El DR 063 cuenta con dos fuentes de abastecimiento de agua superficial: el Río Sinaloa y el Arroyo Ocoroni (Figura 2). Las aguas del Río Sinaloa se captan en la presa Bacurato, que abastece una superficie de 112,000 ha de riego; mientras que las aguas del Arroyo Ocoroni se captan en la presa El Sabinal, abasteciendo una superficie de 11,235 ha de riego (CNA–IMTA, 2001). En el año 2000 se reportaban conductividades eléctricas (C.E.) de 0.14 mS cm–1 en el agua de dichas presas (CNA–IMTA, 2001).
El DR 063 se ubica sobre el acuífero Río Sinaloa, que en el 2001 contaba con una recarga media anual de aproximadamente 300 Mm3 (Payan y Carvajal, 2001) y presentaba condiciones de subexplotación (Valle, 2002). La C.E. del agua en los pozos utilizados para riego era de 1.4 a 2.3 mS cm–1 (CNA–IMTA, 2001), un orden de magnitud mayor que el agua de las presas. La red general de canales contaba con 1,271 km para riego y 848 km para drenaje (CNA–IMTA, 2001). Entre 1997 y 2001, el agua distribuida en el distrito fue en 87% de presas y 13% de pozos (CNA, 1999a, 2000a, 2001a, 2002a). Las corrientes superficiales no contribuyeron de manera directa en el volumen distribuido para el riego. El DR 063 se encuentra transferido a cinco asociaciones de productores agrícolas, que conforman igual número de módulos de riego (Payan y Carbajal, 2001).
Los suelos de la zona costera del DR 063 provienen de productos de la meteorización y descomposición de las rocas que constituyen la Sierra Madre Occidental, cuyos materiales son transportados por las corrientes fluviales quedando depositados en la planicie costera y en parte llegan al mar, originando suelos aluviales con diferente grado de desarrollo (SARH, 1982). En la Figura 2 se presentan los principales tipos de suelo en el distrito (CONABIO–INIFAP, 1995), de acuerdo con el sistema de clasificación FAO/UNESCO de 1970. Estos suelos son de textura media y fina. Los principales tipos de suelo en el distrito son Vertisol crómico (64.9%), Cambisol eútrico (18.3%), Luvisol crómico (9.4%) y Xerosol háplico (6.2% de la superficie del distrito).
En el distrito se presentan problemas de salinidad debido a las altas tasas de evaporación, los niveles freáticos someros, el uso de aguas salinas para el riego y a la brisa salina (CNA, 2002c). En el año de 1991 se reportaba que 8,680 ha estaban afectada por sales y para el año 2001 la superficie afectada aumentó a 19,209 ha (17.6% de la superficie agrícola), de las cuales sólo 934 ha contaban con drenaje subterráneo (CNA–IMTA, 2001). En la Tabla 1 se presenta la cantidad de superficie afectada por sales y la superficie que cuenta con drenaje subterráneo en el DR 063 (CNA–IMTA, 2001).

Desde el punto de vista de superficies sembradas, los diez principales cultivos en el distrito son el maíz, trigo, garbanzo, soya, frijol, tomate, papa, ejote, sorgo y algodón; estos productos se comercializan en el mercado nacional e internacional. Los cultivos donde se ha utilizado atrazina son los de maíz y sorgo (CNA, 1999b, 2000b, 2001b, 2002b).
El análisis de información referente al DR 063 indica que atrazina ha sido uno de los herbicidas más utilizados, con dosis de aplicación de aproximadamente 0.9 kg ha–1 (Villada–Canela, 2006). Sin embargo, no se tiene información completa sobre el historial de aplicación del herbicida y de las zonas donde se ha aplicado. Una referencia respecto a la aplicación histórica de atrazina en el distrito son las superficies sembradas con los cultivos de maíz y sorgo, donde se podría aplicar el herbicida, y que presentaron un incremento del 2,385% en el periodo de 1969 al 2006. En la Figura 3 se presenta el historial de las superficies sembradas con estos cultivos (CNA, 1999b, 2000b, 2001b, 2002b). Durante el ciclo otoño–invierno 1998–1999 se estimó que en todo el distrito se consumió un total de 13.5 toneladas de atrazina (SEMARNAP–IMTA, 2000). Para el ciclo primavera–verano 2004, la aplicación de atrazina en el DR 063 se había reducido a 250 kg (Villada–Canela, 2006) mientras que para el 2007 no se tienen registros del uso este herbicida (Hernández–Antonio, 2008).

MATERIALES Y MÉTODOS
Muestreo y caracterización de suelos
El muestreo de suelos se realizó durante el mes de marzo de 2007. Las estaciones de muestreo (I, II y III) se situaron sobre tres de los principales tipos de suelo en el DR 063 (Vertisol crómico, Cambisol eútrico y Xerosol háplico), en parcelas donde se siembra maíz. La localización de las estaciones se presenta en la Figura 2.
Se tomaron 12 muestras de suelo, en tres perfiles del DR 063. Las muestras se colectaron con una barrenadora manual, obteniendo 2 kg de suelo que se colocaron en bolsas de plástico y bajo refrigeración en hielo durante el transporte al laboratorio. En la Tabla 2 se presentan las coordenadas geográficas y los tipos de suelo en las estaciones, así como la profundidad de muestreo.

Las muestras de suelo fueron secadas a temperatura ambiente, disgregadas, tamizadas (≤ 2 mm) y almacenadas a 4 °C. En todas las muestras de suelo se midió pH, C.E., nitratos y amonio, así como el contenido de M.O. y textura, de acuerdo con los métodos propuestos por Eckert y Sims (1995), Gartley (1995), Griffin et al. (1995), ASTM (2000) y ASTM (1998), respectivamente. Con la información de la textura de las muestras de suelo y el programa Soil Water Characteristics Hydraulic Properties Calculador (USDA, 2003), basado en funciones de pedotransferencia (Saxton, 1986) se estimó la capacidad de campo (C.C.).
Evaluación de la atenuación natural de atrazina en suelos
Adsorción de atrazina
La adsorción de atrazina en el suelo se determinó de acuerdo con la guía 106 de la Organización para la Cooperación y el Desarrollo Económico (OCDE, 2000). Los experimentos se llevaron a cabo en seis recipientes de Teflon®, poniendo en contacto 4 g de suelo y 10 mL de 0.01 M CaCl2 en un rotador (Cole Palmer modelo 7637) a 100 rpm durante 16 hrs para hidratar los suelos. Posteriormente, a los recipientes se les agregaron diferentes concentraciones de atrazina con trazador radiactivo (14C–atrazina). Se utilizó un recipiente adicional sin suelo para evaluar la cantidad total de trazador radiactivo agregado. A uno de los recipientes no se le agregó trazador radiactivo para cuantificar la radiactividad de fondo. Se completaron los volúmenes en cada recipiente a 20 mL con 0.01 M CaCl2 y la concentración final de atrazina en los recipientes fue de 0.002, 0.02, 0.2 y 2 mg L–1, los recipientes se agitaron durante 3 hrs a 25 ± 1 °C, que se había establecido previamente como el tiempo de equilibrio para la adsorción de atrazina en los suelos (Márquez–Pacheco, 2009). Posteriormente, los recipientes fueron centrifugados a 12,000 rpm durante 15 min. Un mililitro de sobrenadante se homogenizó con 9 mL de cóctel de centelleo (BSC® Amersham Biosciences) y se cuantificaron las emisiones beta de 14C–atrazina en un equipo de centelleo líquido (LS 6500 Beckman Coulter). La eficiencia del equipo es de 96.5 %, con base en el conteo de 104 decaimientos de un estándar de 14C (Beckman Coulter, lote S312102). La concentración de atrazina adsorbida se calculó con base en la diferencia entre atrazina total aplicada y la concentración disuelta, cuantificada en el sobrenadante. Los coeficientes de adsorción fueron calculados según la Ecuación 1.

donde Kd es el coeficiente de adsorción de atrazina; Cads es la concentración de atrazina adsorbida; y Cdis es la concentración de atrazina disuelta.
Mineralización de atrazina
Los experimentos de mineralización se llevaron a cabo según la guía 307 de la Organización para la Cooperación y el Desarrollo Económico (OCDE, 2002). A reactores de vidrio de 250 mL se le agregaron 50 g de suelo (base seca), humedecidos con agua MilliQ®, para alcanzar 50% de la C.C., y 1 mg de atrazina con trazador radiactivo por cada kg de suelo (3.688 kBq de 14C por reactor).Los reactores, con frascos abiertos con 1 N NaOH, fueron tapados herméticamente e incubados a 30 ± 1 °C. La mineralización de atrazina se refiere a la transformación de la molécula en CO2 y NH3 (Figura 4) y se evaluó a través de la medición de 14CO2 capturado en la solución alcalina colocada en frascos dentro de cada reactor. La solución alcalina fue renovada después de cada muestreo y el sistema fue monitoreado durante cinco meses. En cada muestreo se tomaron alícuotas de 1 mL de solución alcalina, las cuales fueron homogenizadas con 9 mL de cóctel de centelleo (BSC® Amersham Biosciences). Las emisiones beta producidas por el decaimiento radiactivo de 14C fueron cuantificadas en un contador de centelleo líquido (LS 6500 Beckman Coulter). Los coeficientes cinéticos de mineralización y la vida media de atrazina se calcularon considerando cinéticas de primer orden (Ecuación 2):

donde C es la concentración de atrazina y k es el coeficiente cinético de mineralización de atrazina. Las vidas medias de atrazina fueron calculados de acuerdo con la ecuación 3:

donde t1/2 es la vida media de atrazina.

Análisis estadístico
Los datos individuales de los parámetros coeficientes de adsorción y vidas medias fueron procesados con el programa DODESYS para el manejo de datos univariados derivados de una distribución normal (Verma y Díaz–González, unpublished). DODESYS se basa en los nuevos valores críticos más precisos y exactos para 33 pruebas de discordancia (Verma y Quiroz–Ruiz, 2006a, 2006b, 2008; Verma et al., 2008), así como para el cálculo de límites de confianza este programa incorpora nuevas ecuaciones de interpolación de t de Student (Verma, 2009). El análisis se realizó antes de hacer el ajuste de curvas entre datos experimentales y el modelo de adsorción, con el fin de eliminar valores atípicos. La relación entre las propiedades físicas y químicas de los suelos estudiados (profundidad, textura, pH, C.E., M.O., nitratos y amonio) y la atenuación natural de atrazina (adsorción y mineralización), se evaluó a través del método de correlación lineal de Pearson (Berthouex y Brown, 2002).
RESULTADOS Y DISCUSIÓN
Los resultados de la caracterización de las muestras de suelo del DR 063 se presentan en la Tabla 3. Se observa que los suelos de todas las estaciones muestran algún grado de salinidad. Las muestras de suelo varían entre muy fuertemente salinos y no salinos según la clasificación propuesta por Gartley (1995). La textura de los suelos es principalmente limosa y arcillosa, y el pH varía entre 7.1 y 8.0, con un promedio de 7.7. El contenido de M.O. está en el rango de 0.5 a 3.7 mg kg–1 y el promedio es de 1.7 mg kg–1; estas concentraciones son típicas de suelos minerales (Tinsley, 2004). La concentración de nitrógeno disponible (suma de NO3–N y NH4–N) en los suelos es de 5.9 a 170 mg kg–1, con un promedio de 32 mg kg–1.
Las isotermas de adsorción de atrazina en las muestras de suelo se presentan en la Figura 5. Las isotermas de adsorción del herbicida fueron lineales, permitiendo describirlas a través del modelo de adsorción lineal, Kd. Cabe aclarar que con tres puntos en la regresión se tiene sólo un grado de libertad (v), para lo cual la línea de regresión sería significativa para 95% de nivel de confianza cuando el coeficiente de ajuste (r) sea mayor o igual que 0.9969 y para 99% de nivel de confianza cuando el r sea mayor o igual que 0.9999 (Bevington y Robinson, 2003; Verma, 2005). Los valores de r reportados en la Figura 5, por lo tanto, demuestran que la regresión lineal es válida para 17 de los 21 casos a nivel de confianza de 95%, mientras que es válida para solamente seis de los 21 casos a nivel de confianza de 99%. Lo anterior nos hace reflexionar que, en el futuro, para este tipo de estudios sería recomendable basarse en un número mayor de datos en las regresiones lineales (Verma, 2005).

En la Tabla 4 se presentan los coeficientes de adsorción de atrazina en las muestras de suelo. Los resultados muestran coeficientes de adsorción de atrazina en el rango de 0.18 a 1.54 L kg–1, con promedio de 0.49 L kg–1. Los coeficientes de adsorción obtenidos están en el intervalo de los valores reportados en la literatura para adsorción de atrazina en suelos agrícolas (Socías–Viciana et al., 1999; Coquet, 2003; Drori et al., 2005). Se observa una tendencia a disminuir la adsorción de atrazina respecto a la profundidad en los perfiles de suelo.

Los resultados de la mineralización de atrazina en las muestras de suelo del DR 063 se presentan en la Figura 6. Se observan cinéticas muy lentas, mineralizándose entre 1.4 y 31.1% del herbicida en más de cinco meses de experimentación. A diferencia de lo publicado anteriormente (Kruger et al., 1993; Accinelli et al., 2001; Hang et al., 2003; Blume et al., 2004), en este trabajo no se observó relación directa entre la profundidad y la mineralización de atrazina (Figura 6). Sin embargo, en la mayoría de los perfiles de suelo estudiados se presentaron cinéticas de mineralización más rápidas en las muestras con menor adsorción de atrazina, es decir a profundidades de 100 cm o mayores. Esto obedece a que los compuestos disueltos están disponibles para los microorganismos, mientras que los compuestos adsorbidos no lo están (Barbash y Resek, 1997). Se calcularon los coeficientes de la cinética de mineralización de atrazina así como las vidas medias, considerando cinéticas de primer orden (Tabla 5). De acuerdo con Beulke y Brown (2001), la cinética de primer orden es aceptable, cuando el valor de r es mayor que 0.87; aquí los valores de r fueron superiores a 0.9. Los resultados muestran vidas medias de atrazina entre 0.76 y 25.32 años, la vida media promedio es de 4.93 años. Las vidas medias de atrazina en los suelos estudiados son altas, comparadas con resultados publicados en la literatura (Kruger et al., 1993; Accinelli et al., 2001), y son similares a las reportadas en suelos sin historial de aplicación del herbicida (Hang et al., 2003; Blume et al., 2004), por lo que la lenta mineralización de atrazina puede relacionarse a que los microorganismos de los suelos están poco adaptados al herbicida, ya sea por no haber aplicación reciente del herbicida.

El análisis de la distribución de frecuencias de las vidas medias de atrazina en los suelos analizados se presenta en la Figura 7a. El 66.7% de las muestras de suelo tiene vidas medias en el rango de 0 a 6 años, mientras que 28.5% presenta vidas medias entre 6 y 12 años y 4.8% presenta vidas medias superiores a 24 años. Esto clasifica a la atrazina como persistente en 95.2% de las muestras de suelo y permanente en 4.8% (CICLOPLAFEST, 2004). En la Figura 7b se presenta la distribución de frecuencias de los coeficientes de adsorción (Kd) de atrazina en suelo, donde 90.5% de las muestras presenta coeficientes de adsorción inferiores a 0.9 L kg–1, mientras que 9.5% de las muestras presenta coeficientes mayores a 1.0 L kg–1.
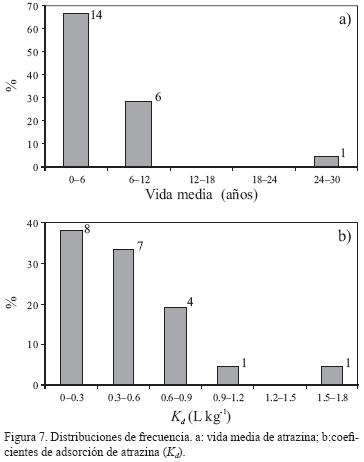
El análisis de valores atípicos se realizó sobre los Kd y los resultados de mineralización en las muestras de suelo, así como a los resultados experimentales de las isotermas de adsorción. Se encontró en estos conjuntos de datos un valor desviado para cada uno de estos parámetros cuando fueron aplicadas solamente las pruebas tipo sencillo. Los límites de confianza de 99% de la media para coeficientes de adsorción fueron 0.297–0.587 L kg–1 y para la vida media 2.0–5.8 a. Como los valores discordantes no difieren del resto de la población, en este estudio se incluyen todos los resultados experimentales en la optimización y en el análisis de correlación (FOCUS, 2006).
Los resultados del análisis de correlación entre la atenuación natural de atrazina y los componentes del suelo se presentan en la Tabla 6. En la región sombreada de la tabla se presentan los niveles de significancia entre los parámetros comparados, mientras que en la parte no sombreada se muestran los coeficientes de correlación de Pearson. Se consideró que los parámetros están relacionados cuando el nivel de significancia es menor que 0.05 (p < 0.05). Los coeficientes de correlación de Pearson para estos casos han sido marcados con celdas negras y letras blancas. Se observa que los coeficientes de mineralización de atrazina, k, presentan correlaciones significativas negativas con la conductividad eléctrica, el pH, el nitrógeno amoniacal y la materia orgánica del suelo. Asimismo, el coeficiente de adsorción presentó correlación negativa con la profundidad del suelo y positiva con la materia orgánica. Estos resultados sugieren que la movilidad de atrazina aumenta con la profundidad del suelo, ya que a mayor profundidad la adsorción de atrazina disminuye, debido a que hay menor cantidad de materia orgánica en el suelo. Típicamente, la atrazina se adsorbe a través de interacciones hidrofóbicas (Barriuso y Calvet, 1992) y tiende a cumularse en la materia orgánica del suelo, mientras que incrementos en salinidad, fertilización o alcalinidad pueden causar que la atrazina se vuelva más persistente, ya que el aumento en la concentración de estos componentes desfavorece la mineralización del herbicida. La relación entre la velocidad de mineralización de atrazina y el contenido de nitrógeno en el suelo se debe a la mayor disponibilidad de nitrógeno inorgánico que de nitrógeno del anillo de la molécula de atrazina (Figura 4) (Guillén–Garcés et al., 2007). Por otro lado, al aumentar la salinidad del suelo, la materia orgánica, que a su vez favorece la adsorción de atrazina, tiende a aglomerarse (González–Márquez y Hansen, 2009), haciendo menos disponible la atrazina para los microorganismos y disminuyendo así su mineralización.
CONCLUSIONES
Los suelos analizados son principalmente salinos y alcalinos, con concentraciones de M.O. típicas de suelos minerales.
La atrazina presentó un comportamiento de adsorción lineal respecto a su concentración. Los coeficientes de adsorción obtenidos para las muestras de suelo del DR 063, representan valores típicos para suelos agrícolas. La mineralización de atrazina fue lenta, la vida media promedio del herbicida en los suelos estudiados es de 4.93 años, lo cual es un indicador de suelos con microorganismos poco adaptados al herbicida, ya sea por no haber aplicación reciente del herbicida en los suelos o por la presencia de componentes que inhiben su mineralización como amonio, materia orgánica, pH y salinidad.
La adsorción de atrazina presenta una tendencia a disminuir respecto a la profundidad en los perfiles de suelo, indicando un mayor riesgo de lixiviación conforme el herbicida migra hacia los mantos freáticos.
Estos resultados tienen implicaciones para el riesgo de contaminar el agua subterránea de la zona de estudio ya que conforme aumenta la salinidad de los suelos y el grado de fertilización, incrementa la persistencia del herbicida. Lo anterior, aunado a la disminución de la adsorción con el aumento de la profundidad del suelo implica mayor riesgo de lixiviación de atrazina hacia el agua subterránea.
AGRADECIMIENTOS
El primer autor agradece a CONACYT la beca de doctorado. Los autores agradecen también a José Antonio Hansen Rodríguez por su apoyo en el muestreo en campo. Los autores agradecen a los tres árbitros – Arturo Carranza Edwards y dos anónimos – con habernos proporcionado valiosos comentarios y sugerencias que nos ayudaron a mejorar nuestra presentación.
REFERENCIAS
Abdelhafid, R., Houot, S., Barriuso, E., 2000, How increasing availabilities of carbon and nitrogen affect atrazine behavior in soils: Biology and Fertility of Soils, 30, 333–340. [ Links ]
Accinelli, C., Dinelli, G., Vicari, A., Catizone, P., 2001, Atrazine and metolachlor degradation in subsoils: Biology and Fertility of Soils, 33, 495–500. [ Links ]
American Society for Testing and Materials (ASTM), 1998, D42–63 Standard test method for particle–size analysis of soils: West Conshohocken, PA, USA, American Society for Testing and Materials, 1–8. [ Links ]
American Society for Testing and Materials (ASTM), 2000, Standard test methods for moisture, ash, and organic matter or peat and other organic soils. D2974–00, in Annual Book of ASTM Standards, 04(08): Philadelphia, PA, USA, 31–33. [ Links ]
Barbash, J., Resek, E.A., 1997, Pesticides in groundwater: distribution, trends, and governing factors: Boca Raton, Florida, Lewis Publishers, 590 pp. [ Links ]
Barriuso, E., Calvet, R., 1992, Soil type and herbicides adsorption: International Journal of Environmental Analytical Chemistry, 46, 117 – 128. [ Links ]
Ben–Hur, M., Letey, J., Farmer, W.J., Williams, C.F., Nelson, S.D., 2003, Soluble and solid organic matter effects on atrazine adsorption in cultivated soils: Soil Science Society of America Journal, 67, 1140–1146. [ Links ]
Berthouex, P.M., Brown, L.C., 2002, Statistics for environmental engineers: United States of America, Lewis Publishers, 2a edición, 489 pp. [ Links ]
Beulke, S., Brown, C.D., 2001, Evaluation of methods to derive pesticide degradation parameters for regulatory modeling: Biology and Fertility of Soils, 33, 558–564. [ Links ]
Bevington, P.R., Robinson, D.K., 2003, Data reduction and error analysis for the physical sciences: New York, McGrawHill, 320 pp. [ Links ]
Blume, E., Bischoff, M., Moorman, T.B., Turco, R.F., 2004, Degradation and binding of atrazine in surface and subsurface soils: Journal of Agricultural and Food Chemistry, 52, 7382–7388. [ Links ]
Brodkin, M.A., Madhoun, H., Rameswaran, M., Vatnick, I., 2007, Atrazine is an immune disruptor in adult northern leopard frogs (Rana pipiens): Environmental Toxicology and Chemistry, 26, 80–84. [ Links ]
Comisión Intersecretarial para el Control del Proceso y Uso de Plaguicidas, Fertilizantes y Sustancias Tóxicas (CICOPLAFEST), 2004, Catálogo de plaguicidas: 201.147.97.103/wb/cfp/catalogo_de_plaguicidas#, acceso libre, consulta: 01 de septiembre de 2009. [ Links ]
Comisión Nacional del Agua (CNA), 1999a, Superficies regadas y volúmenes de agua distribuidos en los distritos de riego. Año agrícola 1997–1998: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico, 125 pp. [ Links ]
Comisión Nacional del Agua (CNA), 1999b, Estadísticas agrícolas de los distritos de riego. Año agrícola 1997–1998: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico, 313 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2000a, Superficies regadas y volúmenes de agua distribuidos en los distritos de riego. Año agrícola 1998–1999: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico, 118 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2000b, Estadísticas agrícolas de los distritos de riego. Año agrícola 1998–1999: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico 2, 321 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2001a, Superficies regadas y volúmenes de agua distribuidos en los distritos de riego. Año agrícola 1999–2000: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico, 146 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2001b, Estadísticas agrícolas de los distritos de riego. Año agrícola 1999–2000: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico 2, 338 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2002a, Superficies regadas y volúmenes de agua distribuidos en los distritos de riego. Año agrícola 2000–2001: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico, 115 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2002b, Estadísticas agrícolas de los distritos de riego. Año agrícola 2000–2001: México, D.F., Subdirección General de Operación, Gerencia de Distritos y Unidades de Riego, Informe Estadístico 1, 347 pp. [ Links ]
Comisión Nacional del Agua (CNA), 2002c, Determinación de la disponibilidad de agua en el acuífero Río Sinaloa, estado de Sinaloa: Subdirección General Técnica, Gerencia de Aguas Subterráneas, Subgerencia de Evaluación y Modelación Hidrogeológica, www.conagua.gob.mx/CONAGUA07/Noticias/DR_2502.pdf, acceso libre, consulta: 01de septiembre de 2009. [ Links ]
Comisión Nacional del Agua (CONAGUA), 2007a, Estadísticas del agua en México: México, D.F., Edición 2007, p. 65. [ Links ]
Comisión Nacional del Agua (CONAGUA), 2007b, Evaluación de resultados del programa de rehabilitación y modernización de distritos de riego del ejercicio fiscal 2006, sujeto a reglas de operación vigentes a cargo de la Comisión Nacional del Agua; Distrito de Riego 063, Guasave, Sinaloa: www.conagua.gob.mx/CONAGUA07/Noticias/INFORMEDR0632007.pdf, acceso libre, consulta: 27 de marzo de 2008. [ Links ]
Comisión Nacional del Agua – Instituto Mexicano de Tecnología del Agua (CNA–IMTA), 2001, Sistema de información hidroagrícola de distritos de riego (SINHDR), versión 2.2., Base de datos: Jiutepec, Morelos, México, Coordinación de Tecnología de Riego y Drenaje. [ Links ]
Comisión Nacional para el Conocimiento y Uso de la Biodiversidad – Instituto Nacional de Investigaciones Forestales y Agropecuarias (CONABIO–INIFAP), 1995, Mapa edafológico, escala 1:250,000. México, http://conabioweb.conabio.gob.mx/metacarto/metadatos.pl, acceso libre, consulta: 11 de junio de 2007. [ Links ]
Coquet, Y., 2003, Sorption of pesticides atrazine, isoproturon, and metamitron in the vadose zone: Vadose Zone Journal, 2, 40–51. [ Links ]
Dorado, J., Tinoco, P., Almendros, G., 2003, Soil parameters related with the sorption of 2,4–D and atrazine: Communications in Soil Science and Plant Analysis, 34, 1119–1133. [ Links ]
Drori, Y., Izenshtat, Z., Chefetz, B., 2005, Sorption–desorption behavior of atrazine in soils irrigated with reclaimed wastewater: Soil Science Society of America Journal, 69, 1703–1710. [ Links ]
Eckert, D., Sims, J.T., 1995, Recommended soil pH and lime requirement tests, in Recommended soil testing procedures for the Northeastern United States: University of Delaware, College of Agriculture & Natural Resources, Northeastern Regional Publication No. 493, 2a edición, http://ag.udel.edu/extension/agnr/soiltesting.htm, acceso libre, consulta: 5 de febrero de 2007. [ Links ]
Food and Agriculture Organization of the United Nations – United Nations Educational, Scientific and Cultural Organization (FAO–UNESCO), 1970, Clave de unidades de suelos para el mapa de suelos del mundo. Proyecto FAO–UNESCO: México, D.F., Secretaría de Recursos Hidráulicos, Dirección General de Estudios, Dirección de Agrología. [ Links ]
Forum for the Co–ordination of Pesticide Fate Models and their Use (FOCUS), 2006, Guidance document on estimating persistence and degradation kinetics from environmental fate studies on pesticides in EU registration: Report of the FOCUS Work Group on Degradation Kinetics, EC Document Reference Sanco/10058/2005 http://focus.jrc.ec.europa.eu/dk/docs/finalreportFOCDegKin04June06linked.pdf, acceso libre, consulta: 9 de noviembre de 2007, version 2.0, 434 pp. [ Links ]
Galindo–Reyes, G., Villagrana, C., Lazcano–Alvarez, G., 1999, Environmental conditions and pesticide pollution of two coastal ecosystems in the Gulf of California, Mexico: Ecotoxicology and Environmental Safety: 44, 280–286. [ Links ]
Gartley, K.L., 1995, Recommended soluble salts tests, in Recommended soil testing procedures for the Northeastern United States: University of Delaware, College of Agriculture & Natural Resources, Northeastern Regional Publication No. 493, 2a edición, http://ag.udel.edu/extension/agnr/soiltesting.htm, acceso libre, consulta: 5 de febrero de 2007. [ Links ]
Gilliom, R.J., Barbash, J.E., Crawford, C.G., Hamilton, P.A., Martin, J.D., Nakagaki, N., Nowell, L.H., Scott, J.C., Stackelberg, P.E., Thelin, G.P., Wolock, D.M., 2006, The quality of our nation's waters – pesticides in the nation's streams and ground water, 1992–2001: United States Geological Survey, Circular 1291, 172 pp. [ Links ]
González–Farías, F., Cisneros–Estrada, X., Fuentes–Ruíz, C., Díaz–González, G., Botello, A.V., 2002, Pesticides distribution in sediments of a tropical coastal lagoon adjacent to an irrigation district in northwest Mexico: Environmental Technology, 23(11), 1247–1256. [ Links ]
González–Márquez, L.C., 2005, Migración de herbicidas (Atrazina y 2,4–D) en suelo del distrito de riego 063, Guasave, Sinaloa: México, Universidad Nacional Autónoma de México, tesis de maestría, 120 pp. [ Links ]
González–Márquez, L.C., Hansen, A.M., 2009, Effects of salinity on the aggregation, composition, and sorption capacity of humic acid: The 237th ACS National Meeting, Salt Lake City, UT, March 22–26.http://www.envirofacs.org/Symposia/Salt%20Lake/SLC%20Web/Metal%206.doc, acceso libre, consulta: 29 de abril de 2009. [ Links ]
Griffin, G., Jokela, W., Ross, D., 1995, Recommended Soil Nitrate–N Tests. Recommended soil testing procedures for the Northeastern United States: University of Delaware, College of Agriculture & Natural Resources, Northeastern Regional Publication No. 493, 2a edición, http://ag.udel.edu/extension/agnr/soiltesting.htm, acceso libre, consulta: 5 de febrero de 2007. [ Links ]
Guillén–Garcés, R.A., Hansen, A.M., Afferden Van, M., 2007, Mineralization of atrazine in agricultural soil: Inhibition by nitrogen: Environmental Toxicology and Chemistry, 26, 844–850. [ Links ]
Hang, S., Barriuso, E., Houot, S., 2003, Behavior of 14C–Atrazine in Argentinean topsoils under different cropping managements: Journal of Environmental Quality, 32, 2216–2222. [ Links ]
Hayes, T.B., Collins, A., Lee, M., Mendoza, M., Moriega, N., Stuart, A.A., Vonk, A, 2002, Hermaphroditic, demasculinized frogs after exposure to the herbicide atrazine at low ecologically relevant doses: Proceedings of the National Academy of Sciences of the United States of America, 99, 5476–5480. [ Links ]
Hernández–Antonio, A., 2008, Evaluación del riesgo de contaminación de aguas superficiales por uso de atrazina en el distrito de riego 063 Guasave, Sinaloa: México, Universidad Nacional Autónoma de México, tesis de doctorado, 36 pp. [ Links ]
Honeycutt, R.C., Schabacker, D.J., 1994, Mechanisms of pesticide movement into ground water: Boca Raton, Florida, Lewis Publishers, 208 pp. [ Links ]
Houot, S., Topp, E., Abdellah Y., Soulas, G., 2000, Dependence of accelerated degradation of atrazine on soil pH in French and Canadian soils: Soil Biology and Biochemistry, 32, 615–625. [ Links ]
Inoue, M.H., Oliveira R.S.Jr., Regitano, J.B., Tormena, C.A., Constantin, J., Tornisielo, V.L., 2006, Sorption–desorption of atrazine and diuron in soils from Southern Brazil: Journal of Environmental Science and Health, Part B, 41, 605–621. [ Links ]
Kruger, E.L.; Somasundaram, L., Kanwar, R., Coats, J., 1993, Persistence and degradation of 14C–Atrazine and 14C–Deisopropylatrazine as affected by soil depth and moisture conditions: Environmental Toxicology and Chemistry, 12, 1959–1967. [ Links ]
Krutz, L.J., Senseman, S.A., McInnes, K.J. Zuberer, D.A., Tierney, D.P., 2003, Adsorption and desorption of atrazine, desethylatrazine, deisopropylatrazine, and hydroxyatrazine in vegetated filter strip and cultivated soil: Journal of Agricultural and Food Chemistry, 51, 7379–7384. [ Links ]
Li, J., Langford, C.H., Gamble, D.S., 1996, Atrazine sorption by a mineral soil: Effects of soil size fractions and temperature: Journal of Agricultural and Food Chemistry, 44, 3680–3684. [ Links ]
Ling, W.T., Wang, H.Z., Xu, J.M., Gao, Y.Z., 2005, Sorption of dissolved organic matter and its effects on the atrazine sorption on soils: Journal of Environmental Sciences, 17, 478–48. [ Links ]
Márquez–Pacheco, H., 2009, Atenuación natural de atrazina en perfiles de suelo de Guasave, Sin.: México, Universidad Nacional Autónoma de México, tesis de maestría, 103 pp. [ Links ]
Organización para la Cooperación y el Desarrollo Económico (OCDE), 2000, Test No. 106, Adsorption – desorption using a batch equilibrium method, in OECD Guidelines for the Testing of Chemicals, Section 1. Physical Chemical Properties, Updated Guideline, adopted 21st January 2000. [ Links ]
Organización para la Cooperación y el Desarrollo Económico (OCDE), 2002, Proposal for a new guideline 307. Aerobic and anaerobic transformation in soil, in OECD Guidelines for the Testing of Chemicals, Section 3. Degradation and Accumulation Updated Guideline, adopted 24th April 2002. [ Links ]
Payan, S.J., Carvajal, J.L., 2001, La participación de los usuarios del distrito de riego 063, ante baja disponibilidad de agua para uso agrícola, así como en los programas hidroagrícolas del p.a.c., en XI Congreso Nacional de Irrigación, ANEI–S30112, Guanajuato, Guanajuato, México, 7 pp. [ Links ]
Saxton, K.E., Rawls, W.J., Romberger, J.S., Papendick, R.I., 1986, Estimating generalized soil–water characteristics from texture: Soil Science Society of America Journal, 50, 1031–1036. [ Links ]
Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación (SAGARPA), 2007, Anteproyecto de Modificación de la Norma Oficial Mexicana NOM–032–FITO–1995: http://www.cofemermir.gob.mx/uploadtests/12437.59.59.1.ANTEPROY.032.FEBu.doc, acceso libre, consulta: 3 de septiembre de 2009. [ Links ]
Secretaria de Agricultura y Recursos Hidráulicos (SARH), 1982, Consideraciones preliminares para el mejoramiento de la producción en el Distrito de Riego 063 – Guasave, Sinaloa: México, SARH, Dirección General de Distritos y Unidades de Riego, 68 pp. [ Links ]
Secretaría de Energía (SENER), 2007, Anuario estadístico de la industria petroquímica: México, D.F., www.sener.gob.mx/webSener/res/PE_y_DT/pub/Anuario%20Estadistico%20de%20la%20Industria%202006.pdf acceso libre, consulta: 1 de abril de 2008. [ Links ]
Secretaría del Medio Ambiente Recursos Naturales y Pesca – Instituto Mexicano de Tecnología del Agua (SEMARNAP–IMTA), 2000, Contaminación y drenaje agrícola: Jiutepec, Morelos, México, Coordinación de Tecnología de Riego y Drenaje, Subcoordinación de Contaminación y Drenaje Agrícola. [ Links ]
Socías–Viciana, M.M., Fernández–Pérez, M., Villafranca–Sánchez, M., González–Pradas, E., Flores–Céspedes, F., 1999, Sorption and leaching of atrazine and MCPA in natural and peat–amended calcareous soils from Spain: Journal of Agricultural and Food Chemistry, 47, 1236–1241. [ Links ]
Tappe, W., Groeneweg, J., Jantsch, B., 2002, Diffuse atrazine pollution in German aquifers: Biodegradation, 13, 3–10. [ Links ]
Tinsley, I.J., 2004, Chemical concepts in pollutant behavior: Hoboken, New Jersey, United States of America, John Wiley & Sons, 2a edición, 75 pp. [ Links ]
Tyess, D.L., Shea, P.J., Parkhurst, A.M., 2006, Mineralization potential of atrazine and degradation intermediates from clustered characteristics in inoculated soils: Soil & Sediment Contamination, 15, 87–102. [ Links ]
United States Department of Agriculture (USDA), 2003, Soil water characteristics hydraulic propierties calculator, http://hydrolab.arsusda.gov/soilwater/Index.htm, acceso libre, consulta: 5 de marzo de 2007. [ Links ]
Valle, M.O., 2002, Planeación regional bidimensional en función de la disponibilidad del recurso hídrico del acuífero de Guasave, Sinaloa: Sinaloa, México, Universidad Autónoma de Sinaloa, Escuela de Administración y Desarrollo Rural, tesis de maestría, 116 p. [ Links ]
Van–Leewen, J.A., Waltner–Toews, D., Abernathy, T., Smith, B., Shokri, M., 1999, Associations between stomach cancer incidence and drinking water contamination with atrazine and nitrate in Ontario (Canada) agroecosystems, 1987–1991: International Journal of Epidemiology, 28, 836–890. [ Links ]
Verma, S.P., 2005, Estadística Básica para el Manejo de Datos Experimentales: Aplicación en la Geoquímica (Geoquimiometría): México, D.F., Universidad Nacional Autónoma de México, 186 pp. [ Links ]
Verma, S.P., 2009, Evaluation of polynomial regression models for the Student t and Fisher F critical values, the best interpolation equations from double and triple natural logarithm transformation of degrees of freedom up to 1000, and their applications to quality control in science and engineering: Revista Mexicana de Ciencias Geológicas, 26(1), 79–92. [ Links ]
Verma, S.P., Quiroz–Ruiz, A., 2006a, Critical values for six Dixon tests for outliers in normal samples up to sizes 100, and applications in science and engineering: Revista Mexicana de Ciencias Geológicas 23(2), 133–161. [ Links ]
Verma, S.P., Quiroz–Ruiz, A., 2006b, Critical values for 22 discordancy test variants for outliers in normal samples up to sizes 100, and applications in science and engineering: Revista Mexicana de Ciencias Geológicas, 23(2), 302–319. [ Links ]
Verma, S.P., Quiroz–Ruiz, A., 2008, Critical values for 33 discordancy test variants for outliers in normal samples of very large sizes from 1,000 to 30,000 and evaluation of different regression models for the interpolation and extrapolation of critical values: Revista Mexicana de Ciencias Geológicas, 25(3), 369–381. [ Links ]
Verma, S.P., Quiroz–Ruiz, A., Díaz–González, L., 2008. Critical values for 33 discordancy test variants for outliers in normal samples up to sizes 1000, and applications in quality control in Earth Sciences: Revista Mexicana de Ciencias Geológicas, 25(1), 82–96. [ Links ]
Villada–Canela, M., 2006, Estimación del riesgo de contaminar mantos freáticos por infiltración de herbicida atrazina en distritos de riego en México: Universidad Nacional Autónoma de México, tesis de maestría, 128 pp. [ Links ]
Weber, J.B., 1993, Bioavailability and bioactivity of sorbed organic chemicals, in Linn, D.M. y Carski, T. (eds.), Sorption and Degradation of Pesticides and Organic Chemicals in Soil: Madison, WI, USA, Soil Science Society of America, Special Publication 32, 153–196. [ Links ]
Weber, J.B., 1995, Physicochemical and mobility studies with pesticides, in Leng, M.L, Leovey, E.M.K. y Zubkoff, P. (eds.), Agrochemical Environmental Fate: Boca Raton, Florida, United States of America, CRC Press, 99–1115. [ Links ]














