Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agricultura técnica en México
versión impresa ISSN 0568-2517
Agric. Téc. Méx vol.35 no.4 México oct./dic. 2009
Artículos
Caracterización morfológica de la calabaza pipiana (Cucurbita argyrosperma Huber)*
Morphological characterization of pipiana squash (Cucurbita argyrosperma Huber)
Ricardo Rodríguez–Amaya1, Salvador Montes–Hernández2§, José Antonio Rangel–Lucio1, Mariano Mendoza–Elos1 y Luis Latournerie–Moreno3
1 SEP–Instituto Tecnológico de Roque. Km 8 Carretera Celaya–Juventino–Rosas. C. P. 3 8110 Roque, Celaya, Guanajuato, México. E–mails: arangel_1@yahoo.com, mmendoza66@hotmail.com.
2 Campo Experimental Bajío, INIFAP, km 6.5 Carretera Celaya–San Miguel de Allende, C. P. 38000 Celaya, Guanajuato, México.
3 División de Estudios de Posgrado e Investigación, Instituto Tecnológico de Conkal. Km 16. 3 antigua carretera Mérida–Motul, C. P. 97345. Conkal, Yucatán. E–mail: napoleon@itaconkal.edu.mx.
§Autor para correspondencia:
montes.salvador@inifap.gob.mx.
* Recibido: Diciembre de 2007
Aceptado: Diciembre de 2009
RESUMEN
La calabaza pipiana (Cucurbita argyrosperma Huber) carece de un registro formal de su diversidad morfológica en México. Con este antecedente, y la importancia de conservar y conocer los recursos genéticos vegetales de esta especie, se realizó esta investigación con el propósito de caracterizar 32 accesiones de calabaza pipiana del banco de germoplasma del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias, Campo Experimental Bajío, durante el ciclo primavera verano 2006. Las plántulas de las poblaciones descritas se distribuyeron en el terreno bajo un diseño de bloques completos al azar, y el manejo agronómico se realizó conforme a las técnicas de la calabaza en el Bajío Guanajuatense de México. Durante el ciclo de cultivo y en post–cosecha se emplearon descriptores que incluyen variables cualitativas (37) y cuantitativas (13) para su caracterización. El soporte estadístico comprendió análisis de componentes principales y de conglomerados jerárquicos. Las variables cualitativas distribución del color terciario, intensidad de moteado, color de margen y testa de la semilla, y forma de borde de hoja, fueron las que mostraron mayor variación en las accesiones caracterizadas y permitieron la formación de siete grupos con las 32 accesiones. Mientras tanto, las variables cuantitativas peso de 100 semillas con testa y sin testa, peso de fruto y días a floración contribuyeron en mayor medida a la distinción de las accesiones y la formación de cinco grupos. Características de interés antropocéntrico, como peso de 100 semillas con y sin testa, mostraron la mayor diversidad del germoplasma de calabaza pipiana estudiado.
Palabras clave: accesiones, caracterización, componentes principales, recursos genéticos.
ABSTRACT
The pipiana squash (Cucurbita argyrosperma Huber) lacks formal descriptors of their existent morphological diversity in Mexico. With this antecedent and regarding the importance of conserving and to describe the genetic resources of this species, a research was carried out with the aim of characterizing 32 accessions of pipiana squash from the gene bank of the Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias, at Campo Experimental Bajio, Mexico during the spring–summer cycle (2006). Seedlings of the 32 populations were distributed in the field under a complete random block design, and the agronomic handling was carried out according to the techniques used for commercial squash production in the "Bajio Guanajuatense" of Mexico. For the characterization, two sets of descriptors were used, one set included 37 qualitative traits and a second set of 13 quantitative traits; traits were recorded during the cultivation cycle and at post harvest. Data handling included principal components and clusters analysis. In the qualitative traits the distribution of the tertiary color, intensity of spots, color of the margin and seed coat plus the form of the leaf border, showed large variation in the evaluated accessions, these traits influenced the formation of seven groups of accessions. Meanwhile, the quantitative traits weight of one hundred seeds with and without coat, fruit weight and days to flowering contributed more to the distinction of the characterized accessions, separating them in five groups. The characteristics of anthropocentric interest, weigh of a hundred seeds with and without coat, showed the most diversity in the germplasm of pipiana squash.
Key words: accessions, characterization, genetic resources, principal components.
INTRODUCCIÓN
Los recursos genéticos representan la materia prima de fitomejoradores y son imprescindibles para los productores. El valor reside en su utilización para producir cultivares nuevos, incrementar el conocimiento de especies útiles y desarrollo de productos. Para ello es necesario conocer características del germoplasma existente, tanto in situ, como ex situ (Chávez, 1993; FAO, 2003). Sin embargo, existe una brecha importante entre materiales conservados, y aquellos caracterizados y evaluados. Entre 80 y 95% de muestras mundiales de accesiones de todas las especies, conservadas en bancos de germoplasma, carecen de caracterización y evaluación agronómica (Peeters y Galway, 1988), que los convierte en depósitos simples de materiales inútiles.
En México, el cultivo de calabaza es importante en sistemas agrícolas tradicionales de diversos estados, como Yucatán, Jalisco, Oaxaca y Veracruz, aunque generalmente como cultivo secundario después de otros básicos (Whitaker y Bohn, 1950; Whitaker y Davis, 1962), caso concreto la milpa en Yucatán, la cual consiste en la siembra asociada de maíz (Zea mays L.), (Phaseolus lunatus), frijol xcoolibuul (P. vulgaris) y calabaza (Cucurbita spp.) junto con otros cultivos hortícolas bajo el sistema agrícola de roza–tumba–quema (Canul et al., 2005).
Existe poca información que describa en forma puntual la diversidad del género Cucurbita y C. argyrosperma Huber no es la excepción Merrick y Bates (1989) hicieron una descripción de la diversidad con fines de la reclasificación y nomenclatura de la especie. Merrick (1990) refiere diferencias entre variantes domesticadas y silvestres de la especie. Vildózola (1998) describió una población de C. argyrosperma y Canul et al. (2005) registraron la diversidad morfológica de calabaza de Yucatán.
Estudios de Lira et al. (1995), Azurdia (1999) señalan que la variabilidad de la calabaza cultivada se encuentra en la morfología y tamaño de frutos y semillas, coloración, tipo y sabor de mesocarpio. La diversidad es menos heterogénea en C. argyrosperma en comparación con las especies cultivadas; aunque con características agronómicas sobresalientes y ciclos biológicos diferentes (Zizumbo, 1992; Lira et al., 1995).
En México, variedades locales de calabaza se han perdido por falta de continuidad de uso, y el desplazamiento que ocurre por selecciones nuevas y productivas; algunas se mantienen aisladas y otras requieren caracterización, selección y mejora para manifestar características sobresalientes (Villanueva, 2007). Lo anterior enfatiza el problemay la necesidad de contar con información suficiente de las colecciones de germoplasma, para su identificación y uso adecuado en programas de mejoramiento genético (Frankel y Brown, 1984). Montes et al. (2005) concluyeron que Cucurbita podría sufrir erosión genética, lo que sugiere conservar el germoplasma en campos agrícolas de productores. Por lo anterior el trabajo planteó como objetivo caracterizar 32 colecciones de calabaza pipiana (C. argyrosperma) del banco de germoplasma del Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias (INIFAP) ubicado en el Campo Experimental Bajío (CEBAJ), con base en caracteres morfológicos y agronómicos de la planta.
MATERIALES Y MÉTODOS
Se seleccionaron 32 accesiones (Cuadro 1) del banco de germoplasma, con base en la disponibilidad de semilla. La siembra se realizó el 08 de abril de 2006 en el laboratorio de análisis de semillas del Instituto Tecnológico de Roque. El papel germinador KIMPAK de Seedburo Equipment Co®, se desinfectó con N–triclorometiltio–4–ciclohexeno–1,2–dicarboximida (2 g L–1). Después, la semilla se colocó en solución de hipoclorito de sodio al 2%, durante 5 min y después se lavó con agua purificada y se sumergió en ácido giberélico (0.5 gL–1) por espacio de 60 min. Las semillas se dispusieron entre hojas de papel germinador, enrolladas en forma de "taco" y colocadas en posición vertical dentro de recipientes de plástico de un litro de capacidad, en la cámara de germinación (Lab–Line® 0405–003), a una temperatura promedio de 25 °C por cuatro días (d) (Moreno, 1996; ISTA, 1999). Las plántulas fueron trasplantadas a vasos de unicel de 500 ml de capacidad con sustrato comercial (Sunshine Núm. 3) y se aplicó un enraizador (ácido idol 3–butirico, 3%; ácidos húmicos y fúlvicos, 12%; humectantes 14%; proteína vegetal hidrolizada, 5 %) para promover el desarrollo radical, en una concentración de 1 %.

El clima es semicálido subhúmedo, precipitación media de 600 a 800 mm, temperatura media entre 18 y 20 °C, temperatura máxima de 30 a 32 °C de mayo a junio (García, 1988). Predominan suelos Vertisoles Pélicos (FAO–UNESCO, 1970).
El terreno se preparó conforme recomendación técnica en la región y el trasplante definitivo se realizó el 03 de mayo de 2006, cuando la plántula había formado las tres primeras hojas verdaderas. El arreglo topológico consistió en separar las plantas 1 m y 3 m entre surcos, para lograr una densidad de población de 3 300 plantas por hectárea.
El diseño experimental en el campo fue de bloques completos al azar, con tres repeticiones. La parcela útil consistió de seis plantas, de 12 que constituyó la unidad experimental. El control de malezas fue manual, mecánico y químico; este último cinco días después del trasplante con 1.5 L ha–1 de Clethodim. Las plagas y enfermedades se controlaron con Imidacloprid, 1 L ha–1; Carbaril, 1–1.5 kg ha–1; Propamocarb–clorhidrato, 1–1.5 L ha–1; Oxicloruro de cobre + Mancozeb, 1 kg ha–1; Azoxystrobin, 0.7–1 kg ha–1. El riego por gravedad se aplicó con una frecuencia de 20 días, aplicando dos riegos antes del inicio de las lluvias. La fertilización química manual comprendió la dosis 100–60–40, con la distribución de la mitad de nitrógeno y todo el fósforo y potasio 10 d después del trasplante; el resto de nitrógeno se suministró 25 d después. La fertilización básica se complementó con aplicación foliar de Bayfolan® [N, 11.5 %; P2O5, 8 %; K2O, 6%; micronutrientes (Bo, 0.036%; Cu, 0.04%; Fe, 0.05%; Mo, 0.005; Zn, 0.08%; S, 0.23%; Ca, 0.025%; Co, 0.002%; Mn, 0.036%; Mg, 0.025%), vitamina B1, auxinas de crecimiento (ácido indol acético, 0.003%)], a razón de 200 mL ha-1, 20 d después del trasplante.
Los caracteres morfológicos se registraron con el descriptor de Cucurbita propuesto por Esquinas–Alcázar y Gulick (1983) y modificado por Villanueva (2007), que incluye 13 variables cuantitativas (Cuadro 2) y 37 cualitativas (Cuadro 3). Esta actividad inició desde el trasplante en invernadero hasta poscosecha.

La cosecha de frutos inició el 22 de agosto y finalizó el 26 de octubre de 2006, y permanecieron en reposo por un mes, bajo condiciones naturales en la azotea de una bodega, para que la semilla alcanzara su madurez fisiológica. Los frutos se abrieron por la mitad para extraer la semilla y la pulpa excedente se eliminó con agua; la semilla se puso a secar por un día, sobre papel periódico al ambiente, con constantes movimientos de la misma. Con base a modas de variables cualitativas y promedio de variables cuantitativas de cada accesión, se realizó el análisis de componentes principales, y el análisis de conglomerados de agrupamiento jerárquico con la distancia euclidiana (SAS, 2002).
RESULTADOS Y DISCUSIÓN
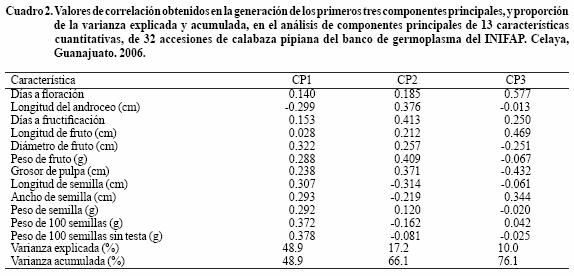
Los tres primeros componentes principales (CP) explicaron 76% de la variabilidad total de las características cuantitativas evaluadas, ya que a partir del CP4 la varianza mostrada fue menor a 10% (8.7%), siendo el CP 1 el más importante con un mayor porcentaje de participación (Cuadro 2). En el mismo Cuadro 2, se registran las variables que más influyeron en la variabilidad, de los tres primeros componentes principales, siendo aquellas que mostraron mayor valor de correlación, por lo tanto, el componente principal 1, se asoció más con características de la semilla, en cambio CP2 y CP3 se relacionaron con características de fruto y fenología de planta (Cuadro 2). De esta forma, las características fenológicas de planta, y morfológicas de semilla y fruto, fueron determinantes en la mayor parte de la diversidad mostrada por la calabaza pipiana.
El análisis de CP mostró resultados similares a los de Canul et al. (2005), al evaluar la diversidad morfológica de calabaza en Yucatán. El hecho de que CP 1 explique la mayor variabilidad de calabaza pipiana, indica relaciones estrechas y efectos de una selección apropiada de genotipos, con características agronómicas y alimenticias sobresalientes durante el proceso de domesticación (Lira y Montes–Hernández, 1992; Lira et al., 1995).
Respecto a la representación gráfica de la distribución de las accesiones estudiadas de calabaza pipiana sobre el CP1 (Figura 1), indica que la distribución de las poblaciones sobre este eje, está relacionada con los valores mayores de correlación relativos a las características evaluadas, así la ordenación de las poblaciones 7, 8, 10 y 13 en el extremo positivo del eje, se atribuye principalmente por registrar las semillas más grandes y pesadas y frutos de mayor anchura, porque manifestaron mayor peso para 100 semillas sin testa y 100 semillas con testa, mientras que las identificadas con los números 29, 20, 15 y 18 [ordenadas hacia la izquierda (valor negativo) de CP1], tuvieron valores bajos en las mismas características.

La ordenación de las accesiones considerando el eje del CP2, nos señala lo mismo que el CP 1, poblaciones ubicadas en la escala mayor, se relaciona con valores mayores de las características que resultaron ser los de mayor influencia en el CP2, las cuales fueron días a fructificación y peso de fruto. Las accesiones 2, 4, 13 y 1 sobresalieron en días a fructificación y peso de fruto, y tienen un origen común, el centro–occidente de la república mexicana. Respecto a la accesión 10, colectada en Veracruz y ordenada en la parte inferior (escala negativa) de CP2, mostró precocidad en fructificación. Por lo tanto, la ordenación de las diferentes poblaciones en este eje, se da en función de la variabilidad registrada en días a fructificación con materiales desde precoces hasta tardíos (en promedio alcanzan desde 147 a 184 días a fructificación), frutos desde pequeños hasta grandes (desde 1 123 hasta 3 755 g en promedio), grosor de pulpa desde 1.0 hasta 2.4 cm. La ubicación de accesiones en la parte intermedia de ambos ejes posiblemente sea el resultado de algunas características comunes compartidas, específicas de la especie, pero con variaciones morfológicas y fisiológicas que hacen que se muestren diferentes, lo que precisa esa ordenación en cada eje.
El análisis de conglomerados formó cinco grupos con las 32 poblaciones de calabaza, a una distancia euclidiana de 0.8 (Figura 2). El grupo I se conformó por accesiones de Guanajuato, Jalisco, Sinaloa y Chiapas, y se caracterizaron por el ciclo tardío; los frutos grandes (longitud de 20.08 cm.), pesados (3 338 g), anchos (21.06 cm de diámetro) y pulpa gruesa (2.1 cm); alto rendimiento de semilla (78.5 g) y semillas grandes (2.1 cm). La dispersión geográfica de las accesiones del grupo IV denota la diversidad intraregional, ya que accesiones procedentes del mismo estado se ubican en diferentes grupos; lo cual a pesar de que se lleva una selección por tipos específicos en una región (Montes et al., 2005), se presenta entre ellas un nivel alto de entrecruzamiento (Montes y Eguiarte, 2002).
El grupo II, integrado por una población procedente de Michoacán, presentó un ciclo vegetativo largo (74 y 183 días a floración y fructificación respectivamente), longitud menor de fruto, peso de fruto menor, rendimiento bajo de semilla, semillas pequeñas, y peso bajo de 100 semillas con testa y sin testa.
El grupo III se integró por 15 accesiones procedentes de Jalisco, Oaxaca, Chihuahua, Sinaloa y Nayarit. Las accesiones de este grupo son precoces a floración (65 d), forman frutos de tamaño intermedio pero de menor diámetro, y pulpa delgada; valores bajos para las características peso de fruto (1 916 g), rendimiento de semilla (62.5 g), peso de 100 semillas con testa y sin testa (17.6 y 13.3 g, respectivamente).
Las accesiones que integraron el grupo IV tienen origen geográfico amplio (Yucatán, Sonora, Guanajuato, Oaxaca, Jalisco, Morelos y Guerrero). Lo que muestra que atributos de precocidad, tamaño de frutos y rendimiento de semilla han sido seleccionados en diferentes partes del país. Este grupo presentó características similares al grupo III.
El grupo V agrupó accesiones originarias de Veracruz, México, con ciclo reproductivo intermedio, los frutos grandes, pesados y pulpa delgada; alto rendimiento de semilla (93.5 g); semillas grandes, y alto peso para 100 semillas con testa y sin testa. El uso principal al que se destina la semilla de calabaza pipiana en Veracruz, es la elaboración de guisos regionales como el mole de pipián y elaboración de dulces con la semilla procesada (Montes, 1991; Lira y Montes, 1992); de ello deriva el interés por semilla de mayor tamaño.
Lira et al. (1995) y Zizumbo (1992) refieren que en C. argyrosperma la diversidad parece ser menos heterogénea, que en otras especies del género Cucurbita (C. moschata, C. pepo y C maxima), sin embargo, en este estudio se demostró la diversidad de resultados en las variables fenológicas, y en aquellas que forman parte de componentes del rendimiento. Por ejemplo la duración del ciclo vegetativo juega un papel importante en las preferencias selectivas de productores y fitomejoradores, particularmente en regiones con condiciones climáticas adversas. En este aspecto se observaron accesiones precoces con 55 d a floración, aunque Canul et al. (2005) afirman que la floración de C. argyrosperma en Yucatán osciló entre 47 y 51 d; evidencia de un posible efecto del ambiente de crecimiento sobre la misma especie, lo que confirma la diversidad observada en este estudio (Villanueva, 2007).
Respecto a las variables cualitativas, después de realizar un análisis de varianza de estas, las accesiones de calabaza pipiana compartieron características como hábito de crecimiento rastrero, presencia de zarcillos y moteado, y color amarillo de la flor; las cuales son intrínsecas de la especie y han sido usadas para la clasificación taxonómica (Merrick y Bates, 1989; Lira y Montes–Hernández, 1992; Lira et al., 1995), ya que al estar controladas por uno o hasta dos pares de genes dominantes, no son afectados por el ambiente; por lo que dichas características son altamente heredables (Strickberger, 1978; Chávez, 1993). Por lo tanto, de las 37 características registradas, el análisis de componentes principales (ACP) se realizó con 22 (Cuadro 3), cuyos resultados mostraron que el CP1 aportó 13.5% de la variabilidad, y los tres primeros componentes explicaron 34.7% de la varianza total (Cuadro 3). El CP1 estuvo determinado en mayor proporción por caracteres de hoja y epidermis de frutos; el CP2 tuvo mayor relación con las características de semilla; en cambio el CP3 se asoció a características de hoja y tallo.
La ordenación de las accesiones con base en el CP1 (Figura 3) indica que la accesión 14 se caracterizó por haber presentado color naranja distribuido en forma de rayas en el fruto, siendo el color terciario en cantidad mostrada, y sin presencia de moteado en las hojas; por otro lado, las accesiones distribuidas en la parte izquierda de eje, se caracterizaron por carecer de este color naranja en los frutos y mostraron moteado de las hojas en forma intensa. Con base en la ordenación mostrada en el CP2, C. argyrosperma se caracteriza por el diferencias en el color del margen de semilla, las accesiones ubicadas en la parte superior (positiva) de la Figura 3, se caracterizan por presentar el margen de semilla de color dorado, y en la parte inferior (negativa) ubicó a las accesiones con margen de semilla gris. Se puede observar que el mayor número de accesiones se distribuyó en la parte central de ambos CP, haciendo mención de que comparten características similares, o sus presentan valores intermedios dentro de los gradientes que se utilizan dentro de cada descriptor, lo cual forma parte de la diversidad del germoplasma evaluado (Esquinas–Alcázar y Gulick, 1983; Canul et al., 2005; Villanueva, 2007).

El resultado del análisis de conglomerados fue la agrupación de las 32 accesiones caracterizadas en siete grupos (Figura 4). El agrupamiento obtenido se dio a una distancia euclidiana de 0.97. Las accesiones que conformaron el grupo I y que representa más de 50%, mostraron color de moteado verde claro en las hojas; pubescencia escasa y suave en el tallo; fruto redondo; pulpa de color naranja; margen de la semilla color dorado y testa color crema.
Las accesiones del grupo II mostraron color plateado en el moteado de hoja e intensidad intermedia; pubescencia de tallo escasa y media suave; fruto redondo; pedúnculo con inserción recta al fruto; semillas con margen gris, grueso e irregular, y testa blanca. Este grupo estuvo integrado por accesiones de Veracruz, Yucatán y Guanajuato.
Las características mencionadas para el grupo II (Figura 4), coinciden con la descripción hecha por Merrick y Bates (1989) para la clasificación de C. argyrosperma spp. argyrosperma var. argyrosperma. Ésta variedad también se localiza en Tamaulipas, San Luis Potosí, Puebla, Veracruz, Tabasco, Chiapas y Yucatán (Merrick y Bates, 1989; Lira y Montes–Hernández, 1992).
Las accesiones del grupo III colectadas en Jalisco, mostraron longitud del ápice de la hoja mayor a 3 cm, que corresponde a una forma de ápice puntiagudo; borde de hoja intermedio; frutos piriformes, de color verde distribuido en forma primaria, de manera secundaria el crema y sin color terciario; lomos en la parte basal y apical en forma de V (estrella) y pulpa de fruto de color amarillo claro. Las semillas con margen dorado, delgado y regular, y testa color crema.
Las accesiones del grupo IV procedentes de Oaxaca presentaron ápices de las hojas menores a 3 cm (forma redonda); fruto de forma elíptica y color crema distribuido en forma primaria, sin lomos en la parte basal y apical; semillas con margen gris, delgado y uniforme, y testa blanca.
La accesión del grupo V originaria de Guanajuato, formó hoja con lóbulos poco pronunciados, intensidad de moteado fuerte y color verde claro; pubescencia abundante en el tallo de consistencia media suave; los frutos de forma aplanada, color primario verde, epidermis dura, la pronunciación marcada de lomos en la base e intermedia en el ápice de fruto, y la inserción del pedúnculo de forma aplanada. Las semillas con margen dorado, delgado y regular, y testa blanca.
La accesión del grupo VI, cuyo origen de colecta fue Oaxaca, presentó ápice redondo de hoja (menos a 3 cm) y borde intermedio; el tallo con pubescencia escasa y suave; fruto redondo y pulpa color naranja; semillas con margen gris, delgado y uniforme, y testa blanca.
Los grupos IV y VI coinciden en el origen de la colecta que fue Oaxaca. La explicación por lo que la accesión del grupo VI no este incluida en el grupo III, se debe a la diversidad fenotípica y genotípica presente en este germoplasma, por lo que la variación podría atribuirse a la composición genética de cada accesión. Los grupos anteriores poseen características (semillas con margen gris, delgado y uniforme y, testa blanca) que las incluyen en la clasificación de Merrick y Bates (1989) para C. argyrosperma spp. argyrosperma var. stenosperma., pero que forma parte de la diversidad morfológica de esta especie (Lira et al., 1995).
La accesión que integró el grupo VII, originaria de Guerrero, mostró hoja con lóbulos pronunciados y ausencia de moteado; tallo con pubescencia escasa y suave; fruto de forma aplanada, color primario verde, poca presencia de lomos en la parte basal y apical y pulpa color naranj a; forma estrellada del pedúnculo al corte. Las semillas manifestaron margen color gris, delgado y uniforme, y testa blanca.
La variación de las características cualitativas de calabaza pipiana no parece ser amplia, debido a que están controladas por uno, o cuando mucho por dos pares de genes dominantes (Chávez, 1993; Villanueva, 2007), aunque se encuentran accesiones con algunos aspectos importantes preferentes para el consumo y entre los que destaca forma y color de fruto, y color de margen y testa de semilla. Finalmente, debido a que el interés principal por ésta especie en México radica en la semilla (Montes, 1991; Lira y Montes–Hernández, 1992), y en Sudamérica los frutos utilizados como forraje, indicaría que los agricultores han mostrado indiferencia por las características cualitativas durante el proceso de domesticación y selección de calabaza pipiana (FAO, 1993). Al respecto Lira et al. (1995), Canul et al. (2005) y Villanueva (2007) señalan la importancia del estudio de la diversidad de germoplasma de esta especie, con fines diversos, pero principalmente en la conservación y utilización (Lira et al., 1995; Esquinas–Alcázar y Gulick, 1983).
CONCLUSIONES
Las características cuantitativas, como son los días afloración y fructificación, peso de fruto y de semilla contribuyeron en mayor medida a la explicación de la diversidad del germoplasma de calabaza evaluado.
Las variables cualitativas que fundamentaron la diversidad del germoplasma fueron color de fruto, color de margen y testa de semilla, y la forma de borde de la hoja.
Se identificaron accesiones con características agronómicas sobresalientes; la accesión 31 fue la más precoz; la accesión 13 presentó mayor peso de frutos; la accesión 4 con mayor peso de semilla por fruto; la accesión 10 presentó mayor peso de 100 semillas con testa, y la accesión 7 registró el mayor peso para 100 semillas sin testa.
AGRADECIMIENTOS
Al Campo Experimental Bajío, del Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias (INIFAP). Como parte del proyecto titulado: "Los recursos genéticos vegetales en el INIFAP: estado actual, perspectivas y desarrollo", con número PRECI: 1015960A; y a la Dirección General de Educación Superior Tecnológica (DGEST) de la SEP, por la beca para los estudios de Maestría en Ciencias del autor responsable, en el Instituto Tecnológico de Roque (ITR) de Celaya, Guanajuato.
LITERATURA CITADA
Azurdia, C. 1999. Las cucúrbitas de Guatemala. Tikalia 17:41–58. [ Links ]
Canul, K. J.; Ramírez, V. P.; Castillo, G. F. y Chávez, S. J. L. 2005. Diversidad morfológica de calabaza cultivada en el centro–oriente de Yucatán, México. Rev. Fitotec. Mex. 28:339–349. [ Links ]
Cruces, C. R. 1987. Lo que México aportó al mundo. Panorama. México. 155 p. [ Links ]
Esquinas–Alcázar, J. T. and Gulick, P. J. 1983. Genetic resources of Cucurbitaceae. International Board for Plant Genetic Resources. AGPG: IBPGR/82/48. Rome, Italy. 113 p. [ Links ]
Food and Agriculture Organization of the United Nations–United Nations Educational, Scientific and Cultural Organization (FAO–UNESCO). 1970. Clave de unidades de suelos para el mapa de suelos del mundo. Traducción de García, A. E. 1974. Dirección de Agrología, Secretaría de Recursos Hidráulicos. México, D. F. [ Links ]
Food and Agriculture Organization of the United Nations (FAO). 1993. Valor nutritivo y usos en alimentación humana de algunos cultivos autóctonos subexplotados de Mesoamérica. Santiago, Chile. Boletín informativo 12:66–68. [ Links ]
Frankel, O. H. and Brown, A. H. D. 1984. Plant genetic resources today: a critical appraisal. In: Holden J. H. W. Williams, J. T. (eds). Crop genetic resources: conservation and evaluation. Allen and Unwin, London, UK. pp. 249–257. [ Links ]
García, E. 1988. Modificaciones al sistema de clasificación climática de Köppen (para adaptarlo a las condiciones de la república mexicana). 4ªEdición. Instituto de Geografía. UNAM, México, D. F. 243 p. [ Links ]
International Seed Testing Association (ISTA). 1999. International Rules for Seed Testing. Seed Science & Technology 27 (Supplement): 27–31. [ Links ]
Lira, R.; T. C. Andres y Nee, M. 1995. Cucurbita L. In: Lira, R. (Ed.), Estudios taxonómicos y ecogeográficos de las Cucurbitaceae latinoamericanas de importancia económica. Cucurbita, Sechium, Sicana y Cyclanthera. International plant genetic resources institute, Rome, Italy. Capítulo 1. pp. 1–115. [ Links ]
Lira, S. R. y Montes–Hernández, S. 1992. Cucúrbitas (Cucurbita spp.). In: Hernández, B. J. E. y León, J. (eds.). Cultivos marginados, otra perspectiva de 1942. Colección FAO: producción y protección vegetal Núm. 26. Roma, Italia. pp. 71–75. [ Links ]
Merrick, L. C. and Bates, D. M. 1989. Classification and nomenclature of Cucurbita argyrosperma. Baileya 23:94–102. [ Links ]
Merrick, L. C. 1990. Systematics and evolution of a domesticated squash, Cucurbita argyrosperma, and its wild and weedy relatives. In: Bates, D. M.; Robinson, R. W. y Jeffrey, C. (eds.). Biology and utilization of the Cucurbitaceae. Cornell Univ. Press, Ithaca, NY. pp 77–95. [ Links ]
Montes, H. S. 1991. Calabazas (Cucurbita spp.). In: Ortega, P. R.; Palomino, H. G.; Castillo, G. F.; Gonzáles, H. V. A. y Livera, M. M. (eds). Avances en el estudio de los recursos fitogenéticos en Mexico. SOMEFI. Chapingo, México. pp. 239–250. [ Links ]
Montes, H. S. and Eguiarte, E. L. 2002. Genetic structure and indirect estimate of gene flow in three taxa of Cucurbita (Cucurbitaceae) in western México. Amer. J. Bot. 89:1156–1163. [ Links ]
Montes, H. S.; Merrick, L. C. and Eguiarte, L. E. 2005. Maintenance of squash (Cucurbita spp.) landrace diversity by farmers' activities in Mexico. Genetic Resource and Crop Evolution 52:697–707. [ Links ]
Moreno, M. E. 1996. Análisis físico y biológico de semillas agrícolas. 3ª edición. UNAM. México, D. F. 393 p. [ Links ]
Organización para las Naciones Unidas para la Agricultura y la Alimentación (FAO). 2003. Comisión de recursos genéticos para la alimentación y la agricultura. Roma Italia. 9 p. [ Links ]
Peeters, J. P. and Galgway, N. W. 1988. Germplasm collections and breeding needs in Europe. Econ. Bot. 42:503–521. [ Links ]
Statistical Analysis System (SAS). 2002. The SAS System for Windows 9.0. SAS Institute, Inc. N. C. USA. [ Links ]
Strickberger, M. 1978. Genética. Ediciones Omega. 2ª. Edición. Barcelona, España. 937 p. [ Links ]
Vildózola, T. J. L. 1998. Caracterización y selección in situ de una población de calabaza pipiana (Cucurbita argyrosperma Huber var. stenosperma). Tesis de Licenciatura. UACh. Chapingo, México. 62 p. [ Links ]
Whitaker, T. W. and Bohn, G. W. 1950. The taxonomy, genetics, production and uses of the cultivated species of Cucurbita. Economic Botany 4:52–81. [ Links ]
Whitaker, T. W. and Davis, G. N. 1962. Cucurbits, botany, cultivation and utilization. Interscience Publishers, Inc. New York. 250 p. [ Links ]
Zizumbo, V. D. 1992. Las calabazas del sistema milpero como recurso genético. In: La modernización de la milpa en Yucatán: utopía o realidad. Zizumbo, V. D.; Rassmusen, C. H.; Arias, R. L. y Terán, C. S. (eds). CICY, Mérida, Yucatán. pp. 161–174. [ Links ]














