Introducción
Globalmente, el consumo indiscriminado de sustancias ilícitas se ha convertido en un problema de salud pública. De acuerdo al Informe Mundial de Drogas (2019), 5.5% de la población entre 15 y 64 años utilizaron drogas durante ese año, lo que equivale a 271 millones de personas. De dichos usuarios, se estima que 11% (35 millones de personas) han desarrollado algún trastorno por abuso de sustancias1.
En México, de acuerdo a la Encuesta Nacional de Consumo de Drogas, Alcohol y Tabaco (ENCODAT, 2016-2017), el consumo de drogas en general (legales e ilegales) se incrementó de 2011 a 2016 de 7.8 a 10.3% en la población; y de drogas ilegales se incrementó de 7.2 a 9.9%2. El último «Informe de la Situación de la Salud Mental y el Consumo de Sustancias Psicoactivas en México-2021» reportó que 38.5% de la población consumió alguna droga (como alcohol, tabaco, drogas ilegales o medicamentos sin prescripción) en el período de un año previo a la encuesta. El alcohol (32.5%), tabaco (24.6%) y la marihuana (14.6%) fueron las sustancias de consumo más frecuentes3.
Por otra parte, en México, durante el año 2019 se registraron 2,609 muertes por el consumo de sustancias psicoactivas, el alcohol fue la principal sustancia asociada (90.2%)3. El Servicio Médico Forense reportó que en el año 2016, de 11,355 muertes, en 8.6% se encontró evidencia de alguna sustancia, la más frecuente fue el alcohol (67%)4.
El consumo excesivo de alcohol es la principal causa de accidentes de tránsito, incluyendo los atropellamientos4. De esta manera, el abuso en el consumo de alcohol y otras sustancias se relaciona directamente con las lesiones traumáticas y con la demanda de atención médica en los servicios de urgencias. No hay reportes en México, pero se estima que en Estados Unidos alrededor de 32% de los pacientes hospitalizados han consumido drogas ilícitas en algún momento de su vida5. A pesar de la alta incidencia de los pacientes consumidores de sustancias psicoactivas que requieren de atención hospitalaria, las guías actuales están encaminadas únicamente al tratamiento ambulatorio del dolor crónico, pero no contemplan la atención del dolor agudo en el contexto traumatológico.
Diversos factores y situaciones, como la tolerancia a algunos medicamentos, el daño al sistema nervioso y a órganos que intervienen en el metabolismo y eliminación de los fármacos analgésicos, el período de hospitalización sin el consumo de la sustancia que puede propiciar un síndrome de abstinencia, la decisión de usar o no opioides en el manejo del dolor agudo postoperatorio, entre otros, suelen hacer complejo el manejo del dolor agudo en estos pacientes6,7. El objetivo del estudio es describir los esquemas de tratamiento analgésico y la dosis promedio de opioide requerido para el control del dolor agudo en consumidores de sustancias hospitalizados en un servicio de traumatología.
Material y métodos
Previa aprobación por el Comité de Ética Local de Investigación en Salud 3401 del Instituto Mexicano del Seguro Social con el número de registro R-2017-3401-21, se realizó un estudio descriptivo, retrospectivo y transversal que consistió en una revisión de los expedientes de pacientes entre 18 y 64 años que fueron ingresados del 1o de enero de 2017 al 31 de agosto de 2018 al área de hospitalización del Hospital de Traumatología «Dr. Victorio de la Fuente Narváez», que refirieron en su historia clínica el antecedente de consumo crónico (mayor a tres meses) de una o más sustancias psicoactivas (marihuana, cocaína, metanfetaminas, solventes o heroína). Se incluyeron los expedientes de pacientes cuyo tratamiento del dolor agudo por evento traumático estuvo exclusivamente a cargo de los médicos especialistas en algología desde su ingreso al área de hospitalización.
Los pacientes fueron manejados de manera continua durante 24 horas con el esquema analgésico que se muestra en la Figura 1, que consiste en un opioide vía infusión intravenosa continua con la posibilidad de dosis de rescate en caso de dolor de intensidad moderada a severa, un antiinflamatorio no esteroideo (metamizol a dosis de 0.5-1g IV c/6 horas) y paracetamol vía oral en dosis de 10-15 mg/kg peso ideal cada seis horas. En caso de que el dolor se caracterizara como neuropático o mixto (nociceptivo somático y neuropático) se agregó gabapentina en dosis de 300 mg cada 12 horas vía oral.
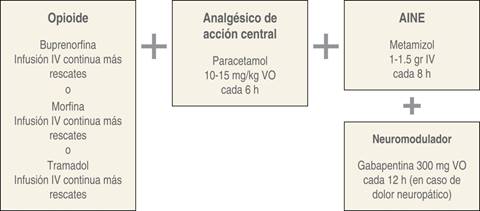
Figura 1: Esquema de analgesia multimodal empleado para el tratamiento de dolor agudo en pacientes con consumo de sustancias.
No se incluyeron expedientes incompletos o de pacientes con antecedente de dolor crónico (mayor a tres meses) o evento quirúrgico una semana previa a su hospitalización o en las 24 horas siguientes al inicio del esquema analgésico; también se excluyeron aquellos pacientes en quienes se administró adyuvante analgésico (lidocaína, dexmedetomidina o ketamina) o que fueron manejados de manera diferente a lo establecido en la Figura 1.
Las variables demográficas estudiadas fueron: edad, género y escolaridad. Las variables clínicas estudiadas fueron: sustancia de consumo, tiempo de consumo, comorbilidad, especialidad tratante de la lesión traumática y tipo de dolor. Las variables de estudio fueron: la intensidad del dolor previo al tratamiento analgésico (a su ingreso al área de hospitalización) y a las ocho, 16 y 24 horas posteriores, número de rescates en 24 horas, la dosis de opioide administrada en 24 horas y la dosis equianalgésica. Para el análisis, los pacientes se dividieron en tres grupos de acuerdo al opioide empleado en el esquema analgésico: grupo buprenorfina, grupo morfina y grupo tramadol.
La intensidad del dolor fue valorada con la escala visual analógica (EVA), la aplicación de esta escala consiste en que el paciente indica al evaluador dónde detenerse al mover lentamente una marca sobre una línea de 10 cm desde una posición «sin dolor» hasta el máximo del «dolor insoportable», la longitud de la línea que el paciente indica es la medida que se registra en centímetros8.
La dosis de opioide en 24 horas se definió como la dosis total administrada por infusión continua intravenosa sumando la dosis de los rescates utilizados en ese tiempo; la dosis se expresó en microgramos en el caso de la buprenorfina y en miligramos para tramadol y morfina; también se realizó el cálculo del requerimiento de dosis por kilogramo de peso ideal/24 horas. El peso ideal se obtuvo con la fórmula: [(talla-100)*(0.9)] para hombres, en el caso de las mujeres [(talla-100)*(0.85)].
Se organizó la información en una base de datos de Excel y el análisis estadístico se realizó a través del programa SPSS versión 24. Para el análisis descriptivo de las variables cuantitativas se realizó una prueba de normalidad Kolmogorov-Smirnov, estas variables se expresaron como medidas de tendencia central y de dispersión de acuerdo a la normalidad de la distribución de los datos. Las variables cualitativas se expresaron en cuadros como frecuencias absolutas y relativas. Se empleó prueba de t de Student para comparar la edad y tiempo de consumo entre los pacientes de los tres grupos de acuerdo al opioide empleado (buprenorfina, morfina y tramadol). La prueba de análisis de varianza por rangos de Friedman se empleó para comparar la intensidad del dolor entre los grupos según el opioide empleado. Se realizó prueba de signos de Wilcoxon para comparar la intensidad del dolor antes y después del tratamiento analgésico con esquema de cada grupo, considerando en todo caso el valor de p < 0.05 como significativo.
Resultados
Se revisaron 89 expedientes de los cuales 14 fueron excluidos por información incompleta o por uso de adyuvante o algún analgésico diferente a lo establecido en la Figura 1, por lo que un total de 75 pacientes fueron incluídos en el estudio; 94.7% (71 pacientes) fueron hombres, la edad promedio fue de 32 (± 9.6) años, mostrando una distribución normal (p = 0.77). El máximo nivel de estudios fue nivel básico en 46%, nivel medio-superior en 41% y educación superior sólo 9%; 14.6% refirió a su ingreso alguna comorbilidad: hipertensión arterial sistémica (8%), diabetes mellitus (7%), insuficiencia renal crónica (4%) y enfermedad psiquiátrica (4%). Las especialidades de traumatología que trataron la lesión de los pacientes se describen en la Tabla 1.
Tabla 1: Especialidad tratante de la lesión traumática (N = 75).
| Especialidad de traumatología | n (%) |
|---|---|
| Poliexpuestas (fracturas) | 18 (24) |
| Unidad de quemados | 15 (20) |
| Columna | 12 (16) |
| Miembro torácico | 9 (12) |
| Cirugía general | 7 (9) |
| Fémur y rodilla | 5 (7) |
| Pie y tobillo | 4 (5) |
| Cadera | 3 (4) |
| Cirugía plástica | 2 (3) |
Antecedente del consumo de sustancias. La droga de mayor consumo fue marihuana con 72% (54 pacientes), de estos casos, una mitad consumía además una o más drogas (no legales) simultáneamente. La segunda droga de mayor consumo fue la cocaína con 51% (38 pacientes). En la Tabla 2 se describe la frecuencia absoluta y relativa del consumo de sustancias psicoactivas en la población estudiada, 51% consumía sólo una sustancia (marihuana o cocaína); mientras que el restante habituaba dos o más drogas. Las sustancias como solventes, metanfetaminas y heroína se reportaron con baja frecuencia, en todos los casos se relacionaron con el consumo de varias sustancias psicoactivas.
Tabla 2: Frecuencia del consumo de sustancias psicoactivas en pacientes con lesiones traumáticas (N= 75).
| Sustancia psicoactiva | n (%) |
|---|---|
| Marihuana | 54 (72) |
| Solo marihuana | 27 (36) |
| Marihuana + cocaína | 16 (21) |
| Marihuana + alcohol | 12 (16) |
| Marihuana + tabaco | 11 (15) |
| Marihuana + solventes | 2 (3) |
| Cocaína | 38 (51) |
| Solo cocaína | 11 (15) |
| Cocaína + marihuana | 15 (20) |
| Cocaína + alcohol | 8 (11) |
| Cocaína + tabaco | 7 (9) |
| Cocaína + solventes | 2 (3) |
| Solventes + otras sustancias | 5 (9) |
| Metanfetaminas + otras sustancias | 3 (4) |
| Heroína + otras sustancias | 1 (1.3) |
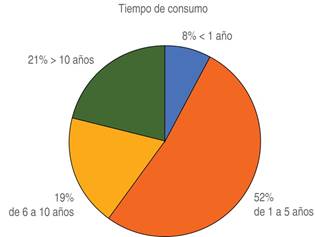
Veintinueve punto cuatro por ciento del total de pacientes afirmaron consumir tabaco y/o alcohol además de la sustancia psicoactiva, 52% refirió un tiempo de consumo de uno a cinco años. En la Figura 2 se muestra el tiempo de consumo de la sustancia psicoactiva.
Tipo e intensidad del dolor. De acuerdo a la valoración clínica, 47% (35 pacientes) fueron diagnosticados con dolor nociceptivo somático, 39% (29 pacientes) con dolor de tipo mixto (nociceptivo somático y dolor neuropático) y sólo 15% (11 pacientes) con dolor de tipo neuropático.
La intensidad del dolor fue una variable con distribución no normal (p > 0.001), por lo que sus resultados se expresaron como medianas y rangos intercuartiles (percentil 25 y percentil 75) (RIC Q1-3); la mediana previo al tratamiento en la población estudiada fue 7 (RIC 5.5-8), a las 8 horas de inicio del esquema analgésico se reportó la mediana 3 (RIC 3-5), 16 h posteriores fue 3 (RIC 3-5) y a las 24 horas fue 3 (RIC 3-4). En la Tabla 3 se muestra el tipo de dolor y la intensidad del dolor por grupo de opioide empleado.
Tabla 3: Tipo e intensidad del dolor por grupo de opioide empleado en esquema analgésico (N = 75).
| Buprenorfina (n = 37) | Morfina (n = 20) | Tramadol (n = 18) | Total | p | |
|---|---|---|---|---|---|
| Edad (años)* | 32 ± 8 | 33 ± 10.5 | 30 ± 11.2 | 32 ± 9.5 | 0.63 |
| Tiempo de consumo (meses)* | 91.7 ± 87.2 | 70.9 ± 67.7 | 60.8 ± 79.3 | 78.6 ± 81.2 | 0.36 |
| Tipo de dolor, n (%) | |||||
| Nociceptivo somático | 17 (46) | 10 (50) | 8 (44) | 35 (47) | |
| Neuropático | 3 (8) | 1 (5) | 7 (17) | 11 (15) | |
| Mixto | 17 (46) | 9 (45) | 3 (39) | 29 (39) | |
| Intensidad del dolor** | |||||
| EVA previo | 7 (6-7) | 6.5 (4-8) | 6 (5-7) | 7 (5.5-8) | 0.43 |
| EVA a las 8 h | 3 (2-5) | 3 (2-5.5) | 3 (3-4) | 3 (3-5) | 0.85 |
| EVA a las 16 h | 3 (3-5) | 3.5 (3-5) | 2 (2-5) | 3 (3-5) | 0.2 |
| EVA a las 24 h | 3 (3-4) | 4 (3-4.5) | 2 (1-3) | 3 (3-4) | 0.014 |
* Media ± desviación estándar. Prueba t de Student para comparar diferencia entre medias.
**Medianas y rangos intercuartiles. Análisis de varianza por rangos de Friedman para comparar diferencia entre medianas.
EVA = Escala Visual Analógica.
La intensidad del dolor fue menor comparando el EVA inicial y el EVA a las ocho, 16 y 24 h posteriores al inicio del esquema analgésico continuo, la diferencia fue estadísticamente significativa (p < 0.001) en todas las mediciones. En la Tabla 4 se muestra la intensidad del dolor previo y posterior al esquema analgésico por grupo de opioide.
Tabla 4: Intensidad del dolor previo y posterior al esquema analgésico continuo por grupo de opioide.
| Escala Visual Analógica | p | ||||
|---|---|---|---|---|---|
| Inicial | A las 8 h | A las 16 h | A las 24 h | ||
| Buprenorfina (n = 37)* | 7 (6-7) | 3 (2-5) | 3 (3-5) | 3 (3-4) | < 0.001 |
| Morfina (n = 20)* | 6.5 (4-8) | 3 (2-5.5) | 3.5 (3-5) | 4 (3-4.5) | < 0.001 |
| Tramadol (n = 18)* | 6 (5-7) | 3 (3-4) | 2 (2-5) | 2 (1-3) | < 0.001 |
* Medianas y rangos intercuartiles. Prueba de signos de Wilcoxon.
Tratamiento farmacológico. El opioide indicado con mayor frecuencia fue la buprenorfina en 48%, seguido de la morfina en 28% y tramadol en 24% de los pacientes, 55% (41 pacientes) requirió una o más dosis de rescate en 24 horas. La dosis promedio de la buprenorfina fue de 644 µg en 24 h (rango de 300-1,100 µg/día), de estos pacientes, 62% requirió al menos una dosis de rescate al día. La morfina se administró en una dosis media de 20 mg en 24 h (rango de 10-25 mg/día), de estos casos, 65% requirió al menos una dosis de rescate en 24 horas. La dosis promedio del tramadol fue de 194 mg en 24 h (rango 120 a 330 mg/día), con dosis de rescate solicitadas en 28%. En la Tabla 5 se muestran las dosis totales del opioide administrado en 24 horas de tratamiento analgésico continuo.
Tabla 5: Dosis total del opioide administrado en 24 horas (N = 75).
| Buprenorfina (n = 37) | Morfina (n = 20) | Tramadol (n = 18) | Total | |
|---|---|---|---|---|
| Dosis en 24 h | 644 ± 182 µg | 20.2 ± 3.9 mg | 194 ± 52.6 mg | |
| Rango de dosis en 24 h | 300-1,100 µg | 10-25 mg | 120-330 mg/24 h | |
| Dosis equianalgésica (mg de morfina en 24 h) | 21.2 (rango 9.9-36.3) | 20.2 (rango 10-25) | 19.4 (rango 12-33) | |
| Dosis peso ideal/24 h | 10.9 ± 3.2 µg/kg | 0.34 ± 0.09 mg/kg | 3.2 ± 0.76 mg/kg | |
| Rango de dosis peso ideal/ 24 h | 5.2-20 µg/kg | 0.13-0.51 mg/kg | 1.83-2.87 mg/kg | |
| Dosis de rescate, n (%) | ||||
| Ninguna | 14 (38) | 7 (35) | 13 (72) | 34 (45) |
| 1-2 en 24 h | 16 (43) | 10 (50) | 5 (28) | 31 (41) |
| 3 o más en 24 h | 7 (19) | 3 (15) | 0 | 10 (13) |
En aquéllos que cursaron con dolor de tipo neuropático al momento de la valoración, el opioide de elección fue tramadol (50%) y buprenorfina (50%). De los casos con dolor nociceptivo somático, 44% fue tratado con buprenorfina, 32% con morfina y 24% con tramadol. Mientras que aquéllos con dolor de tipo mixto (neuropático y nociceptivo somático) recibieron buprenorfina en 55% de los casos, morfina 24% y tramadol 21%. El neuromodulador se empleó en 53% (40 pacientes).
Respecto al control del dolor, se observa que el tratamiento analgésico en los tres grupos (buprenorfina, morfina y tramadol) mostró una reducción de la intensidad del dolor a las ocho, 16 y 24 horas posteriores al inicio del tratamiento; no hubo diferencia estadísticamente significativa (p < 0.05) en el control del dolor entre los tres opioides empleados, excepto que la intensidad del dolor en el grupo de morfina fue mayor respecto a los otros opioides a las 24 horas de tratamiento (p = 0.014) (Tabla 3).
Discusión
De acuerdo a Ahmadi y colaboradores, el objetivo del tratamiento del dolor en casos con trauma es reducir la morbimortalidad, acortar la estancia hospitalaria, reducir costos y mejorar la satisfacción y calidad de vida9. Cuando la lesión traumática se acompaña de un antecedente de abuso de sustancias, cumplir este objetivo del manejo adecuado del dolor se vuelve difícil por diversas circunstancias que incluyen la tolerancia, la dependencia y la supresión a la sustancia; además, es frecuente que se tengan reservas respecto al uso de opioides en estos pacientes, por lo que el dolor tiende a ser subestimado y a no ser tratado adecuadamente. Las consecuencias de ello conllevan un incremento en la incidencia de dolor crónico y en ocasiones a la reactivación o intensificación del problema previo de adicción6.
El presente estudio mostró un predominio de consumidores del género masculino con edad promedio de 32 años. Las principales sustancias de consumo fueron marihuana (72%) y cocaína (51%); la mayoría de los casos eran consumidores de alguna otra droga de manera simultánea. Dichos datos concuerdan con lo reportado previamente por la ENCODAT (2016-2017) respecto al consumo prevalente de marihuana (61%) en población mexicana2.
El analgésico opioide empleado con mayor frecuencia en los esquemas de analgesia multimodal, principalmente en los casos con dolor somático y de origen mixto, fue la buprenorfina con una dosis promedio de 644 µg en infusión al día (rango: 5.2-19.9 µg/kg/día), dicha dosis es alrededor de un 40% mayor de la dosis recomendada en la literatura para pacientes con trauma sin adicción (300-600 µg/día; media de 450 µg/día)10. La buprenorfina es un opioide potente con diferentes mecanismos de acción que le convierte en el opioide de elección en este tipo de pacientes, entre estos se encuentran: 1) es un agonista parcial de los receptores Mu con alta afinidad pero con actividad intrínseca limitada sobre estos receptores; 2) incrementa la expresión del receptor Mu en la membrana celular; 3) es un potente antagonista del receptor Kappa, responsable de efectos disfóricos y de la tolerancia; y 4) es agonista del receptor opioide nociceptina (NOR) que tiene una interacción única en el proceso del dolor; estos efectos favorecen la analgesia al mismo tiempo que se disminuyen los efectos disfóricos y otros mecanismos de tolerancia, dependencia e hiperalgesia asociada a opioides11.
La buprenorfina, junto con la metadona y la naltrexona, ha sido aprobada por la Food and Drug Administration (FDA) para tratamiento a largo plazo de la dependencia a opioides; sin embargo, cabe mencionar que sus propiedades no se limitan sólo al tratamiento de la compulsión en pacientes con adicción a opioides12, la buprenorfina posee además otros efectos a nivel de núcleos específicos del sistema mesolímbico dopaminérgico, que es donde se integran los mecanismos de adaptación y dependencia a cualquier sustancia adictiva, que le permiten mediar la compulsión a sustancias no opioides13.
En el núcleo accumbens y en el área ventral tegmental existen receptores para diversas sustancias, como receptores para cannabis, alcohol, estupefacientes, benzodiazepinas, entre otros; además, también ahí se localiza un sistema opioide endógeno complejo que es el responsable de mediar el efecto hedónico de las sustancias adictivas que estimulan a los centros que forman los circuitos de recompensa, existe evidencia de que su bloqueo reduce la compulsión no sólo en personas adictas a opioides, sino también en caso de adicción a otras sustancias13.
En 26% de los casos se empleó morfina con una dosis media de 20 mg en 24 horas (rango: 0.5-0.14mg/kg/día), cifra que se encuentra en rango inferior recomendado para pacientes con trauma sin adicción (20-30 mg para población latina)10. Cabe destacar que los pacientes de este grupo fueron los que requirieron con mayor frecuencia dosis de rescate respecto a aquéllos tratados con buprenorfina y tramadol. Probablemente, la dosis de morfina fue indicada de manera insuficiente respecto a los requerimientos analgésicos de este tipo de casos.
El resto (24%) fue manejado con tramadol con una dosis media de 194 mg al día (rango: 120 a 330 mg/día), que se encuentra también dentro del rango inferior de la dosis recomendada de 200-400 mg en infusión intravenosa para paciente con trauma10; sin embargo, reportaron un favorable resultado analgésico. Por su efecto sobre la recaptura de noradrenalina y serotonina, el tramadol fue preferentemente indicado en esquema de tratamiento para dolor neuropático14. No se han realizado estudios con tramadol para control de dolor agudo en pacientes con abuso de sustancias, pero debido a este mecanismo de acción dual, es probable que el tramadol pueda tener cierto efecto a nivel del sistema mesocorticolímbico, especialmente a nivel del locus cerúleo, cuya actividad noradrenérgica es la responsable del síndrome de abstinencia ante la interrupción de la sustancia adictiva13. Dicho efecto podría favorecer los mecanismos de antinocicepción, facilitando el manejo del dolor en estos pacientes; cabe destacar que recientemente se ha asociado al tramadol con un aumento de dopamina en el núcleo accumbens. En consecuencia, a diferencia de la morfina, el tramadol no produce la clásica sensibilización conductual, lo que explicaría también la menor incidencia de abuso con el tramadol para tratamiento del dolor crónico. Este efecto también se relaciona con su baja afinidad por los receptores opioides µ y su efecto conjunto sobre el sistema monoaminérgico15.
La analgesia multimodal a base de un opioide en infusión continua con opción de dosis de rescate, más antiinflamatorio no esteroideo (AINE) y paracetamol fue el fundamento del tratamiento del dolor por traumatismo en los pacientes con antecedente de consumo crónico de sustancias adictivas. Los resultados mostraron adecuado control del dolor agudo con una diferencia estadísticamente significativa (p < 0.001) entre la intensidad del dolor previo y el control a las ocho, 16 y 24 horas posteriores al inicio del tratamiento analgésico (Figura 1).
Según Vadivelu y colaboradores, promover el uso de analgésicos no opioides como paracetamol y AINES, así como de adyuvantes analgésicos puede ser benéfico en estos pacientes como parte de la analgesia multimodal16; a su vez, se puede reducir la dosis del opioide y con ello los efectos no deseados de tolerancia, dependencia e hiperalgesia inducida por opioides17.
Este es el primer estudio que describe esquemas de tratamiento analgésico empleados en pacientes consumidores crónicos de sustancias psicoactivas con dolor agudo y sus resultados en términos de analgesia en población latina. Además, se obtuvieron rangos de dosis de opioide empleados para el control del dolor en este tipo de casos; sin embargo, se recomienda individualizar cada caso para integrar los elementos de la analgesia multimodal que puedan responder de manera óptima a las necesidades de cada paciente, valorando aspectos clínicos y antecedentes particulares.
El estudio tiene algunas limitaciones que radican principalmente en el tiempo de seguimiento del estudio de sólo 24 horas, en que no se reportó la presencia o ausencia de reacciones adversas a los fármacos y en que no se consideró el uso de adyuvantes analgésicos (dexmedetomidina, lidocaína y ketamina) en el esquema empleado para el control del dolor. No obstante, el presente estudio apertura la evidencia para que investigaciones posteriores puedan fundamentar la creación de guías de tratamiento analgésico para esta población.
Conclusión
A través de este estudio se identificaron y describieron los esquemas de tratamiento analgésico multimodal y las dosis promedio de opioide empleadas para el control del dolor agudo en consumidores de sustancias psicoactivas hospitalizados en un servicio de traumatología. Los pacientes tratados con buprenorfina tuvieron mejor control del dolor en comparación con el grupo de morfina; aunque se requirieron de dosis 40% mayores a las recomendadas para aquéllos con trauma sin antecedente de consumo de sustancias. Se recomienda el empleo de buprenorfina en el tratamiento del dolor agudo de sujetos con adicciones. El tramadol por su efecto dual podría ser un fármaco de elección en contexto de dolor agudo, pero se requiere mayor investigación al respecto.
Aunque se requiere de mayor evidencia, los resultados de este trabajo mostraron que los opioides, como parte de un esquema de analgesia multimodal, se pueden usar de manera efectiva para el control óptimo del dolor agudo en los pacientes con adicciones, con lo cual se pretende disminuir el riesgo de complicaciones graves como el dolor crónico y el incremento en el abuso de sustancias.











 nueva página del texto (beta)
nueva página del texto (beta)