Introducción
El dolor y agitación postprocedimiento es motivo de tratamientos agresivos con opioides, AINE o ambos1),(2, que pueden provocar depresión respiratoria, peligrosa en cardiópatas congénitos con capacidad funcional limítrofe1.
La anestesia debe constar de hipnosis, amnesia y relajación muscular (teoría unitaria de Gray) y actualmente se propone la anestesia multimodal con el uso de adyuvantes que involucren un mayor número de receptores para garantizar una emersión más tranquila y con menor dolor3. Los objetivos del manejo anestésico en el cateterismo cardíaco en las cardiopatías congénitas son sedación, inmovilización, y manejo agudo de las alteraciones hemodinámicas2.
La ketamina produce depresión del SNC dosis dependiente generando un estado disociativo, mínima depresión cardiorrespiratoria y preservación de reflejos protectores de la vía aérea. Desde su introducción ha sido un anestésico ideal por su alto perfil de seguridad farmacocinético4, actualmente con un papel en el manejo del dolor5 y está siendo estudiado por los posibles efectos antidepresivos6. En pediatría sigue siendo el anestésico de elección en algunos países5),(7, porque aumenta la resistencia vascular sistémica (RVS) y gasto cardíaco sin afectar negativamente los cortocircuitos de izquierda a derecha6.
Como adyuvante analgésico perioperatorio potencializa la analgesia por opioides dependiente de la forma de administración; la combinación de dosis de carga y perfusión en dosis menores de 1-6 μg/kg/min provee efecto antihiperalgésico, analgésico y ahorrador de opioides3),(8 (concentraciones plasmáticas 30-120 ng/mL3),(6). Sus efectos adversos son leves o ausentes reduciendo la incidencia de náuseas y vómitos postoperatorios5),(7),(8.
Las dosis analgésicas varían desde dosis única de 1 mg/kg hasta perfusiones IV 3 μg/kg/min por 48 horas postoperatorias. La dosis subanestésica se definen como < 20 μg/kg/min en perfusión continua intravenosa3),(9),(10. En el centro médico de Pittsburg se ha incluido dentro de los estándares para el cuidado en el manejo del dolor postoperatorio7),(9),(10.
En la evaluación del dolor se usan escalas para diferentes edades, identificando y manejando de forma temprana el dolor mejorando el confort, disminuyendo la agitación y respuesta neurohumoral al estrés quirúrgico11. La escala de FLACC (por su siglas Face, Legs, Activity, Cry, Consolability) fue validada en 2012 para el dolor y agitación en cirugía cardíaca pediátrica para pacientes de dos meses a siete años y con retraso mental12),(13 (Cuadro I). Las tres categorías de dolor de Chen son: 0-3 no dolor o dolor leve, 4-7 moderado y 8-10 severo14. Ésta tiene fiabilidad y validez en la evaluación de dolor pediátrico a nivel internacional15),(16.
Cuadro I: Escala de dolor y agitación FLACC.
| Categorías | Puntaje 0 | 1 | 2 |
|---|---|---|---|
| Face/Expresión facial | Expresión neutra o sonrisa, contacto visual e interés en el medio | Ceño o boca fruncidos ocasionalmente, compungido, ojos parcialmente cerrados | Ceño fruncido permanente, mandíbula apretada, mentón tembloroso, arrugas frontales profundas, ojos cerrados, boca abierta, líneas profundas alrededor de nariz-labios |
| Legs/piernas | Posición normal, relajada | Inquietas, rígidas, flexión/extensión intermitente | Patadas, flexo-extensión exagerada o temblor de extremidades |
| Activity/actividad | Posición normal, tranquilo, movimiento fácil y libremente | Gira de un lado a otro, reacio a moverse, se presiona la parte del cuerpo que le duele | Rígido, arqueado, movimientos espasmódicos, inmóvil, movimientos a un lado y otro de la cabeza |
| Cry/llanto | Sin llanto o quejido (desierto o dormido) | Quejidos suaves, llanto ocasional, suspiros | Llanto mantenido, quejido intenso, gritos |
| Consolability/consolable | Tranquilo, relajado no requiere consuelo | Consolable con caricias ocasionales o palabras, es posible distraerlo | Difícil de consolar o distraerse |
Adaptado de: Cavallieri S, Canepal P. Dolor agudo post-quirúrgico en pediatría evaluación y tratamiento. Rev Mes Crin Condes. 2007;18:207-216.
0-3 no dolor o dolor leve, 4-7 moderado y 8-10 como severo14
La ketamina en el cateterismo cardíaco pediátrico es efectiva y segura17, se usa como adyuvante para tratamiento del dolor postoperatorio agudo18 y dosis subanestésicas como adyuvante de los opioides sistémicos3),(8; por lo que el objetivo general es conocer si la ketamina a dosis subanestésicas disminuye el dolor agudo, agitación postoperatoria, requerimientos de analgésicos postcateterismo cardíaco y valorar su perfil de seguridad.
Material y métodos
Previa autorización del Comité de Investigación-Ética del INCICh y consentimiento informado por los padres, se realizó un estudio prospectivo, longitudinal, comparativo, doble ciego, se incluyeron pacientes de dos meses a siete años de ambos géneros, ASA II-IV, programados para cateterismo cardíaco bajo anestesia general y ayuno completo. Se excluyeron: inestabilidad hemodinámica previa, durante o posterior al procedimiento que requiriera soporte inotrópico o vasopresor, intubación previa al procedimiento y alergias. La aleatorización se realizó con Tabla de números aleatorios.
Se definieron dos grupos: grupo K: ketamina con bolo 1 mg/kg y perfusión 2 μg/kg/min, y grupo F: fentanyl 3 μg/kg e infusión de solución salina + analgésico IV.
Posterior a inducción se coloca dispositivo avanzado de la vía aérea, ventilación mecánica controlada 6-8 mL/kg y mantenimiento sevoflurano 1-1.2 CAM.
Previo al término de procedimiento se administra analgesia con paracetamol 15 mg/kg al grupo F y solución fisiológica al grupo K.
Se registran los signos vitales basales, al inicio del procedimiento (15 minutos) y a la emersión.
Se recolectan datos con la escala de FLACC y Ramsay a la emersión, a los 10 minutos de llegar a piso, y se instruye a enfermera para administrar analgésico sólo en caso de FLACC > 4.
Resultados
Se estudiaron un total de 121 pacientes, n = 64 (52.8%) grupo K y n = 57 (47%) grupo F, con edad media 47.07 ± 26.38 meses, predominó el sexo femenino, n = 82 (67%), y un estado físico preoperatorio ASA III, n = 69 (57%).
La mayoría de los cateterismos fueron intervencionistas, n = 77 (63.6%), predominando el cierre de conducto arterioso, n = 44 (36%), un tiempo de procedimiento con media de 76.02 ± 34.71 minutos y sin diferencia en las variables demográficas entre los grupos (Cuadro II).
Cuadro II: Datos demográficos.
| Variable | Total | Grupo K | Grupo F | p |
|---|---|---|---|---|
| Pacientes (n) | 121 | 64 | 57 | 0.85 |
| Femenino (n) | 82 | 43 | 39 | 0.88 |
| Edad (meses) media ± DE | 47.07 ± 26.38 | 46.33 ± 24.84 | 47.91 ± 28.20 | 0.74 |
| Peso (kg) media ± DE | 14.78 ± 5.89 | 13.98 ± 4.68 | 15.25 ± 6.99 | 0.25 |
| Talla (cm) media ± DE | 103.07 ± 55.89 | 107. 41 ± 74.13 | 98.19 ± 21.16 | 0.34 |
| ASC (m2) media ± DE | 0.61 ± 0.19 | 0.60 ± 0.15 | 0.63 ± 0.22 | 0.34 |
| ASA II (n) | 51 | 29 | 22 | 0.45 |
| ASA III (n) | 69 | 35 | 34 | 0.45 |
| ASA IV (n) | 1 | 0 | 1 | 0.45 |
| Cateterismo diagnóstico (n) | 44 | 22 | 22 | 0.72 |
| Cateterismo terapéutico (n) | 77 | 42 | 35 | 0.63 |
| Tiempo del procedimiento (minutos) media ± DE | 76.02 ± 34.71 | 76.08 ± 37.2 | 75.96 ± 32.03 | 0.98 |
| Tiempo de la anestesia (minutos) media ± DE | 100.22 ± 38.78 | 98.52 ± 41.14 | 102.14 ± 36.23 | 0.6 |
| Vía aérea TET (n) | 97 | 51 | 46 | 0.88 |
Los datos se presentan en media ± desviación estándar. No se observan cambios significativos entre los grupos.
ASA = American Society of Anesthesiologists; K = grupo ketamina, F = grupo fentanyl.
Sin diferencias intergrupos en las variables hemodinámicas perioperatorias analizadas con la prueba t2 de Hotelling en las diferentes tomas con respecto al tiempo, demostrando estabilidad hemodinámica en la presión arterial sistólica (PAS) (p = 0.63), diastólica (PAD) (p = 0.76) y media (PAM) (p = 0.44) (Figura 1). Con diferencias estadísticamente significativas en la frecuencia cardíaca intergrupo en las diferentes tomas (FC1 p = 0.02, FC2 p = 0.03 y FC3 p = 0.03), pero no significativas en cada grupo con respecto al tiempo (p = 0.31) (Cuadro III).
Cuadro III: Variables hemodinámicas.
| Variables | Total | Grupo K | Grupo F | p | t2 de Hotelling |
|---|---|---|---|---|---|
| PAS1 (mmHg) | 93.07 ± 12.69 | 93.89 ± 11.39 | 92.14 ± 14.06 | 0.45 | 0.63 |
| PAD1 (mmHg) | 51.78 ± 12.38 | 52.77 ± 13.03 | 50.67 ± 11.61 | 0.35 | 0.76 |
| PAM1 (mmHg) | 65.54 ± 11.39 | 66.47 ± 11.35 | 64.49 ± 11.45 | 0.34 | 0.44 |
| PAS2 (mmHg) | 84.32 ± 12.12 | 86.70 ± 9.99 | 81.65 ± 13.74 | 0.21 | - |
| PAD2 (mmHg) | 47.09 ± 10.03 | 47.92 ± 10.66 | 46.16 ± 9.28 | 0.33 | - |
| PAM2 (mmHg) | 59.50 ± 9.67 | 60.85 ± 9.12 | 57.99 ± 10.12 | 0.1 | - |
| PAS3 (mmHg) | 91.88 ± 12.60 | 94.08 ± 12.06 | 89.42 ± 12.85 | 0.042 | - |
| PAD3 (mmHg) | 52.79 ± 11.99 | 53.11 ± 12.79 | 52.42 ± 11.14 | 0.75 | - |
| PAM3 (mmHg) | 65.82 ± 11.03 | 66.77 ± 11.51 | 64.75 ± 10.45 | 0.31 | - |
| FC1 (lpm) | 104.57 ± 22.42 | 108.89 ± 20.91 | 99.76 ± 23.24 | 0.024 | 0.31 |
| FC2 (lpm) | 96.32 ± 21.96 | 100.39 ± 20.70 | 91.75 ± 22.61 | 0.03 | - |
| FC3 (lpm) | 100.62 ± 20.05 | 104.27 ± 18.47 | 96.53 ± 21.10 | 0.033 | - |
| SO2 1 (%) | 88.02 ± 8.68 | 88.22 ± 9.05 | 87.79 ± 8.33 | 0.78 | 0.49 |
| SO2 2 (%) | 94.31 ± 6.56 | 94.38 ± 6.99 | 94.23 ± 6.09 | 0.9 | - |
| SO2 3 (%) | 92.94 ± 6.91 | 93.47 ± 7.03 | 92.35 ± 6.79 | 0.37 | - |
Los datos se presentan en media ± desviación estándar (DE).
1: basal, 2: al inicio del procedimiento, 3: a la extubación.
K = grupo ketamina, F = grupo fentanyl; PAS = presión arterial sistólica, PAM = presión arterial media, PAD = presión arterial diastólica; SO2 = saturación arterial de oxígeno.
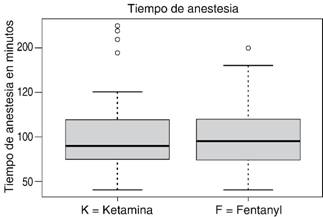
Sin diferencias estadísticas significativas entre grupos (p = 0.6) (Figura 2) en tiempo de anestesia, con una media de 100.22 ± 38.7 minutos.
El grado de sedación de acuerdo con la escala de Ramsay a la extubación fue menor en el grupo K (p = 0.03) y sin diferencias intergrupo a la llegada al piso (p = 0.31).
Los pacientes, de acuerdo con la escala de FLACC, presentaban en su mayoría dolor y agitación leve a la emersión (86.8%), predominando en el grupo K con diferencia estadísticamente significativa (p = 0.02), a su llegada a piso, el FLACC leve (92%), continuando el grupo K con significancia estadística (p = 0.002). Sin embargo, el FLACC a las seis horas fue de moderado a severo en los pacientes del grupo K con diferencia estadísticamente significativa (p = 0.002) (Cuadro IV).
Cuadro IV: Dolor y agitación a la extubación.
| Total | Grupo K | Grupo F | p | |
|---|---|---|---|---|
| Dolor y agitación a la extubación | ||||
| FLACC leve o nulo (n%) | 105 (86.8) | 60 (49.5) | 45 (37.1) | |
| FLACC moderado (n%) | 16 (13.2) | 4 (3.3) | 12 (9.9) | |
| Total (n%) | 121 (100) | 64 | 57 | 0.029 |
| Dolor y agitación al ingresar a piso | ||||
| FLACC leve o nulo (n%) | 105 (86.8) | 60 (49.5) | 45 (37.1) | |
| FLACC moderado (n%) | 16 (13.2) | 4 (3.3) | 12 (9.9) | |
| Total (n%) | 121 (100) | 64 | 57 | 0.016 |
| Tiempo entre fin del estudio y primera dosis, media ± DE (horas) | 8.63 ± 6.185 | 6.89 ± 3.94 | 10.58 ± 7.56 | 0.001 |
El requerimiento de analgésico posterior al procedimiento se presentó a las seis horas en el grupo K, comparado con el grupo F más analgésico, requiriéndolo hasta las 10 horas con diferencia estadística (p = 0.001) (Figura 3).
Tres pacientes del grupo K presentaron laringoespasmo (p = 0.098), tratados sólo con presión positiva intermitente VPPi. No hubo hematoma, ni reacciones de emergencia.
Discusión
Los pacientes pediátricos sometidos a cateterismo cardíaco requieren que la técnica anestésica sea administrada por personal con conocimientos sólidos y experiencia, ya que el número de intervenciones ha incrementado en los últimos años y la incidencia de paro cardíaco en éstos es de 0.49%, con una mortalidad de 0.08%19),(20.
Las indicaciones para la administración de anestesia general (AG) son: paciente en estado crítico y/o poco cooperador, procedimientos prolongados, necesidad de realizar ecocardiograma transesofágico durante el cateterismo19),(21. El uso de AG con ventilación mecánica con presión positiva alterará las presiones intracardíacas y cortocircuitos. Debe valorarse la sedación con respiración espontanea22 porque interfiere poco con la fisiología, aunque no se ha estudiado por completo el impacto de las diferentes técnicas anestésicas para el cateterismo cardíaco pediátrico23; en nuestra población se prefiere el uso de anestesia general.
Durante la inducción, las dosis de agentes anestésicos tolerados en los pacientes pediátricos con anatomía cardiovascular normal podrían llevar a un colapso hemodinámico en niños con cardiopatías congénitas complejas24.
Hasija et al. compararon el uso de ketamina, etomidato y sevoflurano concluyendo que en la inducción para cateterismos cardíacos pediátricos el etomidato condiciona menor perturbación hemodinámica, el sevoflurano mayores fluctuaciones y la ketamina proporciona efectos intermedios24.
La ketamina, usada por primera vez para cateterismo cardíaco en 1971, con ventajas de mantener ventilación espontánea, proporciona equilibrio hemodinámico, provee analgesia y mantiene al paciente sedado e inmóvil, se considera la opción preferente para procedimientos fuera de quirófano19),(22),(25.
A dosis de bolo de 2-2.5 mg/kg eleva significativamente la frecuencia cardíaca, presión arterial pulmonar (PAP) y la resistencia vascular pulmonar (RVP), sin generar cambios significativos en la presión arterial media, RVS, gasto cardíaco, corto circuito, PaO2 o PaCO2 en niños con cardiopatías congénitas sometidos a cateterismo cardíaco26, que correlaciona con las variables hemodinámicas observadas en el presente estudio donde no se documentaron diferencias entre los grupos.
La perfusión de ketamina a 50-75 μg/kg/min incrementa la PAM, pero no la PAP, RVS o RVP2),(27. Las dosis utilizadas en este ensayo son subanestésicas (2 μg/kg/min), por lo que no se observaron incrementos en la PAM, hallazgo que indica que preserva la hemodinamia con pocos efectos secundarios28.
Existe controversia en el uso de ketamina en pacientes con hipertensión arterial pulmonar HAP, ya que éste puede alterar el perfil de seguridad; Williams et al. documentaron su uso exitoso en pacientes con HAP severa29, aunque existen otros autores que tienen resultados controversiales2),(19),(26. La administración de ketamina en HAP no se asocia con aumento de complicaciones, ya sea como agente único o en combinación con propofol y/o anestésicos volátiles, las tasas de reanimación cardiopulmonar y mortalidad fueron inferiores a lo reportado previamente en los niños con HAP30.
Meretoja et al. describen que los opioides como fentanyl son de inicio rápido, corta duración y proveen adecuada estabilidad y analgesia, pero deben usarse con precaución en pacientes en los que la depresión respiratoria puede generar condiciones deletéreas, como en este grupo tan susceptible31.
El uso de ketamina para cateterismo cardíaco en este estudio demuestra que no se prolonga el tiempo de emersión anestésica en contraposición a lo referido en la revisión de Lam et al.32 donde mencionan que prolonga el despertar3),(24),(26),(33),(34; en la mayoría de estos estudios se combinó con midazolam o propofol, en contraposición con este ensayo, donde se utilizó como agente único. La sedación medida con la escala de Ramsay demostró que la recuperación en el grupo K fue mejor al momento de la extubación y al arribo a piso ambos grupos se comportaron de manera similar.
La descripción del efecto analgésico de ketamina es difícil debido a las diferentes vías de administración, perfusiones, distintas dosis y uso de analgésicos de rescate35. Sin embargo, la intensidad del dolor medida en diferentes escalas es menor 25-87.5% cuando se utilizó ketamina3),(8),(36),(37.
El dolor y agitación valorado con la escala de FLACC a la emersión, arribar a piso y hasta las seis horas posteriores al procedimiento fue significativamente menor en el grupo K, siendo eficaz para valoración en el período postprocedimiento, como lo demuestran diferentes autores13),(38.
Kamarmaz et al. describieron reducción de las escalas de dolor en las primeras seis horas postoperatorio cuando se administró ketamina en bolo de 0.5 mg/kg y perfusión transoperatoria de 8 mg/kg/min39.
Roelofse y colaboradores encontraron que en las primeras 12 horas sólo 1.6% necesitó dosis adicionales de analgésicos7, en contraposición con lo observado en nuestro estudio, donde los requerimientos analgésicos se observaron hasta las seis horas.
El estudio de Bell et al.8 que indica que la ketamina reduce la náusea y vómito postoperatorios, concuerda con nuestro análisis, ya que esta complicación no se observó.
Karapinar et al. describieron que las reacciones de emergencia o complicaciones se presentan en 2% de los casos40, que correlaciona con lo encontrado en nuestro estudio, 2.5%, siendo el laringoespasmo la única documentada, además sin presentar broncoespasmo, disforia, náusea, vómito y/o movimientos involuntarios.
Conclusiones
El uso de ketamina en bolo y perfusión transoperatoria presenta estabilidad hemodinámica, sin prolongar el tiempo anestésico, disminuye la agitación y el dolor postprocedimiento hasta las primeras seis horas, sin presentar mayor grado de sedación.
La ketamina se puede utilizar como coadyuvante anestésico en los cateterismos diagnósticos y terapéuticos de forma segura sin que se presenten eventos adversos significativos y sin que influya en el diagnóstico.











 nueva página del texto (beta)
nueva página del texto (beta)