Introducción
La Organización Mundial de la Salud (OMS) estima que la hipertensión arterial sistémica (HTAS) causa la muerte de 7.5 millones de personas y representa 12.8% del total de las muertes, además señala que uno de cada tres adultos padece hipertensión arterial sistémica, lo que preocupa por las complicaciones que genera (insuficiencia cardiaca, enfermedad vascular periférica, insuficiencia renal, retinopatía y discapacidad visual).1
Se define como hipertensión arterial resistente la persistencia de valores de presión arterial por arriba de la meta (< 140/90 mmHg en la mayoría de los pacientes, y < 130/80 mmHg en las personas con enfermedad isquémica del corazón, diabetes o insuficiencia renal) a pesar de una buena adherencia al tratamiento antihipertensivo apropiado que incluya tres o más fármacos de diferentes clases (incluyendo un diurético) en una combinación recomendada, y a dosis óptima (individualizada), cumpliendo con las medidas conductuales en forma adecuada.2,3
Las directrices internacionales recomiendan el monitoreo ambulatorio continuo durante 24 horas en pacientes con hipertensión resistente para excluir pseudorresistencia y para evaluar con mayor precisión el control de la presión arterial.4
El sistema nervioso simpático y su influencia en la hipertensión arterial sistémica
El sistema nervioso autónomo, mediante el tronco simpático torácico y lumbar, provee a los riñones una red de nervios eferentes y aferentes, siendo éstos los principales reguladores de su función en cuanto a la homeostasis de volumen y de la presión arterial sistémica.5
La etiología de la HTASR es multifactorial; sin embargo, existe numerosa evidencia que indica que la hiperactividad del sistema simpático es importante, y en particular a nivel renal por promover la retención de volumen, aumentar la absorción de sodio y activar el sistema renina-angiotensina.6,7
La variabilidad de la frecuencia cardiaca
Se define como la variación de la frecuencia del latido cardiaco durante un intervalo de tiempo (nunca superior a 24 horas).8 El concepto de la frecuencia cardiaca es uno de los parámetros no invasivos que más se utiliza en el análisis y en la valoración de la actividad cardiaca.9 La manera habitual de medir esta variabilidad es a partir del electrocardiograma, en el cual se detecta cada una de las ondas R y se calcula el tiempo entre las diferentes ondas R consecutivas. La serie de intervalos RR o intervalos NN (latido Normal a latido Normal) es lo que llamamos variabilidad de la frecuencia cardiaca.10,11
Esta variabilidad es el resultado de las interacciones del sistema nervioso autónomo y el sistema cardiovascular. El sistema nervioso autónomo se basa en un equilibrio entre el sistema nervioso simpático (SNS) y el sistema nervioso parasimpático (SNP).
En un estado de reposo predomina la estimulación vagal o SNP, mientras que en estado de ansiedad, estrés y ejercicio físico predomina la estimulación del SNS.10,11
La variabilidad de la frecuencia cardiaca está influida por otros factores como género, edad, respiración, acondicionamiento físico, actividad física entre otros. Hay distintos métodos para analizar la variabilidad de la frecuencia cardiaca, los que más se utilizan son los que se basan en métodos lineales (dominio temporal y el dominio de la frecuencia) y los no lineales (las medidas geométricas de los intervalos RR).12
Métodos lineales
Dominio temporal. Se refiere a los diferentes parámetros estadísticos que resultan de la medición electrocardiográfica de los intervalos RR o NN. Los parámetros que más se utilizan de primera categoría son: SDNN, SDANN y el SD.
SDNN: es la desviación estándar de todos los intervalos NN, se expresa en milisegundos (ms), su valor normal es de 141 ± 39 ms.
Dominio de la frecuencia. El análisis de la densidad espectral de la energía describe las oscilaciones periódicas de la señal del ritmo cardiaco descompuesta en diversas frecuencias y amplitudes, obteniendo diferentes componentes frecuenciales que se encuentran en un margen de 0 a 0.4 hertzios (Hz) y se puede dividir en cuatro bandas:
Ultra muy baja frecuencia (ULF). Abarca el rango de frecuencias inferiores a 0.003 Hz. Son más visibles en periodos largos de medida (24 horas).
Muy baja frecuencia (VLF): en este rango (0.003 a 0.04 Hz) se muestran las influencias hormonales, vasomotoras y termorreguladoras y también la influencia del sistema renina-angiotensina aldosterona.
Baja frecuencia (LF): situada entre 0.04 y 0.15 Hz. Es la zona más controvertida en su interpretación, ya que puede atribuirse a influencias del SNS y/o a las del SNP. También se considera una zona representativa de la actividad barorreceptora.
Alta frecuencia (HF): se encuentra situada entre 0.15 y 0.4 Hz. Está claramente relacionada con la actividad del SNP y tiene un efecto relacionado con la relajación en la frecuencia cardiaca.13
Variabilidad de la frecuencia cardiaca y enfermedad cardiaca
La disminución en la variabilidad de la frecuencia cardiaca ha sido reportada en enfermedad cardiaca.14 En infarto al miocardio, la reducción de la variabilidad de la frecuencia cardiaca refleja un decremento en la actividad vagal que conduce a la prevalencia de sistema simpático y conlleva a inestabilidad eléctrica cardiaca, lo que incrementa seis veces más la probabilidad de riesgo de muerte súbita por fibrilación ventricular.15
En insuficiencia cardiaca está relacionada con disfunción ventricular izquierda, baja tolerancia a la actividad física y estado caquéctico, entre otros.16
Denervación renal en la HTARS
De acuerdo con las Guías 2013 de la Sociedad Europea de la Hipertensión (ESH) y la Sociedad Europea de Cardiología (ESC), para el manejo de la hipertensión arterial sistémica se puede realizar la denervación renal en pacientes con hipertensión resistente verdadera, confirmada con monitorización ambulatoria continua, con nivel de evidencia I y grado de recomendación C. Actualmente se considera un procedimiento seguro y que podría ser efectivo en subgrupos específicos.17,18
HTASR y variabilidad de la frecuencia cardiaca
Los resultados encontrados hasta el momento apoyan la asociación entre el sistema nervioso simpático y la hipertensión refractaria;19 sin embargo, la medición de la actividad simpática en humanos es difícil de medir y requiere de técnicas complejas.20 La asociación entre hipertensión arterial sistémica refractaria y frecuencia cardiaca no ha sido ampliamente valorada.21
Denervación renal por radiofrecuencia y análisis de la variabilidad
En un estudio prospectivo efectuado en 14 pacientes con HTASR tratados mediante ablación renal con radiofrecuencia se realizó el análisis de la variabilidad de la frecuencia cardiaca en el dominio del tiempo y de las frecuencias mediante monitoreo Holter de 24 horas, previo a la denervación renal y tres meses después del procedimiento. Los resultados obtenidos fueron incremento en la media de los intervalos RR (924 + 8.5 ms versus 957 + 8.9 ms, p < 0.01), así como reducción de las bajas frecuencias para el dominio frecuencia (398 + 30.1 ms2 versus 324 + 16.5 ms2, p < 0.05). Se concluyó que la disminución en el tono simpático a nivel cardiaco implicaría un efecto benéfico en la disminución del riesgo cardiovascular.22
En el reporte de un caso de un paciente con HTASR tratado con denervación renal por radiofrecuencia se encontró una disminución en las bajas frecuencias en el dominio frecuencia al mes de seguimiento, concluyéndose que es necesaria la realización de más estudios que incluyan un número mayor de pacientes y a mayor seguimiento.23,24
Material y métodos
Estudio observacional, descriptivo y analítico realizado en derechohabientes en el Hospital Central Militar de mayo a octubre de 2014 en pacientes con diagnóstico de hipertensión arterial sistémica refractaria tratados mediante denervación renal por radiofrecuencia.
El diagnóstico de HTARS se realizó en pacientes de ambos géneros con edad entre 18 y 80 años, con presión arterial en el consultorio por encima de la meta apropiada del tratamiento (> 140/90 mmHg para la mayoría de los pacientes y < 130/80 mmHg para las personas con cardiopatía isquémica, diabetes o insuficiencia renal) a pesar del uso de tres o más fármacos antihipertensivos de diferentes clases a dosis completas, uno de los cuales fue un diurético.
El diagnóstico de HTASR se estableció después de tres consultas médicas con una semana de separación y se corroboró mediante monitoreo continuo de la presión arterial (MAPA).
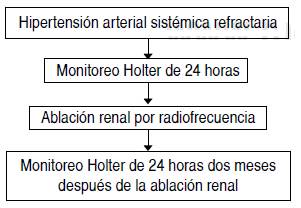
A los pacientes a quienes se les realizó el monitoreo Holter con el dispositivo de monitoreo Holter Cardiopoint BTL-H600®, antes y dos meses después de la denervación renal, se efectuó el análisis de la variabilidad de la frecuencia cardiaca en el dominio temporal a largo plazo en la variable SDNN (Figura 1).
La denervación renal por radiofrecuencia mediante el dispositivo Symplicity® con la técnica habitual. De distal a proximal con parámetros de 8 wats, 120 segundos, temperatura de 50 a 60 oC, en cinco sitios siguiendo la secuencia inferior, anterior, superior, posterior y ostial para cada arteria renal. El operador que llevó a cabo la denervación renal debía haber realizado por lo menos tres procedimientos anteriormente (Figura 2).
Análisis estadístico
Para el tratamiento de las variables y su estadística se usó el Software Microsoft Excel® 2007, en el cual se ingresaron los datos para la representación gráfica de resultados y aplicación de formularios para la prueba t de Student. Los resultados se expresaron como promedios y desviación estándar (DE). Los valores de p < 0.05 se consideraron como significativos.
Resultados
Para la realización de este estudio fueron elegibles nueve pacientes, de los cuales dos no contaron con estudio de monitoreo Holter previo a la denervación renal y uno no acudió a su seguimiento; se incluyeron seis pacientes. Las características de los pacientes fueron de la siguiente manera: tres pacientes masculinos y tres pacientes femeninos, con edad promedio de 65 ± 8.6 años, con diagnóstico de hipertensión arterial sistémica de 20 ± 8 años, con índice de masa corporal de 30.7 ± 3.7 kg/mt2 (Cuadro 1).
Cuadro 1 Características de los pacientes.
| Características de la muestra (promedio ± desviación estándar o %) | |
| Número de pacientes | n = 6 |
| Edad (años) | 65 ± 8.6 |
| Hombres | 3 |
| Mujeres | 3 |
| Años diagnóstico de hipertensión arterial sistémica | 20 ± 8.3 |
| Presión arterial sistólica consultorio (mmHg) | 143 ± 8.0 |
| Presión arterial diastólica consultorio (mmHg) | 75 ± 12.0 |
| Presión arterial sistólica MAPA (mmHg) | 143 ± 18.0 |
| Presión arterial diastólica MAPA (mmHg) | 70 ± 10.0 |
| Índice de masa corporal (kg/m2) | 30.7 ± 3.7 |
| Historia médica | n (%) |
| Diabetes tipo 2 | 3 (50) |
| Cardiopatía isquémica | 1 (16) |
| Dislipidemia | 3 (50) |
| Estenosis aórtica/TAVI | 1 (16) |
Respecto al tratamiento antihipertensivo observado, los pacientes tenían en promedio 5 ± 1 fármacos, constituyendo su tratamiento antihipertensivo inhibidores de la enzima convertidora de angiotensina (n = 3, 50%), bloqueadores del receptor de angiotensina (n = 6, 100%), antagonistas de aldosterona (n = 3, 50%), betabloqueadores (n = 6, 100%), calcioantagonistas (n = 6, 100%) y diuréticos (n = 6, 100%) (Cuadro 2).
Cuadro 2 Tratamiento antihipertensivo observado.
| n (%) | |
| Número de fármacos antihipertensivos | 5 ± 1 |
| Inhibidores de la enzima convertidora de angiotensina | 3 (50) |
| Bloqueadores del receptor de angiotensina | 6 (100) |
| Antagonista de aldosterona | 3 (50) |
| Betabloqueadores | 6 (100) |
| Calcioantagonistas | 6 (100) |
| Diuréticos | 6 (100) |
La presión arterial sistólica promedio detectada en el consultorio antes de la denervación renal fue de 143 ± 8 mmHg y la diastólica fue de 75 ± 12 mmHg. Dos meses después del procedimiento de denervación renal, el promedio de la presión arterial sistólica observada en el consultorio fue de 120 ±10 mmHg y para la diastólica fue de 70 ± 9 mmHg. Se redujo la presión arterial sistémica sistólica en 23 mmHg sin modificar el tratamiento médico previo (p = 0.0025) y la diastólica en 5 mmHg (p = 0.47) (Figuras 3 y 4).
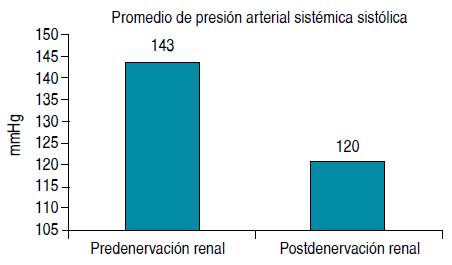
Figura 3 Presión arterial sistémica sistólica promedio en el consultorio antes y dos meses después de la denervación renal. Se observó una disminución de la presión arterial de 23 mmHg (IC 95%, p = 0.0025).
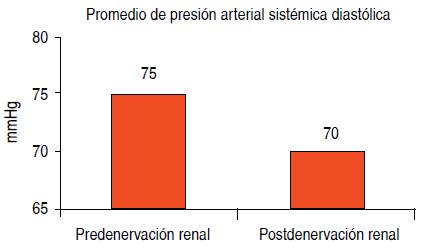
Figura 4 Presión arterial sistémica diastólica promedio en el consultorio antes y dos meses después de la denervación renal. Se observó una disminución de la presión arterial diastólica de 5 mmHg (IC 95%, p = 0.47).
Para la medición de la variabilidad de la frecuencia cardiaca en el dominio temporal a largo término se obtuvo la variable SDNN mediante el equipo de monitoreo cardiaco Holter de 24 horas, previo y dos meses posteriores a la denervación renal. El SDNN promedio observado antes de la denervación renal fue de 126 ± 17 ms, y dos meses después de la denervación renal el promedio fue de 133 ± 41 ms. Se detectó aumento de la variabilidad en 7 ms (IC 95%, p = 0.58) (Figura 5).
Discusión
La variabilidad de la frecuencia cardiaca está influida por factores como género, edad, respiración, acondicionamiento físico, actividad física entre otros. En la actualidad existen distintos métodos para su análisis, los que más se utilizan son los que se basan en métodos lineales (dominio temporal y el dominio frecuencial) y no lineales (las medidas geométricas de los intervalos RR). En nuestro estudio, debido al Software del monitoreo ambulatorio cardiaco Holter, sólo fue posible realizar el análisis en el dominio temporal.
De los seis pacientes que se incluyeron en este estudio, cada paciente tenía en promedio 5 ± 1 fármacos antihipertensivos; alteran la variabilidad de la frecuencia cardiaca los betabloqueadores y calcioantagonistas por su efecto cronotrópico negativo; sin embargo, todos los pacientes recibían estos dos fármacos.
Las enfermedades concomitantes en la población de estudio fueron diabetes tipo 2 (n = 3, 50%), cardiopatía isquémica estable (n = 1, 16%), dislipidemia (n = 3, 50%) y estenosis aórtica tratada mediante implante de válvula aórtica transcatéter (n = 1, 16%). Se observó de forma basal un SDNN de 126 ± 17 ms, siendo considerado como normal. Los pacientes no se encontraban en falla cardiaca sintomática descompensada con cardiopatía isquémica inestable o con arritmia, lo cual consideramos que influyó en un SDNN basal normal. Dos meses después de la denervación renal por radiofrecuencia se observó un SDNN de 133 ± 41 ms, incrementándose en 7 ms, sin significancia estadística (p = 0.58).
También se detectó que la presión arterial sistólica de consultorio disminuyó en un promedio de 23 mmHg (basal 143 ± 8 mmHg, postdenervación renal 120 ± 10 mmHg) sin modificar el tratamiento médico, siendo estadísticamente significativa (p = 0.0025); la presión arterial diastólica de consultorio disminuyó en un promedio de 5 mmHg (basal 75 ± 12 mmHg, postdenervación renal 70 ± 9 mmHg), sin significancia estadística (p = 0.47).
El incremento no significativo de la variabilidad de la frecuencia cardiaca en el dominio temporal de este estudio podría ser explicado por:
1. Muestra insuficiente.
2. Los pacientes incluidos no tenían cardiopatía isquémica inestable, falla cardiaca sintomática o descompensada, por lo que la variabilidad de la frecuencia cardiaca basal no resultó alterada.
3. Todos los pacientes se encontraban con fármacos con efecto cronotrópico negativo, lo cual altera la variabilidad basal y postdenervación de la frecuencia cardiaca.
4. La denervación renal sólo tendría efecto en la presión arterial al disminuir la expresión del tono simpático a nivel renal, en el eje renina angiotensina aldosterona y no tendría efecto en la variabilidad de la frecuencia cardiaca.
5. Que la técnica de denervación renal no haya sido realizada de manera correcta y la disminución en la presión arterial sistólica observada, sin haberse afectado la variabilidad de la frecuencia cardiaca, haya sido por un apego estricto del paciente a su tratamiento farmacológico antihipertensivo, al percibirse como sujeto de estudio.
El mejor escenario para valorar el efecto de la denervación renal en la variabilidad de la frecuencia cardiaca sería en pacientes con hipertensión arterial sistémica refractaria que:
1. No tengan fármacos antihipertensivos con efectos cronotrópicos negativos.
2. Tengan enfermedades cardiovasculares con disminución basal de la variabilidad de la frecuencia cardiaca.
3. Sean grupos con enfermedades específicas concomitantes como falla cardiaca sintomática.
Consideramos que determinar el efecto real de la ablación renal con radiofrecuencia en la variabilidad de la frecuencia cardiaca en diferentes escenarios clínicos permitirá al cardiólogo clínico hacer un óptimo ajuste de fármacos antihipertensivos en el seguimiento, es decir, que el paciente con adecuada respuesta a la denervación renal y con disminución de la variabilidad se beneficiaría al continuar con fármacos inotrópicos negativos y el retiro gradual de los fármacos dirigidos al eje renina-angiotensina-aldosterona.
Durante el procedimiento de denervación renal no hubo complicaciones, determinando que es un procedimiento seguro para el paciente hipertenso.
Conclusión
En nuestro estudio se observó que en pacientes con hipertensión arterial sistémica refractaria tratados mediante ablación renal por radiofrecuencia, dos meses posteriores al procedimiento, la variabilidad de la frecuencia cardiaca en el dominio temporal para la desviación estándar de los intervalos NN (SDNN) se incrementó 7 ms, siendo estadísticamente no significativo (p = 0.58).
Perspectivas y recomendaciones
Continuar con la inclusión de pacientes a fin de incrementar la muestra. Llevar un estricto control del cumplimiento del tratamiento antihipertensivo. Realizar el análisis específico de la variabilidad de la frecuencia cardiaca por grupos para identificar el perfil del paciente con variabilidad disminuida; este grupo sería el ideal para el análisis de la denervación sobre la variabilidad de la frecuencia cardiaca. Incluir en los próximos estudios de denervación renal niveles séricos de renina, angiotensina II y aldosterona, y así poder valorar el efecto de la ablación a nivel del eje renina, angiotensina y aldosterona. Gestionar la mejora del Software del monitoreo cardiaco Holter para la medición correcta de la variabilidad de la frecuencia cardiaca en el dominio frecuencial.











 nueva página del texto (beta)
nueva página del texto (beta)