Introducción
Las fracturas acetabulares han sido y siguen siendo un problema difícil de tratar.1-4 Las complicaciones que pueden presentarse con frecuencia dejan secuelas disfuncionales que incapacitan al paciente.3,5 El hueso iliaco puede quedar debilitado tanto en la zona de carga acetabular como en el fondo del mismo, la placa cuadrilátera y las columnas anterior y posterior como resultado de la pérdida de la vascularidad de estas áreas y, por tanto, desarrollo de hueso con baja densidad mineral incompetente para la carga; de ahí la importancia del tratamiento inicial adecuado, con reducción anatómica y fijación estable para evitar el aflojamiento y migración de la copa acetabular.6 Letournel y Judet demostraron una importante correlación entre la aparición de artrosis y la calidad de la reducción, con un 10.2% después de una reducción perfecta y un 32.7% con una reducción inadecuada (2-3 mm de desplazamiento).2
Las pérdidas óseas extensas como complicación tardía de la cirugía artroplástica significan problemas difíciles de resolver y su frecuencia va en aumento, porque la patología degenerativa articular es quizás la más frecuente en ortopedia, así como por el incremento en el número de sustituciones articulares, aun en pacientes jóvenes. La literatura médica crece en este tema de tratamientos no artroplásticos.7-10
Existen diferentes métodos para abordar los defectos óseos acetabulares e intentar colocar los componentes en posición anatómica, como son las cajas de reconstrucción, megacopas, copas cementadas en hueso huésped, copas con repisas o cejas, copas con aumentos de metal trabecular, sin que ninguno demuestre superioridad significativa sobre los demás.11,12
Caso clínico
Paciente del sexo femenino; fecha de nacimiento: 26 de julio de 1947. Inició su padecimiento en 1983 (a los 36 años de edad), en un accidente automovilístico que ocasionó fractura bilateral del acetábulo; fue tratada con reducción abierta y fijación interna con tornillos. Se retiró el material de osteosíntesis en 1984. En abril de 1985, a los 37 años de edad, se colocó una prótesis total de cadera del lado izquierdo, modelo St. George Mark II, CII (Link, Hamburgo), con injerto autólogo de la cabeza femoral, copa 54 x 33.5 mm (cabeza del implante: 33 mm), ambos componentes cementados. En septiembre de 1986, con 39 años de edad, se colocó una prótesis total de cadera derecha, con los mismos diseños de implantes cementados. Evolucionó satisfactoriamente hasta marzo de 1994, cuando inició con molestias en la cadera izquierda, que progresaron a limitantes. En enero de 1995, se realizó la primera cirugía de revisión, limpieza de osteofitos periacetabulares y tejido fibroso cicatricial; no se reportó aflojamiento de la copa. Mejoró unos meses y recayó; se obtuvo evidencia radiográfica de aflojamiento del implante acetabular; se reoperó en septiembre de 1995: segunda revisión de la cadera izquierda, colocación de un anillo de reforzamiento tipo Müller de 56 mm (Synthes, Suiza) fijado con tornillos de 6 mm más injerto autólogo de cresta iliaca y hueso de bovino, colocando copa cementada igual a la primaria (Figura 1). La evolución fue satisfactoria. En septiembre de 1998, en controles radiográficos, se reportó una ligera migración cefálica del anillo de reforzamiento; aparecieron pequeñas molestias relacionadas a posición y esfuerzos realizados, sin mayores limitaciones. En diciembre de 2001, aumentó el dolor; se observó ruptura de los tornillos del anillo de reforzamiento. En enero de 2002, se llevó a cabo una tercera revisión de la cadera izquierda; los análisis preoperatorios reportaron serología positiva para el virus de la hepatitis C (multitransfundida). Se observaron en Rx todos los tornillos rotos, desplazamiento cefálico y anterior del anillo de reforzamiento, gran pérdida ósea de la columna anterior, techo acetabular anterior y fondo del mismo. Se colocó una copa Mathys 64 mm (Mathys Orthopaedics, Suiza) más injerto ChronOS (Synthes, Suiza), concentrado plaquetario autólogo y trombina bovina; el vástago femoral también se encontró flojo, con acentuado debilitamiento de las corticales anterior y lateral. Se colocó un vástago de revisión Wagner 225 x 19 mm (Zimmer, Warsaw, Ind.) (Figura 2). La estabilidad de la copa se perdió rápidamente, a pesar de no apoyar peso corporal en la pierna izquierda, por lo que se reintervino en junio de 2002 (cuarta revisión), colocándose una placa DCP angosta de nueve orificios, fija a la rama iliopúbica e iliaco a modo de columna anterior acetabular para dar soporte a la nueva copa Mathys (Mathys Orthopaedics, Suiza) de 66 mm más ChronOS (Synthes, Suiza) y concentrado plaquetario autólogo más trombina (Beriplast). El fémur evolucionó de manera satisfactoria (Figura 3). Presentó luxación de la cadera izquierda en agosto de 2002, que se volvió recurrente, de fácil reducción (deficiente musculatura) y con una función articular aceptable. La evidencia radiográfica parecía indicar recuperación ósea, con aumento de la densidad mineral y aparente integración de injertos, por lo que, ante la luxación recurrente de la prótesis, se reintervino. La quinta revisión se efectuó en septiembre de 2003, retirándose la placa DCP, sin encontrar evidencia de integración ósea de los injertos previos ni desarrollo de hueso nuevo; al limpiar el iliaco, se encontró el mismo defecto óseo ya reportado, un poco mayor ahora; se colocó un nuevo anillo de reforzamiento tipo Wagner 68 mm (Sulzer Orthopaedics, Suiza), con gancho obturador y dos alerones para fijación con tornillos al iliaco; se injertó con chips de hueso liofilizado más concentrado plaquetario autólogo y trombina (Tissucol) (Figura 4). Evolucionó muy bien, temerosa por las luxaciones anteriores; recuperó una buena función. En junio de 2004, desarrolló edema de la pierna izquierda, se detectó una masa pulsátil en la región inguinal izquierda; la arteriografía reportó pseudoaneurisma de la arteria iliaca externa, que fue tratada por un cirujano vascular con stent largo. Recuperó una buena circulación, desapareció el edema. La cicatriz de la cirugía vascular evolucionó eritematosa, con área periférica endurada, dolorosa; aunque cicatrizó bien, reinició el malestar en cadera que ya no tenía, con sensación de subluxación casi constante. Por tomografía axial computarizada (TAC) se detectó una gran colección líquida en el área de la cadera, que se drenó (octubre de 2002) por vía anterior a la articulación, obteniendo líquido seroso con gran cantidad de grumos, presencia de células gigantes y acentuada reacción a cuerpo extraño con cultivo negativo (recibía antibióticos recetados por un infectólogo desde la cirugía vascular). Evolucionó bien hasta julio de 2009; nuevamente, reportó una masa pulsátil en la región inguinal y anterior de la cadera izquierda; fue reintervenida por un cirujano vascular con derivación larga de iliaca externa derecha a izquierda. Los síntomas mejoraron, pero, de nuevo, la herida se presentó eritematosa, dolorosa, con aumento de temperatura en la región inguinal y anterior de la cadera izquierda. Una nueva TAC reportó colección líquida en el área de la cadera; artrocentesis por el radiólogo (octubre 2009). Persistió el dolor e inestabilidad en la cadera izquierda; se suspendieron los antibióticos. Se obtuvo una muestra para cultivo por punción de la cadera13,14 (enero de 2010), en la que se observó desarrollo de Staphylococcus aureus. La radiografía mostró ruptura de casi todos los tornillos del anillo de reforzamiento, pero con mínimo desplazamiento del mismo (Figura 5). La paciente podía apoyar con ayuda de muletas. En febrero de 2010, se reintervino (sexta revisión): desbridamiento y limpieza extensa del campo quirúrgico, retiro del hueso desvitalizado en la zona trocantérica, recubriendo el área con un manto de polimetilmetacrilato más clindamicina y vancomicina.13,15,16 Se retiró todo el material metálico en iliaco y detritus de los injertos anteriores de coralina, hueso bovino y liofilizado, sin ninguna evidencia de actividad osteogenética, salvo en el origen de la rama iliopúbica; quedó una enorme pérdida ósea, Paprosky IIIb, AAOS III,17,18 la cual se reconstruyó con dos capas de cemento óseo con clindamicina y vancomicina. Una placa de cemento se colocó intrapélvica inmediata y subyacente al músculo iliaco; se le hicieron varias perforaciones con broca de 4.5 mm para fijar dos porciones de cemento óseo, igualmente con antibiótico, rellenando toda la cavidad faltante acetabular y labrando en el mismo un neoacetábulo para la cabeza femoral de 32 mm. Se obtuvo una articulación estable y móvil, reconstrucción que funcionó bien, controlando la infección, hasta enero de 2011 (un año) (Figura 6).19,20 Se luxó por ruptura de la ceja posterior del espaciador de cemento, se reoperó de nuevo (séptima revisión) para retirar el cemento: limpieza del campo quirúrgico, sin encontrar evidencia de infección; se hallaron tejidos sanos tanto en fémur como iliaco; se construyó una nueva articulación por medio de un componente de rescate modular de 80 mm en silla de montar (Link, Hamburgo)21,22 armado sobre el cono del vástago femoral (Figura 7).

Figura 1 Revisión de prótesis de cadera izquierda con anillo de reforzamiento tipo Müller con tornillos 6 mm más injerto.

Figura 2 Prótesis copa Mathys 64 mm más injerto ChronOS con vástago femoral de revisión. Wagner 225 x 19 mm.

Figura 3 Reintervención con placa DCP angosta de 9 orificios en columna anterior acetabular y revisión con copa Mathys 66 mm.

Figura 4 Retiro de placa DCP y revisión de acetábulo con anillo de reforzamiento Wagner 68 mm, gancho obturador y 2 alerones para fijación con tornillos al iliaco.
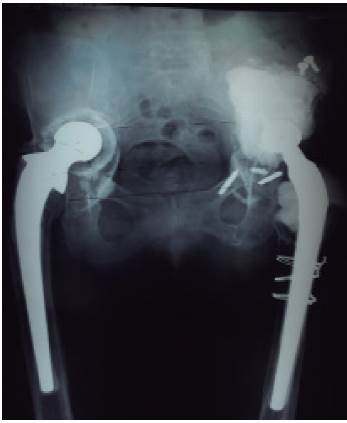
Figura 6 Revisión con recubrimiento con manto de polimetilmetacrilato con antibiótico de soporte para la cabeza femoral de 32 mm temporal.
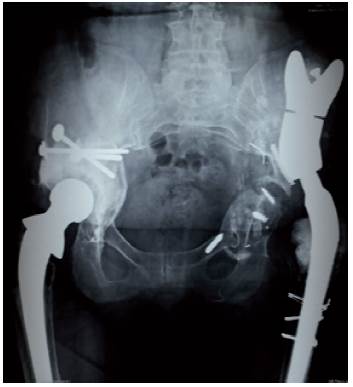
Figura 7 Revisión con componente de rescate modular de 80 mm en silla de montar sobre el cono del vástago femoral.
Ante la buena evolución de la cadera izquierda, se operó la derecha en noviembre de 2011, la cual era dolorosa, inestable, con copa cementada desplazada verticalmente, cefálica y medial, con la cabeza del implante femoral apoyada parte en polietileno y, en mayor extensión, en hueso iliaco, con desarrollo de reforzamiento óseo de la tabla interna del iliaco que contenía la copa desplazada (Figura 6). Se extrajo la cabeza del implante femoral (monobloque) del lugar en que estaba atrapada; se retiraron la copa y los restos de cemento, limpiando la cavidad ósea resultante, Paprosky IIIa,17 y rellenando a presión el defecto con injerto estructural de cabeza femoral de cadáver (Biograft),23-25 fijándola al hueso huésped con tres tornillos corticales de 4.5 mm; una segunda cabeza de cadáver se recortó en lajas óseas para complementar el llenado del defecto óseo, todas colocadas a presión. Se fresó sobre esta reconstrucción el nuevo acetábulo para cementar una nueva copa, 54 mm x 33.5 St. George Mark II (Link, Hamburgo); se hizo así por tener estable el vástago femoral monobloque cementado con cabeza de 33 mm (25 años de evolución al día de esta cirugía) (Figura 7).
La evaluación por la escala de Harris hip score26 (octubre 2014) es de 100 puntos para la cadera derecha, reportada como excelente. La cadera izquierda, con 64 puntos; es un resultado pobre, con limitación para algunas actividades, sobre todo para recorrer distancias mayores a dos cuadras por cansancio y con limitación marcada a la flexión por el modelo de prótesis, pero no es dolorosa y le permite hacer sus actividades domiciliarias diarias.
Discusión
Los pacientes jóvenes tratados con prótesis totales de cadera están expuestos a complicaciones más tempranas y complejas.27-29 Esta paciente recibió la primera prótesis izquierda a los 37 años de edad, en abril de 1985, y la última cirugía de revisión en enero de 2011; la prótesis de cadera derecha a los 39 años, en septiembre de 1986, y la única y última revisión en noviembre de 2011.
Existen varios sistemas para la reestructuración de pérdidas óseas en acetábulo,12,30 razón por la cual es necesario conocer y dominar adecuadamente estas técnicas, para obtener los mejores resultados posibles. La experiencia vivida con la difícil situación del acetábulo izquierdo nos deja claro esto. En nuestra experiencia, utilizar injertos óseos en bloque31,32 nos ha dado buenos resultados en defectos acetabulares.
La cadera izquierda de este caso no tiene una solución definitiva, ya que está expuesta a seguir perdiendo tejido óseo del hueso iliaco restante por el apoyo directo del implante metálico (silla de montar).22 Debido a esto, debe utilizar en forma permanente la asistencia de un bastón y, en ocasiones, de una muleta para esfuerzos mayores. No hay reportes en la literatura sobre el posible manejo de una prótesis en silla de montar que llegara a fallar. A diferencia de esto, la cadera derecha tiene ahora una recuperación plena de sustancia ósea, que permitiría revisiones futuras, si llegara a ser necesario.
La infección profunda en la cadera izquierda se resolvió en forma efectiva y rápida por la acción in situ de los antibióticos adecuados (por antibiograma del cultivo), liberados a partir del polimetilmetacrilato colocado en el iliaco13,14,33,34 después del retiro de todo el tejido contaminado e implantes.
Un caso no es suficiente para llegar a conclusiones definitivas sobre la mejor manera de resolver las complicaciones que pueden presentarse en cirugía con prótesis de la cadera. Aquí se presenta una combinación de múltiples complicaciones, resultando una importante aportación de cómo afrontar y resolver algunas de ellas. A nuestro entender, serían: un manejo adecuado por personal capacitado de las fracturas acetabulares por la complejidad que conllevan,1,2,35,36 correcta elección de los implantes en pacientes sometidos a cirugía previa, reducción abierta y fijación interna (RAFI) del acetábulo, pensando en sus posibles complicaciones y la manera de solucionarlas.36,37 Asimismo, en caso de otras complicaciones, hacer uso de guías o consensos actualizados para el mejor resultado posible;14 también, la existencia de implantes de salvamento como último recurso y la comunicación clara y honesta con los pacientes.











 nueva página del texto (beta)
nueva página del texto (beta)



