INTRODUCCIÓN
La electromiografía o electromiograma (EMG) ha sido usado hasta hace poco, únicamente con objetivos diagnósticos; sin embargo, con el avance de la tecnología, estos registros se han convertido en un importante recurso para lograr el control artificial del movimiento de miembros prostéticos [1]. El registro superficial es usado con mayor frecuencia en diversos estudios, debido a la practicidad de uso y colocación, además de que al utilizar este método no se interfiere con funciones naturales y el valor medio de la señal registrada varía casi linealmente con respecto a la fuerza generada [2].
La señal de EMG ha sido ampliamente utilizada para controlar prótesis electrónicas y dispositivos de rehabilitación. En particular, para prótesis de miembro superior, se utilizan principalmente dos tipos: las prótesis de funcionamiento corporal (mecánico) y las de funcionamiento eléctrico (electrónico). Las ventajas principales de una prótesis mecánica son su bajo peso, costo moderado y que ofrecen buena durabilidad a costa de la estética y óptima funcionalidad [3]. Por otra parte, las prótesis electrónicas utilizan motores usualmente colocados en el codo, muñeca y/o efector final. Estos motores son controlados con actividad eléctrica proveniente del miembro superior residual del sujeto. Si bien estas prótesis ofrecen un mejor control que las mecánicas, tienden a tener costos y pesos elevados [3].
En los últimos años se ha explorado e implementado la creación de dispositivos de asistencia mediante impresoras 3D debido a las facilidades que ofrecen los tipos de software de diseño asistido por computadora (CAD). Estos programas permiten diseñar, moldear e imprimir dichos dispositivos de una manera práctica y con muy bajo costo, a comparación de las prótesis comerciales ya existentes [4].
Durante el desarrollo de prótesis electrónicas, el análisis de la señal de EMG ha sido abordado en una gran cantidad de estudios con la finalidad de extraer características, modelar la señal y reconocer patrones para lograr diferenciar entre varios estados del músculo, así como la distinción entre varios tipos de movimiento. Sin embargo, la selección de características que representen adecuadamente el estado en el que se encuentra un músculo, es un tema que aún está en discusión y desarrollo, ya que existen diferentes formas de caracterizar la señal de EMG [5]. Dentro de este contexto, la selección adecuada de características y su correcta clasificación permiten una estimación precisa del estado del músculo, así como una adecuada utilización y control de la prótesis.
El conjunto ideal, utilizado para lograr una buena clasificación y estimación de los diferentes estados de la señal de EMG, debe tener una gran separabilidad en el espacio de características de esta señal. Se han realizado estudios en los que se utilizan, como discriminantes para la clasificación, índices clásicos del dominio temporal de la señal de EMG, tales como la integral del valor absoluto, la varianza y los cruces por cero. Estos índices han sido utilizados junto con modelos auto-regresivos para obtener una clasificación adecuada utilizando músculos diferentes como señales de entrada al sistema [6]. Otros índices utilizados para el análisis en el dominio del tiempo son la amplitud de Willison, el valor absoluto medio, la pendiente del valor absoluto medio, la longitud de onda, los cambios de signo en la pendiente y el valor cuadrático medio. Por otro lado, en el dominio de la frecuencia se ha utilizado la transformada wavelet y la función de densidad de potencia espectral, la cual indica cómo se distribuye la potencia total de la señal analizada sobre el espectro de frecuencia [7].
En cuanto a los métodos de clasificación de EMG, se han utilizado clasificadores Bayesianos, funciones discriminantes no-lineales, máquinas de soporte vectorial, lógica difusa y redes neuronales [7, 8]. El clasificador bayesiano tiene una variante conocida como Naive Bayes la cual provee un método sencillo y eficiente para los problemas de clasificación supervisada, teniendo como desventaja la incapacidad de generalización de resultados ante datos inesperados presentados [9]; mientras que las redes neuronales poseen la ventaja de tener una estructura distribuida en paralelo y la habilidad para aprender, es decir, son capaces de obtener salidas razonables para entradas que no fueron usadas durante su etapa de entrenamiento [10].
Recientemente, los avances en prótesis de miembro superior se han centrado en el desarrollo de falanges funcionales de los dedos controlados por medio de electromiografía. Los diseños de manos antropomórficas permiten distintos tipos de sujeción gracias a la cantidad de grados de libertad que poseen. Dentro de las problemáticas que presentan estos sistemas se encuentran el alto costo del dispositivo al requerir de alta tecnología y de software especializado, la falta de una interfaz intuitiva y confiable que mapee movimientos en actividad real de la prótesis, la necesidad de un entrenamiento extensivo requerido para manejar adecuadamente el sistema y la falta de retroalimentación de los sensores implementados [11].
En la actualidad, existe una amplia gama de este tipo de dispositivos prostéticos, que incluyen desde prótesis de alta tecnología, tales como las manos Be-Bionic y i-Limb, hasta aquellas con pocos grados de libertad [11]. Un aspecto importante en el desarrollo de dispositivos prostéticos es el método seleccionado para activar algún movimiento. Existen sistemas que incluyen arreglos preestablecidos de electrodos superficiales para la adquisición de EMG, permitiendo al dispositivo prostético realizar una amplia gama de movimientos al emplear un clasificador discriminante lineal (LDC, por sus siglas en inglés) [12]. Además, a pesar del alto costo computacional requerido, se ha optado en algunos casos por utilizar la transformada wavelet para controlar prótesis junto con un LDC debido a su eficiencia para lograr una discriminación adecuada de hasta veinte movimientos diferentes [13]. De igual forma, se han implementado sistemas que consideren la variación en la intensidad de las contracciones musculares en los registros de EMG, generando aumentos en la eficiencia de clasificación [14]. Algunos sistemas prostéticos utilizan la implantación de sensores mioeléctricos para controlar prótesis de miembro superior de hasta tres grados de libertad que permite un funcionamiento adecuado del dispositivo [15]. Sin embargo, se presenta la limitante de ser un método invasivo y de requerir un entrenamiento extenso por parte del sujeto, por lo que se ha propuesto utilizar registros superficiales de EMG de pares de músculos antagonistas, debido a la facilidad de activación independiente de éstos, para controlar prótesis de hasta tres grados de libertad [16].
Considerando las características de los dispositivos actuales, el proyecto presentado tiene como objetivo el desarrollo de una prótesis electrónica funcional de miembro superior utilizando una impresora 3D, con la finalidad de aprovechar el alto grado de control que este tipo de prótesis le otorga al usuario y la practicidad de utilizar un prototipado de impresión 3D. La motivación del mismo es el ofrecer una alternativa funcional y económica a comparación de los precios actuales en el mercado; esto es logrado debido al bajo costo de producción del prototipo propuesto.
En cuanto al control de la prótesis, se propone realizar la clasificación de la señal de EMG por medio de un clasificador bayesiano (CB) en una plataforma portátil y de una red neuronal artificial (RNA); utilizando un conjunto de características clásicas de la señal de EMG en el dominio del tiempo, con la adición de una medida no lineal, la entropía aproximada (ApEn), con el objetivo de diferenciar entre los movimientos de flexión, extensión y el estado de relajación.
METODOLOGÍA
En esta sección se describen los métodos utilizados para realizar la adquisición y caracterización de la señal de EMG; así como los clasificadores utilizados, el diseño de la prótesis y el funcionamiento de ésta utilizando cada uno de los clasificadores.
Adquisición de EMG
Durante este trabajo, se adquirió la señal de EMG utilizando el sistema Biopac MP36® y un circuito impreso diseñado para el control de la prótesis. En ambos casos, los electrodos fueron colocados en un arreglo bipolar en el músculo flexor radial del carpo (músculo flexor) y el músculo extensor de los dedos (músculo extensor), como se muestra en la Figura 1, mientras que ambos electrodos de referencia se colocaron en el codo. Estos métodos son explicados a continuación.
Biopac
La adquisición de la señal de EMG se realizó con el sistema Biopac MP36®, el cual fue configurado para utilizar una frecuencia de muestreo de 1 kHz. Las señales de EMG se obtuvieron de 30 sujetos sanos de ambos sexos, 14 hombres y 16 mujeres, con una edad media de 23.1±2.9 años.
Para la adquisición de los datos se realizó un protocolo que consistió en la realización de tres maniobras por parte de los sujetos. Durante la primera maniobra los sujetos realizaron contracciones máximas voluntarias (MVC, por sus siglas en inglés); en la segunda maniobra se realizaron contracciones con una amplitud aproximada al 50% de la MVC de cada sujeto; finalmente en la tercera maniobra los sujetos realizaron movimientos simples de flexión y extensión sin realizar fuerza activa. En todas las maniobras se realizaron 3 flexiones de muñeca seguidas de 3 extensiones de muñeca. Estas maniobras fueron utilizadas ya que se cubre un amplio rango de posibles movimientos realizados por los sujetos, incluyendo los movimientos cotidianos.
Cada contracción realizada en las maniobras tuvo una duración de 5 segundos con un periodo de relajación de 10 segundos existente entre cada contracción.
Sistema diseñado para la adquisición de EMG
Considerando las características del sistema Biopac®, su uso dentro de la implementación de la prótesis no es factible debido al alto costo y la nula portabilidad de este sistema. Por lo tanto, la obtención de la señal de EMG para generar el movimiento de la prótesis se realizó con un sistema implementado para las funciones de adquisición, filtrado y procesamiento. Las señales de entrada de este sistema se adquirieron de los músculos flexor y extensor antes mencionados.
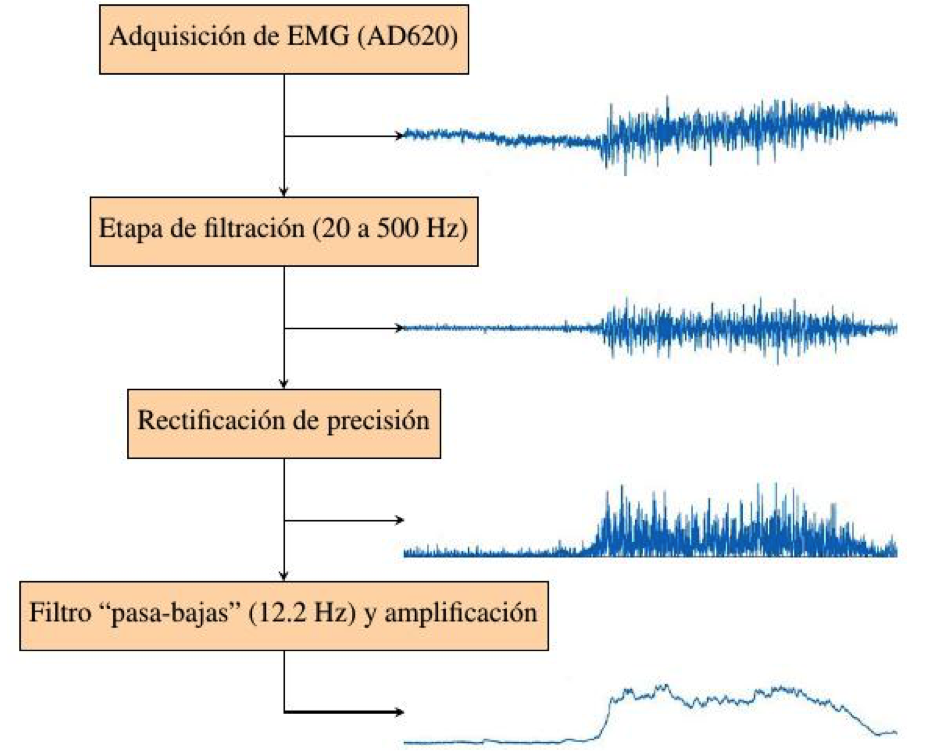
El sistema completo consta de cinco etapas. La primera etapa consiste en un amplificador de instrumentación AD620 con una ganancia de amplificación de 495. Durante la segunda etapa se aplican a la señal dos filtros con ganancia unitaria, el primero de tipo “pasa-bajas” con una frecuencia de corte de 500 Hz y el segundo de tipo “pasa-altas” con una frecuencia de corte de 20 Hz, de acuerdo al ancho de banda de la señal de EMG [1]. En la tercera etapa se realiza un proceso de rectificación de precisión y en la cuarta etapa se aplica un segundo filtro “pasa-bajas” con frecuencia de corte de 12.2 Hz para obtener un suavizado de la señal de EMG rectificada (envolvente). Durante la quinta etapa se realiza un proceso de amplificación de la señal con una ganancia de 5. Estas etapas se muestran en la Figura 2 como un diagrama de bloques, indicando la morfología de la señal de salida obtenida en cada etapa.
Posterior a este procesamiento analógico, se utilizó la plataforma Arduino MEGA 2560 para capturar las señales analógicas. Las salidas obtenidas después del proceso de rectificación del sistema implementado son introducidas al convertidor analógico-digital (ADC) del Arduino, el cual cuenta con 10 bits de resolución (aproximadamente 4.88 mV) [17]. Finalmente, esta señal digital es normalizada respecto al valor máximo registrado en la señal de EMG.
Caracterización de EMG
La caracterización de la señal normalizada de EMG se realizó utilizando los siguientes índices: Integral (ITG, por sus siglas en inglés), Integral Cuadrática Simple (SSI, por sus siglas en inglés) y Entropía Aproximada (ApEn, por sus siglas en inglés); descritos en la Tabla 1.
Los índices de ITG y SSI son dependientes de la amplitud de la señal de EMG, mientras que la ApEn es un índice no lineal que expresa la semejanza que existe entre dos segmentos, en este caso segmentos de contracción o relajación muscular, con base en dos parámetros: la longitud m que tendrá cada segmento y el umbral de similitud r, que determina si un segmento es similar a otro sólo si el umbral r no es superado por la resta del valor absoluto de los dos segmentos a comparar. Esto es útil para poder diferenciar si un segmento de la señal de EMG es parte de un evento de contracción muscular o de reposo. Para este trabajo se consideró una longitud fija m=2, mientras que el valor de r es de 0.1 veces la desviación estándar de una muestra de contracción muscular, ya sea flexión, extensión o relajación, dependiendo de la maniobra evaluada. Con estos parámetros establecidos, la señal de electromiografía x se divide en N segmentos, de manera que:
Posteriormente, se selecciona un segmento p para compararlo con cada uno de los segmentos n=1, ..., N restantes de x y así determinar la cantidad de segmentos n similares a p. Dos segmentos son similares cuando c<r, con:
donde abs( ) es la función de valor absoluto. El siguiente paso es calcular la media de la cantidad de patrones de longitud m que son similares a cada uno de los demás patrones dentro de la muestra; es decir,
donde nm es la cantidad de segmentos n similares al segmento p. Cm+1 se calcula de manera similar a Cm siendo la única diferencia la longitud de los segmentos, la cual será de m+1. De esta forma se puede establecer si los segmentos dentro de una muestra son similares o no [18]. En la Figura 3 se muestra el diagrama de flujo para el cálculo de este índice no lineal.
Clasificadores de EMG
En este trabajo se utilizaron dos clasificadores para evaluar la señal de EMG; estos son un CB y una RNA. Se eligió el CB debido a la practicidad de su utilización en plataformas portátiles como lo es Arduino y a la eficiencia que presenta este clasificador. La RNA fue implementada para obtener clasificaciones robustas al poder generalizar los datos de entrada, siendo esta una limitante importante del CB. Estos clasificadores son descritos en esta sección.
Clasificador Bayesiano
El CB seleccionado utiliza una variación del teorema de Bayes llamada Naive Bayes, el cual considera los atributos a evaluar como independientes entre sí, es decir, tienen independencia condicional. Para este clasificador se plantearon 3 clases: flexión, extensión y relajación.
Considerando el teorema de Bayes:
donde P(A|B) es la probabilidad condicional de A dado B, P(B|A) es la probabilidad condicional de B dado A, P(A) es la probabilidad de A y P(B) es la probabilidad de B [19]; y aplicando las definiciones de probabilidad condicional y de independencia condicional [20], la probabilidad de cada clase se calcula a partir de:
donde Ii representan los índices característicos de la señal de EMG, Z es una constante de normalización dependiente de estos índices y P(Ii|C) la probabilidad de que los índices pertenezcan a una de las clases.
Se asumió que los valores de cada clase se asignan según una distribución normal [21], por lo que la probabilidad de que los índices pertenezcan a alguna clase se calcula utilizando la Ecuación (6):
donde Ii es el índice a evaluar, y μc y σc son la media y la desviación estándar para cada índice de cada clase, respectivamente.
Los valores de la media y la desviación estándar utilizados en la Ecuación (6) fueron obtenidos de la segunda maniobra del protocolo establecido (MVC al 50%) adquirida con el sistema Biopac®. Aunque el sistema EMG diseñado será el implementado en la prótesis, se utilizó el sistema Biopac® para obtener los parámetros del clasificador debido a cuestiones de logística. Una vez obtenidas las probabilidades de cada clase, se utilizó la estrategia de máxima verosimilitud, en la que el clasificador selecciona como resultado aquella que obtuvo la mayor probabilidad de las tres.
Red Neuronal Artificial
La RNA es un sistema inspirado en los modelos biológicos del sistema nervioso central de animales. Las RNAs son usadas para obtener un resultado específico y dependiente de las entradas recibidas, su objetivo principal es aprender parámetros no lineales al mismo tiempo que parámetros lineales; ésta es la razón por la que estos clasificadores aceptan algoritmos relativamente sencillos donde la no linealidad es aprendida de datos de entrenamiento y les otorga la capacidad de generalización [10]. El modelo utilizado por una RNA es compacto y, por lo tanto, proporciona una evaluación más rápida de los datos de entrada [22].
La RNA fue utilizada para clasificar entre movimientos de flexión, extensión y relajación, utilizando un vector de características que contiene los índices establecidos anteriormente. La arquitectura de la RNA se determinó de acuerdo a pruebas realizadas con diferentes configuraciones, seleccionando la red que obtuviera el menor error cuadrático medio (MSE) y el mejor desempeño. La RNA implementada, al igual que el CB, consideró 3 clases: flexión, extensión y relajación; y utilizó una función de transferencia tangencial sigmoidea.
El entrenamiento fue de tipo supervisado, el cual consiste en presentar un conjunto de entrenamiento a la RNA, encontrar la salida de la red y ajustar los pesos sinápticos para que la salida actual se aproxime a las etiquetas deseadas y definidas a priori. Los datos de entrenamiento utilizados fueron aquellos obtenidos durante las tres maniobras descritas anteriormente y, de igual manera que en el caso del CB, se utilizó el sistema Biopac® para obtener los datos de entrenamiento y no el sistema EMG diseñado debido a cuestiones de logística. Los vectores de entrenamiento se presentaron de forma aleatoria a la RNA para que tuviera un mejor desempeño y evitar una predisposición de los resultados obtenidos por la red [10]. La asignación de etiquetas a los vectores de características consistió en definir cada ventana temporal como etapa de flexión, extensión o relajación.
La RNA fue entrenada en MATLAB® a través del algoritmo de aprendizaje de retropropagación, los valores de los pesos y el sesgo se actualizaron de acuerdo a la optimización de Levenberg-Marquardt y se utilizó una función de aprendizaje de gradiente descendente con momento [23]. El entrenamiento se llevó a cabo durante aproximadamente 40 épocas y el desempeño de la red fue evaluado con el MSE alcanzado, con base en la curva de aprendizaje. Para la asignación de valores de salida de la red a las clases, se considera un umbral, así que valores fuera de éste son descartados y no se asignan a ninguna clase.
Para detener el entrenamiento y el ajuste de los pesos sinápticos de la RNA, los datos disponibles se dividieron de forma aleatoria en tres subconjuntos: entrenamiento (80% de los datos), validación (10%) y prueba (10%), para brindar una mejor generalización [10]. Los datos de entrada para las etapas de entrenamiento, prueba y validación de la red consisten en una matriz de seis renglones donde cada columna pertenece únicamente a una clase, ya sea flexión, extensión o relajación. En los primeros 3 renglones se encuentran los 3 índices adquiridos pertenecientes al músculo flexor y en los últimos 3 están los índices obtenidos del músculo extensor con el siguiente orden: ITG, SSI y ApEn. El tamaño total de la matriz de vectores de características para la RNA fue de 6x4860, de la cual se reservó una matriz de 6x3888 para el subconjunto de entrenamiento y matrices de 6x486 tanto para el subconjunto de validación como para el de prueba. La RNA fue entrenada para obtener a la salida (1,0,0) como flexión, (0,1,0) como relajación y (0,0,1) para extensión, dichos valores establecidos como el caso ideal. Para esta red se consideró un umbral de 0.2.
Durante la etapa de entrenamiento, también se utilizó el subconjunto de validación para estimar el error de generalización. Típicamente, el error obtenido con el subconjunto de validación disminuye conforme avanza el entrenamiento de la red, pero éste puede aumentar, lo cual es una indicación que el clasificador está sobre-ajustando los datos del subconjunto de entrenamiento. El entrenamiento y ajuste de parámetros se detiene cuando el error de validación empieza a aumentar [10].
Evaluación de desempeño de los clasificadores de EMG
Para evaluar el desempeño del CB y de la RNA se utilizaron dos indicadores, la curva ROC (Receiver Operating Characteristic) y la matriz de confusión. Para cada clase, la curva ROC aplica umbrales dentro del intervalo de 0 a 1 a las salidas. Para cada umbral se calculan dos valores, los cuales son la proporción de positivos verdaderos y la de falsos positivos. Mientras la curva obtenida de cada una de las clases tenga una proporción mayor de valores verdaderos positivos se considera que la clasificación obtuvo resultados favorables [24]. La matriz de confusión es apropiada para métodos de clasificación en los cuales valores específicos pueden ser asignados a una sola clase y en los que las medidas de precisión están basadas en la proporción de datos correctamente clasificados, ya que muestra la cantidad de ventanas temporales clasificadas de manera correcta e incorrecta [25].
Diseño de la prótesis
La prótesis se diseñó de tal forma que permitiera la rotación de muñeca (pronación/supinación) y el movimiento de pinza para sujetar objetos (flexión/extensión). Para producir estos movimientos se emplearon dos servomotores modelo Dynamixel XL-320 [26], los cuales fueron controlados por comunicación serial utilizando la plataforma Arduino. Las piezas de la prótesis fueron diseñadas mediante el software SolidWorks® utilizando dimensiones que consideraran tanto el tamaño de los servomotores como el tamaño proyectado de una mano promedio [27].
Funcionamiento de la prótesis
Como se mencionó anteriormente, una vez obtenidas y procesadas las señales de EMG de los músculos flexor y extensor utilizando el sistema diseñado, se utilizó la plataforma Arduino MEGA 2560 para capturar las señales analógicas. Estas ventanas adquiridas de datos no traslapados tienen una duración de 0.12 y 3 segundos aproximadamente para el CB y la RNA, respectivamente. Estas señales digitales normalizadas son utilizadas por los clasificadores para tomar una decisión y así generar movimiento en los servomotores de la prótesis.
El movimiento del servomotor del dedo está restringido a un máximo de 60° (los servomotores Dynamixel XL-320 poseen una libertad de giro de 300° [26]) para evitar que durante el movimiento de extensión, éste se golpee contra la palma de la prótesis. Al recibir una respuesta generada por una clase de extensión, el Arduino activará el servomotor para “abrir” la mano 20°. De manera similar, cuando el Arduino reciba una respuesta generada por una clase de flexión, el servomotor se activará para “cerrar” la mano 20°. Cuando se haya obtenido una clase de relajación el servomotor no se moverá.
El movimiento de rotación de muñeca se genera cuando la señal obtenida después de la quinta etapa de procesamiento del músculo flexor supera un umbral significativo en relación a la fuerza máxima del sujeto, la cual es determinada por un proceso de normalización de la señal de EMG. Cuando el umbral ya no sea superado, el servomotor no se moverá. El servomotor continuará moviéndose en la misma dirección cada vez que se supere el umbral hasta que llegue a su límite de movimiento de 300° y, una vez alcanzado este límite, el movimiento tendrá una dirección opuesta hasta llegar a su límite de 0° y nuevamente se cambie la dirección del movimiento. Se seleccionó este tipo de activación debido a que la clasificación no es afectada por la fuerza ejercida por el sujeto, por lo que contracciones del músculo flexor de menor intensidad al umbral serán usadas para realizar el movimiento del dedo.
Funcionamiento con el CB
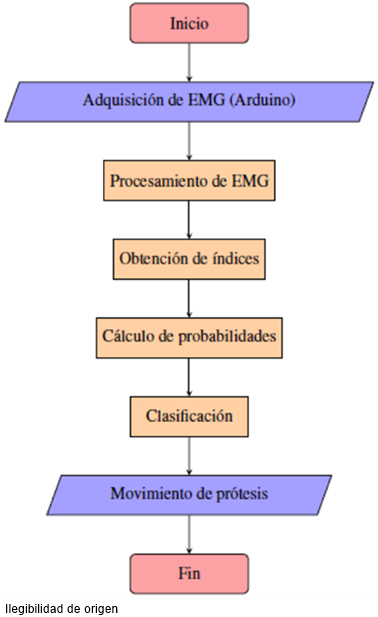
El CB fue implementado directamente en la plataforma Arduino y obtiene los índices utilizados en la clasificación a partir de ventanas de 290 elementos adquiridas mediante el sistema EMG diseñado. La cantidad de elementos en las ventanas fue menor, en comparación a la utilizada en la RNA, debido a las limitaciones de memoria en la tarjeta Arduino. Una vez obtenidos los índices, se realiza el cálculo de probabilidades de cada clase y se genera una respuesta para activar los servomotores por comunicación serial. En la Figura 4 se muestra un diagrama de flujo del funcionamiento de la prótesis al utilizar el CB como clasificador.
Funcionamiento con la RNA
La RNA fue implementada en una computadora personal utilizando MATLAB® y recibe por comunicación serial ventanas de 500 elementos, provenientes de la plataforma Arduino a una frecuencia de muestreo aproximada de 160 Hz, con las que se realiza el cálculo de los índices descritos anteriormente. El tamaño de las ventanas fue seleccionado de tal manera que se realizara una clasificación exitosa a una velocidad adecuada. Enseguida, los índices obtenidos son utilizados por la RNA para realizar la clasificación de estas ventanas y una vez que se obtiene un resultado de la clasificación, se envía una respuesta desde MATLAB® hacia la tarjeta Arduino para que, dependiendo de la clasificación, se transmita la acción a los servomotores por comunicación serial. En la Figura 5 se muestra un diagrama de flujo del funcionamiento de la prótesis al utilizar la RNA como clasificador.
RESULTADOS Y DISCUSIÓN
Adquisición y procesamiento de EMG
En la Figura 6 se muestra la señal de EMG adquirida con el dispositivo diseñado, correspondiente a un sujeto masculino durante una flexión máxima, haciendo evidente la salida de cada etapa de procesamiento analógico. En estas gráficas se observa que la señal de EMG adquirida tiene un acondicionamiento adecuado para realizar la caracterización de la señal.
Caracterización de EMG
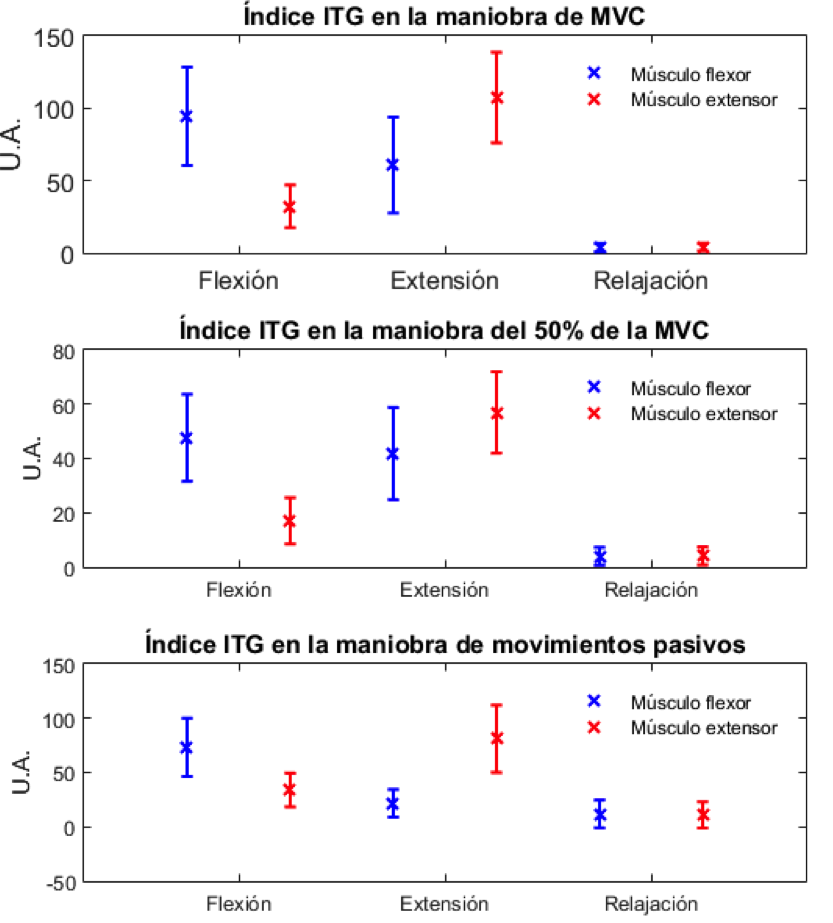
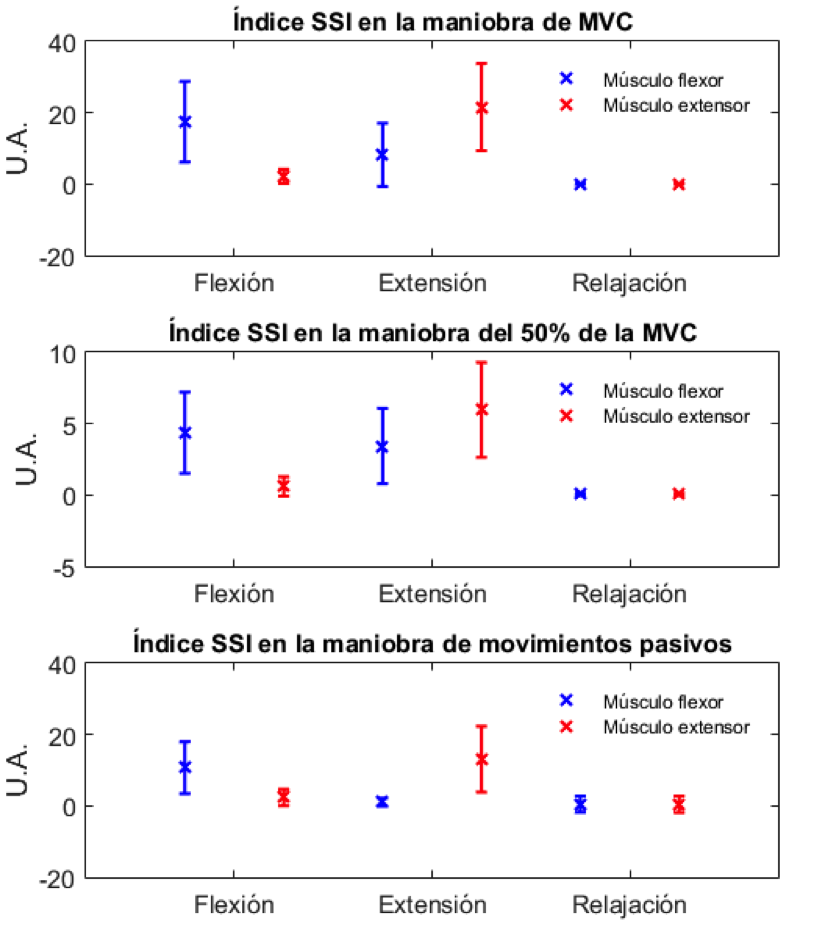
Una vez obtenidas las señales de las 3 maniobras propuestas, se extrajeron los índices característicos de la señal de EMG previamente establecidos; los índices obtenidos fueron graficados de acuerdo a la maniobra realizada. El índice ITG se muestra en la Figura 7; el índice SSI se observa en la Figura 8; y finalmente, el índice ApEn se presenta en la Figura 9.
Las Figuras 7, 8 y 9 muestran que los índices ITG y SSI permitieron distinguir adecuadamente entre los músculos flexor y extensor; y, aunque en el índice no lineal, ApEn, no se observaron diferencias considerables entre estos músculos, se obtuvo una diferencia evidente entre contracción, esto es flexión o extensión, y etapas de relajación.
Implementación del CB
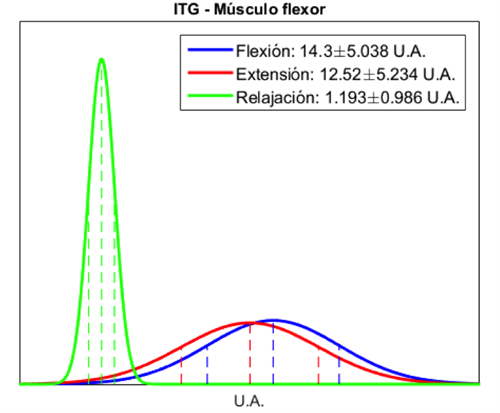
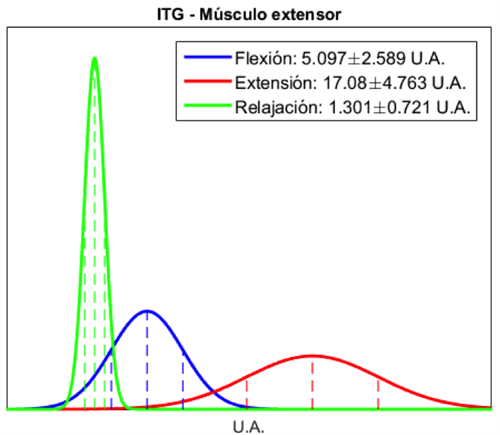
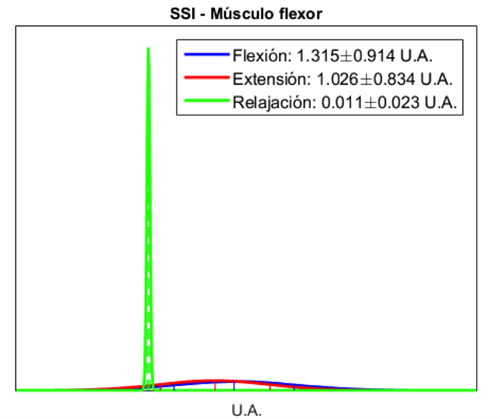
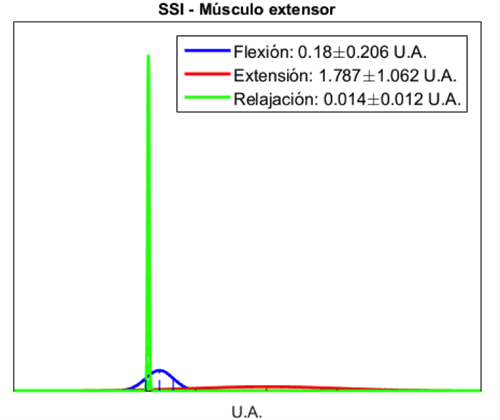
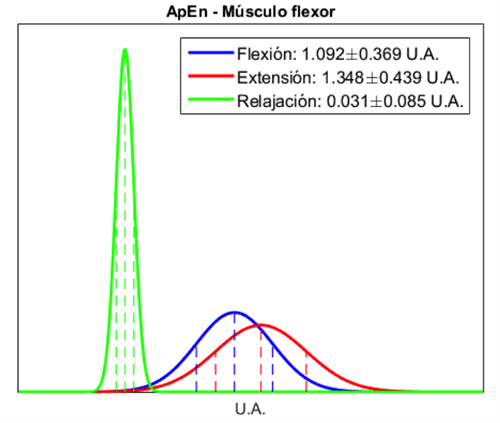
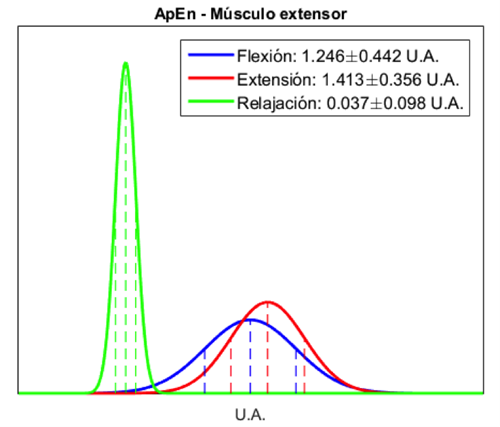
Las distribuciones de probabilidad normal de los índices extraídos, utilizadas para el funcionamiento del CB, se muestran en las Figuras 10, 11, 12, 13, 14 y 15. En estas curvas se muestran las medias y desviaciones estándar obtenidas durante la segunda maniobra del protocolo establecido (MVC al 50%). En las gráficas se observa la diferencia que existe entre cada una de las clases obtenidas de cada músculo. El CB utilizó esta separabilidad para poder determinar, dependiendo de los índices extraídos y la probabilidad calculada con el teorema de Bayes, el tipo de movimiento que se esté realizando. Los índices de ITG y SSI mostraron en el músculo extensor una mayor separabilidad entre cada una de las tres clases, mientras que en el músculo flexor, si bien se observó una menor diferencia entre las clases de flexión y extensión, se mantuvo la separabilidad entre estas dos clases y la clase de relajación. La distribución de probabilidad normal del índice ApEn de ambos músculos mostró una mejor separabilidad entre la clase de relajación y las clases de flexión y extensión, en comparación con los índices ITG y SSI, lo que facilita la diferenciación entre contracciones musculares y etapas de relajación.
La combinación de los 3 índices permitió una adecuada caracterización de los movimientos de flexión y extensión y de la etapa de relajación. Los índices ITG y SSI permitieron diferenciar adecuadamente entre flexión y extensión, como se observa en los valores medios obtenidos de la población estudiada (Figura 7 y Figura 8) y en las distribuciones de probabilidad normal (Figura 10, Figura 11, Figura 12 y Figura 13), debido a que son índices basados en la amplitud de la señal de EMG reflejando la activación de los músculos agonistas y antagonistas; mientras que la ApEn, al ser una medida de la regularidad de la señal, permitió separar claramente las etapas de contracción y relajación, debido al cambio evidente en la morfología de la señal causado por la activación de las fibras musculares involucradas al realizar una contracción, lo cual aumenta la complejidad de la señal.
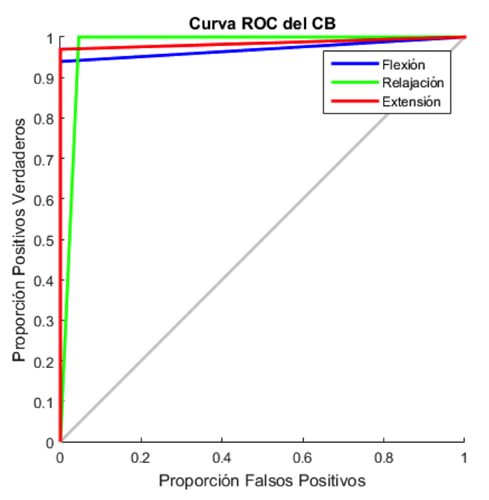
Para la evaluación del CB, se consideraron 5 sujetos sanos donde cada uno realizó una serie de 20 movimientos conformados por etapas de flexión, extensión y relajación. Las clases resultantes fueron comparadas con los movimientos realizados para evaluar la eficiencia del clasificador. La curva ROC de esta prueba se muestra en la Figura 16, donde se puede observar que las curvas correspondientes a cada clase tienen una mayor cantidad de positivos verdaderos que de falsos positivos, por lo que el clasificador tiene una buena eficiencia.
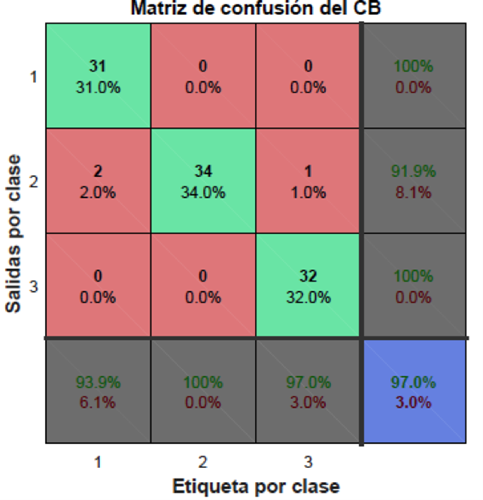
La tasa de error obtenida fue de 6.1%, 0% y 3% en las clases de flexión, relajación y extensión, respectivamente. La matriz de confusión muestra una eficiencia de clasificación del 97% durante la prueba; esta gráfica se muestra en la Figura 17.
El modelo probabilístico del CB permitió una correcta clasificación de movimientos musculares debido a la diferenciación obtenida por los índices característicos y a las probabilidades calculadas durante estos movimientos.
Implementación de la RNA
Al construir la RNA se evaluaron distintas estructuras, cada una generando un MSE durante la etapa de entrenamiento y un porcentaje de eficiencia durante la etapa de prueba obtenido mediante la matriz de confusión; ambos resultados de cada RNA son mostrados en la Tabla 2.
Las redes neuronales de 6, 7 y 8 neuronas en la capa oculta mostraron un desempeño adecuado durante su entrenamiento y etapa de prueba y, tras pruebas de clasificación en tiempo real, la arquitectura seleccionada para la implementación en el control de la prótesis fue aquella con 6 neuronas en la capa de entrada, 8 neuronas en la capa oculta y 3 neuronas en la capa de salida; esta estructura se muestra en la Figura 18. Esta red fue elegida debido al bajo MSE obtenido, al desempeño que mostró en la etapa de prueba y a la eficiencia obtenida durante las pruebas de clasificación en tiempo real; además, se consideró que esta estructura es la más grande que se podría programar en la plataforma de Arduino.
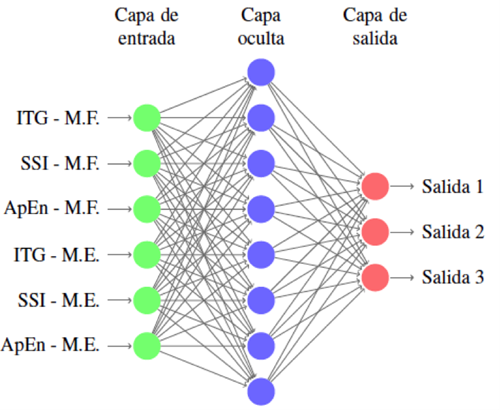
FIGURA 18 Estructura seleccionada para la RNA, donde M.F. es músculo flexor y M.E. es músculo extensor.
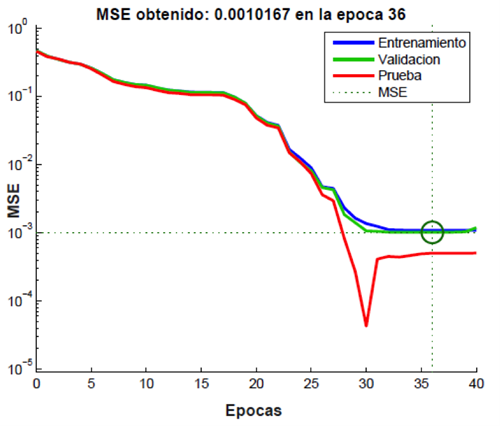
La Figura 19 muestra la curva de aprendizaje durante el entrenamiento de la RNA seleccionada. Se presenta el MSE alcanzado, además del comportamiento de los conjuntos de validación y prueba. El entrenamiento se llevó a cabo hasta la época 36 alcanzando el MSE anteriormente mencionado de 0.001067, lo cual muestra que el entrenamiento fue apropiado para, en consecuencia, generar clasificaciones adecuadas.
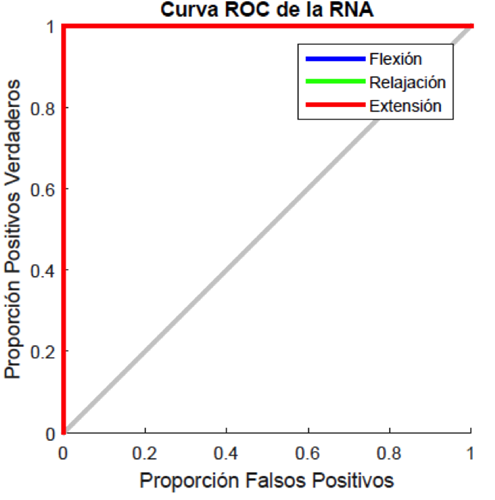
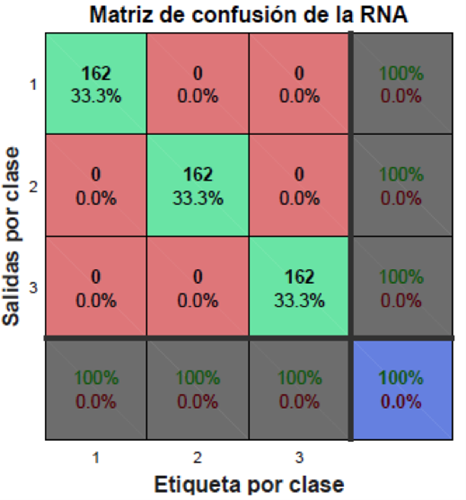
La curva ROC de la etapa de prueba de la RNA se muestra en la Figura 20, donde se puede observar que las curvas correspondientes a cada clase tienen únicamente valores positivos verdaderos, por lo que la red tiene una excelente eficiencia. La tasa de error obtenida fue de 0% en las clases de flexión, relajación y extensión. La matriz de confusión, mostrada en la Figura 21, muestra al igual que la curva ROC, una eficiencia de clasificación del 100% durante la etapa de prueba.
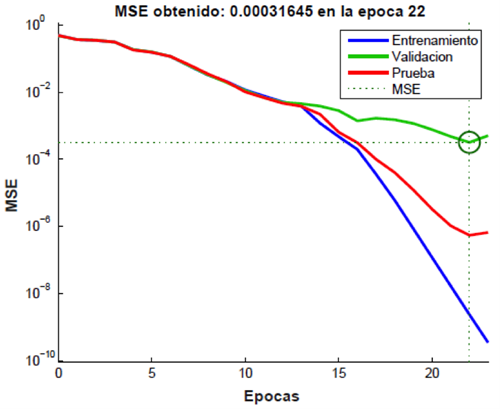
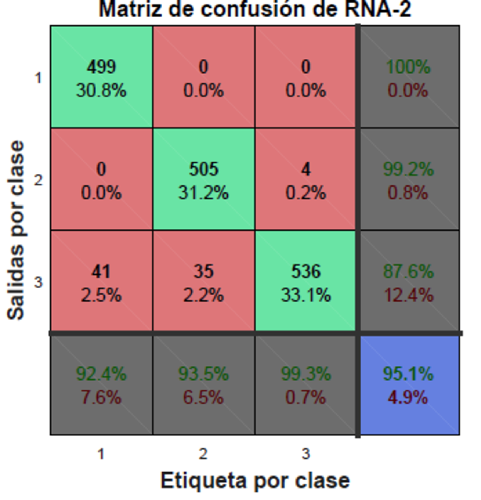
Para probar la eficiencia de la RNA propuesta con movimientos no presentados durante el entrenamiento, se realizó una prueba adicional; ésta consistió en evaluar el desempeño de una segunda red neuronal (RNA-2) con las mismas clases y arquitectura que la RNA seleccionada, con la diferencia de haber recibido un entrenamiento distinto. El objetivo de esta prueba es el evaluar la RNA-2 con movimientos totalmente ajenos a su entrenamiento. Se seleccionaron las maniobras de MVC y del 50% de la MVC para el entrenamiento de esta segunda red y fue probada con los datos de la maniobra de movimientos simples. Esta red obtuvo un MSE en el entrenamiento de aproximadamente 0.0003, lo que significa que la RNA-2 tuvo un entrenamiento apropiado. El resultado de la etapa de entrenamiento se muestra en la Figura 22.
En los resultados obtenidos de la etapa de prueba por medio de la curva ROC, presentados en la Figura 23, y por la matriz de confusión de la RNA-2, mostrados en la Figura 24, se observa una cantidad mucho mayor de valores positivos verdaderos en las tres clases y una eficiencia del 95.1%.
El excelente desempeño de la RNA-2 al lograr una eficiencia del 95.1% con movimientos no presentados durante el entrenamiento sugiere que la RNA, al recibir un entrenamiento con maniobras que cubren un amplio rango de movimientos, será capaz de clasificar correctamente movimientos cotidianos, ya que estos se encuentran dentro del rango del entrenamiento recibido.
Fabricación de la prótesis
Para el diseño de la prótesis, se desarrollaron cinco piezas: las dos primeras sirven para contener el primer servomotor (servomotor 1) utilizado para generar el movimiento de rotación de la muñeca; éstas conforman la base de la prótesis y las dimensiones de cada una son de 7.6 cm de ancho, 4.8 cm de profundidad y 1.3 cm de altura. La tercera pieza simula la palma de la mano y en ésta se colocó el segundo servomotor (servomotor 2) encargado de la función de extender y flexionar el dedo; esta pieza tiene 3.5 cm de altura y 6 cm de diámetro. La cuarta pieza es un dedo que se fija a la pieza anterior y sirve de punto de apoyo para el agarre que ejercerá la quinta pieza, un dedo móvil que va unido al servomotor 2. Ambos dedos poseen un ancho de 2.4 cm y una altura de 8.3 cm. En la Figura 25 se observan estas 5 piezas.
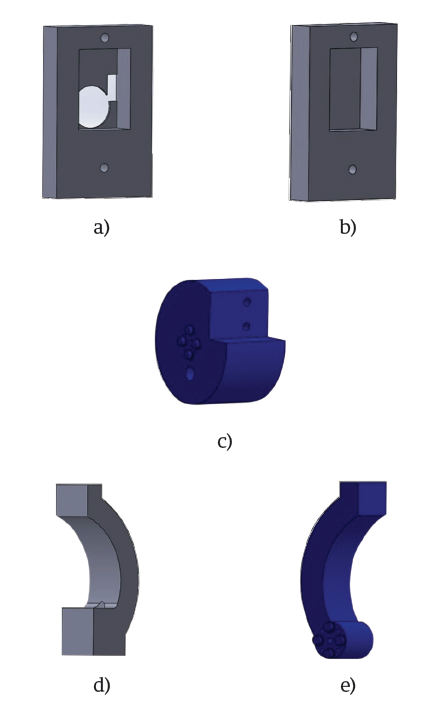
FIGURA 25 Piezas diseñadas en SolidWorks: (a) carcasa superior de la base de la prótesis, (b) carcasa inferior de la base de la prótesis, (c) palma de la mano, (d) dedo fijo, (e) dedo móvil.
Una vez que se diseñaron las piezas, éstas fueron construidas utilizando la impresora 3D CubePro® con material ABS. El peso total de la prótesis, incluyendo los servomotores, es de aproximadamente 171 g. Considerando la estructura diseñada, los servomotores del dedo y de la muñeca son capaces de mover una carga máxima de 1.24 kg y 7.94 kg, respectivamente. En la Figura 26 se muestra la prótesis completa.
El costo de producción de la prótesis que incluye: el sistema de EMG diseñado, la tarjeta arduino, los servomotores y la impresión 3D de las piezas, fue de alrededor de 125 dólares. Considerando que el rango aproximado del precio de prótesis mioeléctricas similares oscila entre 270 y 1000 dólares [28], la prótesis implementada ofrece una alternativa funcional y una mejor accesibilidad económica a las presentes en el mercado.
Movimiento de la prótesis
Cada clasificador fue evaluado durante pruebas en vivo junto con el dispositivo EMG diseñado. Los resultados obtenidos correspondientes a la eficiencia de clasificación y a los movimientos generados en la prótesis se muestran en esta sección.
Clasificación y desempeño de la prótesis utilizando el CB
En la Figura 27 se observan los resultados obtenidos durante las pruebas en vivo del CB. Estas pruebas consistieron en realizar 11 movimientos conformados por etapas de flexión, extensión y relajación. En esta gráfica se muestran los efectos producidos en cada servomotor a causa de la clasificación conseguida con los movimientos realizados. La eficiencia de clasificación lograda durante esta etapa fue del 100%.

FIGURA 27 Prueba de movimiento del servomotor de la muñeca (azul) y del servomotor del dedo (rojo) utilizando el CB como clasificador. Las líneas punteadas representan la realización de cada uno de los movimientos de la prueba.
Durante esta prueba, el CB logró una clasificación adecuada con cada uno de los movimientos realizados. El proceso completo, es decir, desde la etapa de adquisición de EMG hasta el movimiento de los servomotores tiene una duración aproximada de 2.34 segundos.
Al realizar contracciones musculares cercanas a los valores de MVC, el CB mostró la característica de obtener esporádicamente errores de clasificación debido a que estos valores salían del rango en el que se encontraban las medias y desviaciones estándar del modelo probabilístico.
Clasificación y desempeño de la prótesis utilizando la RNA
Al evaluar la RNA en pruebas en vivo se obtuvieron los resultados mostrados en la Figura 28. Similar a la prueba del CB, se realizaron 11 movimientos conformados por etapas de flexión, extensión y relajación. En esta gráfica se muestran los grados de movimiento de cada servomotor producidos por la clasificación conseguida con los movimientos realizados y, al igual que en la etapa de prueba de la RNA, se obtuvo una eficiencia de clasificación del 100%.
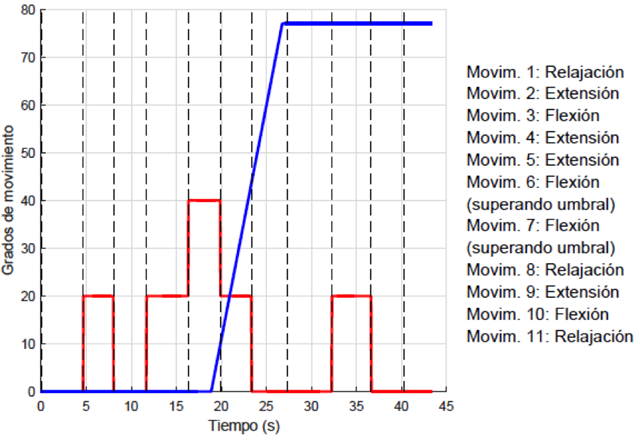
FIGURA 28 Prueba de movimiento del servomotor de la muñeca (azul) y del servomotor del dedo (rojo) utilizando la RNA como clasificador. Las líneas punteadas representan la realización de cada uno de los movimientos de la prueba.
Este resultado muestra un buen desempeño por parte de la red neuronal al clasificar diferentes tipos de ventanas temporales además de hacerlo con diferentes tipos de movimientos realizados. Este proceso tiene una duración aproximada de 3.94 segundos desde la adquisición de EMG hasta el movimiento de los servomotores.
A diferencia del CB, la RNA no presentó problemas de clasificación con contracciones musculares cercanas a los valores de MVC debido a que el entrenamiento que recibió cubre un amplio rango de movimientos. Sin embargo, en la implementación de la RNA existió un retraso de tiempo mayor en comparación al CB debido al proceso de transmisión y recepción de datos entre la plataforma de Arduino y MATLAB® por comunicación serial, mientras que al utilizar el CB, tanto la adquisición de los índices característicos como la clasificación se realizó en la plataforma Arduino.
CONCLUSIONES
La adquisición y procesamiento de la señal de EMG extraída de los músculos flexor y extensor fue la adecuada para la obtención de los índices característicos de esta señal. De igual manera, la combinación de índices lineales y no lineales para caracterizar la señal de EMG provenientes de dos músculos resultó ser apta para lograr diferenciar entre flexión, extensión y relajación a través de los clasificadores propuestos, los cuales lograron eficiencias altas durante las etapas de prueba. Al realizar la implementación de los clasificadores en conjunto con la prótesis se observó que ambos tuvieron un buen desempeño durante la clasificación y el movimiento de los servomotores. Este resultado permitió un control apropiado de la prótesis que, junto con las ventajas de la impresión 3D, cumple el objetivo de ofrecer una alternativa funcional y económica a las ofrecidas en el mercado actual de prótesis de miembro superior.
Si bien la RNA permite un control eficiente de la prótesis, la utilización de este clasificador requirió de una mayor cantidad de tiempo para el funcionamiento del dispositivo a comparación del CB, por lo que como perspectiva del trabajo se encuentra la implementación de la RNA en la plataforma Arduino con la finalidad de incrementar la autonomía del dispositivo prostético y la velocidad de procesamiento para así lograr un funcionamiento en tiempo real de la prótesis. De igual forma, como trabajo a futuro, se plantea el incorporar un mayor número de músculos que generen una gama más amplia de movimientos, con la finalidad de caracterizarlos de forma que el control de la prótesis sea más fino, además de evaluar el desempeño de los clasificadores con el método de validación cruzada y realizar la comparación con otros clasificadores como máquinas de soporte vectorial y redes neuronales con entrenamiento no supervisado.











 nueva página del texto (beta)
nueva página del texto (beta)