Introducción
El cáncer de seno es una enfermedad que afecta de modo inquietante a la mujer a nivel mundial y es considerada la neoplasia maligna femenina más frecuente en países desarrollados y en vías de desarrollo, impactando en 2012 al 25.2 % de la población total que pertenece a este género [1]. En 2013, a nivel nacional provocó casi el 15 % de fallecimientos por tumores malignos en mujeres mexicanas de 20 años y más [2]. Aunado a ello, la demora en la detección y diagnóstico, provocada en gran parte por la falta de infraestructura suficiente, genera altos costos en el control del cáncer, pues en estadios más avanzados la atención médica requerida aumenta su complejidad [3]. En torno a ello, pese a que la probabilidad de sobrevida a cinco años es mucho mayor si la paciente diagnosticada recibe el tratamiento médico en estadios I y II de la enfermedad, solo del 5 al 10 % de los casos detectados se encuentra en estas dos primeras etapas [4].
Tan solo el costo promedio del proceso diagnóstico de cáncer de seno, en mujeres a partir de los 40 años, reportado para las Unidades de Medicina Familiar del Instituto Mexicano del Seguro Social (UMF del IMSS) se aproxima a los $900 MXN, donde, al analizar los diferentes escenarios durante todo el procedimiento se aprecian variaciones que van desde $599 MXN a $5160 MXN, porte calculado en 2012 [5].
En adición a esto, las técnicas utilizadas por excelencia en el Sector Salud presentan limitantes en cuanto a la movilidad de los instrumentos de detección, su exactitud y competencia. Así pues, la mastografía depende de la diferencia de densidad de los tejidos involucrados, siendo las mamas jóvenes difíciles de examinar dada su alta densidad [6]; además de la radiación y la compresión de los senos recibidas durante dicho procedimiento, lo cual impide que mujeres con padecimientos de tiroides, con marcapasos, embarazadas o con implantes mamarios se realicen esta prueba.
Adicionalmente, durante un ultrasonido (US) mamario es necesario poner en contacto con la piel del seno un gel conductor y el transductor, provocando molestias y, en ocasiones dolores, para algunas pacientes. Con dicha prueba la determinación de microcalcificaciones y la examinación en senos lipoideos (de gran volumen) se complica debido a la naturaleza mecánica de la técnica, incluso su uso se considera totalmente complementario para casos en los que la mastografía no es capaz de detectar anomalías mamarias o cuando está contraindicada [7].
En ambos casos existen unidades móviles a nivel nacional, sin embargo, su alcance hacia las localidades de difícil acceso aún no es suficiente [8]. Por otro lado, debido a la estrecha relación endocrina que manifiesta esta enfermedad, los factores que modifican el riesgo de padecerla se ven afectados por la edad en que ocurre cada evento hormonal y su duración (ya sea endógeno1 o exógeno2) [9]. También influyen los factores ambientales tales como la exposición a la radiación, la contaminación y la presencia o ausencia de hábitos saludables, mismos que intervienen indirectamente en las rutas metabólicas [10].
Entonces, como resultado de la necesidad de métodos integrales para la detección temprana que impliquen bajos costos, sean seguros y cómodos para los operadores y pacientes, i.e., no sufrir radiaciones ni contacto físico doloroso durante un proceso de tamizaje; y que además sean fáciles de utilizar y transportar para lograr su alcance a una comunidad mayor, en los últimos años se han implementado y mejorado distintas técnicas para complementar la detección temprana y acercar a la población más vulnerable hacia estas nuevas tecnologías. Específicamente, el Centro de Física Aplicada y Tecnología Avanzada (CFATA) del Campus Juriquilla, Querétaro, de la Universidad Nacional Autónoma de México (UNAM) ha llevado a cabo un proyecto de investigación donde se han realizado exámenes termográficos a más de 10 000 voluntarias en el transcurso de los últimos 4 años. Durante la ejecución de las evaluaciones térmicas se captura información respecto de las características físicas (edad, tipo somático, tamaño del seno, etc.), hormonales (etapa del ciclo menstrual, terapia hormonal presente) y clínicas (enfermedades que afecten a la temperatura superficial, así como patologías benignas previas en el seno, antecedentes de cáncer en familiares de línea materna, consumo de medicamentos, tabaco y otros, actividad física semanal, etc.). Además, se analizan los patrones térmicos presentes en los termogramas, buscando las características más importantes para la detección mediante infrarrojo.
Las imágenes termográficas entregan información sobre la temperatura superficial, sin embrago, es necesario crear un sistema de apoyo a la toma de decisiones que realice una clasificación termográfica para auxiliar en el diagnóstico médico bajo el criterio termográfico y proporcionar mayor información acerca de cada paciente relativa a sus signos y síntomas, no solo desde el punto de vista radiológico (proporcionado por la mastografía), sino desde una visión integral y fisicoquímica, con perspectiva hacia la evolución fisiológica de cada persona y de su padecimiento, en caso de tener alguno. Asimismo, con los resultados que arroja el sistema se busca lograr un seguimiento adecuado al grado de pertinencia que requiere cada circunstancia en particular.
Fundamentos
Termografía
La termografía genera mapas térmicos (termogramas) al utilizar una cámara que contiene un sensor de infrarrojo. Dicho medidor detecta cambios localizados de la distribución térmica superficial de la piel, la cual se asocia a la temperatura de órganos y tejidos sanos o con alguna patología. Se piensa que dichos cambios resultan del incremento de la vascularización, la vasodilatación y la perfusión regional, así como de la generación de un hipermetabolismo y la congregación de células inflamatorias asociadas a la zona del crecimiento tumoral [11]. La anatomía del seno facilita la observación térmica, con lo que la detección temprana de anomalías en él mediante dicha tecnología es plausible. Por lo tanto, desde 1956 se presentó la primera termografía de glándulas mamarias para la detección de carcinoma en seno [12]. Las mencionadas alteraciones fisiológicas normalmente no son detectadas por los métodos de imagenología médica más comunes, pues proporcionan información acerca de la morfología y estructura anatómica, donde a veces es difícil determinar si en la zona se encuentra una masa tumoral, ya que un tumor agresivo puede albergar casi 500 000 células contenidas en tan solo 2 mm de diámetro [13]. En cambio, la termografía es funcional [14], i.e., dependiendo de las características metabólicas de la paciente se apreciarán diferentes patrones de temperatura, para los cuales se requiere utilizar una gran cantidad de criterios térmicos y hormonales con el fin de analizar correctamente los resultados termográficos.
Particularmente, en el análisis de termogramas hay una pequeña proporción de especialistas, con lo que se requiere el auxilio de otros métodos para divisar un diagnóstico térmico correcto. La termografía para uso clínico aún no ha sido totalmente aceptada a pesar de su carácter inocuo, entre otras razones, debido a la falta de modelos de referencia y a la ambigüedad en la interpretación de los resultados al ser analizados de forma aislada, i.e., la determinación de supuestas patologías depende de los factores físicos, ambientales, genéticos, hormonales y del estado de salud previo y actual de la persona en cuestión, en conjunción con la información extraída del termograma.
Sistemas expertos
Diferentes definiciones de los sistemas expertos (SE), también conocidos como sistemas basados en el conocimiento, han sido propuestas hasta la fecha en la literatura de la Inteligencia Artificial, sin embargo, a pesar de los diferentes enfoques y caracterizaciones utilizados, una base o fundamento común puede ser extraído de todas ellas: un sistema experto es un sistema con pericia en la solución de problemas. Esto es, que posee conocimientos acerca de un dominio particular, comprensión de problemas del dominio y métodos de inferencia o razonamiento para manipular este conocimiento y resolver los problemas en la misma forma en que lo haría un experto humano.
Puede apreciarse a un SE como un sistema de procesamiento de datos el cual hace uso de elementos computacionales, conocimientos, reglas y hechos disponibles para resolver algún problema no formal3. Asimismo, contiene las integrantes que se requieren para la representación del saber y la adquisición de nueva información, la manifestación de los resultados y el análisis de los mismos. Con ello, un SE es capaz de imitar el proceso de razonamiento de un humano con experiencia en cierto tema, con lo que proporciona un apoyo para la toma de decisión en un dominio específico y justifica su resolución tanto en problemas triviales como en multiparamétricos [16], siendo así considerados como sistemas inteligentes que toman decisiones de forma automática. Además, en un sistema experto puede incluirse representación simbólica y búsqueda heurística para lograr la solución, lo cual implica una aproximación mayor a la que puede lograrse con los programas de procesamiento de datos comunes. Estos últimos se encuentran constituidos por lenguajes de programación algorítmicos destinados a la solución de una cuestión en particular, propiedades o parámetros concretos. En contraste, los sistemas expertos, prioritariamente, utilizan lenguajes de programación declarativa, donde los mecanismos lógicos poseen carácter general y pueden ser aplicados a cualquier propiedad, parámetro, situación y dominio. Por consiguiente, las tareas de diagnóstico y apoyo para toma de decisiones han sido las más utilizadas entre las diferentes topologías de los SE [17], ofreciendo así aplicaciones para una gran variedad de dominios, entre ellos, la medicina.
El objetivo principal de los sistemas expertos de diagnóstico es capturar el estado de una entidad con base en una serie de datos (variables observables) y producir una diagnosis [17]. De este modo, los sistemas de apoyo para toma de decisiones clínicas (del inglés Clinical Decision Support Systems, CDSS) ayudan a los terapeutas en el análisis de las variables médicas de cada paciente con lo que mejoran la calidad de los diagnósticos y tratamientos al no verse afectados por el estado físico o emocional del experto o especialista y, debido a su complementariedad para lograr el mejor consenso, contribuyen en la prevención de los errores humanos [18]; igualmente reducen los costos en salud, producto del bajo precio que supone su desarrollo y mantenimiento en comparación con los honorarios que generan los recursos humanos; aparte de la consistencia presente en el proceso de razonamiento, permitiendo la reproducibilidad de los resultados. De la misma manera facilitan la transferencia o reproducción del conocimiento existente por medios electrónicos [19].
Un SE se conforma de distintos componentes (unidades independientes y separadas), algunos de ellos son esenciales ya que están siempre presentes, como la memoria temporal de trabajo o base de hechos, el motor de razonamiento o motor de inferencia, la base de conocimientos y la interfaz de usuario, pero existen otros componentes que pueden formar parte de los sistemas expertos como el módulo de explicaciones y el módulo de aprendizaje, entre otros.
Los datos son extraídos de una memoria temporal de la información dinámica, la denominada base de hechos, abastecida por la información fáctica (datos de entrada) independientemente del algoritmo utilizado para resolver el problema. Dicho saber se almacena en la base de conocimientos conformada por las estructuras y reglas que los rigen, con lo que el desempeño del SE depende de ella y de la forma en que estas nociones se organizan por medio de un mecanismo de inferencia de datos. Así, conjuntando la información de la base de hechos y la base de conocimientos, el proceso de razonamiento se genera mediante el motor de inferencia. Dicha arquitectura permite la modificación del SE a través de la transformación de la base de conocimientos, sin necesidad de reescribir el programa total o parcialmente.
En tanto, los métodos utilizados para la resolución de problemas comúnmente no son procedimientos matemáticos o procesos de datos, sino técnicas de razonamiento, entendiéndose desde el punto de vista de la lógica, que enlazan los elementos mediante reglas de juicio o heurística, a través de leyes y definiciones teóricas. Por ello, el diseño de un SE es un proceso que se consigue con iteraciones de los conocimientos transmitidos por uno o varios expertos. Adicionalmente, las operaciones lógico-matemáticas que contribuyen a la búsqueda de la solución, o a definir el estado de la entidad, se adquieren a través de una interfaz de usuario [19].
Árboles de decisión
Ya que la interpretación de las imágenes puede ser asistida mediante el procesamiento con computadoras, en los últimos años se ha buscado el empleo de algoritmos de Inteligencia Artificial (haciendo uso de redes neuronales o árboles de decisión, entre otros) [20,7] para tal fin. Un árbol de decisión es un grafo que utiliza el método de ramificación como herramienta para determinar el mejor camino dentro de la toma de decisiones, sobretodo cuando hay una gran cantidad de alternativas que llevan a distintas soluciones. Así, el diagrama en forma de árbol exhibe la estructura de una decisión particular, además de su correlación con otras posibles opciones y decisiones, considerándolos entonces como clasificadores. Dichos clasificadores se componen de nodos prueba, donde se toman las decisiones, y nodos hoja, donde se expresa el valor final más acertado alcanzado mediante el flujo de decisión. Debido a que dividen el espacio de instancias (casos), de manera recursiva, en pequeños conjuntos o clases de acuerdo a un criterio de discriminación [21], suponen una gran ayuda para la evaluación termográfica e integral de las patologías mamarias. Por lo tanto, se han realizado intentos por mejorar la clasificación térmica diagnóstica haciendo uso de ellos, como los trabajos realizados en [22,23,24].
Los árboles de decisión poseen ventajas sobre las redes neuronales en cuanto a requerimientos en la capacidad de cómputo y al tiempo de generación de resultados. Específicamente, en las redes neuronales el tiempo de aprendizaje es elevado, además no pueden interpretar lo que han aprendido, y se requiere una amplia cantidad de datos para el entrenamiento; mientras que en los árboles de decisión se identifica el orden de verificación de las condiciones y las acciones que se deben llevar a cabo y se plantea el problema para que todas las opciones sean analizadas, con lo que se facilita la interpretación de la decisión tomada.
Metodología
Para realizar la detección y la clasificación de las patologías que presentan las glándulas mamarias de una paciente se desarrolló un sistema integral de apoyo a la toma de decisiones clínicas conformado por un sistema experto expresamente realizado “ad hoc” y nuestro Modelo estadístico referencial de distribución térmica de las glándulas mamarias para prediagnóstico por termogramas (anteriormente creado como parte de la investigación). Con base en valores dados por personal del área médica con conocimientos de la temática y experiencia empírica, el sistema realiza la clasificación térmica y estadística de los riesgos patológicos más comunes en las glándulas mamarias femeninas según su grado de pertenencia con respecto a un grupo de valores definidos mediante el análisis de imágenes termográficas y la correlación de los patrones térmicos detectados con respecto a agentes fisiológicos. Esto se lleva a cabo mediante un algoritmo representado con árboles de decisión, mismos que incluyen factores de peso constantes encontrados a través de la correlación de las variables involucradas en el desarrollo de los padecimientos mamarios, i.e., las características termográficas y fisicoquímicas de cada individuo (afectadas por la carga genética, nivel hormonal y hábitos personales, entre otros).
Con el fin de mostrar los resultados obtenidos a través del uso del sistema inteligente, se determinó estadísticamente su capacidad de detección de una anomalía en el seno de acuerdo a la Tabla 1, donde se utilizó la sensibilidad, también llamada tasa de verdaderos positivos (TVP), calculada a través de la Ecuación (1):
El sistema de apoyo para la toma de decisiones en termografía de glándulas mamarias
La arquitectura de nuestro sistema experto se muestra en la Figura 1, a través de 4 componentes independientes y separados. En ella, la base de hechos se compone de las variables determinadas, a través del conocimiento de los expertos en conjunto con el empirismo, para el proyecto “Tipificación de las glándulas mamarias por medio de termografía” llevado a cabo en CFATA-UNAM en los últimos 4 años. En la base de conocimientos las reglas del tipo if<condición>-then<conclusión>, i.e., cláusulas de Horn con cabeza, se representan mediante una estructura de árbol binario, en donde la premisa y la conclusión de dichas reglas toman los valores de los parámetros de las variables obtenidos y de los factores de peso que determinan la solución, respectivamente. El motor de razonamiento se conforma por las metarreglas que aplican los árboles de decisión, quien al emplear la estrategia de razonamiento, recorre los árboles, obteniendo como resultado las presuntas patologías. Por último, la entrada y salida de la información se realiza dentro de la interfaz de usuario o interfaz usuario-máquina, Human-Machine Interface (HMI).
Previamente, como parte de la metodología del desarrollo de un sistema experto, se realizó la ingeniería del conocimiento. De esta forma, la información referente a los parámetros físicos, el estado hormonal, la carga genética y los hábitos de la paciente, fue obtenida de un oncólogo en funciones, quien basado en su experiencia y conocimientos, y haciendo uso de estudios de mamografías, ultrasonidos y resultados de biopsias, determinó las variables, sus valores y los factores de peso correspondientes.
Para conformar la base de conocimientos se realizó la recopilación y análisis de 10,000 patrones termográficos y su correlación con los factores externos e individuales de cada paciente que acudió a la prueba de termografía en el CFATA-UNAM y UNEME-DEDICAM, lo cual permitió obtener los pesos de los valores de las variables obtenidas acorde a un modelo base, el cual se declara más adelante en este documento, generado y desarrollado con anterioridad en el mismo Centro de Investigación. Todos los termogramas4 destinados al desarrollo y evaluación del sistema inteligente se tomaron del banco de imágenes del Grupo de Detección Óptica Tumoral (DOT) del CFATA-UNAM. Todo ello conforma la base de conocimientos.
Cabe señalar que, en el desarrollo de nuestra investigación se utilizó el razonamiento deductivo. El razonamiento deductivo o guiado por los datos (también llamado razonamiento con encadenamiento hacia adelante o razonamiento “forward”) consiste en enlazar los conocimientos a partir del uso de datos (hechos o propiedades de la entidad) con el fin de obtener la solución de un problema. Particularmente, en este caso, la entidad es la paciente, los hechos se conforman del historial (clínico y termográfico) y su estado será la supuesta patología. Dado que en dicho razonamiento se generan nuevos hechos, existen dos formas de tratarlos, que son: en profundidad, cuando un hecho se introduce a la base de conocimientos en cuanto es generado, o en anchura, cuando no se incorporan los hechos a esta base hasta que se ha terminado. Ambos tratamientos son posibles en el presente SE. Tal encadenamiento está basado en la regla de inferencia del modus ponens de la lógica formal que dice que: ‘si conocemos la regla “si A entonces B”, y A es cierto, entonces podemos deducir que B también es cierto’. De un hecho así deducido se puede asegurar su verdad [25].
Por otro lado, recientemente se ha introducido el concepto de sistemas expertos integrados en donde se combinan diversos constituyentes, tales como ingeniería de bases de datos, producción y administración de la información, paquetería software con herramientas gráficas, de cálculo y de modelado, sistemas educativos, o simuladores para aplicaciones dinámicas, entre otros [26]. En este caso, su arquitectura se representa de la forma SE + C, donde el SE queda a cargo de los componentes con estructura formal débil5 del problema planteado y C supone un complemento que provee apoyo a la toma de decisiones para la parte formal [26]. Por lo tanto, el presente sistema consiste en el sistema experto (SE) como tal, el cual está conformado por
› los datos identificadores y clínicos (que comprenden la base de hechos), mismos que abarcan la información proporcionada por la paciente, tal como es la edad, el tamaño de seno, sus hábitos, los antecedentes heredo familiares (carga genética) que posee, presencia de signos y síntomas, etc. y las observaciones obtenidas mediante la examinación y la prueba termográfica, donde se busca la detección de asimetría y manchas térmicas significativas, entre otros,
› los árboles de decisión (algoritmo utilizado por el motor de razonamiento), que implican las reglas a seguir por el SE. Son una técnica utilizada para predecir y explicar la relación entre los datos obtenidos durante la entrevista y las mediciones térmicas, así como los resultados según su pertenencia estadística, pues discriminan una fracción de la información en cada entrada y dividen los datos de manera recursiva en pequeños conjuntos o clases de acuerdo a las reglas del tipo if<condición>-then<conclusión>,
› los factores de peso y las reglas de secuencia (lo cual se encuentra dentro de la base de conocimientos), ambos determinados heurísticamente con base en la información suministrada por el oncólogo y el experto en termografía. Estas reglas y factores de peso se van tomando por el SE según sea el caso de estudio, i.e., depende de la base de hechos,
› la interfaz de usuario, denominada aquí interfaz usuario-máquina (HMI), donde el médico o especialista en termografía captura los datos otorgados por la paciente en las diferentes pestañas de la HMI. Complementariamente incorpora los termogramas más significativos, previamente analizados y captura información perteneciente a estas imágenes. Finalmente, se obtiene como resultado un porcentaje de correlación de los presuntos hallazgos encontrados con respecto a un modelo base (mencionado más adelante) que funge como complemento (C),
y, su complemento (C), que está configurado por un “Modelo estadístico referencial de distribución térmica de las glándulas mamarias para prediagnóstico por termogramas”6 desarrollado a finales de 2012 en CFATA-UNAM; el cual llamaremos modelo de referencia (MR). Del MR se obtuvieron los parámetros de análisis de manera heurística considerando los factores de peso extraídos del conocimiento de un experto, y el SE hace un comparativo de los termogramas con dicho modelo aunado a los parámetros de carga genética y hábitos, entre otros, arrojando como resultado un porcentaje de pertenencia con respecto a los parámetros estadísticos normales o patológicos, tomando en cuenta todos los datos de la base de hechos.
En consiguiente, el sistema desarrollado en nuestra investigación, denominado sistema de apoyo (SA) está conformado por el sistema experto (SE) y el modelo de referencia (MR); es decir:
tal que
y
Donde K es el conjunto de contextos K i u objetos que pertenecen a la base de conocimientos (BC) con K = {K i }, i = 1...n, los cuales modifican o implementan las reglas, i.e., son los factores de peso que se modifican en cuanto a la presencia o ausencia de las variables. P es un programa o software específico que administra la entrada de datos y el proceso de aprovechamiento del conocimiento para el motor de razonamiento. H son las herramientas adicionales que se utilizan para la generación del sistema experto, con H = {H i }, i = 1...m, como es el uso de imágenes termográficas y el software de análisis y discriminación de termogramas. P I corresponde a los parámetros de imagen, P CG a los de carga genética, P H a los de hábitos, P EH al estado hormonal y P F a los parámetros físicos de cada paciente tomada en cuenta para la generación de los modelos de referencia de normalidad, patología benigna y carcinoma.
Los árboles de decisión con factores de peso heurísticos
Las principales variables que intervienen en el diagnóstico del cáncer de seno en nuestra investigación, así como sus factores de peso correspondientes, fueron otorgados por personal con experticia en la temática. La asignación de los pesos por el sistema se realizó mediante la aplicación de los algoritmos representados por los diagramas de flujo de las Figuras 2, 3, 4 y 5, donde la Figura 2 concierne a las características físicas de la paciente: el tipo somático (ectomorfo, mesomorfo, endomorfo), la edad (≤13, >13 y ≤24, >24 y ≤50, ≥72) y el tamaño del seno (A, B, C, D, X); la Figura 3 hace referencia a su situación hormonal: la fase hormonal en la que se encuentra la paciente al momento del estudio (ovulatoria, folicular, menstrual, lútea) y la presencia/ausencia de terapia hormonal a lo largo de su vida; en la Figura 4 se relaciona la carga genética que es susceptible de heredar la voluntaria (cáncer de madre, cáncer de abuela materna, cáncer de hermana) y se incluyen aquí los antecedentes de mastopatías; y la Figura 5 se refiere a sus hábitos de salud (tabaquismo, alcohol, actividad física, insomnio).
Los algoritmos representados por dichos diagramas de flujo fueron plasmados en grafos etiquetados conexos acíclicos, i.e., en árboles. En consecuencia, se modeló un árbol de decisión binario por cada diagrama de flujo, dadas las características de los algoritmos que involucran alternativas de elección “sí” o “no”. De esta manera, los diagramas de flujo de las Figuras 2, 3, 4 y 5 se corresponden con los árboles de decisión de las Figuras 6, 7, 8 y 9.
En los diagramas de flujo se muestran las principales variables y sus factores de peso correspondientes para los árboles de decisión destinados a las características físicas de la paciente, a la situación hormonal, a la carga genética que hereda incluyendo antecedentes de mastopatías, a sus hábitos de salud y a los termogramas analizados, respectivamente. Así, las variables presentes en una paciente y sus respectivos valores, pueden ser modelados haciendo uso de árboles binarios que actúen como una herramienta para la decisión. Dichos valores son dados por el usuario (e.g. médico, analista de laboratorio, técnico especialista) al sistema. Estos valores fueron considerados como nodos de los árboles, y modelados de forma que al considerar un sí o un no, en cada uno de dichos valores, se marca el camino del árbol en cuestión, i.e., cada rama es un diferente camino, que inicia en la raíz y termina en una hoja. En las hojas de cada uno de los árboles, se indica el valor de la suma resultante de la adición de cada peso del nodo seleccionado acorde al camino recorrido en el árbol (desde la raíz hasta la hoja en cuestión), mismo que se va acumulando a una variable referida como Σ. Tal cantidad es tomada en cuenta en una etapa preliminar para el análisis de los termogramas de la paciente, como lo muestra el algoritmo del diagrama de flujo de la Figura 10, mismo que es plasmado mediante un último árbol de decisión, exhibido en la Figura 11. De esta forma, cada hoja Σ de este árbol es el resultado de la suma acumulada de los 4 árboles (i.e., la adición correspondiente a los parámetros físicos, al estado hormonal, a la carga genética y a los hábitos) y del camino recorrido del propio árbol del termograma.
Este algoritmo contempla la suma preliminar (>113, ≤113) que proviene de la suma de las ponderaciones de los grupos de parámetros anteriores, además la simetría, la cima térmica (> 2◦C, ≤ 2◦ C), la forma de la mancha (vascular, difusa, ovoide, palomita de maíz), el cuadrante (I, II, III, IV, retroareolar) y el gradiente de temperatura (≥ 1,4◦C, <1.4◦C). Entonces, al final se obtiene la Σ que, dependiendo de los rangos en los que se encuentre, el sistema indica la medida a tomar para cada caso particular, ya sea repetir el examen en un periodo que va desde el mes hasta los 6 meses, o complementar inmediatamente con otra técnica de detección y, a continuación, proceder a una toma de muestra de tejido, en casos muy especiales y de extrema urgencia de diagnóstico patológico.
Nuestros árboles de decisión pueden describirse como árboles etiquetados, con raíz, donde cada rama realiza un recorrido desde el nodo raíz hasta los nodos terminales u hojas, de tal forma que las hojas son la suma de los pesos de cada camino. Asimismo podemos definir a nuestros árboles G como un par ordenado G(N, A) donde N es el número de nodos y A es el número de aristas o arcos (a, b) que relacionan a un par ordenado de nodos, donde a es el nodo inicial y b es el nodo terminal de la arista. Las etiquetas de todas las aristas son “sí=#” o “no=#”, donde # son los pesos.
De esta forma podemos brevemente comentar que los dos árboles de la Figura 6 involucran a los parámetros físicos de la paciente: el árbol G(6,5) de la izquierda, tiene de altura 4, y el árbol G(54,53) de la derecha, tiene de altura 10; en ambos, sus hojas se corresponden con la suma de los pesos de cada camino. El árbol G(6, 17) de la Figura 7 que representa al estado hormonal de la paciente, tiene de altura 6, y en sus nodos hoja se encuentra la suma de los pesos de cada camino en el recorrido.
Los árboles binarios G(31, 30) de las Figuras 8 y 9 que contemplan a la carga genética y a los hábitos de la paciente respectivamente, son estrictamente balanceados, con una altura 5, conteniendo los mismos nodos y aristas en cada una de sus ramas; sus hojas se corresponden con la suma de los pesos de cada camino del árbol en cuestión. El árbol G(26,34) de la Figura 11 que compete al termograma de la paciente, tiene de altura 14. Y todas sus hojas son Σ (la suma de los pesos de cada camino recorrido en (G(26,34)); como previamente se mencionó, este árbol contempla la suma acumulada de cada uno de los otros árboles (como sumas parciales de los pesos de los caminos recorridos en cada árbol, plasmadas en sus hojas), la cual denominamos “suma”.
Adicionalmente, se expone en la Figura 12 un grafo ponderado para visualizar la correlación entre las variables pertenecientes a diferentes árboles de decisión. Esta correlación implica un factor de peso extra que será considerado en el resultado de las sumas individuales; e.g., si la paciente fuma, se considera un peso de 12, además si su madre tuvo cáncer se considera un peso de 15, pero el valor final no será la suma de ambos, es decir 12+15=27, sino que habrá que adicionar un peso extra de 8 al tener ambas situaciones la paciente; por lo que el peso de fumar y de haber tenido cáncer su madre es de 12+15+8=35. Por ende, según el recorrido llevado a cabo en cada uno de los árboles, se obtiene un resultado, procedente de la suma de las ponderaciones correspondientes. Cada una de ellas se contempla para alcanzar un valor final el cual determina en un último árbol de decisión el resultado de presunción patológica.
Modelo estadístico térmico referencial
Los estudios para establecer las patologías en glándulas mamarias por termografía requieren del conocimiento de múltiples variables que determinan el factor de riesgo. Para esto, se analiza la carga genética mediante el historial clínico y los hábitos alimenticios y de comportamiento, entre otros, aunados a la información termográfica. La determinación del modelo térmico de referencia (MR) se realizó obteniendo parámetros, tales como el valor máximo de temperatura por cuadrante de la glándula mamaria, la simetría térmica, la forma de la mancha térmica y los parámetros máximo, mínimo y promedio por cuadrante y zona retroareolar, de 2532 personas voluntarias. De ellas se obtuvieron grupos de edad, tipo somático, estadio hormonal, volumen de seno, forma del seno, etc. Dentro de esta población se reportaron como sanas 1911 y el resto con alguna patología. Los grupos patológicos son a) lesiones benignas (1816 voluntarias), b) trastornos inflamatorios o infecciosos (63 voluntarias) y c) lesiones malignas (32 voluntarias). Las cuantificaciones se analizaron estadísticamente para obtener campos de desviación acordes a cada grupo de edad y parámetros identificados. Con esto se tienen plantillas donde gráficamente se ilustra la pertenencia porcentual a los grupos de normalidad o patológicos. Los casos patológicos que forman parte de este estudio fueron diagnosticados mediante otras técnicas de imagen y corroborados clínicamente con base en resultados de patología en la Unidad de Especialidades Médicas en Detección y Diagnóstico de Cáncer de Mama (UNEME-DEDICAM) del Estado de Querétaro.
Implementación del sistema de apoyo a la toma de decisiones en termografía de glándulas mamarias
El sistema fue implementado en LabVIEW® con 6 menús diferentes para la interfaz humano-máquina (HMI). Así pues, se presentan en las Figuras 13 y 14 las diferentes ventanas en las que se capturan los datos de la paciente (información de entrada que corresponde a cada voluntaria). En el primer menú se incluyen los parámetros físicos, la carga genética, las características hormonales, los signos y síntomas orientados a las patologías mamarias y los hábitos. Complementariamente, se anotan los estudios de seno y sus diagnósticos previos, así como la fecha de realización y otras observaciones, en caso de requerirse así. El segundo menú permite al especialista en termografía añadir los valores identificados durante el análisis térmico, tanto en la vista general de ambos senos para detectar simetría y la cima térmica en manchas significativas, como en una toma más cercana para analizar cada seno por separado donde se incluye la forma de la mancha y el cuadrante en el que se localizan las mismas. El sistema utilizado recibe como entrada los datos de la paciente que el usuario (médico, analista de laboratorio, técnico especialista) introduce a través de las interfaces presentadas en las Figuras 13 y 14 7. El sistema realiza una sugerencia de la presunta patología que, según los hechos especificados durante el examen termográfico en su totalidad, se apega estadísticamente mejor a uno de los modelos (de normalidad o patología) del MR, arrojando entonces como salida la probabilidad clínica de padecerla, i.e., el porcentaje de certeza de sufrir ese tipo de patología, la cual puede ser, principalmente: trastornos inflamatorios (e.g. mastitis) o infecciosos, mastopatía fibroquística, necrosis grasa o cáncer de seno en las etapas III y IV. De esta forma, los resultados que arroja el SE se declaran en un reporte termográfico y se asocian a una escala experimental de clasificación térmica de factor de riesgo patológico (Tabla 2) diseñada por el grupo DOT. Dicho reporte, puede ser entregado al médico especialista, quien se apoyará del estudio termográfico para complementar el diagnóstico mamario con base en otras técnicas de detección adicionales8. La Figura 15 muestra una metáfora de las entradas y salidas del sistema experto en cuestión.
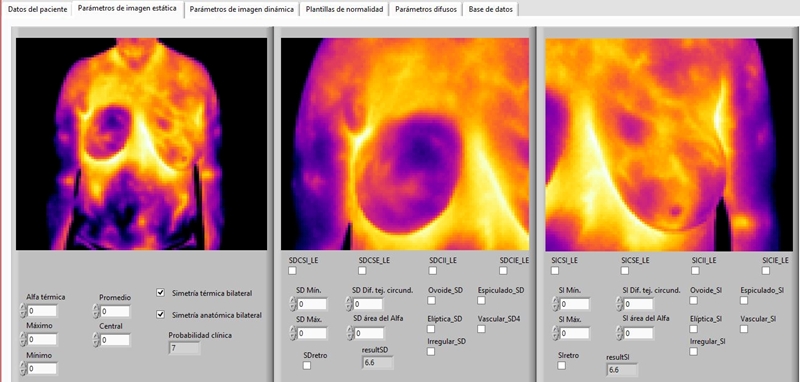
Figura 14: Menú 2 de la HMI. Según las características térmicas de la paciente (detectadas a través del análisis previo de los termogramas), en conjunción con los datos anteriores, se arroja la probabilidad clínica de padecer alguna patología.
Resultados y discusión
Con los resultados obtenidos a través del uso del sistema inteligente, se determinó estadísticamente su capacidad en la detección de anomalías en el seno, i.e., los porcentajes de certeza del sistema, mostrados en la Tabla 1. Se consideraron 300 muestras entre las que se incluyen casos de 40 mujeres sanas y 260 casos patológicos con confirmación diagnóstica de la UNEME-DEDICAM Querétaro, entre las cuales se hallaron patologías benignas desde la etapa preclínica en 181 pacientes de 230 diagnosticadas como tal y casos de cáncer en etapas desde IIIA hasta IVB en 26 de las 30 diagnosticadas.
Durante el análisis de los termogramas ocurre la mayor parte del error generalizado, ya que existe la posibilidad de haber factores no tomados en cuenta asociados a la paciente o al ambiente por los cuales el mismo puede arrojar falsos positivos. La sensibilidad reportada en la Tabla 1 varía del 62 % al 96 % debido, posiblemente, a la versatilidad del tejido del seno y a la profundidad tisular a la que se encuentre dicha patología (ubicación), influyendo entonces en la representación térmica captada durante la adquisición de imágenes.
Así, en los trastornos inflamatorios o infecciosos se tuvo una certeza del 96% lo cual se considera aceptable pues los estadios patológicos estaban en franca declaración, lo que implica que las imágenes termográficas obtenidas reporten valores contrastantes en la región de la patología con respecto al tejido circundante. El porcentaje de certeza de la mastopatía fibroquística (MFQ) también se considera aceptable, sin embargo, el valor de 78% es debido a que esta patología benigna termográficamente tiene un gradiente de temperatura relativamente bajo con respecto a las etapas hormonales. La necrosis grasa tiene un valor de 62% en certeza ya que, al ser una condición avascular, las ponderaciones térmicas desde el punto de vista de medición dinámica no permiten identificar lesiones de volúmenes inferiores a 1 cm cúbico. El cáncer de seno, reporta 86% de confiabilidad debido a que algunos de los pacientes se encontraban en etapa IV, donde la lesión es palpable (nodular) y los factores de vascularidad son amplios. El 14% de error se debe a que tales lesiones se asocian a microcalcificaciones mismas que con la técnica termográfica reportada no es posible diferenciar. Por lo tanto, a pesar de que los resultados obtenidos para la detección de patologías benignas son ligeramente menores que los que entrega un equipo de US, se aprecian favorables en cuanto a la detección de cáncer en etapas III y IV. Asimismo, de los 40 casos de mujeres sanas, se diagnosticaron como enfermas a 939, con lo cual la tasa de falsos positivos es bastante alta aún, sin embargo, la técnica es complementaria y se requiere de confirmación diagnóstica con los demás métodos disponibles.
Conclusiones
Se creó una primera aproximación hacia un sistema de apoyo para la toma de decisiones clínicas destinado a la detección y clasificación de patologías en las glándulas mamarias. Con él se mejora la posibilidad de aplicación de pruebas de detección temprana en la población que sufre de contraindicaciones para realizarse los exámenes con otros métodos, además permite un diagnóstico integral para las demás pacientes. Asimismo, la realización del análisis termográfico de manera periódica (lo cual no conlleva efectos secundarios) favorece la atención personalizada y el seguimiento del progreso metabólico de cada individuo.
El sistema de clasificación respondió apropiadamente, clasificando correctamente el 78% de casos benignos y el 86 % de malignos. No obstante se requiere mejorar el sistema mediante el incremento de las variables o parámetros contemplados, así como el ajuste de los factores de peso considerando los nuevos casos de estudio existentes.
Adicionalmente, se ha observado que los árboles de decisión son de fácil implementación debido a la sencillez de entendimiento y seguimiento del proceso, así como a su accesibilidad para modificar los factores de peso. La ventaja desde el punto de vista técnico de utilizar el razonamiento deductivo es su sencillez, aunado a que la entrada de datos es única y se da al principio del programa. Ello muestra que el sistema de clasificación de patologías basado en árboles de decisión para evaluación de termogramas puede ser de gran apoyo en el tamizaje de cáncer de seno debido a la inocuidad de la técnica, la simplicidad del sistema y su bajo costo de operación.
Aunque la termografía superficial no permite determinar la posición cartesiana de la lesión, sino el cuadrante en el que se encuentra presente, bien puede estimarse como una técnica complementaria a las convencionales, con resultados que mejoran cada vez más al combinarla con sistemas inteligentes para el análisis y clasificación de imágenes en apoyo de la toma de decisiones.
Por ende, la importancia de este sistema radica en el aprovechamiento de los patrones termográficos y su correlación con los factores externos e individuales de cada paciente que acude a la prueba de termografía. Con él, se genera una sugerencia de patologías que pudiera padecer la paciente en cuestión, conforme al apego estadístico de la ponderación obtenida al final del examen térmico en su conjunto. Por último, la interfaz de usuario desarrollada permite que el analista no requiera de mayores conocimientos más que la información proporcionada por la paciente y los parámetros detectados en sus termogramas para utilizar el sistema y lograr obtener un resultado de los presuntos padecimientos, con una adquisición fácil y rápida, pero sobretodo confiable, basado en comparaciones con un modelo referencial.











 nova página do texto(beta)
nova página do texto(beta)


















