Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Hidrobiológica
versão impressa ISSN 0188-8897
Hidrobiológica vol.20 no.3 Ciudad de México Jan. 2010
Artículos
Estimación de la emigración del camarón café Farfantepenaeus aztecus a través de la boca del Mezquital, Tamaulipas, México
Emigration assessment of the Brown Shrimp Farfantepenaeus aztecus through Mezquital Inlet, Tamaulipas, Mexico
Armando T. Wakida–Kusunoki,1,2 Alejandro González Cruz,3 Margarita Medellín Ávila3 y Francisco Arreguín–Sánchez4
1 Instituto Nacional de Pesca, Dirección General de Investigación Pesquera del Atlántico. Ave. Héroes del 21 de abril s/n Col. Playa Norte, Ciudad del Carmen, Campeche 24120. México.
2 Estudiante del Programa de Doctorado en Ciencias Biológico Agropecuarias de la Universidad Autónoma de Nayarit. Unidad Académica de Agricultura. Km 9 Carretera Tepic–Compostela. Jalisco, Nayarit. México.
3 Instituto Nacional de la Pesca, Centro Regional de Investigación Pesquera de Tampico. Prolongación Altamira s/n Col. Isleta Pérez. Tampico, Tampico 89090, México.
4 Centro Interdisciplinario de Ciencias Marinas. Instituto Politécnico Nacional. Apartado Postal 592, La Paz, Baja California Sur 23000, México. E–mail: armandowakida@yahoo.com.mx.
Recibido: 17 de diciembre de 2009
Aceptado: 10 de diciembre de 2010
RESUMEN
Se presentan la variación en abundancia de juveniles de camarón café (Farfantepeneaeus aztecus) durante su principal periodo de emigración hacia el mar, en la boca del Mezquital, Tamaulipas. Los muestreos fueron realizados entre mayo y julio del 2003 al 2007 y consistieron en el uso de una red de corriente experimental durante el periodo nocturno y durante periodos de bajamar, en los tres días anteriores y posteriores a la presencia de luna nueva y llena. La información fue complementada con datos de abundancia obtenidos con arrastres en cruceros de investigación realizados en la costa de Tamaulipas durante mayo a julio del 2003 al 2007. Los resultados muestran que los máximos valores de emigración (kg/noche) se presentan durante el periodo lunar a finales de mayo y/o principios de junio, indistintamente de la fase lunar y se relacionaron directamente con aumentos en los valores de abundancia en la zona costera y marina. Estos resultados son de gran importancia porque demuestran que mayo y junio son meses críticos para esta especie, y sirven como base para la definición de los periodos de veda para la pesca de camarón, tanto en la zona lagunar como en altamar.
Palabras clave: Farfantepenaeus aztecus, camarón café, emigración, Tamaulipas.
ABSTRACT
Variations of juvenile abundance of brown shrimp (Farfantepenaeus aztecus) during its main period of migration in Mezquital Inlet, Tamaulipas are presented. Sampling was carried out from 2003 to 2007 between May and July and consisted in the use of an experimental net during the nocturnal period and ebb tide, three days before and after full and new moon. The information was complemented with abundance data of trawl research cruises carried out off the coast of Tamaulipas between May and July from 2003 to 2007. The results showed that the higher values of emigration (kg/night) occurred during the moon period in late May or early June, independently of the lunar phase. The higher values of emigration toward the sea are directly related to the increase in the abundance in the coastal and marine zones. These results are of great importance because the significance of the months of May and June was demonstrated, and can be useful to set the limits of the closed season of the inshore and offshore shrimp fishery.
Key words: Farfantepenaeus aztecus, brown shrimp, emigration, Tamaulipas.
INTRODUCCIÓN
La pesca del camarón en la zona de Tamaulipas es la más importante del litoral mexicano del Golfo de México (INAPESCA, 2007). Esta se sustenta principalmente en la captura del camarón café Farfantepenaeus aztecus (Ives, 1891).
La captura anual reportada en la zona de Tamaulipas en el año 2005 fue de alrededor de las 18,000 t lo que equivale el 81% de la captura total mexicana del Golfo de México (CONAPESCA, 2005).
Actualmente se considera que la situación de la pesquería de camarón en esta zona, tanto en la zona lagunar, como en altamar, se encuentra aprovechada al máximo sostenible (Wakida–Kusunoki et al., 2006)
El camarón café presenta un ciclo de vida conocido para los camarones peneidos (Garcia y LeReste, 1981; Dall et al., 1990; Ehrhardt et al., 2001; Arreguín–Sánchez & Castro, 2000; Haas et al. 2001, Haas et al. 2004) que se caracteriza por presentar dos etapas: la primera en el mar, donde se lleva a cabo la maduración y reproducción, así como el desarrollo de las etapas larvales y una segunda donde las postlarvas penetran a lagunas y esteros para su crecimiento y etapa juvenil, para iniciar su proceso de migración de la laguna hacia el mar. Estos procesos de migración del camarón tienen como consecuencia el aumento de la abundancia en la zona marina (Gracia, 1997a, Wakida–Kusunoki et al., 2005).
Debido a las características de su ciclo de vida, la pesca del camarón en esta zona es de carácter secuencial ya que es capturado en la zona lagunar de forma artesanal y en altamar por una flota industrial. (Arreguín–Sánchez et al., 1997; Gracia, 1997a; Wakida–Kusunoki et al., 2005).
La boca del Mezquital se localiza en el área norte de la Laguna Madre. Esta boca es la única boca funcional, siendo en consecuencia el área más importante de entrada y salida de camarones que son capturados en la zona lagunar y costera de Tamaulipas (Wakida–Kusunoki et al., 2008).
La captura del camarón en los cuerpos lagunares se realiza por medio de charangas, que son artes de pesca fijos, que dependen de las mareas de reflujo para su captura y del proceso de emigración del camarón hacia aguas marinas (Gracia, 1997b). Este reflujo, generalmente ocurre en horas nocturnas. Por lo anterior, las capturas efectuadas en la laguna podría considerarse como un indicador de emigración del camarón café hacia zona marina.
El análisis de la emigración de los camarones de la laguna a la zona marina permite conocer la intensidad del reclutamiento hacia altamar, además de ser un evento relevante para la pesquería de arrastre de la plataforma adyacente, es información fundamental para efectos de manejo del recurso pues permite estimar el periodo de veda en los cuerpos lagunares y la fecha de apertura de veda en la zona marina, donde se tiene como objetivo la optimización biológica y económica de la biomasa (INAPESCA, 2007). En los cuerpos lagunares, el periodo de veda tiene como objetivo proteger parte de este periodo de emigración masiva que permite el escape de reclutas a altamar, con esto se asegura la sustentabilidad de la pesquería en altamar y del recurso. Para la parte de altamar el conocimiento del periodo y tallas de emigración masiva permite estimar mediante modelos matemáticos el periodo de veda con el objetivo de que los organismos crezcan hasta una talla donde se alcance el máximo beneficio económico, lo que generalmente se presenta alrededor de 75 días después de la fecha estimada como la de mayor reclutamiento (INAPESCA, 2008).
El presente trabajo tiene como objetivos: 1) Evaluar la variación en abundancia y tallas de juveniles de camarón café (Farfantepenaeus aztecus) en la boca del Mezquital, Tamaulipas durante su principal periodo de emigración (mayo a julio del 2003 al 2008); y 2) Relacionar el máximo periodo de emigración con los rendimientos obtenidos en la zona costera y marina.
MATERIAL AND METHODS
Se realizaron campañas de muestreo en la boca del Mezquital (Fig. 1) durante los periodos de mayo a julio del 2003 al 2007, épocas donde se presentan los mayores picos de emigración de juveniles de camarón café hacia el mar (Benefield & Baker, 1980; Divita et al., 1983; Sheridan et al., 1987; Larson, 1989, Baron–Mounce et al., 1991; Li & Clarke, 2005). Estos muestreos se realizaron de dos a cuatro días antes de la luna nueva y llena, periodo cuando se presentan las alturas de mareas y velocidades de corrientes más altas que estimulan la emigración del camarón (Lassuy, 1983).
Para la realización de los muestreos se utilizó una red experimental de corriente (Fig. 2), ya que por la profundidad y zona de muestreo no es posible usar el arte de pesca tradicional. La red fue fijada en un punto único durante todas las campañas de muestreo en el canal de la boca del Mezquital. La colecta de organismos se realizó durante el reflujo de marea y abarcó el crepúsculo y parte de la noche. Es durante este periodo cuando se presenta con mayor intensidad el reflujo y el camarón café probablemente presenta mayor actividad migratoria (King, 1971; Lassuy, 1983; NMFS,2008; INAPESCA, 2007).
Se registró la hora de comienzo y término de muestreo y el número de organismos capturados por hora. Se tomó una muestra al azar cada hora de los organismos capturados para realizarle biometrías, consistentes en la medición de la longitud total en mm y su peso en gramos. Con esta información se calculó el peso total obtenido durante el periodo de muestreo por medio de la siguiente fórmula:
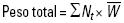
Donde Nt es número de camarones capturados y  es el peso promedio de los camarones de la muestra. Este procedimiento no se efectuó durante 2004 y 2005, cuando el número de organismos no se registró por hora, sino por noche.
es el peso promedio de los camarones de la muestra. Este procedimiento no se efectuó durante 2004 y 2005, cuando el número de organismos no se registró por hora, sino por noche.
La captura por hora obtenida se comparó con la altura de marea, obtenida del programa MAR VO.8. (González et al., 2009).
Así mismo, se analizó la información obtenida en cruceros de investigación de pesca exploratoria que se realizaron en la zona marina de Tamaulipas durante mayo, junio y julio del 2003 al 2007. El diseño del muestreo y las especificaciones de estos cruceros se pueden consultar en Wakida–Kusunoki et al. (2005). Se realizaron cálculos de los rendimientos por estratos de profundidad, uno costero que fue de 9.1 a 21.9 m (5 a 12 brazas), otro de 21.9 a 45.7m (12 a 25 brazas) y el ultimo a profundidades mayores de 45.7 m (>25 brazas). Estos estratos fueron limitados entre los grados de 24 y 26 °N, con la finalidad de que un aumento en los rendimientos en cada uno de los estratos nos indicará con mayor probabilidad, la posible entrada masiva de organismos provenientes de la laguna o de un estrato de menor profundidad, ya que se conoce que el comportamiento del camarón café es moverse progresivamente a zonas de mayor profundidad conforme aumenta su tamaño. (Lassuy, 1983, NMFS,2008).
RESULTADOS
El comportamiento de la captura obtenida durante los periodos de muestreo se puede observar en la Fig. 3, donde se aprecia que los mayores valores se observaron a finales de mayo y principios de junio. En la Tabla 1 se muestran los días donde se presentaron los mayores valores y su relación con las fases lunares. Estos máximos valores se presentaron indistintamente en periodos de influencia de luna llena o nueva. Los valores más altos del índice de abundancia de juveniles variaron de 46 a 150 kg de camarón por noche.

En cuanto al comportamiento de la captura de juveniles, se encontró que el valor más alto se presenta en horas cercanas al momento que la altura de mar alcanza su mínimo valor (Fig. 4).
Las tallas de los organismos capturados durante el día de mayor emigración estuvieron entre los 55 y 125 mm de longitud total (LT) con modas de 70 y 80 mm LT (Fig. 5a–e). En la mayoría de los años, el rango de tallas fue de 55 a 110 mm. Sólo en el 2007 (Fig. 5e) se presentaron algunos organismos entre 120 y 125 mm de LT.
Los periodos con mayor valor de emigración mostraron una concordancia con los valores de abundancia obtenidos en los cruceros de investigación. Es decir después de la fecha de la presencia de alta emigración, en la zona costera y en los estratos de mayor profundidad se presentó un aumento en los rendimientos de pesca. En el 2003, la fecha estimada como la de mayor índice de migración fue el 29 de mayo (Tabla 1; Fig. 3a). Esto se refleja en la zona marina con un aumento de los rendimientos en el estrato más costero (9.1 a 21.9 m) y en la primera quincena de junio. El rendimiento aumentó de 18 a 35 kg/h (Fig. 6a). En el 2004, no se efectuó el muestreo que se debió haber realizado en la segunda quincena de mayo, sino que únicamente se efectuaron los de junio (Tabla 1; Fig. 3b). Los valores de rendimientos no mostraron diferencias. En cuanto a los valores de emigración, no se observó un pico de migración bien definido durante el periodo estudiado (Fig. 6b). En el 2005 la fecha estimada con mayor emigración fue el 7 de junio (Tabla 1; Fig. 3c), el aumento de la abundancia en la zona marina se observa hasta la segunda quincena de junio en el estrato de 21.9 a 45. 7 m (Fig. 6c). En el 2006, el aumento de la abundancia en el mar se observa hasta la segunda quincena de junio (Fig. 6d), lo cual concuerda con la fecha estimada para mayor emigración que fue el 11 de junio (Tabla 1; Fig. 3d). Por último en el 2007, se presenta el mayor valor de rendimiento para los estratos marinos en todo el periodo estudiado con un valor alrededor de los 150 kg/hora (Fig. 6e). El cual se presentó durante la segunda quincena de junio y en el estrato de 21.9 a 45.7 m. La fecha estimada de mayor emigración fue el 31 de mayo (Tabla 1; Fig. 3e).
DISCUSIÓN
Los resultados muestran que los mayores valores de emigración se presentan indistintamente a la fase lunar, durante el periodo de bajamar y a finales de mayo ó a principios de junio. Esto concuerda con lo mencionado por otros autores en la zona de Texas para la misma especie (Trent, 1966; King, 1971; Benefield & Baker, 1980; Matthews, 1982). El efecto combinado del incremento de la altura de la marea y las velocidades de las corrientes, asociados con el efecto lunar, así como cambios en el la temperatura han sido sugeridos como un estímulo para la emigración de los juveniles hacia el mar (Copeland, 1965; Blackmon, 1974; Garcia & LeReste, 1981; Lassuy, 1983; Turner & Brody, 1983).
Wakida–Kusunoki et al. (2008) menciona que en la zona norte de la laguna Madre, el camarón café presenta valores más altos de abundancia de juveniles en las zonas someras durante abril–mayo, lo cual precede a la época de mayor emigración de esta especie hacia el mar, que se presenta en mayo a junio.
Los resultados ponen de manifiesto la gran variabilidad en el proceso de reclutamiento al mar del camarón café, tanto en el periodo como en su magnitud. Esto es resultado de la combinación de varios factores que intervienen en este proceso como lo son: las mareas, los ciclos lunares, estado de maduración y parámetros ambientales tales como la temperatura y salinidad (St Amant et al,. 1965; Gaidry & White, 1973; Blackmon, 1974).
En cuanto a la hora que ocurren los mayores valores de emigración, en el presente trabajo se encontró que es alrededor de las 21 horas, cuando la marea alcanza su mínima altura. Estos resultados no concuerdan con otros trabajos realizados en Texas, que mencionan que existe poca diferencia entre los valores de emigración obtenidos de día y noche (Clark & Caillouet, 1975) y los que reportan altos porcentajes de emigración del camarón café durante las horas crepusculares (Anónimo, 1996). Estas diferencias sin embargo parecen estar relacionadas con la hora en que se presenta el periodo de reflujo de la marea durante los periodos lunares en mayo y junio. En caso de la zona de estudio, el reflujo de la marea se presenta con mayor intensidad en horas nocturnas (Fig. 4). Esta diferencia posiblemente tenga un efecto en los mecanismos de la emigración en las diferentes zonas.
El rango de tallas encontradas durante este estudio, son similares a las encontradas en otros trabajos. Clark & Caillouet (1975) encontraron para un canal estuarino de Texas, un rango de organismos entre 46 y 114 mm.
Zein–Eldin & Renaud (1986) mencionan que la talla de emigración pueden ser de hasta 135 mm de LT. Las modas de las distribuciones de tallas de los organismos encontradas son similares a las descritas en otros trabajos, donde se menciona que las tallas de emigración se encuentran entre los 80 y 100 mm de LT (Trent, 1966; Zein–Eldin & Renaud, 1986) y en su mayoría menores de 114 mm de LT (Divita et al., 1983). Copeland (1965) menciona que la mayoría de los camarones café que emigran hacia la zona costera está entre los 70 y 80 mm de LT.
Algunos autores mencionan que una reducción en la salinidad debido a descargas de ríos o de lluvias produce la emigración de los juveniles del camarón café (St. Amant et al., 1965; Rulifson, 1983; Zein–Eldin & Renaud, 1986; Gracia,1997b; Clark et al., 2004). Aunque en este trabajo no se registró simultáneamente una serie de salinidad en la laguna para los periodos analizados, Wakida–Kusunoki et al., (2008) presenta una serie de salinidad en el periodo del 2006, donde se muestra que en junio es cuando se presenta el menor valor de salinidad, lo cual está relacionado con la temporada de lluvia en la zona, y con los mayores registros de emigración de camarón. Por otra parte King (1971) no encontró una correlación entre capturas de juveniles de camarón que se encontraban emigrando con cambios en temperatura y salinidad, lo cual pone en evidencia la complejidad del mecanismo de emigración. Saoud & Allen (2003) encuentra que la salinidad afecta la distribución del camarón café en las lagunas costeras y menciona que quizá esta variable tenga un gran efecto sobre el camarón y su pesca.
Al tratar de relacionar los índices de migración con los rendimientos obtenidos en la zona marina adyacente por medio de cruceros, se encontró que existe una coincidencia de la estimación de la fecha de máxima migración con aumentos en los rendimientos en la zona marina adyacente. Esto se puede apreciar con el aumento de los rendimientos en los diferentes estratos de profundidad en tiempos posteriores a los estimados como las fechas de máxima emigración. Existen algunos factores que probablemente provoquen que esta relación en algunos casos no sea tan clara. Una posible causa, es que el movimiento de los organismos no solo es batimétrico en la zona, sino también de forma latitudinal. Sheridan et al. (1987), basado en un estudio de marcado y recaptura efectuado en la misma zona de estudio y realizado durante mayo a agosto, encontraron que los camarones cafés mostraban un patrón con grandes movimientos hacia el sur. Aunque por el tamaño del área y el corto periodo de muestreo, podemos suponer que este tipo de movimiento no tendría un efecto considerable.
Finalmente, de los resultados obtenidos se puede concluir o siguiente: Los picos más altos de captura de juveniles emigrando en la boca del Mezquital fueron a finales de mayo o a inicio de junio, indistintamente del periodo lunar, pero siempre asociado a cambios lunares. Los valores más altos de emigración de juveniles de camarón café en la boca del Mezquital se presentaron generalmente de 9 a 10 pm y siempre asociados a los niveles más bajos de las mareas.
AGRADECIMIENTOS
Se agradece al personal de CRIP Tampico, Antonio González, José Luis Gómez, Guillermo Acosta, Juan Balderas Leobardo García y Enrique Conde por el apoyo en las actividades de campo. FAS agradece apoyos parciales de SIP–IPN 20080932, EDI y COFAA del Instituto Politécnico Nacional.
REFERENCIAS
Anónimo. 1996. (DRAFT)–Taxonomy Species shrimp, brown Species Id M070006. http://fwie.fw.vt.edu/WWW/macsis/lists/M070006.htm. [ Links ]
Arreguín–Sánchez. & R. G. Castro. 2000. On the interdependence of sequential fisheries: the brown shrimp, Farfantepenaeus aztecus, fisheries in the northwestern Gulf of Mexico. Crustaceana 73 (3): 333–343. [ Links ]
Arreguín–Sánchez, F., L. E. Schultz–Ruíz, A. Gracia, J. A. Sánchez & T. Alarcón. 1997. Estado actual y perspectivas de las pesquerías de camarón. In: D. Flores–Hernández, P. Sánchez–Gil, J.C. Seijo & F. Arreguín–Sánchez (Eds.). Análisis y diagnóstico de los recursos pesqueros críticos del Golfo de México. Univ. Autón. Campeche, EPOMEX Ser. Cient. 7, Campeche, México. pp. 185–203. [ Links ]
Baron–Mounce, E., W. Keithly & K. Roberts. 1991. Shrimp facts. Louisiana Sea Grant College Program. http://nsgl.gso.uri.edu/lsu/lsug91001.pdf. [ Links ]
Benefield, R. L. & W. B. Baker Jr. 1980. Studies of shrimp populations in selected coastal bays of Texas. Texas Park Wildlife Department. Coastal Fisheries Branch. Data series 13: 1–102. [ Links ]
Blackmon, J. H., Jr. 1974. Observation on the immigration of the brown shrimp, Penaeus aztecus, throught a tidal pass in the Caminada Bay, Lousiana area. M. S. Thesis. Louisiana State University, Baton Rouge. 58 p. [ Links ]
Clark , S. H. & C. W. Caillouet. 1975. Diel fluctuations in catches of juvenile Brown and White shrimp in a Texas estuarine canal. Contributions in Marine Sciences 19: 119–124. [ Links ]
Clark, R. D., J. D. Christensen, M. E. Monaco, P. A. Caldwell, G. A. Matthews & T. J. Minello. 2004. A habitat–use model to determine essential fish habitat for juvenile brown shrimp (Farfantepenaeus aztecus) in Galveston Bay, Texas. Fishery Bulletin, U.S. 102: 264–277. [ Links ]
CONAPESCA (Comisión Nacional de la Pesca). 2005. Anuario estadístico de pesca 2005. SAGARPA. http://www.sagarpa.gob.mx/pesca/anuario/anuario2001. [ Links ]
Copeland, B. J. 1965. Fauna of the Aransas Pass Inlet, Texas. Emigration as shown by tide trap collections. Publication of Institute of Marine Science. University of Texas 10 (1): 9–21. [ Links ]
Dall, W., B. J. Hill, P. C. Rothlisberg & D. J. Staples. 1990. The Biology of the Penaeidae. In: Blaxter, J. H. S. & A. J. Southward (Eds.). Advances in Marine Biology Vol. 27. Academic Press, Cornwall, 489 pp. [ Links ]
Divita, R.; M. Creel & P. Sheridan. 1983. Foods of coastal fishes during Brown shrimp, Penaeus aztecus, migration from Texas estuaries (June–July, 1981). Fishery Bulletin 81 (2): 396–404. [ Links ]
Ehrardt, C. E., Legault, C. M. & V. R. Restrepo. 2001. Density dependent linkage between juveniles and recruitment for pink shrimp (Farfantepenaeus duorarum) in Southern Florida. ICES Journal of Marine Science 58: 1100–1105. [ Links ]
Garcia, S. & L. Le Reste. 1981. Life cycles, dynamics, exploitation and management of coastal penaeid shrimp stocks. FAO Fisheries Technical Paper 203: 1–215. [ Links ]
Gaudry, W. J. Jr. Ill & C. J. White. 1973. Investigations of commercially important penaeid shrimp in Louisiana estuaries. Louisiana Wild Life and Fisheries Commission. Technical bulletin 8. 154 p. [ Links ]
González, J., R. Soto & J. Ochoa. 2009. Predicción de mareas en México. http://oceanografia.cicese.mx/predmar/marques.html. [ Links ]
Gracia, A. 1997a. Simulated and actual effects of the Brown Shrimp, Penaeus aztecus, closure in Mexico. Marine Fisheries Review. 59 (2): 18–24. [ Links ]
Gracia, A. 1997b. Pesquería artesanal del camarón. En: D. Flores–Hernandez, P. Sanchez–Gil, J.C. Seijo & F. Arreguin–Sanchez (Eds.) Analisis y Diagnóstico de los recursos pesqueros críticos del Golfo de México. Universidad Autonoma de Campeche. EPOMEX Serie Científica 7. 173–184. [ Links ]
Haas, H. L., Lamon Ill, E. C., Rose, K. A., & R. F. Shaw. 2001. Environmental and biological factors associated with the stage specific abundance of brown shrimp (Penaeus aztecus) in Louisiana: applying a new combination of statistical techniques to long–term monitoring data. Canadian Journal of Fisheries and Aquatic Sciences 58: 2258–2270. [ Links ]
Haas, H. L., K. A. Rose, B. Fry, T. J. Minello & L. P. Rozas. 2004. Brown shrimp on the edge: linking habitat to survival using an individual–based simulation model. Ecological Applications 14: 1232–1247. [ Links ]
INAPESCA (Instituto Nacional de Pesca). 2007. Fundamento técnico para el establecimiento de vedas a la pesca de camarón en el Golfo de México y Mar Caribe (2007). Informe Técnico. Instituto Nacional de Pesca. 35 pp. http://www.inapesca.gob.mx/portal/sala–de–prensa/dictamenes/cat_view/16camaron?limit=5 & order=date & dir=DESC & start=30. [ Links ]
Instituto Nacional de Pesca (INAPESCA). 2008. Estimación de la fecha óptima para la apertura de la temporada 2008–2009 de la pesquería de camarón café (Farfantepeneaus aztecus) en las costas de Tamaulipas y Veracruz. Informe Técnico. Instituto Nacional de Pesca. 35 pp. http://www.inapesca.gob.mx/portal/sala–de–prensa/dictamenes/cat_view/16–camaron. [ Links ]
King, B. D., Ill. 1971. Study of migratory pattern of fish of shellfish through a natural pass. Technical Service Texas Park Wildlife. 9: 1–54. [ Links ]
Lassuy, D. 1983. Species Profiles: Life Histories and Environmental Requirements (Gulf of Mexico) –– Brown Shrimp. U.S. Fish and Wildlife Service Biol. Rep. 82 (11.1): 1–15. [ Links ]
Larson, S. C., M. J. Van Den Avyle & E. L. Bozeman, J. R. 1989. Species profiles: life histories and environmental requirements o f coastal fishes and invertebrates (South Atlantic): brown shrimp. U.S Fish and Wildlife Services. Biology Report. 82 (11.90). 14 p. [ Links ]
Li, J. & A. J. Clarke. 2005. Sea surface temperature and the brown shrimp (Farfantepenaeus aztecus) population on the Alabama, Mississippi, Louisiana and Texas continental shelves. Estuarine Coastal and Shelf Science 4: 261–266. [ Links ]
Matthews, G. A. 1982. Relative abundance and size distributions of commercially important shrimp during the 1981 Texas Closure. Marine Fisheries Review44 (9–10): 5–15. [ Links ]
NMFS. 2008. FishWactch. U.S. Seafood Facts: Brown Shrimp. http://www.st.nmsf.noaa.gov/st1/commercial/landigns/annual_landings.html. [ Links ]
Rulifson, R. A. 1983. Behavioral aspects of juvenile penaeid shrimps, P. aztecus and P. duorarum, during tidal transport. Contributions of Marine. Science 26: 55–63. [ Links ]
Saoud, I. P. & D. Allen. 2003. Salinity tolerance of brown shrimp Farfantepenaeus aztecus as it relates to postlarval and juvenile survival, distribution, and growth in estuaries. Estuaries 26 (4A): 970–974 [ Links ]
Sheridan, P. F., F. J. Patella, N. Baxter & D. A. Emiliani. 1987. Movements of brown shrimp, Penaeus aztecus, and pink shrimp, P. duorarum, relative to the U.S. – Mexico border in the western Gulf of Mexico. Marine Fisheries Review49 (1): 14–19. [ Links ]
St. Amant, L. S., J. G. Broom & T. B. Ford. 1965. Studies of the brown shrimp, Penaeus aztecus, in Barataria Bay, Louisiana. Bulletin of Marine Science Gulf Caribb. 18: 1–16. [ Links ]
Trent, L. 1966. Size of brown shrimp and time of emigration from the Galveston Bay System, Texas. Proceedings of the Gulf and Caribbean Fisheries Institute. Nineteenth Annual Session. November, 1966. pp. 7–16. [ Links ]
Turner, R. E. & M. S. Brody. 1983. Habitat suitability index model: northern Gulf of Mexico brown shrimp and white shrimp. U. S. Dept. of Int. Fish. Wildl. Serv. FWS/OBS–82/10.54. 24 p. [ Links ]
Wakida–Kusunoki, A. T., L. Garcia–Solorio & N. G. Vázquez Benavides. 2008 Abundancia de juveniles de camarones peneidos comerciales en la zona norte de Laguna Madre, México. Hidrobiológica 18 (1): 85–88. [ Links ]
Wakida–Kusunoki, A. T., R. Solana–Sansores, R. & A. González–Cruz. 2005. Estimación de la abundancia de camarón café (Farfantepenaeus aztecus) en las costas de Tamaulipas, 2002. Oceánides 20 (1,2):17–27. [ Links ]
Wakida–Kusunoki, A. T., R. Solana Sansores, M. E. Sandoval Quintero, G. Núñez Márquez, J. Uribe Martínez, A. González Cruz y M. Medellín Ávila. 2006. Camarón del Golfo de México y Mar Caribe. In: Arreguín Sánchez, F., L. Beléndez Moreno, I. Méndez Gómez–Humarán, R. Solana Sansores y C. Rangel Dávalos (Eds.). Sustentabilidad y pesca responsable en México, Evaluación y Manejo. Instituto Nacional de Pesca, pp. 425–476. [ Links ]
Zein–Eldin, Z. & M. L. Renaud. 1986. Inshore environmental effects on brown shrimp, Penaeus aztecus, and white shrimp, P. setiferus, Populations in coastal Water, particularly of Texas. Marine Fisheries Review 48 (3): 9–19. [ Links ]














